北京课改版九下化学 12.2盐的性质 课件(34张PPT)
文档属性
| 名称 | 北京课改版九下化学 12.2盐的性质 课件(34张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-08 00:00:00 | ||
图片预览











文档简介
课件34张PPT。盐的性质 学习目标 1、利用部分酸碱盐的溶解性表,
归纳出常见盐的溶解性并记忆;
2、能自己总结出盐的化学性质;
3、会运用复分解反应发生的条
件,判断反应能否发生。
提出问题 盐有哪些化学性质?化学性质1、能与金属反应,Fe+CuSO4=生成新盐和新金属Cu+FeSO4知识回顾:把铁钉放到硫酸铜溶液中的现象1.盐 + 金属 = 新盐 + 新金属 (可溶)CaCO3 + 2 HCl ===【讨论】
Na2CO3 、NaHCO3、CaCO3在组成上有什么共同点?
Na2CO3和NaHCO3能否与稀盐酸反应?
如果能反应,请问它们又会生成
什么物质? 化学性质CaCl2 + H2CO3 请回忆实验室制取二氧化碳的化学方程式?
生成的气体是如何检验的呢? CO2+Ca(OH)2=CaCO3↓+H2O 实验探究产生气泡,生成白色沉淀生成蓝色沉淀
生成红褐色沉淀生成白色沉淀不溶于稀硝酸 生成白色沉淀
不溶于稀硝酸迅速用带导管的胶塞塞紧试管口,并通入盛有澄清石灰水的试管中
此气体能使澄清的石灰水变浑浊。讨论揭秘1、与盐酸反应产生二氧化碳的物质的组成里,一定含碳酸根吗?有哪些可能?如何鉴别含有碳酸根或碳酸氢根的物质?
2、你能总结出盐可以与哪几类物质反应,又生成哪类物质吗?
3、酸与盐、碱与盐、盐与盐之间发生的反应,属于化合、分解、置换反应类型吗?有何特点?酸与碱作用属于什么反应类型?你能用通式表示这种反应类型吗?
4、分析、归纳上述几个酸、碱、盐之间的化学反应,它们的生成物有什么特点?请归纳盐的化学性质(可溶)(可溶)(可溶)(可溶)(可溶)(至少有一种沉淀)(至少有一种沉淀)1.盐 + 金属 = 新盐 + 新金属 2.盐 + 酸 = 新盐 + 新酸 3.盐 + 碱 = 新盐 + 新碱4.盐 + 盐 = 新盐 + 新盐讨论下列四个反应跟以前所学的反应有哪些不同?从单质、化合物的角度及反应物、生成物的结构关系讨论各反应的共同点。
??? ? ???
??? ???
Na2CO3+Ca(OH)2 2NaOH+CaCO3↓
Na2SO4+ BaCl2 BaSO4 ↓+ 2NaCl
Na2CO3 + 2 HCl 2NaCl + H2CO3NaHCO3 + HCl NaCl + H2CO33、复分解反应(1)定义: 两种化合物互相交换成分,生成另外两种化合物的反应。(2)特征:里里外外,价不变Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
Na2CO3+ CaCl2==CaCO3 ↓+ 2NaCl
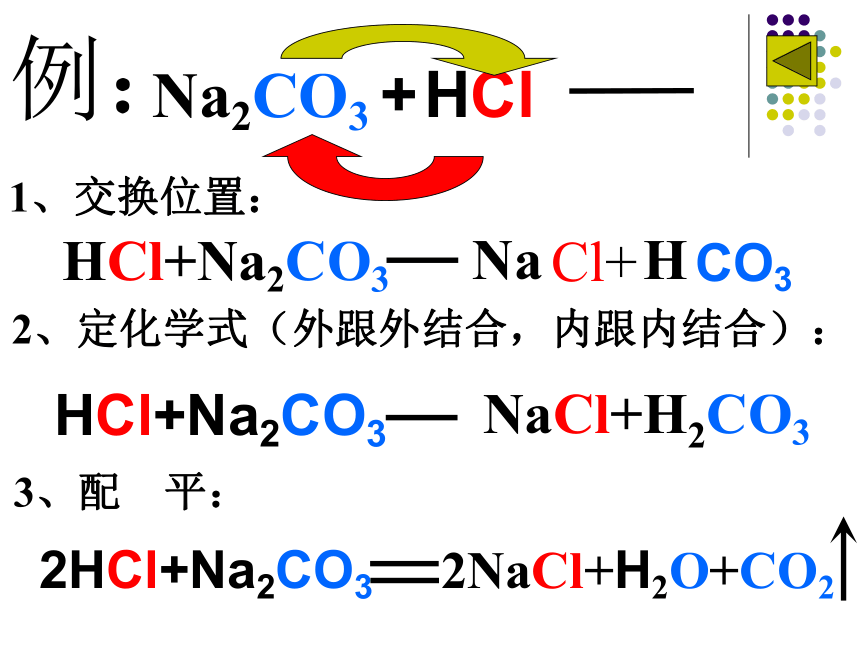
互相交换成分化合物化合物( AB + CD AD + CB )1、交换位置: Cl+ CO3Na H2、定化学式(外跟外结合,内跟内结合):NaCl+H2CO3例:3、配 平:2NaCl+H2O+CO2基本反应类型比较:“多变一”“一变多”单化单化里里外外,
价不变由两种或
两种以上
物质生成
另一种物
质的反应由一种物质
生成两种或
两种以上其
它物质的反
应由一种单质
与一种化合
物反应,生
成另一种单
质与另一种
化合物的反
应由两种化合
物互相交换
成分生成另
外两种化合
物的反应
A+B→ABAB→A+B+ ……C + AB →A +CBAB + CD→ AD+ BC讨论: NaOH + HCl = NaCl +H2O 1、酸与碱作用生成盐和水的反应是否属于复分解反应? 为什么?2、以下反应是否是复分解反应:
CO2 +2NaOH =Na2CO3 +H2O
Fe2O3+6HCl =2FeCl3+3H2O是不是是练一练指出下列反应各属于什么反应类型:
2KClO3 2KCl+ 3O2 ↑( ) 2Cu + O2 2CuO ( )C+ 2CuO 2Cu + CO2↑ ( ) 2HCl + Ca(OH)2 CaCl2 + 2H2O ( ) 2HCl +CaCO3 CaCl2 + H2O + CO2↑( )分解反应化合反应复分解反应置换反应复分解反应讨论分析、归纳下列几个酸、碱、盐之间的复分解反应,它们的生成物有什么特点?(现象)
??? ? ???
Na2CO3 + Ca(OH)2 = 2NaOH + CaCO3↓
Na2SO4 + BaCl2 = BaSO4 ↓+ 2NaCl
NaOH + HCl == NaCl + H2O
Na2CO3 + 2 HCl === 2NaCl + CO2↑+H2ONaHCO3 + HCl === NaCl +CO2↑+H2O
(3)复分解反应发生的条件 两种化合物交换成分时,必需有
沉淀或气体或水生成。想一想:化学方程式是否正确?
KNO3+NaOH=NaNO3+KOH练习书写下列化学方程式:①Na2CO3+H2SO4-
②NH4Cl+ AgNO3-
③FeCl3+ NaOH-
④ AgNO3+Cu-
附录 1 部分酸、碱和盐的溶解性表(20摄氏度) P114 这些物质间
能否反应【思考】1、AgNO3 + HCl ----------
2、 K2CO3+ Ca(OH)2-----
3、Na2CO3+ CaCl2 --------
4、Na2SO4 + HCl ----------5、H2SO4 + BaCl2--------
6、Ba(OH)2+ KCl --------
7、CuSO4 + NH4NO3-----
8、HNO3 + NaOH -------【思考】
1、AgNO3 + HCl --------
2、 K2CO3+ Ca(OH)2---
3、Na2CO3+ CaCl2 -----
4、Na2SO4 + HCl -------5、H2SO4 + BaCl2-------
6、Ba(OH)2+ KCl ------
7、CuSO4 + NH4NO3---
8、HNO3 + NaOH -----AgCl↓+HNO3CaCO3↓+ KOHCaCO3↓+ NaClBaSO4↓+ HClNaNO3 + H2O【课堂练习】×√√√×√ 课后反馈 下列物质间能否发生复分解反应?若能,写出有关反应的化学方程式。
1.硫酸和硝酸钠溶液
2.氢氧化钠溶液和硝酸
3.硫酸钠溶液和氯化钡溶液
4.硝酸和碳酸钾溶液
5.硝酸钾溶液和氢氧化钠溶液写出下列反应的方程式,并讨论它们是否属于复分解反应。
1.盐酸除铁锈。
2.氢氧化镁中和胃酸
3纯碱制烧碱。
4硫酸铜溶液与氢氧化钠溶液反应。
5.硫酸溶液与碳酸钠反应6HCl+2Fe2O3===2FeCl3+3H2OMg(OH)2+2HCl==MgCl2+2H2OCa(OH)2+Na2CO3==2NaCl+CaCO3↓CuSO4+2NaOH==Cu(OH)2↓+Na2SO4H2SO4+Na2CO3==Na2SO4+H2O+CO2↑下列物质能否发生反应?写出能发生反应的化学方 程式,并注明反应类型
(1)银与稀盐酸
(2)铜与硫酸锌溶液
(3)铝与硝酸银溶液
(4)硫酸和硝酸钠溶液
(5)氢氧化钾溶液和硝酸
(6)氯化钠溶液和硝酸银溶液
(7)碳酸钾溶液和盐酸
(8)硫酸铜溶液和氯化钡溶液
警钟长鸣 复分解反应一般是指酸、碱、盐之间在溶液里进行的反应。对反应物而言,还要注意:
1、酸和碱的反应中,一般强酸(盐酸、硫酸、硝
酸)与所有的碱都能反应;
2、酸和盐反应中,盐可以不溶于水,但一定要能
溶于酸;
3、碱和盐、盐和盐反应中,参加反应的碱和盐一
般都要能溶于水。
2、分别将下列各组物质同时放入水中,能发生复分解反应的是( )。
H2SO4 + Ba(NO3)2 B) HCl+CaCO3
C) HCl+Na2SO4 D)HNO3+AgCl
E) Cu(OH)2+NaCl F)NaOH+CaCO3
G)NaOH+KCl H)KOH+MgCl2
I)BaCO3+Na2SO4 J)K2SO4+AgCl
K)KCl+Na2SO4 L)AgNO3+MgCl2
ABHL新知旧识 碳酸根离子或碳酸氢根离子的检验方法:
取少量样品放入试管中,向其中滴加稀盐酸,迅速用带导管的胶塞塞紧试管口,并将导管的另一端通入盛有澄清石灰水的试管中,如果有气泡产生,且澄清石灰水变浑浊,则证明样品中含碳酸根离子或碳酸氢根离子。复分解反应发生的条件:
两种化合物互相交换成分,生成
物中有沉淀或有气体或有水生成。
归纳出常见盐的溶解性并记忆;
2、能自己总结出盐的化学性质;
3、会运用复分解反应发生的条
件,判断反应能否发生。
提出问题 盐有哪些化学性质?化学性质1、能与金属反应,Fe+CuSO4=生成新盐和新金属Cu+FeSO4知识回顾:把铁钉放到硫酸铜溶液中的现象1.盐 + 金属 = 新盐 + 新金属 (可溶)CaCO3 + 2 HCl ===【讨论】
Na2CO3 、NaHCO3、CaCO3在组成上有什么共同点?
Na2CO3和NaHCO3能否与稀盐酸反应?
如果能反应,请问它们又会生成
什么物质? 化学性质CaCl2 + H2CO3 请回忆实验室制取二氧化碳的化学方程式?
生成的气体是如何检验的呢? CO2+Ca(OH)2=CaCO3↓+H2O 实验探究产生气泡,生成白色沉淀生成蓝色沉淀
生成红褐色沉淀生成白色沉淀不溶于稀硝酸 生成白色沉淀
不溶于稀硝酸迅速用带导管的胶塞塞紧试管口,并通入盛有澄清石灰水的试管中
此气体能使澄清的石灰水变浑浊。讨论揭秘1、与盐酸反应产生二氧化碳的物质的组成里,一定含碳酸根吗?有哪些可能?如何鉴别含有碳酸根或碳酸氢根的物质?
2、你能总结出盐可以与哪几类物质反应,又生成哪类物质吗?
3、酸与盐、碱与盐、盐与盐之间发生的反应,属于化合、分解、置换反应类型吗?有何特点?酸与碱作用属于什么反应类型?你能用通式表示这种反应类型吗?
4、分析、归纳上述几个酸、碱、盐之间的化学反应,它们的生成物有什么特点?请归纳盐的化学性质(可溶)(可溶)(可溶)(可溶)(可溶)(至少有一种沉淀)(至少有一种沉淀)1.盐 + 金属 = 新盐 + 新金属 2.盐 + 酸 = 新盐 + 新酸 3.盐 + 碱 = 新盐 + 新碱4.盐 + 盐 = 新盐 + 新盐讨论下列四个反应跟以前所学的反应有哪些不同?从单质、化合物的角度及反应物、生成物的结构关系讨论各反应的共同点。
??? ? ???
??? ???
Na2CO3+Ca(OH)2 2NaOH+CaCO3↓
Na2SO4+ BaCl2 BaSO4 ↓+ 2NaCl
Na2CO3 + 2 HCl 2NaCl + H2CO3NaHCO3 + HCl NaCl + H2CO33、复分解反应(1)定义: 两种化合物互相交换成分,生成另外两种化合物的反应。(2)特征:里里外外,价不变Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
Na2CO3+ CaCl2==CaCO3 ↓+ 2NaCl
互相交换成分化合物化合物( AB + CD AD + CB )1、交换位置: Cl+ CO3Na H2、定化学式(外跟外结合,内跟内结合):NaCl+H2CO3例:3、配 平:2NaCl+H2O+CO2基本反应类型比较:“多变一”“一变多”单化单化里里外外,
价不变由两种或
两种以上
物质生成
另一种物
质的反应由一种物质
生成两种或
两种以上其
它物质的反
应由一种单质
与一种化合
物反应,生
成另一种单
质与另一种
化合物的反
应由两种化合
物互相交换
成分生成另
外两种化合
物的反应
A+B→ABAB→A+B+ ……C + AB →A +CBAB + CD→ AD+ BC讨论: NaOH + HCl = NaCl +H2O 1、酸与碱作用生成盐和水的反应是否属于复分解反应? 为什么?2、以下反应是否是复分解反应:
CO2 +2NaOH =Na2CO3 +H2O
Fe2O3+6HCl =2FeCl3+3H2O是不是是练一练指出下列反应各属于什么反应类型:
2KClO3 2KCl+ 3O2 ↑( ) 2Cu + O2 2CuO ( )C+ 2CuO 2Cu + CO2↑ ( ) 2HCl + Ca(OH)2 CaCl2 + 2H2O ( ) 2HCl +CaCO3 CaCl2 + H2O + CO2↑( )分解反应化合反应复分解反应置换反应复分解反应讨论分析、归纳下列几个酸、碱、盐之间的复分解反应,它们的生成物有什么特点?(现象)
??? ? ???
Na2CO3 + Ca(OH)2 = 2NaOH + CaCO3↓
Na2SO4 + BaCl2 = BaSO4 ↓+ 2NaCl
NaOH + HCl == NaCl + H2O
Na2CO3 + 2 HCl === 2NaCl + CO2↑+H2ONaHCO3 + HCl === NaCl +CO2↑+H2O
(3)复分解反应发生的条件 两种化合物交换成分时,必需有
沉淀或气体或水生成。想一想:化学方程式是否正确?
KNO3+NaOH=NaNO3+KOH练习书写下列化学方程式:①Na2CO3+H2SO4-
②NH4Cl+ AgNO3-
③FeCl3+ NaOH-
④ AgNO3+Cu-
附录 1 部分酸、碱和盐的溶解性表(20摄氏度) P114 这些物质间
能否反应【思考】1、AgNO3 + HCl ----------
2、 K2CO3+ Ca(OH)2-----
3、Na2CO3+ CaCl2 --------
4、Na2SO4 + HCl ----------5、H2SO4 + BaCl2--------
6、Ba(OH)2+ KCl --------
7、CuSO4 + NH4NO3-----
8、HNO3 + NaOH -------【思考】
1、AgNO3 + HCl --------
2、 K2CO3+ Ca(OH)2---
3、Na2CO3+ CaCl2 -----
4、Na2SO4 + HCl -------5、H2SO4 + BaCl2-------
6、Ba(OH)2+ KCl ------
7、CuSO4 + NH4NO3---
8、HNO3 + NaOH -----AgCl↓+HNO3CaCO3↓+ KOHCaCO3↓+ NaClBaSO4↓+ HClNaNO3 + H2O【课堂练习】×√√√×√ 课后反馈 下列物质间能否发生复分解反应?若能,写出有关反应的化学方程式。
1.硫酸和硝酸钠溶液
2.氢氧化钠溶液和硝酸
3.硫酸钠溶液和氯化钡溶液
4.硝酸和碳酸钾溶液
5.硝酸钾溶液和氢氧化钠溶液写出下列反应的方程式,并讨论它们是否属于复分解反应。
1.盐酸除铁锈。
2.氢氧化镁中和胃酸
3纯碱制烧碱。
4硫酸铜溶液与氢氧化钠溶液反应。
5.硫酸溶液与碳酸钠反应6HCl+2Fe2O3===2FeCl3+3H2OMg(OH)2+2HCl==MgCl2+2H2OCa(OH)2+Na2CO3==2NaCl+CaCO3↓CuSO4+2NaOH==Cu(OH)2↓+Na2SO4H2SO4+Na2CO3==Na2SO4+H2O+CO2↑下列物质能否发生反应?写出能发生反应的化学方 程式,并注明反应类型
(1)银与稀盐酸
(2)铜与硫酸锌溶液
(3)铝与硝酸银溶液
(4)硫酸和硝酸钠溶液
(5)氢氧化钾溶液和硝酸
(6)氯化钠溶液和硝酸银溶液
(7)碳酸钾溶液和盐酸
(8)硫酸铜溶液和氯化钡溶液
警钟长鸣 复分解反应一般是指酸、碱、盐之间在溶液里进行的反应。对反应物而言,还要注意:
1、酸和碱的反应中,一般强酸(盐酸、硫酸、硝
酸)与所有的碱都能反应;
2、酸和盐反应中,盐可以不溶于水,但一定要能
溶于酸;
3、碱和盐、盐和盐反应中,参加反应的碱和盐一
般都要能溶于水。
2、分别将下列各组物质同时放入水中,能发生复分解反应的是( )。
H2SO4 + Ba(NO3)2 B) HCl+CaCO3
C) HCl+Na2SO4 D)HNO3+AgCl
E) Cu(OH)2+NaCl F)NaOH+CaCO3
G)NaOH+KCl H)KOH+MgCl2
I)BaCO3+Na2SO4 J)K2SO4+AgCl
K)KCl+Na2SO4 L)AgNO3+MgCl2
ABHL新知旧识 碳酸根离子或碳酸氢根离子的检验方法:
取少量样品放入试管中,向其中滴加稀盐酸,迅速用带导管的胶塞塞紧试管口,并将导管的另一端通入盛有澄清石灰水的试管中,如果有气泡产生,且澄清石灰水变浑浊,则证明样品中含碳酸根离子或碳酸氢根离子。复分解反应发生的条件:
两种化合物互相交换成分,生成
物中有沉淀或有气体或有水生成。
