粤教版九年级下册化学 8.3酸和碱的反应 同步练习(含解析)
文档属性
| 名称 | 粤教版九年级下册化学 8.3酸和碱的反应 同步练习(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 131.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-09 00:00:00 | ||
图片预览



文档简介
粤教版九年级下册化学练习 8.3酸和碱的反应
一、单选题
1.下列物质中很难导电的是(?? ) ???
A.?蔗糖溶液????????????????????????????????B.?铜????????????????????????????????C.?石墨????????????????????????????????D.?氯化钠溶液
2. 人体摄入过量的铝会对脑、肾等器官造成损害,世界卫生组织奖铝确定为食品污染物.但现实生活中,却“铝禁不止”.下列关于铝的应用不科学的是( )
A.?使用含铝膨松剂制作油条????????????????????????????????????B.?使用铁锅代替铝制炊具 C.?用纸盒代替铝制品易拉罐盛装饮料??????????????????????D.?用氢氧化镁代替氢氧化铝中和过多胃酸
3. 下列推断正确的是( )?
A.?在加压条件下,6000L氧气可装入容积为40L的钢瓶中,由此推断氧气分子变小了 B.?蔗糖在热水中的溶解速度更快,由此推断在受热情况下分子运动速率加快 C.?中和反应生成盐和水,由此推断生成盐和水的反应一定是中和反应 D.?碱能使酚酞试液变红,由此推断能使酚酞试液变红的物质一定是碱
4.在A+B→盐+水的反应中,A和B不可能是( )
A.?HCl和NaOH??????????????????B.?CO2和NaOH?????????????????C.?H2SO4和CuO??????????????????D.?H2SO4和BaCl2
5.下列曲线能正确表达对应的反应或过程的是(?? )
A.?向一定量的盐酸中逐滴加水稀释 B.?某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分 C.?金属与一定量的稀硫酸反应,由图象可知,金属N比金属M活泼 D.?将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液中溶质质量分数大小关系是:a>b>c
6.下列叙述正确的是(?? )
A.?氧化物中含有氧元素,而含氧元素的化合物不一定是氧化物 B.?中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 C.?酸中都含有氢元素,所以含有氢元素的化合物一定是酸 D.?置换反应一定有单质生成,所以有单质生成的反应一定是置换反应
7.类推是化学学习中常用的方法。以下类推结果正确的是{???? }
A.?溶液是由溶质和溶剂组成,所以溶液一定是混合物 B.?中和反应有盐和水生成,所以有盐和水生成的化学反应一定是中和反应 C.?有一些金属与稀硫酸反应放出气体,所以与稀硫酸反应放出气体的物质是金属 D.?燃烧一般都伴随发光和放热现象,所以有发光和放热现象的变化都是燃烧
8.在实验室里,欲使碱性溶液变成中性,下列试剂中最好选用哪一种组合( ) ① NaOH溶液②稀盐酸 ③石灰水 ④酚酞试液
A.?①或③????????????????????????????????B.?只有②????????????????????????????????C.?只有①????????????????????????????????D.?②和④
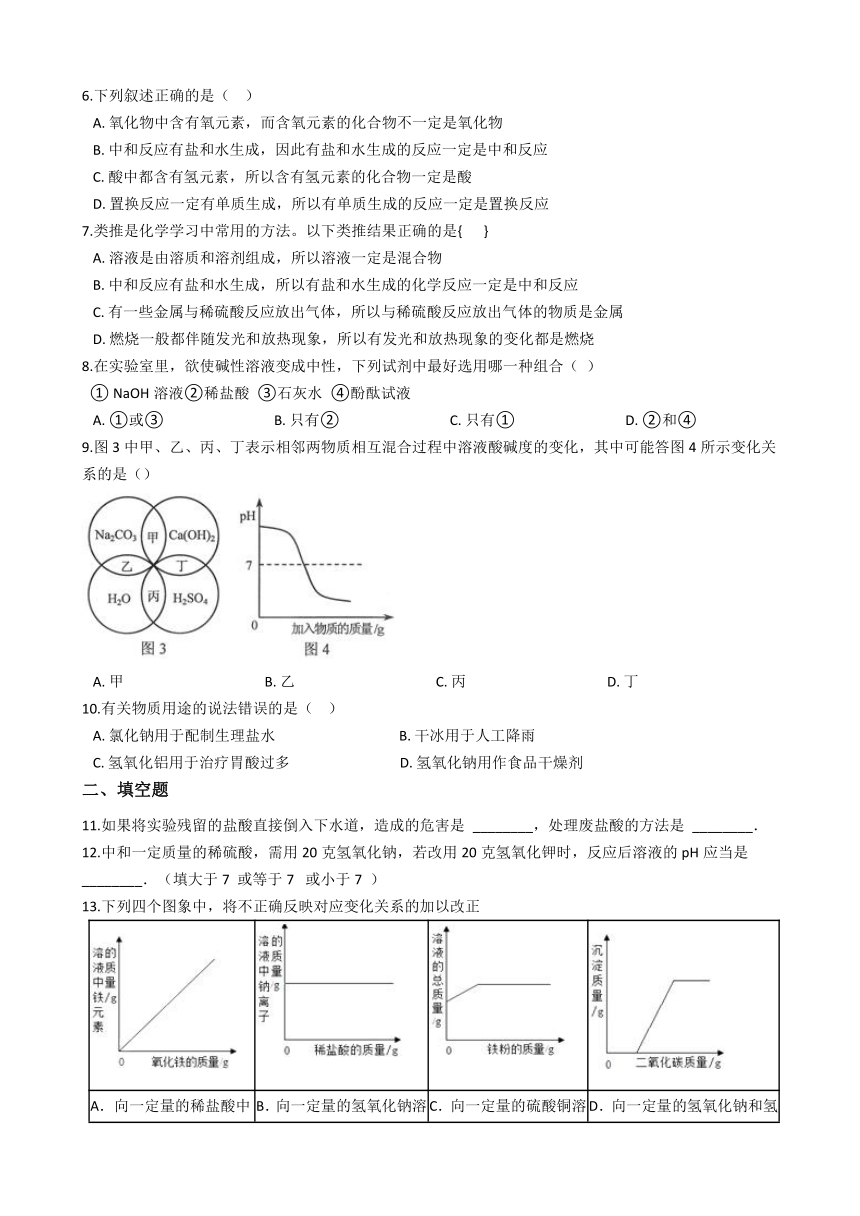
9.图3中甲、乙、丙、丁表示相邻两物质相互混合过程中溶液酸碱度的变化,其中可能答图4所示变化关系的是()
A.?甲?????????????????????????????????????????B.?乙?????????????????????????????????????????C.?丙?????????????????????????????????????????D.?丁
10.有关物质用途的说法错误的是(?? )
A.?氯化钠用于配制生理盐水????????????????????????????????????B.?干冰用于人工降雨 C.?氢氧化铝用于治疗胃酸过多????????????????????????????????D.?氢氧化钠用作食品干燥剂
二、填空题
11.如果将实验残留的盐酸直接倒入下水道,造成的危害是 ________,处理废盐酸的方法是 ________.
12.中和一定质量的稀硫酸,需用20克氢氧化钠,若改用20克氢氧化钾时,反应后溶液的pH应当是________.(填大于7 或等于7? 或小于7 )
13.下列四个图象中,将不正确反映对应变化关系的加以改正
A.向一定量的稀盐酸中加入氧化铁
B.向一定量的氢氧化钠溶液中滴加稀盐酸
C.向一定量的硫酸铜溶液中加入铁粉
D.向一定量的氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳
A.________B.________C.________D.________
三、解答题
14.(1)用石灰浆粉刷墙壁,干燥后墙面就变硬了,这是为什么?请写上相应的化学方程式.
(2)中和反应在实际中的应用很广,请你任写两点.
四、综合题
15.如图是反应的微观示意图.
(1)图中单质的化学式为________;写出该反应的化学方程式:________.
(2)已知HClO是一种酸,能与碱反应生成盐和水.将氯气通入过量NaOH溶液,所得溶液中的溶质有哪些?
16.化学与我们的生活有着密切的联系。请从下列物质中选择相应的序号填空:
①淀粉? ②活性炭?? ③熟石灰??? ④小苏打?? ⑤石墨????
(1)可作干电池电极的是________;??????
(2)能用于吸附冰箱异味的是________;
(3)可用来改良酸性土壤的是________;??
(4)米和面中含有的糖类物质主要是 ________;
(5)可用来治疗胃酸过多症的一种药剂是________ 。
答案解析部分
一、单选题
1.【答案】 A
【解析】【解答】蔗糖溶液中含有蔗糖分子和水分子,不能导电; 故答案为:A。
【分析】根据电流的形成是有自由移动的微粒定向移动分析,蔗糖溶液中是分子,不能导电。
2.【答案】 A
【解析】【解答】A、糕点、油条使用含铝膨化剂,食物中的铝元素就会通过食物进入人体,该做法必须加以控制;
B、使用铁锅代替铝制炊具不含铝元素,可以使用;
C、铝制易拉罐,饮料中会含有铝元素,其中的铝元素会随饮料喝进人体内,用纸盒代替铝制品易拉罐盛装饮料,防止铝元素进入人体,可以使用;
D、使用含氢氧化铝的胃药,人在服药时铝元素也会进入人体,氢氧化镁代替氢氧化铝中和过多胃酸,防止铝元素进入人体,可以使用;
故选A.
【分析】根据人体摄入铝的途径判断,人体摄入铝元素主要是通过消化系统完成的,凡是使用铝制炊具、餐具、食品包装或吃含有铝的药物、食品都会摄入过多的铝,应加以控制使用.
3.【答案】 B
【解析】【解答】A、分子间有间隔,气体受压后,分子间隔变小,气体的体积减小.氧分子之间有一定的间隔,在加压时分子之间的间隔变小,故6000L氧气加压后可装入容积为40L的钢瓶中,故选项解释错误;
B、蔗糖在热水中的溶解速度更快,是因为受热情况下,分子运动速率加快,故选项解释正确;
C、中和反应是酸和碱的反应,生成盐和水的反应不一定是酸和碱的反应,故生成盐和水的反应不一定是中和反应;故选项解释错误;
D、碱性溶液能使酚酞变红,有些盐的溶液也显碱性,例如碳酸钠,故此选项错误;
故选B.
【分析】根据分子间有间隔,气体受压后,分子间隔变小,气体的体积减小,蔗糖在热水中的溶解速度更快,是因为受热情况下,分子运动速率加快,中和反应是酸和碱的反应,生成盐和水的反应不一定是酸和碱的反应,碱性溶液能使酚酞变红,有些盐的溶液也显碱性进行解答.
4.【答案】 D
【解析】【解答】A、HCl和NaOH属于中和反应,能够生成盐和水,故A不符合题意;
B、二氧化碳和氢氧化钠反应生成了碳酸钠和水,其中碳酸钠为盐类,故B不符合题意;
C、硫酸和氧化铜反应生成了硫酸铜和水,其中硫酸铜为盐类,故C不符合题意;
D、硫酸和氯化钡反应生成了硫酸钡沉淀和盐酸,故D符合题意.
故选D.
【分析】根据所学物质的性质来解答该题,其中能够生成盐和水的反应通常为:金属氧化物和酸的反应、部分非金属氧化物和碱的反应以及酸碱中和反应,可以据此解答该题.
5.【答案】 B
【解析】【解答】解:A、酸在稀释过程中,pH值不断增加,但是pH值不会大于7,故A错误;
B、某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分,溶质质量分数不断壮增大,然后不变,故B正确;
C、金属与一定量的稀硫酸反应,由图象可知,金属M比金属N活泼,故C错误;
D、将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,a、b物质的溶解度增大,c物质的溶解度减小,会析出晶体,所得溶液中溶质质量分数大小关系是:a=b>c,故D错误.
故选:B.
【分析】A、根据酸在稀释过程中,pH值不断增加,但是pH值不会大于7进行分析;
B、根据某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分,溶质质量分数不断壮增大,然后不变进行分析;
C、根据金属活动性顺序进行分析;
D、根据将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,a、b物质的溶解度增大,不会析出晶体,c物质的溶解度减小,会析出晶体进行分析.
6.【答案】A
【解析】【解答】解:A、氧化物中含有氧元素,但含氧元素的化合物不一定是氧化物,例如KMnO4中含有氧元素,但它由三种元素组成,所以它不是氧化物;故A正确.
B、金属氧化物与酸反应也生成盐和水,但不是中和反应;故B不正确.
C、水中含有氢元素,氢氧化钠中也含有氢元素,但它们都不是酸;故C不正确.
D、高锰酸钾受热分解产生单质氧气,但不是置换反应;故D不正确.
故选A
【分析】氧化物是指由两种元素组成,其中有一种是氧元素的化合物;中和反应特指酸与碱生成盐和水的反应;酸和碱中都含有氢元素;置换反应不仅要求生成物中是一种单质和一种化合物,还要求反应物也是一种单质和一种化合物.
7.【答案】 A
【解析】【解答】A、混合物是由两种或两种以上物质组成的物质,所以溶质和溶剂最少有两种物质,所以属于混合物,故A正确;
B、中和反应必须是酸和碱反应生成盐和水,金属氧化物与酸反应生成盐和水,但不属于中和反应,故B错; C、与稀硫酸反应放出气体的物质不一定是金属,可以是碳酸盐,故C错; D、灯泡发光放热,但属于物理变化,故D错. 故选A.
【分析】A、根据溶液的特点考虑;B、根据中和反应的定义考虑;C、根据酸的化学性质考虑本题;D、根据发光放热但属于物理变化的特例来考虑.解答本题关键是要知道混合物的定义、中和反应的定义、酸的化学性质和燃烧的特点.
8.【答案】 B
【解析】①是碱,不可中和。②是酸可以与碱中和反应;③是碱,不可以中和;④是酸碱指示剂,只能判断酸碱性,不能中和碱。
故选B
【分析】欲使碱性溶液变成中性,需要加入适量的酸进行中和反应;
9.【答案】 D
【解析】【分析】右图而可以看出该反应是碱性溶液与酸性溶液相互结合至恰好反应,此时PH等于7,再滴加酸液溶液会显酸性,PH小于7,利用这一过程对图一进行分析判断即可. 【解答】在图二中根据PH的变化情况可知,PH由大于7到等于7最后小于7,正好是碱的溶液加酸后的过程,在图一中只有氢氧化钙与硫酸的反应正好符合. 故选D 【点评】此题是一道反应与图示的结合题,解题的关键是对图二PH的分析,找到反应物的PH特点,进而作出判断.
10.【答案】 D
【解析】【解答】A. 氯化钠用于配制生理盐水,不符合题意;
B. 干冰用于人工降雨,不符合题意;
C. 氢氧化铝用于治疗胃酸过多,不符合题意;
D. 氢氧化钠有强烈的腐蚀性,不能用作食品干燥剂,符合题意。
故答案为:D。
【分析】A、生理盐水是0.9%的氯化钠溶液; B、干冰升华吸热,可使周围环境的温度降低,使空气中的水蒸气冷凝; C、氢氧化铝能够与胃液中的盐酸发生中和反应; D、氢氧化钠具有强烈的腐蚀性。
二、填空题
11.【答案】腐蚀下水道;加适量氢氧化钙中和
【解析】【解答】解:盐酸显酸性会腐蚀铁制管道,排放前可以加碱性物质氢氧化钙处理成中性在排放,所以本题答案为:腐蚀下水道,加适量氢氧化钙中和. 【分析】盐酸具有酸性,直接倒入下水道,会造成管道腐蚀,所以需处理成中性后在排放.
12.【答案】小于7
【解析】【解答】解:氢氧化钠、氢氧化钾与硫酸反应的化学方程式分别是:
2NaOH+
H2SO4=Na2SO4+2H2O
80
98
2KOH+
H2SO4═K2SO4+2H2O
112
98
可知,80份质量的氢氧化钠与98份质量的硫酸恰好完全反应,而98份质量的硫酸能与112份质量的氢氧化钾恰好完全反应;中和一定质量的稀硫酸,需用20克氢氧化钠,则改用20克氢氧化钾后,稀硫酸有剩余,溶液显酸性,反应后溶液的pH应当是小于7.
故答案为:小于7.
【分析】根据氢氧化钠、氢氧化钾与硫酸反应的化学方程式,判断改用20克氢氧化钾反应后剩余的是哪一种溶液,再根据当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;进行分析解答.
13.【答案】;正确;;
【解析】【解答】解:A、向一定量的稀盐酸中加入氧化铁,则溶液中铁元素的质量逐渐增大,当盐酸全部反应,则铁元素的质量不变,故填: ; B、向一定量的氢氧化钠溶液中滴加稀盐酸,则钠离子的质量不变,正确; C、向一定量的硫酸铜溶液中加入铁粉,则铁会将铜置换出来,溶液的总质量逐渐减小,最后不变,故填: ; D、向一定量的氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳,则一开始就产生碳酸钙沉淀,故填: . 【分析】A、根据稀盐酸与氧化铁的反应解答; B、根据氢氧化钠与盐酸的反应解答; C、根据硫酸铜与铁粉的反应解答; D、根据常见的碱与二氧化碳的反应解答.
三、解答题
14.【答案】 (1)氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水,碳酸钙是坚硬的物质,故墙壁会变硬?????? Ca(OH)2+CO2═CaCO3↓+H2O;
(2)熟石灰改良酸性土壤,氢氧化铝治疗胃酸过多.
【解析】【解答】解:(1)氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水,碳酸钙是坚硬的物质,故墙壁会变硬,故答案为:Ca(OH)2+CO2═CaCO3↓+H2O;
(2)氢氧化钙具有碱性,可以用于改良酸性土壤,氢氧化铝能用于治疗胃酸过多,都是中和反应的应用,故答案为:熟石灰改良酸性土壤,氢氧化铝治疗胃酸过多.
【分析】根据已有的知识进行分析解答,氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水,根据中和反应的应用进行分析解答即可.
四、综合题
15.【答案】(1)Cl2;Cl2+H2O═HCl+HClO; (2)NaCl、NaClO、NaOH
【解析】【解答】解:(1)观察图示可得,该反应是氯气和水生成了氯化氢和次氯酸;反应的化学方程式:Cl2+H2O═HCl+HClO;因此图中的单质为氯气;故填:Cl2;Cl2+H2O═HCl+HClO(2)解:氯气和水生成了氯化氢和次氯酸,HClO是一种酸,能与碱反应生成盐和水,因此氯气与NaOH溶液反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;因此溶液中的溶质为NaCl、NaClO和过量的NaOH;故填:NaCl、NaClO、NaOH
【分析】(1)观察微观示意图,根据微粒的构成分析物质的类别及名称,分析反应物、生成物,写出反应的化学方程式;(2)根据题目信息结合方程式的书写方法写出反应的方程式.
16.【答案】(1)⑤ (2)② (3)③ (4)① (5)④
【解析】【解答】⑴石墨具有导电性, 可作干电池电极的是; ⑵ 活性炭具有吸附性,能用于吸附冰箱异味;⑶ 熟石灰是弱碱性的物质,可用来改良酸性土壤的是;?? ⑷ 米和面中含有的糖类物质主要是淀粉;⑸小苏打是碳酸氢钠,可以与稀盐酸反应,故可用来治疗胃酸过多症。
【分析】物质的性质决定物质的用途,根据题中所给物质的性质分析解答
一、单选题
1.下列物质中很难导电的是(?? ) ???
A.?蔗糖溶液????????????????????????????????B.?铜????????????????????????????????C.?石墨????????????????????????????????D.?氯化钠溶液
2. 人体摄入过量的铝会对脑、肾等器官造成损害,世界卫生组织奖铝确定为食品污染物.但现实生活中,却“铝禁不止”.下列关于铝的应用不科学的是( )
A.?使用含铝膨松剂制作油条????????????????????????????????????B.?使用铁锅代替铝制炊具 C.?用纸盒代替铝制品易拉罐盛装饮料??????????????????????D.?用氢氧化镁代替氢氧化铝中和过多胃酸
3. 下列推断正确的是( )?
A.?在加压条件下,6000L氧气可装入容积为40L的钢瓶中,由此推断氧气分子变小了 B.?蔗糖在热水中的溶解速度更快,由此推断在受热情况下分子运动速率加快 C.?中和反应生成盐和水,由此推断生成盐和水的反应一定是中和反应 D.?碱能使酚酞试液变红,由此推断能使酚酞试液变红的物质一定是碱
4.在A+B→盐+水的反应中,A和B不可能是( )
A.?HCl和NaOH??????????????????B.?CO2和NaOH?????????????????C.?H2SO4和CuO??????????????????D.?H2SO4和BaCl2
5.下列曲线能正确表达对应的反应或过程的是(?? )
A.?向一定量的盐酸中逐滴加水稀释 B.?某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分 C.?金属与一定量的稀硫酸反应,由图象可知,金属N比金属M活泼 D.?将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液中溶质质量分数大小关系是:a>b>c
6.下列叙述正确的是(?? )
A.?氧化物中含有氧元素,而含氧元素的化合物不一定是氧化物 B.?中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 C.?酸中都含有氢元素,所以含有氢元素的化合物一定是酸 D.?置换反应一定有单质生成,所以有单质生成的反应一定是置换反应
7.类推是化学学习中常用的方法。以下类推结果正确的是{???? }
A.?溶液是由溶质和溶剂组成,所以溶液一定是混合物 B.?中和反应有盐和水生成,所以有盐和水生成的化学反应一定是中和反应 C.?有一些金属与稀硫酸反应放出气体,所以与稀硫酸反应放出气体的物质是金属 D.?燃烧一般都伴随发光和放热现象,所以有发光和放热现象的变化都是燃烧
8.在实验室里,欲使碱性溶液变成中性,下列试剂中最好选用哪一种组合( ) ① NaOH溶液②稀盐酸 ③石灰水 ④酚酞试液
A.?①或③????????????????????????????????B.?只有②????????????????????????????????C.?只有①????????????????????????????????D.?②和④
9.图3中甲、乙、丙、丁表示相邻两物质相互混合过程中溶液酸碱度的变化,其中可能答图4所示变化关系的是()
A.?甲?????????????????????????????????????????B.?乙?????????????????????????????????????????C.?丙?????????????????????????????????????????D.?丁
10.有关物质用途的说法错误的是(?? )
A.?氯化钠用于配制生理盐水????????????????????????????????????B.?干冰用于人工降雨 C.?氢氧化铝用于治疗胃酸过多????????????????????????????????D.?氢氧化钠用作食品干燥剂
二、填空题
11.如果将实验残留的盐酸直接倒入下水道,造成的危害是 ________,处理废盐酸的方法是 ________.
12.中和一定质量的稀硫酸,需用20克氢氧化钠,若改用20克氢氧化钾时,反应后溶液的pH应当是________.(填大于7 或等于7? 或小于7 )
13.下列四个图象中,将不正确反映对应变化关系的加以改正
A.向一定量的稀盐酸中加入氧化铁
B.向一定量的氢氧化钠溶液中滴加稀盐酸
C.向一定量的硫酸铜溶液中加入铁粉
D.向一定量的氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳
A.________B.________C.________D.________
三、解答题
14.(1)用石灰浆粉刷墙壁,干燥后墙面就变硬了,这是为什么?请写上相应的化学方程式.
(2)中和反应在实际中的应用很广,请你任写两点.
四、综合题
15.如图是反应的微观示意图.
(1)图中单质的化学式为________;写出该反应的化学方程式:________.
(2)已知HClO是一种酸,能与碱反应生成盐和水.将氯气通入过量NaOH溶液,所得溶液中的溶质有哪些?
16.化学与我们的生活有着密切的联系。请从下列物质中选择相应的序号填空:
①淀粉? ②活性炭?? ③熟石灰??? ④小苏打?? ⑤石墨????
(1)可作干电池电极的是________;??????
(2)能用于吸附冰箱异味的是________;
(3)可用来改良酸性土壤的是________;??
(4)米和面中含有的糖类物质主要是 ________;
(5)可用来治疗胃酸过多症的一种药剂是________ 。
答案解析部分
一、单选题
1.【答案】 A
【解析】【解答】蔗糖溶液中含有蔗糖分子和水分子,不能导电; 故答案为:A。
【分析】根据电流的形成是有自由移动的微粒定向移动分析,蔗糖溶液中是分子,不能导电。
2.【答案】 A
【解析】【解答】A、糕点、油条使用含铝膨化剂,食物中的铝元素就会通过食物进入人体,该做法必须加以控制;
B、使用铁锅代替铝制炊具不含铝元素,可以使用;
C、铝制易拉罐,饮料中会含有铝元素,其中的铝元素会随饮料喝进人体内,用纸盒代替铝制品易拉罐盛装饮料,防止铝元素进入人体,可以使用;
D、使用含氢氧化铝的胃药,人在服药时铝元素也会进入人体,氢氧化镁代替氢氧化铝中和过多胃酸,防止铝元素进入人体,可以使用;
故选A.
【分析】根据人体摄入铝的途径判断,人体摄入铝元素主要是通过消化系统完成的,凡是使用铝制炊具、餐具、食品包装或吃含有铝的药物、食品都会摄入过多的铝,应加以控制使用.
3.【答案】 B
【解析】【解答】A、分子间有间隔,气体受压后,分子间隔变小,气体的体积减小.氧分子之间有一定的间隔,在加压时分子之间的间隔变小,故6000L氧气加压后可装入容积为40L的钢瓶中,故选项解释错误;
B、蔗糖在热水中的溶解速度更快,是因为受热情况下,分子运动速率加快,故选项解释正确;
C、中和反应是酸和碱的反应,生成盐和水的反应不一定是酸和碱的反应,故生成盐和水的反应不一定是中和反应;故选项解释错误;
D、碱性溶液能使酚酞变红,有些盐的溶液也显碱性,例如碳酸钠,故此选项错误;
故选B.
【分析】根据分子间有间隔,气体受压后,分子间隔变小,气体的体积减小,蔗糖在热水中的溶解速度更快,是因为受热情况下,分子运动速率加快,中和反应是酸和碱的反应,生成盐和水的反应不一定是酸和碱的反应,碱性溶液能使酚酞变红,有些盐的溶液也显碱性进行解答.
4.【答案】 D
【解析】【解答】A、HCl和NaOH属于中和反应,能够生成盐和水,故A不符合题意;
B、二氧化碳和氢氧化钠反应生成了碳酸钠和水,其中碳酸钠为盐类,故B不符合题意;
C、硫酸和氧化铜反应生成了硫酸铜和水,其中硫酸铜为盐类,故C不符合题意;
D、硫酸和氯化钡反应生成了硫酸钡沉淀和盐酸,故D符合题意.
故选D.
【分析】根据所学物质的性质来解答该题,其中能够生成盐和水的反应通常为:金属氧化物和酸的反应、部分非金属氧化物和碱的反应以及酸碱中和反应,可以据此解答该题.
5.【答案】 B
【解析】【解答】解:A、酸在稀释过程中,pH值不断增加,但是pH值不会大于7,故A错误;
B、某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分,溶质质量分数不断壮增大,然后不变,故B正确;
C、金属与一定量的稀硫酸反应,由图象可知,金属M比金属N活泼,故C错误;
D、将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,a、b物质的溶解度增大,c物质的溶解度减小,会析出晶体,所得溶液中溶质质量分数大小关系是:a=b>c,故D错误.
故选:B.
【分析】A、根据酸在稀释过程中,pH值不断增加,但是pH值不会大于7进行分析;
B、根据某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分,溶质质量分数不断壮增大,然后不变进行分析;
C、根据金属活动性顺序进行分析;
D、根据将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,a、b物质的溶解度增大,不会析出晶体,c物质的溶解度减小,会析出晶体进行分析.
6.【答案】A
【解析】【解答】解:A、氧化物中含有氧元素,但含氧元素的化合物不一定是氧化物,例如KMnO4中含有氧元素,但它由三种元素组成,所以它不是氧化物;故A正确.
B、金属氧化物与酸反应也生成盐和水,但不是中和反应;故B不正确.
C、水中含有氢元素,氢氧化钠中也含有氢元素,但它们都不是酸;故C不正确.
D、高锰酸钾受热分解产生单质氧气,但不是置换反应;故D不正确.
故选A
【分析】氧化物是指由两种元素组成,其中有一种是氧元素的化合物;中和反应特指酸与碱生成盐和水的反应;酸和碱中都含有氢元素;置换反应不仅要求生成物中是一种单质和一种化合物,还要求反应物也是一种单质和一种化合物.
7.【答案】 A
【解析】【解答】A、混合物是由两种或两种以上物质组成的物质,所以溶质和溶剂最少有两种物质,所以属于混合物,故A正确;
B、中和反应必须是酸和碱反应生成盐和水,金属氧化物与酸反应生成盐和水,但不属于中和反应,故B错; C、与稀硫酸反应放出气体的物质不一定是金属,可以是碳酸盐,故C错; D、灯泡发光放热,但属于物理变化,故D错. 故选A.
【分析】A、根据溶液的特点考虑;B、根据中和反应的定义考虑;C、根据酸的化学性质考虑本题;D、根据发光放热但属于物理变化的特例来考虑.解答本题关键是要知道混合物的定义、中和反应的定义、酸的化学性质和燃烧的特点.
8.【答案】 B
【解析】①是碱,不可中和。②是酸可以与碱中和反应;③是碱,不可以中和;④是酸碱指示剂,只能判断酸碱性,不能中和碱。
故选B
【分析】欲使碱性溶液变成中性,需要加入适量的酸进行中和反应;
9.【答案】 D
【解析】【分析】右图而可以看出该反应是碱性溶液与酸性溶液相互结合至恰好反应,此时PH等于7,再滴加酸液溶液会显酸性,PH小于7,利用这一过程对图一进行分析判断即可. 【解答】在图二中根据PH的变化情况可知,PH由大于7到等于7最后小于7,正好是碱的溶液加酸后的过程,在图一中只有氢氧化钙与硫酸的反应正好符合. 故选D 【点评】此题是一道反应与图示的结合题,解题的关键是对图二PH的分析,找到反应物的PH特点,进而作出判断.
10.【答案】 D
【解析】【解答】A. 氯化钠用于配制生理盐水,不符合题意;
B. 干冰用于人工降雨,不符合题意;
C. 氢氧化铝用于治疗胃酸过多,不符合题意;
D. 氢氧化钠有强烈的腐蚀性,不能用作食品干燥剂,符合题意。
故答案为:D。
【分析】A、生理盐水是0.9%的氯化钠溶液; B、干冰升华吸热,可使周围环境的温度降低,使空气中的水蒸气冷凝; C、氢氧化铝能够与胃液中的盐酸发生中和反应; D、氢氧化钠具有强烈的腐蚀性。
二、填空题
11.【答案】腐蚀下水道;加适量氢氧化钙中和
【解析】【解答】解:盐酸显酸性会腐蚀铁制管道,排放前可以加碱性物质氢氧化钙处理成中性在排放,所以本题答案为:腐蚀下水道,加适量氢氧化钙中和. 【分析】盐酸具有酸性,直接倒入下水道,会造成管道腐蚀,所以需处理成中性后在排放.
12.【答案】小于7
【解析】【解答】解:氢氧化钠、氢氧化钾与硫酸反应的化学方程式分别是:
2NaOH+
H2SO4=Na2SO4+2H2O
80
98
2KOH+
H2SO4═K2SO4+2H2O
112
98
可知,80份质量的氢氧化钠与98份质量的硫酸恰好完全反应,而98份质量的硫酸能与112份质量的氢氧化钾恰好完全反应;中和一定质量的稀硫酸,需用20克氢氧化钠,则改用20克氢氧化钾后,稀硫酸有剩余,溶液显酸性,反应后溶液的pH应当是小于7.
故答案为:小于7.
【分析】根据氢氧化钠、氢氧化钾与硫酸反应的化学方程式,判断改用20克氢氧化钾反应后剩余的是哪一种溶液,再根据当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;进行分析解答.
13.【答案】;正确;;
【解析】【解答】解:A、向一定量的稀盐酸中加入氧化铁,则溶液中铁元素的质量逐渐增大,当盐酸全部反应,则铁元素的质量不变,故填: ; B、向一定量的氢氧化钠溶液中滴加稀盐酸,则钠离子的质量不变,正确; C、向一定量的硫酸铜溶液中加入铁粉,则铁会将铜置换出来,溶液的总质量逐渐减小,最后不变,故填: ; D、向一定量的氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳,则一开始就产生碳酸钙沉淀,故填: . 【分析】A、根据稀盐酸与氧化铁的反应解答; B、根据氢氧化钠与盐酸的反应解答; C、根据硫酸铜与铁粉的反应解答; D、根据常见的碱与二氧化碳的反应解答.
三、解答题
14.【答案】 (1)氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水,碳酸钙是坚硬的物质,故墙壁会变硬?????? Ca(OH)2+CO2═CaCO3↓+H2O;
(2)熟石灰改良酸性土壤,氢氧化铝治疗胃酸过多.
【解析】【解答】解:(1)氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水,碳酸钙是坚硬的物质,故墙壁会变硬,故答案为:Ca(OH)2+CO2═CaCO3↓+H2O;
(2)氢氧化钙具有碱性,可以用于改良酸性土壤,氢氧化铝能用于治疗胃酸过多,都是中和反应的应用,故答案为:熟石灰改良酸性土壤,氢氧化铝治疗胃酸过多.
【分析】根据已有的知识进行分析解答,氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水,根据中和反应的应用进行分析解答即可.
四、综合题
15.【答案】(1)Cl2;Cl2+H2O═HCl+HClO; (2)NaCl、NaClO、NaOH
【解析】【解答】解:(1)观察图示可得,该反应是氯气和水生成了氯化氢和次氯酸;反应的化学方程式:Cl2+H2O═HCl+HClO;因此图中的单质为氯气;故填:Cl2;Cl2+H2O═HCl+HClO(2)解:氯气和水生成了氯化氢和次氯酸,HClO是一种酸,能与碱反应生成盐和水,因此氯气与NaOH溶液反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;因此溶液中的溶质为NaCl、NaClO和过量的NaOH;故填:NaCl、NaClO、NaOH
【分析】(1)观察微观示意图,根据微粒的构成分析物质的类别及名称,分析反应物、生成物,写出反应的化学方程式;(2)根据题目信息结合方程式的书写方法写出反应的方程式.
16.【答案】(1)⑤ (2)② (3)③ (4)① (5)④
【解析】【解答】⑴石墨具有导电性, 可作干电池电极的是; ⑵ 活性炭具有吸附性,能用于吸附冰箱异味;⑶ 熟石灰是弱碱性的物质,可用来改良酸性土壤的是;?? ⑷ 米和面中含有的糖类物质主要是淀粉;⑸小苏打是碳酸氢钠,可以与稀盐酸反应,故可用来治疗胃酸过多症。
【分析】物质的性质决定物质的用途,根据题中所给物质的性质分析解答
