科粤版九年级化学下册 8.1 溶液的酸碱性 教案(表格式)
文档属性
| 名称 | 科粤版九年级化学下册 8.1 溶液的酸碱性 教案(表格式) |

|
|
| 格式 | zip | ||
| 文件大小 | 9.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-09 00:00:00 | ||
图片预览

文档简介
第八章 常见的酸、 碱、 盐
8.1溶液的酸碱性
教材
分析
首先根据日常生活中的酸性、酸味、碱性等说法引出溶液的酸碱性及其测定,又由溶液的酸碱程度不同引出酸碱度及其测定,知识自然深入。用pH试纸测定某种物质的酸碱度,是日常生活中常用的手段,也是学生必须具备的一项技能。在本节课中,要让学生知道酸碱度与溶液酸碱性的关系,了解其在实际生活中的应用,并通过实验培养学生的探究能力、思维能力和解决实际问题的能力。
教
学
目
标
知识与
技能
1.认识溶液的酸碱性,会用石蕊溶液、酚酞溶液等指示剂判断溶液的酸碱性。
2.认识溶液酸碱性的强弱程度,懂得使用pH试纸检验溶液的pH,并用溶液的pH判断溶液的酸碱性及酸碱度。
过程与方法
1.通过分组实验提高学生的动手能力、观察、分析、归纳及表达能力。
2.设计情景结合学生的生活经验对课本知识进行讲解。
情感、态度
与价值观
1.培养学生严谨的科学态度和团结协作精神。
2.了解化学测量在化学研究和生产、生活中的重要作用。
教学重点
教学难点
重点:溶液的酸碱性、溶液的酸碱度及指示剂的颜色变化三者之间的关系。
难点: 会使用pH试纸,并用测定溶液pH的方法来判断溶液的酸碱性和酸碱度。
教学环节
师生活动
设计意图
[引入]
出示一个青苹果。
师:咬一口会有什么感觉?
生:会觉得酸。
师:在日常生活中还有哪些物质给我们留下酸的感觉呢?
生:酸奶、醋、柠檬等。
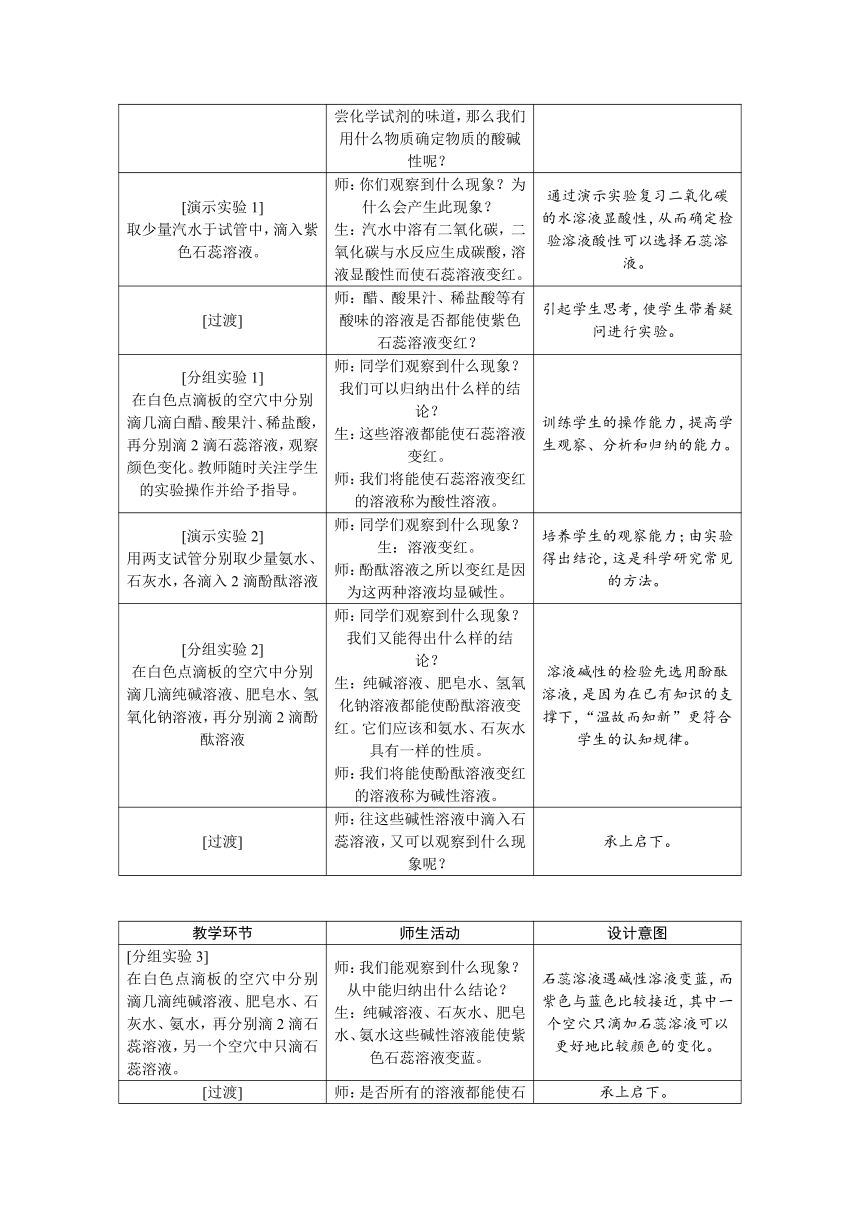
师:通常情况下不允许我们品尝化学试剂的味道,那么我们用什么物质确定物质的酸碱性呢?
结合学生的生活经验,利用条件反射原理,激发学生的学习兴趣。
[演示实验1]
取少量汽水于试管中,滴入紫色石蕊溶液。
师:你们观察到什么现象?为什么会产生此现象?
生:汽水中溶有二氧化碳,二氧化碳与水反应生成碳酸,溶液显酸性而使石蕊溶液变红。
通过演示实验复习二氧化碳的水溶液显酸性,从而确定检验溶液酸性可以选择石蕊溶液。
[过渡]
师:醋、酸果汁、稀盐酸等有酸味的溶液是否都能使紫色石蕊溶液变红?
引起学生思考,使学生带着疑问进行实验。
[分组实验1]
在白色点滴板的空穴中分别滴几滴白醋、酸果汁、稀盐酸,再分别滴2滴石蕊溶液,观察颜色变化。教师随时关注学生的实验操作并给予指导。
师:同学们观察到什么现象?我们可以归纳出什么样的结论?
生:这些溶液都能使石蕊溶液变红。
师:我们将能使石蕊溶液变红的溶液称为酸性溶液。
训练学生的操作能力,提高学生观察、分析和归纳的能力。
[演示实验2]
用两支试管分别取少量氨水、石灰水,各滴入2滴酚酞溶液
师:同学们观察到什么现象?
生:溶液变红。
师:酚酞溶液之所以变红是因为这两种溶液均显碱性。
培养学生的观察能力;由实验得出结论,这是科学研究常见的方法。
[分组实验2]
在白色点滴板的空穴中分别滴几滴纯碱溶液、肥皂水、氢氧化钠溶液,再分别滴2滴酚酞溶液
师:同学们观察到什么现象?我们又能得出什么样的结论?
生:纯碱溶液、肥皂水、氢氧化钠溶液都能使酚酞溶液变红。它们应该和氨水、石灰水具有一样的性质。
师:我们将能使酚酞溶液变红的溶液称为碱性溶液。
溶液碱性的检验先选用酚酞溶液,是因为在已有知识的支撑下,“温故而知新”更符合学生的认知规律。
[过渡]
师:往这些碱性溶液中滴入石蕊溶液,又可以观察到什么现象呢?
承上启下。
教学环节
师生活动
设计意图
[分组实验3]
在白色点滴板的空穴中分别滴几滴纯碱溶液、肥皂水、石灰水、氨水,再分别滴2滴石蕊溶液,另一个空穴中只滴石蕊溶液。
师:我们能观察到什么现象?从中能归纳出什么结论?
生:纯碱溶液、石灰水、肥皂水、氨水这些碱性溶液能使紫色石蕊溶液变蓝。
石蕊溶液遇碱性溶液变蓝,而紫色与蓝色比较接近,其中一个空穴只滴加石蕊溶液可以更好地比较颜色的变化。
[过渡]
师:是否所有的溶液都能使石蕊溶液和酚酞溶液改变颜色呢?
承上启下。
[分组实验4]
在白色点滴板的两个空穴中各滴几滴食盐水,再分别滴入石蕊溶液和酚酞溶液;另两个空穴中各滴几滴蔗糖溶液,再分别滴入石蕊溶液和酚酞溶液。
师:我们能观察到什么现象?生:食盐水和蔗糖溶液都不能使石蕊溶液和酚酞溶液改变颜色。说明这两种溶液不具有酸性和碱性。
师:我们将像食盐水、蔗糖溶液这样不具有酸性也不具有碱性的溶液称为中性溶液。
与溶液的酸碱性相呼应,有助于学生的理解。
[归纳总结]
师:像石蕊溶液和酚酞溶液这样在不同酸碱性溶液中呈现出不同的颜色,可用于检验溶液酸碱性的物质,我们将之称为酸碱指示剂。
师:为帮助同学们更好地记住指示剂在不同酸碱性溶液中的颜色变化,老师将这两种指示剂的颜色变化做以下归纳:石蕊紫色中性显,遇酸变红遇碱蓝;酚酞本来无颜色,碱液惹它则红脸。
用顺口溜的形式总结指示剂颜色的变化,生动形象,且很有针对性。
[拓展讲解]
师:为了使用方便,我们也常用蓝色石蕊试纸和红色石蕊试纸来检验溶液的酸碱性。
扩大学生的知识面。
[演示实验3]
取一张红色石蕊试纸放在表面皿中,用玻璃棒蘸取纯碱溶液滴在试纸上,另取一张蓝色石蕊试纸,用玻璃棒蘸取稀盐酸滴在试纸上。观察试纸的颜色变化。
师:从实验中我们可以发现碱性溶液能使红色石蕊试纸变蓝,而酸性溶液能使蓝色石蕊试纸变红。
做好演示实验为学生使用pH试纸打下基础。
[过渡]
师:我们知道有许多溶液显酸性或碱性,那么它们的酸碱性谁更强一些呢?
引入酸碱度的概念。
教学环节
师生活动
设计意图
[情景设置]
古时候有一个小和尚,他向师父抱怨他干的琐事很累,师父便拿出一些盐让他尝一下,他觉得又咸又涩,师父把他带到一个大湖边让他把那些盐放入湖水中,再尝一下湖水的味道,奇怪的是,苦涩味消失了。
师:醋是我们生活中常用的调味品,同样的道理,如果我们把它直接喝下去,大家都会觉得受不了,然而如果我们把这些醋滴入到一大杯水中,再尝水的味道我们会觉得酸味弱了很多。
设置情景吸引学生的注意力,同学生的生活经验相结合,为以下的实验设计做好准备。
[分组实验5]
(一)用两支试管各取1 mL的同种稀盐酸,向其中一支试管中加满蒸馏水,表面皿中放两张pH试纸,用玻璃棒(洗净擦干)分别蘸取两种盐酸滴到pH试纸上,变色后再与标准比色卡进行比较。
(二)另取两支试管各取1 mL同种纯碱溶液,按实验(一)进行操作。
学生展示实验结果。
师:变色后的试纸与标准比色卡上的哪一种颜色接近,我们就认定该溶液的pH是多少,用广泛pH试纸测定的pH都为整数值。
生:展示实验结果
盐酸:pH=1(未加水,酸性强)
pH=3(加水,酸性弱)
纯碱溶液:
pH=10(未加水,碱性强 )
pH=8(加水,碱性弱)
用实验事实说明pH大小与溶液酸碱性之间的关系。
[分组实验6]
再用pH试纸检验食盐水、蔗糖溶液的pH。
学生展示实验结果
生:食盐水pH=7
蔗糖溶液pH=7
师:很显然中性溶液的pH都为7。
培养学生的实验能力和归纳总结的能力。
[问题设置]
师:pH试纸使用前能否用水润湿?玻璃棒洗净后为什么要擦干?
生:润湿pH试纸和玻璃棒上的水都会对溶液进行稀释,影响实验的结果。
强化实验过程中的注意事项。
[总结归纳]
师:pH的范围在0~14之间,pH=7,溶液呈中性;pH<7,溶液呈酸性;pH>7溶液呈碱性。pH越小,酸性越强,pH越大,碱性越强。
引导学生进一步概括和综合实验的结果。
[布置作业]
师:请同学们尽可能多地收集各种颜色的花,自制酸碱指示剂,并用它们来检验溶液的酸碱性。
知识拓展,进一步增强学生学习化学的兴趣。
8.1溶液的酸碱性
教材
分析
首先根据日常生活中的酸性、酸味、碱性等说法引出溶液的酸碱性及其测定,又由溶液的酸碱程度不同引出酸碱度及其测定,知识自然深入。用pH试纸测定某种物质的酸碱度,是日常生活中常用的手段,也是学生必须具备的一项技能。在本节课中,要让学生知道酸碱度与溶液酸碱性的关系,了解其在实际生活中的应用,并通过实验培养学生的探究能力、思维能力和解决实际问题的能力。
教
学
目
标
知识与
技能
1.认识溶液的酸碱性,会用石蕊溶液、酚酞溶液等指示剂判断溶液的酸碱性。
2.认识溶液酸碱性的强弱程度,懂得使用pH试纸检验溶液的pH,并用溶液的pH判断溶液的酸碱性及酸碱度。
过程与方法
1.通过分组实验提高学生的动手能力、观察、分析、归纳及表达能力。
2.设计情景结合学生的生活经验对课本知识进行讲解。
情感、态度
与价值观
1.培养学生严谨的科学态度和团结协作精神。
2.了解化学测量在化学研究和生产、生活中的重要作用。
教学重点
教学难点
重点:溶液的酸碱性、溶液的酸碱度及指示剂的颜色变化三者之间的关系。
难点: 会使用pH试纸,并用测定溶液pH的方法来判断溶液的酸碱性和酸碱度。
教学环节
师生活动
设计意图
[引入]
出示一个青苹果。
师:咬一口会有什么感觉?
生:会觉得酸。
师:在日常生活中还有哪些物质给我们留下酸的感觉呢?
生:酸奶、醋、柠檬等。
师:通常情况下不允许我们品尝化学试剂的味道,那么我们用什么物质确定物质的酸碱性呢?
结合学生的生活经验,利用条件反射原理,激发学生的学习兴趣。
[演示实验1]
取少量汽水于试管中,滴入紫色石蕊溶液。
师:你们观察到什么现象?为什么会产生此现象?
生:汽水中溶有二氧化碳,二氧化碳与水反应生成碳酸,溶液显酸性而使石蕊溶液变红。
通过演示实验复习二氧化碳的水溶液显酸性,从而确定检验溶液酸性可以选择石蕊溶液。
[过渡]
师:醋、酸果汁、稀盐酸等有酸味的溶液是否都能使紫色石蕊溶液变红?
引起学生思考,使学生带着疑问进行实验。
[分组实验1]
在白色点滴板的空穴中分别滴几滴白醋、酸果汁、稀盐酸,再分别滴2滴石蕊溶液,观察颜色变化。教师随时关注学生的实验操作并给予指导。
师:同学们观察到什么现象?我们可以归纳出什么样的结论?
生:这些溶液都能使石蕊溶液变红。
师:我们将能使石蕊溶液变红的溶液称为酸性溶液。
训练学生的操作能力,提高学生观察、分析和归纳的能力。
[演示实验2]
用两支试管分别取少量氨水、石灰水,各滴入2滴酚酞溶液
师:同学们观察到什么现象?
生:溶液变红。
师:酚酞溶液之所以变红是因为这两种溶液均显碱性。
培养学生的观察能力;由实验得出结论,这是科学研究常见的方法。
[分组实验2]
在白色点滴板的空穴中分别滴几滴纯碱溶液、肥皂水、氢氧化钠溶液,再分别滴2滴酚酞溶液
师:同学们观察到什么现象?我们又能得出什么样的结论?
生:纯碱溶液、肥皂水、氢氧化钠溶液都能使酚酞溶液变红。它们应该和氨水、石灰水具有一样的性质。
师:我们将能使酚酞溶液变红的溶液称为碱性溶液。
溶液碱性的检验先选用酚酞溶液,是因为在已有知识的支撑下,“温故而知新”更符合学生的认知规律。
[过渡]
师:往这些碱性溶液中滴入石蕊溶液,又可以观察到什么现象呢?
承上启下。
教学环节
师生活动
设计意图
[分组实验3]
在白色点滴板的空穴中分别滴几滴纯碱溶液、肥皂水、石灰水、氨水,再分别滴2滴石蕊溶液,另一个空穴中只滴石蕊溶液。
师:我们能观察到什么现象?从中能归纳出什么结论?
生:纯碱溶液、石灰水、肥皂水、氨水这些碱性溶液能使紫色石蕊溶液变蓝。
石蕊溶液遇碱性溶液变蓝,而紫色与蓝色比较接近,其中一个空穴只滴加石蕊溶液可以更好地比较颜色的变化。
[过渡]
师:是否所有的溶液都能使石蕊溶液和酚酞溶液改变颜色呢?
承上启下。
[分组实验4]
在白色点滴板的两个空穴中各滴几滴食盐水,再分别滴入石蕊溶液和酚酞溶液;另两个空穴中各滴几滴蔗糖溶液,再分别滴入石蕊溶液和酚酞溶液。
师:我们能观察到什么现象?生:食盐水和蔗糖溶液都不能使石蕊溶液和酚酞溶液改变颜色。说明这两种溶液不具有酸性和碱性。
师:我们将像食盐水、蔗糖溶液这样不具有酸性也不具有碱性的溶液称为中性溶液。
与溶液的酸碱性相呼应,有助于学生的理解。
[归纳总结]
师:像石蕊溶液和酚酞溶液这样在不同酸碱性溶液中呈现出不同的颜色,可用于检验溶液酸碱性的物质,我们将之称为酸碱指示剂。
师:为帮助同学们更好地记住指示剂在不同酸碱性溶液中的颜色变化,老师将这两种指示剂的颜色变化做以下归纳:石蕊紫色中性显,遇酸变红遇碱蓝;酚酞本来无颜色,碱液惹它则红脸。
用顺口溜的形式总结指示剂颜色的变化,生动形象,且很有针对性。
[拓展讲解]
师:为了使用方便,我们也常用蓝色石蕊试纸和红色石蕊试纸来检验溶液的酸碱性。
扩大学生的知识面。
[演示实验3]
取一张红色石蕊试纸放在表面皿中,用玻璃棒蘸取纯碱溶液滴在试纸上,另取一张蓝色石蕊试纸,用玻璃棒蘸取稀盐酸滴在试纸上。观察试纸的颜色变化。
师:从实验中我们可以发现碱性溶液能使红色石蕊试纸变蓝,而酸性溶液能使蓝色石蕊试纸变红。
做好演示实验为学生使用pH试纸打下基础。
[过渡]
师:我们知道有许多溶液显酸性或碱性,那么它们的酸碱性谁更强一些呢?
引入酸碱度的概念。
教学环节
师生活动
设计意图
[情景设置]
古时候有一个小和尚,他向师父抱怨他干的琐事很累,师父便拿出一些盐让他尝一下,他觉得又咸又涩,师父把他带到一个大湖边让他把那些盐放入湖水中,再尝一下湖水的味道,奇怪的是,苦涩味消失了。
师:醋是我们生活中常用的调味品,同样的道理,如果我们把它直接喝下去,大家都会觉得受不了,然而如果我们把这些醋滴入到一大杯水中,再尝水的味道我们会觉得酸味弱了很多。
设置情景吸引学生的注意力,同学生的生活经验相结合,为以下的实验设计做好准备。
[分组实验5]
(一)用两支试管各取1 mL的同种稀盐酸,向其中一支试管中加满蒸馏水,表面皿中放两张pH试纸,用玻璃棒(洗净擦干)分别蘸取两种盐酸滴到pH试纸上,变色后再与标准比色卡进行比较。
(二)另取两支试管各取1 mL同种纯碱溶液,按实验(一)进行操作。
学生展示实验结果。
师:变色后的试纸与标准比色卡上的哪一种颜色接近,我们就认定该溶液的pH是多少,用广泛pH试纸测定的pH都为整数值。
生:展示实验结果
盐酸:pH=1(未加水,酸性强)
pH=3(加水,酸性弱)
纯碱溶液:
pH=10(未加水,碱性强 )
pH=8(加水,碱性弱)
用实验事实说明pH大小与溶液酸碱性之间的关系。
[分组实验6]
再用pH试纸检验食盐水、蔗糖溶液的pH。
学生展示实验结果
生:食盐水pH=7
蔗糖溶液pH=7
师:很显然中性溶液的pH都为7。
培养学生的实验能力和归纳总结的能力。
[问题设置]
师:pH试纸使用前能否用水润湿?玻璃棒洗净后为什么要擦干?
生:润湿pH试纸和玻璃棒上的水都会对溶液进行稀释,影响实验的结果。
强化实验过程中的注意事项。
[总结归纳]
师:pH的范围在0~14之间,pH=7,溶液呈中性;pH<7,溶液呈酸性;pH>7溶液呈碱性。pH越小,酸性越强,pH越大,碱性越强。
引导学生进一步概括和综合实验的结果。
[布置作业]
师:请同学们尽可能多地收集各种颜色的花,自制酸碱指示剂,并用它们来检验溶液的酸碱性。
知识拓展,进一步增强学生学习化学的兴趣。
