北京课改版九下化学 11.1对酸和碱的初步认识 课件(23张ppt)
文档属性
| 名称 | 北京课改版九下化学 11.1对酸和碱的初步认识 课件(23张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-14 00:00:00 | ||
图片预览







文档简介
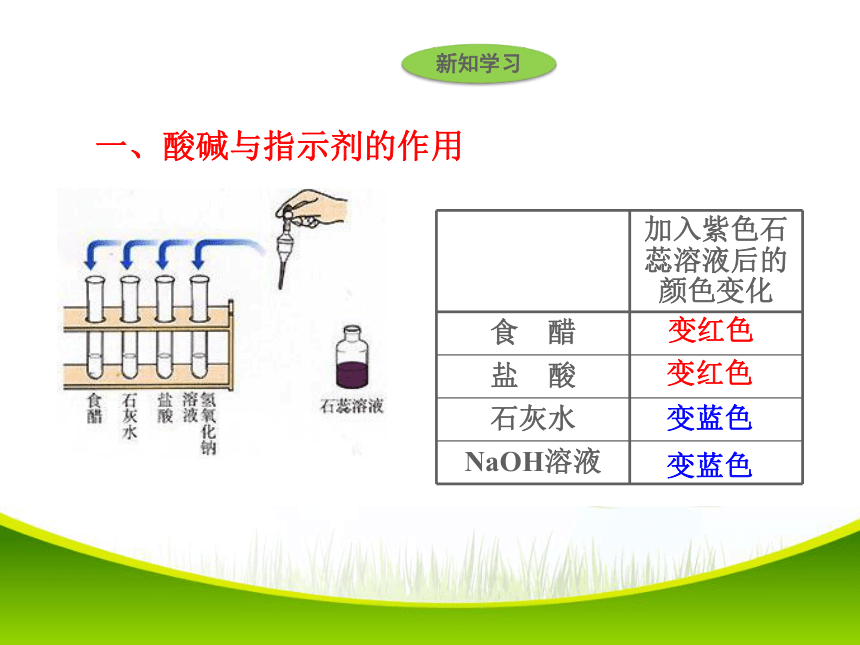
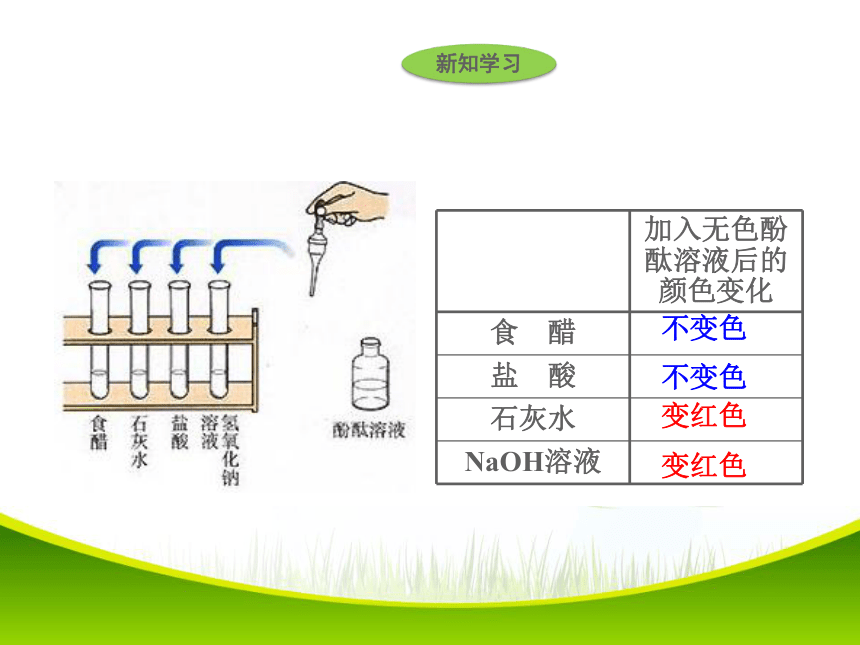
课件23张PPT。酸和碱的初步认识 二氧化碳与水反应生成的碳酸能使紫色石蕊溶液变色;氨水能使酚酞溶液变色,还有哪些物质能使紫色石蕊溶液、酚酞溶液变色呢?新知学习变蓝色变红色变蓝色变红色一、酸碱与指示剂的作用新知学习变红色不变色变红色不变色新知学习酸碱指示剂
1.酸碱指示剂(简称:指示剂)能跟酸或碱的溶液起作用而显示不同的颜色。
2.常见的有:紫色石蕊溶液、无色酚酞溶液
3.变色规律:
紫色石蕊溶液:遇酸溶液变红色,遇碱溶液变蓝色
无色酚酞溶液:遇酸不变色,遇碱溶液变红色新知学习 几种常见的酸新知学习浓盐酸和浓硫酸新知学习 观察浓硫酸和浓盐酸的颜色和状态;比较它们与同体积水的质量大小;打开瓶塞,观察发生的现象;闻一闻是否有气味?1.浓硫酸和浓盐酸二、常见的酸新知学习认识浓硫酸和浓盐酸无色白雾1.84g/mL油状无味刺激性气味无明显现象1.19g/mL36%-38%98%无色液体H2SO4HCl新知学习新知学习浓硫酸有很强的吸水性,溶于水放出大量的热量。可以利用浓硫酸的吸水性将其作为干燥剂。浓硫酸具有很强的腐蚀性,浓硫酸滴到纸张、蔗糖上,会使纸张、蔗糖炭化。稀硫酸滴到纸张上,在水分挥发的过程中使纸张逐渐炭化。浓硫酸还会腐蚀衣物和皮肤。新知学习 浓硫酸的特性之腐蚀性浓硫酸能夺取含碳、氢、氧等元素组成的化合物里的水分( 氢、氧元素 ), 生成黑色的炭和水。新知学习 你知道稀释浓硫酸时为什么不能将水倒进浓硫酸里而是要将浓硫酸沿着容器壁慢慢注入水中,而且还要不断搅拌吗?思考:怎样稀释浓硫酸?新知学习 注意:
1.正确稀释浓硫酸;
2.浓硫酸溅到皮肤或衣物上的处理:立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液。新知学习石蕊:变红色 ;酚酞:不变色除铜外,有气泡产生,反应速率:镁>锌>铁铁锈溶解,溶液变黄
氧化铜溶解,溶液变蓝 实验探究新知学习(1)酸与指示剂的作用
酸溶液能使紫色石蕊试液变红色;无色酚酞试液不变色 2.酸的通性(2)酸与某些金属的反应 金属 + 酸 → 盐 + 氢气如:Zn + 2HCl === ZnCl2 + H2↑
Zn + H2SO4 === ZnSO4 + H2↑
Mg + H2SO4 === MgSO4 + H2↑
Fe + H2SO4 === FeSO4 + H2↑
Fe + 2HCl === FeCl2 + H2↑新知学习 金属氧化物 + 酸 → 盐 + 水Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O
Fe2O3 + 6HCl === 2FeCl3 + 3H2O
CuO + H2SO4 === CuSO4 + H2O(3)酸与金属氧化物的反应新知学习酸在水溶液中都能电离出氢离子(H+),即不同的酸溶液中都含有氢离子(H+),所以它们具有相似的化学性质。想一想 酸为什么具有相似的化学性质? 活动天地新知学习小结:一.常见的酸
1.几种常见的酸
2.浓硫酸的腐蚀性
稀释浓硫酸时:一定要注酸入水切莫引水入酸
二.酸的化学性质
1.酸能跟指示剂反应
2.酸跟金属的反应
3.酸跟金属氧化物的反应 【典例1】下列物质中能使紫色的石蕊试液变红的是( )
A.食盐 B.石灰水
C.氢氧化钠溶液 D.稀盐酸
知识点一、酸、碱与指示剂作用D经典例题【典例2】下列物质质量置于空气中,一段时间后,质量减小的是( )
A.碳酸钙 B.氯化钠
C.浓盐酸 D.氢氧化钠
知识点二、常见的酸C经典例题知能训练1.下列物质中,能使无色酚酞试液变红的是( )
A.稀盐酸 B.澄清石灰水 C.稀硫酸 D.食盐水
2.酸具有酸的通性的原因是( )
A.酸都能电离出H+
B.酸都含有酸根
C.酸中都含有氢元素
D.酸中都含有氧元素
BA3.下列物质长时间暴露在空气中,会变质的是( )
A.CaCO3 B.浓盐酸 C.浓硫酸 D.烧碱
4.人体内的一些液体和排泄物的正常pH范围如下表所示:
其中酸性最强的是( )
A.胃液 B.血浆 C.乳汁 D.尿液AD知能训练
3.变色规律:
紫色石蕊溶液:遇酸溶液变红色,遇碱溶液变蓝色
无色酚酞溶液:遇酸不变色,遇碱溶液变红色新知学习 几种常见的酸新知学习浓盐酸和浓硫酸新知学习 观察浓硫酸和浓盐酸的颜色和状态;比较它们与同体积水的质量大小;打开瓶塞,观察发生的现象;闻一闻是否有气味?1.浓硫酸和浓盐酸二、常见的酸新知学习认识浓硫酸和浓盐酸无色白雾1.84g/mL油状无味刺激性气味无明显现象1.19g/mL36%-38%98%无色液体H2SO4HCl新知学习新知学习浓硫酸有很强的吸水性,溶于水放出大量的热量。可以利用浓硫酸的吸水性将其作为干燥剂。浓硫酸具有很强的腐蚀性,浓硫酸滴到纸张、蔗糖上,会使纸张、蔗糖炭化。稀硫酸滴到纸张上,在水分挥发的过程中使纸张逐渐炭化。浓硫酸还会腐蚀衣物和皮肤。新知学习 浓硫酸的特性之腐蚀性浓硫酸能夺取含碳、氢、氧等元素组成的化合物里的水分( 氢、氧元素 ), 生成黑色的炭和水。新知学习 你知道稀释浓硫酸时为什么不能将水倒进浓硫酸里而是要将浓硫酸沿着容器壁慢慢注入水中,而且还要不断搅拌吗?思考:怎样稀释浓硫酸?新知学习 注意:
1.正确稀释浓硫酸;
2.浓硫酸溅到皮肤或衣物上的处理:立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液。新知学习石蕊:变红色 ;酚酞:不变色除铜外,有气泡产生,反应速率:镁>锌>铁铁锈溶解,溶液变黄
氧化铜溶解,溶液变蓝 实验探究新知学习(1)酸与指示剂的作用
酸溶液能使紫色石蕊试液变红色;无色酚酞试液不变色 2.酸的通性(2)酸与某些金属的反应 金属 + 酸 → 盐 + 氢气如:Zn + 2HCl === ZnCl2 + H2↑
Zn + H2SO4 === ZnSO4 + H2↑
Mg + H2SO4 === MgSO4 + H2↑
Fe + H2SO4 === FeSO4 + H2↑
Fe + 2HCl === FeCl2 + H2↑新知学习 金属氧化物 + 酸 → 盐 + 水Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O
Fe2O3 + 6HCl === 2FeCl3 + 3H2O
CuO + H2SO4 === CuSO4 + H2O(3)酸与金属氧化物的反应新知学习酸在水溶液中都能电离出氢离子(H+),即不同的酸溶液中都含有氢离子(H+),所以它们具有相似的化学性质。想一想 酸为什么具有相似的化学性质? 活动天地新知学习小结:一.常见的酸
1.几种常见的酸
2.浓硫酸的腐蚀性
稀释浓硫酸时:一定要注酸入水切莫引水入酸
二.酸的化学性质
1.酸能跟指示剂反应
2.酸跟金属的反应
3.酸跟金属氧化物的反应 【典例1】下列物质中能使紫色的石蕊试液变红的是( )
A.食盐 B.石灰水
C.氢氧化钠溶液 D.稀盐酸
知识点一、酸、碱与指示剂作用D经典例题【典例2】下列物质质量置于空气中,一段时间后,质量减小的是( )
A.碳酸钙 B.氯化钠
C.浓盐酸 D.氢氧化钠
知识点二、常见的酸C经典例题知能训练1.下列物质中,能使无色酚酞试液变红的是( )
A.稀盐酸 B.澄清石灰水 C.稀硫酸 D.食盐水
2.酸具有酸的通性的原因是( )
A.酸都能电离出H+
B.酸都含有酸根
C.酸中都含有氢元素
D.酸中都含有氧元素
BA3.下列物质长时间暴露在空气中,会变质的是( )
A.CaCO3 B.浓盐酸 C.浓硫酸 D.烧碱
4.人体内的一些液体和排泄物的正常pH范围如下表所示:
其中酸性最强的是( )
A.胃液 B.血浆 C.乳汁 D.尿液AD知能训练
