人教版高中化学选修五1.2有机化合物的结构特点(共48张PPT)
文档属性
| 名称 | 人教版高中化学选修五1.2有机化合物的结构特点(共48张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-20 00:00:00 | ||
图片预览










文档简介
课件48张PPT。 第二节 有机化合物的结构特点有机化合物的特点之一就是:仅由氧和氢构成的化合物只有两种:H2O和H2O2仅由碳和氢构成的化合物超过了几百万种!——由碳元素所形成的化合物种类非常多!也就是有机化合物的种类非常多!为什么有机化合物的种类如此繁多呢?种类繁多——3000万多种!一、有机物中C的成键特点形成4个共价键
可以形成单键、双键、三键
可以结合成碳链、碳环
同分异构现象1、可以形成4个化学键 碳原子最外层有4个电子,不易失去或
获得电子而形成阳离子或阴离子。碳原子通过共价键(共用电子对)与
其他原子(H、O、N、P、S、Cl等)形
成共价化合物。例如:甲烷分子(CH4)归纳甲烷分子的结构特点: 碳与氢形成四个共价键,以C原子为中心,
四个氢位于四个顶点的正四面体立体结构。
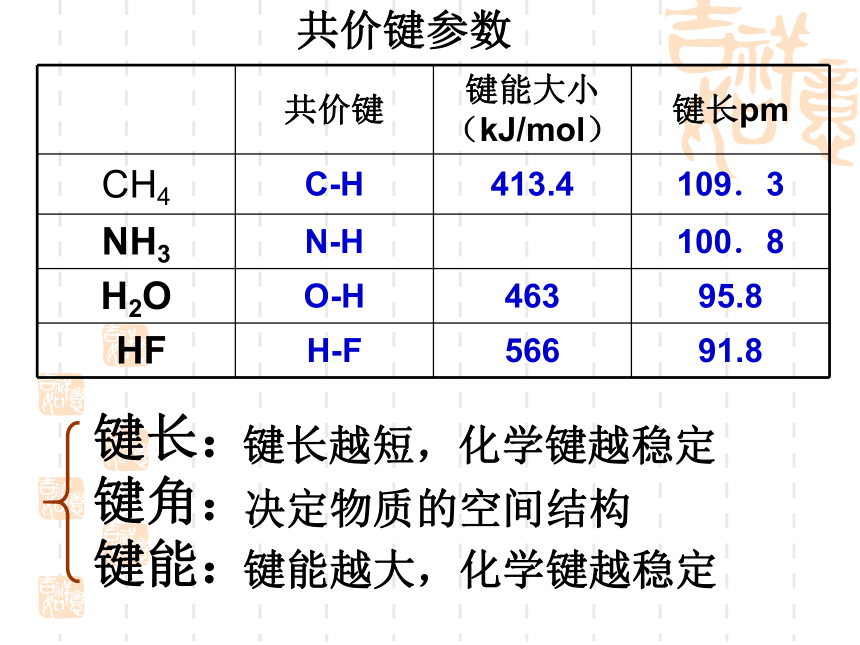
所以4个键的键长是相等的,4个键的键角是相等的,4个H原子是等同的。共价键参数键长:
键角:
键能:键长越短,化学键越稳定决定物质的空间结构键能越大,化学键越稳定2、碳原子间的结合方式 碳原子不仅能与H或其他原子形成4个共价键,
碳原子之间也能相互以共价键结合。(1)碳原子之间可以形成稳定的单键、双键、叁键;(2)多个碳原子可以相互结合成长短不一的碳链,
碳链可带有支链;(3)多个碳原子还可以相互结合成环,碳环和碳链
还可以相互结合。轨道杂化理论: 成键过程中,由于原子间的相互影响,
同一原子中几个能量相近的不同类型的原
子轨道,可以线性组合,重新分配能量和
确定空间,组成数目相等的新的原子轨道C的杂化方式(1)烷烃中C均为sp3杂化,每个C有4个相同化学键,故烷烃中的C成键均为四面体结构。例如:甲烷
(2)烯烃中形成双键的C为sp2杂化,这些C中有3个杂化轨道,一个未杂化轨道。未杂化轨道与其中一个杂化轨道形成双键,故烯烃中参与形成双键的C成键为平面结构。例如:乙烯
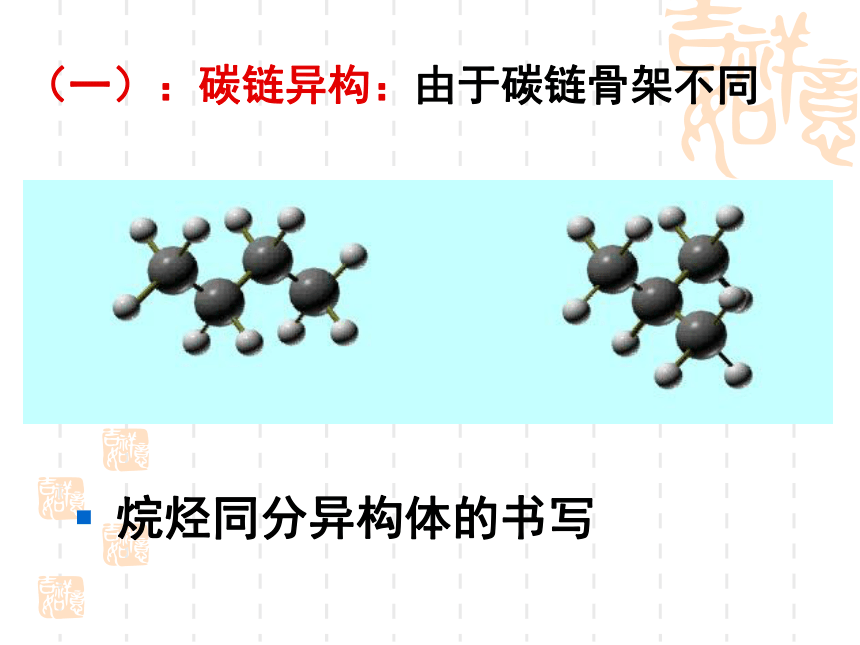
(3)炔烃中形成叁键的C为sp杂化,这些C中有2个杂化轨道和2个未杂化轨道。2个未杂化轨道与其中一个杂化轨道形成叁键,故炔烃中参与形成叁键的C成键为直线型。例如:乙炔三个相同:分子组成元素相同、相对分子质量相同、分子式相同两个不同:结构不同、性质不同注意 同分异构现象:化合物具有相同的分子式,但具有不同结构式的现象 具有同分异构现象的化合物互为同分异构体。二、有机物的同分异构现象 碳原子数目越多,同分异构体越多下面是烷烃的同分异构体的数目随C原子数变化有机物分子普遍存在同分异构现象(这是有机物种类繁多的主要原因)(一):碳链异构:由于碳链骨架不同烷烃同分异构体的书写写出分子式为C6H14 、C7H16的烷烃的同分异构体同分异构体的书写口诀:主链由长到短;支链由整到散;位置由心到边;排布由对、邻、间、最后用氢原子补足碳原子的四个价键。 (二)团位置异构:官能团位置不同有机物的同分异构除了碳链异构,
还有其它类型的异构吗?思考:1.写出分子式为C5H10的烯烃的
同分异构体2.写出丁醇同分异构体方法:
写出碳链异构的种数,再移动官能团!思考:
分子式为C3H6的有同分异构体吗?如果有,你写出它可能的同分异构体吗?C—C—CC=C—CCH2=CH—CH3烃类的互变异构通式 互变物质的种类
CnH2n 烯、环烷烃
CnH2n-2炔、二烯、环烯烃的含氧衍生物的互变异构通式 互变物质的种类
CnH2n+2O 醇、醚
CnH2nO 醛、酮
CnH2nO2 羧酸、酯具有不同的官能团(三)官能团异构烃的含氮、氧衍生物的互变异构 通式 互变物质的种类
CnH2n+1NO2 氨基酸、硝基化合物
例:C3H7NO2 CH3CHCOOH
NH2
CH3CH2CH2NO2
?
常见的官能团︿类别﹀异构现象碳链异构:由于碳链骨架不同
位置异构:官能团位置不同
官能团异构:具有不同官能团
有机物的同分异构现象 【判断】下列异构属于何种异构?
1CH3COOH和 HCOOCH3
2CH3–CH2–CHO和 CH3 –CO–CH3
3 CH3 -CH-CH3和 CH3-CH2-CH2-CH3
? ∣
CH3
4CH3–CH=CH–CH2–CH3
和 CH3–CH2–CH2- CH=CH2
官能团异构官能团异构碳链异构位置异构注 意:烷烃只存在碳链异构 烷烃同分异构体的书写讨论:(1)书写C7H16 的同分异构体
(2)书写C4H8的异构体
(3)书写C4H10O的异构体(1)减碳法 (适用于烷烃)
同分异构体的书写口诀:
主链由长到短;支链由整到散;
位置由心到边;排布对临间。
(2)插入法(适用于烯烃、炔烃、酯等)
先根据给定的碳原子数写出烷烃的同分异构体的碳链骨架,再将官能团插入碳链中。
如书写分子式为C4H8的烯烃的同分异构体(插入双键),双键可分别在①、②、③号位置: (3)取代法(适用于醇、卤代烃异构)
先碳链异构,后位置异构。如书写分子式为
C5H12O的醇的同分异构体。如图(图中数字即
为—OH接入后的位置,即这样的醇合计为8种):【观察1】分子式为C6H14的烷烃在结构式中含有3个甲基的同分异构体有( )个
(A)2个 (B)3个 (C)4个 (D)5个
【练习2】写出分子式为C5H10的同分异构体。 ①按直链烯烃的位置异构书写 ②按碳链异构书写 ③按官能团异构书写
√3.下列各组物质中,哪些属于同分异构体,是同分异构体的属于何种异构?
① H2N—CH2—COOH 和 H3C-CH2—NO2
② CH3COOH和 HCOOCH3
③ CH3CH2CHO和 CH3COCH3
④ CH3CH2CH2OH 和 CH3CH2OCH3
4、下列各组化合物中具有相同分子式
的是( )
①甲醚和乙醇 ②甲酸乙酯和丙酸
③甲酸和甲醛 ④甲苯和苯酚【随堂练习】
5. 碳原子最外层含有____个电子,一个碳原子可以跟
其他非金属原子形成____个 ____键,碳原子之间也
能以共价键相结合,形成____键____ 键或 ____键 。
6. 如果甲烷分子中的四个氢原子被四个 -CH3取代,
生成物的分子式是_______五个碳原子是否在同一平面?
如果生成物中的一个氢被氯原子取代,
写出它的结构简式______________。
确定一卤代物同分异构方法--等效氢法
1、同一碳原子上的氢等效。
2、同一碳原子上所连甲基上的氢原子等效
3、处于镜面对称的氢原子等效。
4、 处于对称轴两端的氢原子或碳原子是等效的。123[思考]2.已知蒽的二氯代物有15种同分异构体,则蒽的八氯代物有( )
A、12种 B、13种 C、14种 D、15种
蒽可写成C14H10, C14H10中的2个H被2个Cl取代与C14Cl10中2个Cl被2个H取代的产物的种数应相同,后者即是蒽的八氯代物,故选D。确定多卤代物同分异构体的数目—换元法
D已知C6H4Cl2 有三种异构体,则C6H2Cl4
有_____异构体。(将H代替Cl)三种确定同分异构体的数目--基元法
如丁基有4种同分异构体,则丁醇有4种同分异构体。
烃基:
烃分子失去一个或几个H所剩余的部分叫烃基。
一般用-R表示,如:-CH3(甲基),-CH2CH3(乙基)。 定一移二法
对于二元取代物的同分异构体的判定,
可固定一个取代基位置,再移动另一个取代基,
以确定同分异构体的数目。----苯的同系物在书写同分异构体时,先考虑哪种异构类型?官能团异构碳链异构位置异构例:写出化学式C3H8O的所有可能物质的
结构简式醇:醚:C—C—CC—C—C—OHC—C—CC—C—CC—O—C—C重点例1.(2006,全国理综Ⅱ)主链含5个碳原子,有甲基、乙基2个支链的烷烃有( )
A.2种 B.3种 C.4种 D.5种A例2、某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是( )
A.C3H8 B.C4H10 C.C5H12 D.C6H14例3、(CH3CH2)2CHCH2CH(CH3)2的一氯代物的有 种。C6链接高考同时属于酯类和酚类的同分异构体分别是: 水杨酸的结构简式为
(1)水杨酸的同分异构体中,属于酚类同时还属于酯类的化合物有 种。
(2)水杨酸的同分异构体中,属于酚类,但不属于酯类也不属于羧酸的化合物必定含有 (填写官能团名称)。3醛基例4、例6、联三苯的结构是 ,其一氯代物(C8H13Cl)有 种。 例5.菲的结构简式 ,从菲的结构简式 分析,菲的一氯取代产物共有( )
A.4种 B.5种 C.10种 D.14种B4 “立方烷”是新合成的一种烃,其分子呈立方体结构。如图所示:(1)“立方烷”的分子式为 ________
(2)其一氯代物共有______种
(3)其二氯代物共有______种
Cl123C8H813例7:例8、C11H16 的苯的同系物中, 只含有一个支链, 且支链上含有两个“—CH3”的结构有四种, 写出其结构简式. 同分异构体——分子式相同,而分子结构不同的化合物互称同分异构体。 同系物——结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称同系物。 同素异形体——同种元素的不同单质互称同素异形体。 同位素——质子数相同而中子数不同的同种元素的原子互称同位素。四同:同系物注意事项: 一差(分子组成差一个或若干个CH2);二同(同通式,同结构);三注意:
①必为同一类物质②结构相似(有相似的原子连接方式或相同 的官能团种类和数目)③同系物间物理性质不同,化学性质相似,因此,具有相同通式的有机物除烷烃外都不能确定是不是同系物。如乙醇与丙醇为同系物,但丙烯与环丙烷
就不属同系物了。 练习:
下列各组物质的相互关系正确的是( )A、同位素:1H 、2H、3H B、同素异形体:C60、C70、金刚石C、同系物:C2H4、C3H6、C4H8D、同分异构体:B三、常用化学用语
——有机物结构和组成的几种图示比较⑴化学式:用元素符号表示物质分子组成的式子,可反映出一 个分子中原子的种类和数目。⑵最简式(实验式):表示物质组成的各元素原子最简整数
比的式子。⑶电子式:用小黑点等记号代表电子,表示原子最外层电子成
键情况的式子。⑷结构式:表示分子中原子的结合或排列顺序的式子,能反映
物质的结构,但不表示物质的空间构型。⑸结构简式:结构式的简便写法,省去结构式中代表碳氢单 键,碳碳单键等键的短线,着重突出结构特点(官能团)。⑺球棍模型:小球表示原子,短棍表示价键,表示分子的空间
结构。⑻ 比例模型:用不同体积的小球表示不同的原子大小,,用于
表示分子中各原子的相对大小和结合顺序。⑹键线式:进一步省去碳氢符号,剩下有机物分子中键的连接
情况,每个拐点和终点均表示连接一个碳原子。苯的构造式 电子式结构式键线式结构简式2-甲基丙醇的表示方法: 电子式书写麻烦结构式较麻烦结构简式较为常用键线式较为常用书写结构简式的注意点1、表示原子间形成单键的‘——’可以省略2、C=C C≡C中的双键和三键不能省略,
但是醛基羧基的碳氧双键可以简写为
—CHO, —COOH。3、准确表示分子中原子成键的情况如乙醇的结构简式:
CH3CH2OH,HO—CH2CH31.键线式:结构简式:骨架式:练习请写出:深海鱼油分子中有______个碳原子_____个氢原子____个氧原子,分子式为________22322C22H32O22.
可以形成单键、双键、三键
可以结合成碳链、碳环
同分异构现象1、可以形成4个化学键 碳原子最外层有4个电子,不易失去或
获得电子而形成阳离子或阴离子。碳原子通过共价键(共用电子对)与
其他原子(H、O、N、P、S、Cl等)形
成共价化合物。例如:甲烷分子(CH4)归纳甲烷分子的结构特点: 碳与氢形成四个共价键,以C原子为中心,
四个氢位于四个顶点的正四面体立体结构。
所以4个键的键长是相等的,4个键的键角是相等的,4个H原子是等同的。共价键参数键长:
键角:
键能:键长越短,化学键越稳定决定物质的空间结构键能越大,化学键越稳定2、碳原子间的结合方式 碳原子不仅能与H或其他原子形成4个共价键,
碳原子之间也能相互以共价键结合。(1)碳原子之间可以形成稳定的单键、双键、叁键;(2)多个碳原子可以相互结合成长短不一的碳链,
碳链可带有支链;(3)多个碳原子还可以相互结合成环,碳环和碳链
还可以相互结合。轨道杂化理论: 成键过程中,由于原子间的相互影响,
同一原子中几个能量相近的不同类型的原
子轨道,可以线性组合,重新分配能量和
确定空间,组成数目相等的新的原子轨道C的杂化方式(1)烷烃中C均为sp3杂化,每个C有4个相同化学键,故烷烃中的C成键均为四面体结构。例如:甲烷
(2)烯烃中形成双键的C为sp2杂化,这些C中有3个杂化轨道,一个未杂化轨道。未杂化轨道与其中一个杂化轨道形成双键,故烯烃中参与形成双键的C成键为平面结构。例如:乙烯
(3)炔烃中形成叁键的C为sp杂化,这些C中有2个杂化轨道和2个未杂化轨道。2个未杂化轨道与其中一个杂化轨道形成叁键,故炔烃中参与形成叁键的C成键为直线型。例如:乙炔三个相同:分子组成元素相同、相对分子质量相同、分子式相同两个不同:结构不同、性质不同注意 同分异构现象:化合物具有相同的分子式,但具有不同结构式的现象 具有同分异构现象的化合物互为同分异构体。二、有机物的同分异构现象 碳原子数目越多,同分异构体越多下面是烷烃的同分异构体的数目随C原子数变化有机物分子普遍存在同分异构现象(这是有机物种类繁多的主要原因)(一):碳链异构:由于碳链骨架不同烷烃同分异构体的书写写出分子式为C6H14 、C7H16的烷烃的同分异构体同分异构体的书写口诀:主链由长到短;支链由整到散;位置由心到边;排布由对、邻、间、最后用氢原子补足碳原子的四个价键。 (二)团位置异构:官能团位置不同有机物的同分异构除了碳链异构,
还有其它类型的异构吗?思考:1.写出分子式为C5H10的烯烃的
同分异构体2.写出丁醇同分异构体方法:
写出碳链异构的种数,再移动官能团!思考:
分子式为C3H6的有同分异构体吗?如果有,你写出它可能的同分异构体吗?C—C—CC=C—CCH2=CH—CH3烃类的互变异构通式 互变物质的种类
CnH2n 烯、环烷烃
CnH2n-2炔、二烯、环烯烃的含氧衍生物的互变异构通式 互变物质的种类
CnH2n+2O 醇、醚
CnH2nO 醛、酮
CnH2nO2 羧酸、酯具有不同的官能团(三)官能团异构烃的含氮、氧衍生物的互变异构 通式 互变物质的种类
CnH2n+1NO2 氨基酸、硝基化合物
例:C3H7NO2 CH3CHCOOH
NH2
CH3CH2CH2NO2
?
常见的官能团︿类别﹀异构现象碳链异构:由于碳链骨架不同
位置异构:官能团位置不同
官能团异构:具有不同官能团
有机物的同分异构现象 【判断】下列异构属于何种异构?
1CH3COOH和 HCOOCH3
2CH3–CH2–CHO和 CH3 –CO–CH3
3 CH3 -CH-CH3和 CH3-CH2-CH2-CH3
? ∣
CH3
4CH3–CH=CH–CH2–CH3
和 CH3–CH2–CH2- CH=CH2
官能团异构官能团异构碳链异构位置异构注 意:烷烃只存在碳链异构 烷烃同分异构体的书写讨论:(1)书写C7H16 的同分异构体
(2)书写C4H8的异构体
(3)书写C4H10O的异构体(1)减碳法 (适用于烷烃)
同分异构体的书写口诀:
主链由长到短;支链由整到散;
位置由心到边;排布对临间。
(2)插入法(适用于烯烃、炔烃、酯等)
先根据给定的碳原子数写出烷烃的同分异构体的碳链骨架,再将官能团插入碳链中。
如书写分子式为C4H8的烯烃的同分异构体(插入双键),双键可分别在①、②、③号位置: (3)取代法(适用于醇、卤代烃异构)
先碳链异构,后位置异构。如书写分子式为
C5H12O的醇的同分异构体。如图(图中数字即
为—OH接入后的位置,即这样的醇合计为8种):【观察1】分子式为C6H14的烷烃在结构式中含有3个甲基的同分异构体有( )个
(A)2个 (B)3个 (C)4个 (D)5个
【练习2】写出分子式为C5H10的同分异构体。 ①按直链烯烃的位置异构书写 ②按碳链异构书写 ③按官能团异构书写
√3.下列各组物质中,哪些属于同分异构体,是同分异构体的属于何种异构?
① H2N—CH2—COOH 和 H3C-CH2—NO2
② CH3COOH和 HCOOCH3
③ CH3CH2CHO和 CH3COCH3
④ CH3CH2CH2OH 和 CH3CH2OCH3
4、下列各组化合物中具有相同分子式
的是( )
①甲醚和乙醇 ②甲酸乙酯和丙酸
③甲酸和甲醛 ④甲苯和苯酚【随堂练习】
5. 碳原子最外层含有____个电子,一个碳原子可以跟
其他非金属原子形成____个 ____键,碳原子之间也
能以共价键相结合,形成____键____ 键或 ____键 。
6. 如果甲烷分子中的四个氢原子被四个 -CH3取代,
生成物的分子式是_______五个碳原子是否在同一平面?
如果生成物中的一个氢被氯原子取代,
写出它的结构简式______________。
确定一卤代物同分异构方法--等效氢法
1、同一碳原子上的氢等效。
2、同一碳原子上所连甲基上的氢原子等效
3、处于镜面对称的氢原子等效。
4、 处于对称轴两端的氢原子或碳原子是等效的。123[思考]2.已知蒽的二氯代物有15种同分异构体,则蒽的八氯代物有( )
A、12种 B、13种 C、14种 D、15种
蒽可写成C14H10, C14H10中的2个H被2个Cl取代与C14Cl10中2个Cl被2个H取代的产物的种数应相同,后者即是蒽的八氯代物,故选D。确定多卤代物同分异构体的数目—换元法
D已知C6H4Cl2 有三种异构体,则C6H2Cl4
有_____异构体。(将H代替Cl)三种确定同分异构体的数目--基元法
如丁基有4种同分异构体,则丁醇有4种同分异构体。
烃基:
烃分子失去一个或几个H所剩余的部分叫烃基。
一般用-R表示,如:-CH3(甲基),-CH2CH3(乙基)。 定一移二法
对于二元取代物的同分异构体的判定,
可固定一个取代基位置,再移动另一个取代基,
以确定同分异构体的数目。----苯的同系物在书写同分异构体时,先考虑哪种异构类型?官能团异构碳链异构位置异构例:写出化学式C3H8O的所有可能物质的
结构简式醇:醚:C—C—CC—C—C—OHC—C—CC—C—CC—O—C—C重点例1.(2006,全国理综Ⅱ)主链含5个碳原子,有甲基、乙基2个支链的烷烃有( )
A.2种 B.3种 C.4种 D.5种A例2、某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是( )
A.C3H8 B.C4H10 C.C5H12 D.C6H14例3、(CH3CH2)2CHCH2CH(CH3)2的一氯代物的有 种。C6链接高考同时属于酯类和酚类的同分异构体分别是: 水杨酸的结构简式为
(1)水杨酸的同分异构体中,属于酚类同时还属于酯类的化合物有 种。
(2)水杨酸的同分异构体中,属于酚类,但不属于酯类也不属于羧酸的化合物必定含有 (填写官能团名称)。3醛基例4、例6、联三苯的结构是 ,其一氯代物(C8H13Cl)有 种。 例5.菲的结构简式 ,从菲的结构简式 分析,菲的一氯取代产物共有( )
A.4种 B.5种 C.10种 D.14种B4 “立方烷”是新合成的一种烃,其分子呈立方体结构。如图所示:(1)“立方烷”的分子式为 ________
(2)其一氯代物共有______种
(3)其二氯代物共有______种
Cl123C8H813例7:例8、C11H16 的苯的同系物中, 只含有一个支链, 且支链上含有两个“—CH3”的结构有四种, 写出其结构简式. 同分异构体——分子式相同,而分子结构不同的化合物互称同分异构体。 同系物——结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称同系物。 同素异形体——同种元素的不同单质互称同素异形体。 同位素——质子数相同而中子数不同的同种元素的原子互称同位素。四同:同系物注意事项: 一差(分子组成差一个或若干个CH2);二同(同通式,同结构);三注意:
①必为同一类物质②结构相似(有相似的原子连接方式或相同 的官能团种类和数目)③同系物间物理性质不同,化学性质相似,因此,具有相同通式的有机物除烷烃外都不能确定是不是同系物。如乙醇与丙醇为同系物,但丙烯与环丙烷
就不属同系物了。 练习:
下列各组物质的相互关系正确的是( )A、同位素:1H 、2H、3H B、同素异形体:C60、C70、金刚石C、同系物:C2H4、C3H6、C4H8D、同分异构体:B三、常用化学用语
——有机物结构和组成的几种图示比较⑴化学式:用元素符号表示物质分子组成的式子,可反映出一 个分子中原子的种类和数目。⑵最简式(实验式):表示物质组成的各元素原子最简整数
比的式子。⑶电子式:用小黑点等记号代表电子,表示原子最外层电子成
键情况的式子。⑷结构式:表示分子中原子的结合或排列顺序的式子,能反映
物质的结构,但不表示物质的空间构型。⑸结构简式:结构式的简便写法,省去结构式中代表碳氢单 键,碳碳单键等键的短线,着重突出结构特点(官能团)。⑺球棍模型:小球表示原子,短棍表示价键,表示分子的空间
结构。⑻ 比例模型:用不同体积的小球表示不同的原子大小,,用于
表示分子中各原子的相对大小和结合顺序。⑹键线式:进一步省去碳氢符号,剩下有机物分子中键的连接
情况,每个拐点和终点均表示连接一个碳原子。苯的构造式 电子式结构式键线式结构简式2-甲基丙醇的表示方法: 电子式书写麻烦结构式较麻烦结构简式较为常用键线式较为常用书写结构简式的注意点1、表示原子间形成单键的‘——’可以省略2、C=C C≡C中的双键和三键不能省略,
但是醛基羧基的碳氧双键可以简写为
—CHO, —COOH。3、准确表示分子中原子成键的情况如乙醇的结构简式:
CH3CH2OH,HO—CH2CH31.键线式:结构简式:骨架式:练习请写出:深海鱼油分子中有______个碳原子_____个氢原子____个氧原子,分子式为________22322C22H32O22.
