苏教版高中选修实验化学专题1物质的分类与提纯课题1海带中碘元素的分离及检验 (共24张PPT)
文档属性
| 名称 | 苏教版高中选修实验化学专题1物质的分类与提纯课题1海带中碘元素的分离及检验 (共24张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-21 00:00:00 | ||
图片预览








文档简介
课件24张PPT。《实验化学》甲亢碘酒淀粉碘化钾试纸人工降雨吸附富集碘如何检验及提取海带中的碘元素?课题一 海带中碘元素的分离及检验专题1 物质的分离与提纯海带的主要成分:蛋白质、糖类、脂肪、纤维素、褐藻胶、甘露醇、维生素、有机碘化物等有机物。
海带的次要成分:氯化钠、碳酸钠、硫酸钠、碘化钠等无机盐。
探究:
1.如何将海带中的有机态碘转化成无机态碘?
2.设计检验海带中含碘元素的实验方案。
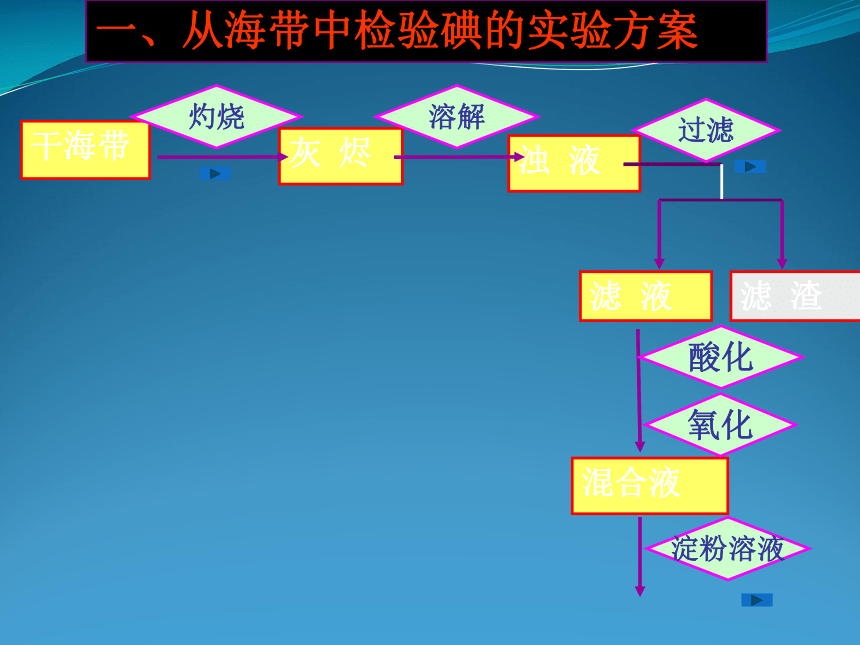
(提示:有机态的碘转化为无机态的碘时主要以 I- 的形式存在)干海带灰 烬?
浊 液滤 液
混合液灼烧滤 渣一、从海带中检验碘的实验方案溶解过滤酸化氧化淀粉溶液实验注意事项:应在通风处加热灼烧,或使用通风设备去除白烟和难闻的气味。应边加热边搅拌,用坩埚钳夹持坩埚,玻璃棒小心搅拌,使海带均匀受热,加快灰化的速度。
至干海带逐渐变的更干燥、卷曲,最后变成黑色粉末或细小颗粒。灼烧完毕,应将坩埚和玻璃棒放在石棉网上冷却,不可直接放在冷的实验台上,防止温度很高的坩埚骤冷而破裂 溶解过滤①操作要点:
取一药匙海带灰置于小烧杯中,加入约15ml蒸馏水,煮沸,过滤。②实验注意事项:
应隔着石棉网加热小烧杯中的混合物。
加热过程中应不断搅拌,加快溶解,同时防止液 体受热不均而溅出。
过滤操作应注意“一贴、二低、三靠” 。 4、酸化作用是什么?海带灰的浸出液中含有碳酸钠(碳酸钾)等使溶液显碱性的物质,酸化的目的是使溶液呈弱酸性,有利于氧化剂把I-氧化为I2。5、常用的氧化剂是什么?氯水、氧气、臭氧、高锰酸钾、双氧水、浓硫酸等。干海带灰 烬?
浊 液滤 液
混合液灼烧滤 渣一、从海带中检验碘的实验方案溶解过滤酸化氧化淀粉溶液4、取1-2ml混合液滴加淀粉溶液检验,其余保留待用。2、滤液中加1ml 2mol/L的H2SO4溶液进行酸化。
3、氧化剂可选择2-3ml6%的双氧水或0.5ml的新制氯水。注意:
1、溶解时加15ml蒸馏水,煮沸。1.两种氧化剂选用哪种更好一些?为什么? 3.怎样操作确保用氯水检验出碘元素?过滤液中先加入淀粉,后逐滴加入氯水,边加边振荡。思考与讨论:2.为什么用氯水溶液作氧化剂可能检验不出碘元素?干海带灰 烬?
浊 液滤 液
混合液(I2)上 层
下 层
灼烧滤 渣二、从海带中提取碘的实验方案水浸过滤酸化CCl4
萃取分液氧化分液漏斗的使用1.使用前必须进行什么操作?
2.分液漏斗加液体的量控制在什么范围?
3.分液漏斗振摇时,左右手分别做什么动作?
4.振摇后为何要放气?
5.静置后,需进行什么操作再放液?目的是什么?
6.两层液体分别从哪里放出? 萃取分液①操作要点:
将氧化检验后的余液转入分液漏斗中,加入1-2mlCCl4,充分振荡及放气,将上口塞子打开,静置,待完全分层后,分液。②实验注意事项:
下层液体下口放出,上层液体上口倒出。若要分离碘的CCl4溶液,分别得到碘和CCl4,应采用什么方法?
已知:四氯化碳的沸点:77℃
碘单质的沸点:184.35 ℃将碘的四氯化碳溶液进行蒸馏。干海带灰 烬?
浊 液滤 液
混合液(I2)上 层
下 层
碘单质
灼烧滤 渣二、从海带中提取碘的实验方案水浸过滤酸化CCl4
萃取分液蒸馏氧化小结:海带中碘的分离及检验1、实验原理2I- + 2H+ + H2O2 = I2 + 2H2O2I- + Cl2 = I2 + 2Cl-2、实验流程:称取样品灼烧灰化溶解过滤氧化检验萃取分液物质分离方法巩固练习1、向碘化钾溶液中加入适量的氯水,发生化学反应生成单质碘和氯化钾,要将单质碘从海水中分离出来,下列方法中最好的是( )
A、过滤 B、蒸馏 C、结晶 D、萃取巩固练习2、下列实验操作中错误的是( )
A、分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面
D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中 1、灼烧操作中需要哪些仪器?操作中有哪些注意要点?2、提供给你淀粉碘化钾试纸,如何利用厨房里的常用物品检验食用盐中是否含有碘元素?课后作业
海带的次要成分:氯化钠、碳酸钠、硫酸钠、碘化钠等无机盐。
探究:
1.如何将海带中的有机态碘转化成无机态碘?
2.设计检验海带中含碘元素的实验方案。
(提示:有机态的碘转化为无机态的碘时主要以 I- 的形式存在)干海带灰 烬?
浊 液滤 液
混合液灼烧滤 渣一、从海带中检验碘的实验方案溶解过滤酸化氧化淀粉溶液实验注意事项:应在通风处加热灼烧,或使用通风设备去除白烟和难闻的气味。应边加热边搅拌,用坩埚钳夹持坩埚,玻璃棒小心搅拌,使海带均匀受热,加快灰化的速度。
至干海带逐渐变的更干燥、卷曲,最后变成黑色粉末或细小颗粒。灼烧完毕,应将坩埚和玻璃棒放在石棉网上冷却,不可直接放在冷的实验台上,防止温度很高的坩埚骤冷而破裂 溶解过滤①操作要点:
取一药匙海带灰置于小烧杯中,加入约15ml蒸馏水,煮沸,过滤。②实验注意事项:
应隔着石棉网加热小烧杯中的混合物。
加热过程中应不断搅拌,加快溶解,同时防止液 体受热不均而溅出。
过滤操作应注意“一贴、二低、三靠” 。 4、酸化作用是什么?海带灰的浸出液中含有碳酸钠(碳酸钾)等使溶液显碱性的物质,酸化的目的是使溶液呈弱酸性,有利于氧化剂把I-氧化为I2。5、常用的氧化剂是什么?氯水、氧气、臭氧、高锰酸钾、双氧水、浓硫酸等。干海带灰 烬?
浊 液滤 液
混合液灼烧滤 渣一、从海带中检验碘的实验方案溶解过滤酸化氧化淀粉溶液4、取1-2ml混合液滴加淀粉溶液检验,其余保留待用。2、滤液中加1ml 2mol/L的H2SO4溶液进行酸化。
3、氧化剂可选择2-3ml6%的双氧水或0.5ml的新制氯水。注意:
1、溶解时加15ml蒸馏水,煮沸。1.两种氧化剂选用哪种更好一些?为什么? 3.怎样操作确保用氯水检验出碘元素?过滤液中先加入淀粉,后逐滴加入氯水,边加边振荡。思考与讨论:2.为什么用氯水溶液作氧化剂可能检验不出碘元素?干海带灰 烬?
浊 液滤 液
混合液(I2)上 层
下 层
灼烧滤 渣二、从海带中提取碘的实验方案水浸过滤酸化CCl4
萃取分液氧化分液漏斗的使用1.使用前必须进行什么操作?
2.分液漏斗加液体的量控制在什么范围?
3.分液漏斗振摇时,左右手分别做什么动作?
4.振摇后为何要放气?
5.静置后,需进行什么操作再放液?目的是什么?
6.两层液体分别从哪里放出? 萃取分液①操作要点:
将氧化检验后的余液转入分液漏斗中,加入1-2mlCCl4,充分振荡及放气,将上口塞子打开,静置,待完全分层后,分液。②实验注意事项:
下层液体下口放出,上层液体上口倒出。若要分离碘的CCl4溶液,分别得到碘和CCl4,应采用什么方法?
已知:四氯化碳的沸点:77℃
碘单质的沸点:184.35 ℃将碘的四氯化碳溶液进行蒸馏。干海带灰 烬?
浊 液滤 液
混合液(I2)上 层
下 层
碘单质
灼烧滤 渣二、从海带中提取碘的实验方案水浸过滤酸化CCl4
萃取分液蒸馏氧化小结:海带中碘的分离及检验1、实验原理2I- + 2H+ + H2O2 = I2 + 2H2O2I- + Cl2 = I2 + 2Cl-2、实验流程:称取样品灼烧灰化溶解过滤氧化检验萃取分液物质分离方法巩固练习1、向碘化钾溶液中加入适量的氯水,发生化学反应生成单质碘和氯化钾,要将单质碘从海水中分离出来,下列方法中最好的是( )
A、过滤 B、蒸馏 C、结晶 D、萃取巩固练习2、下列实验操作中错误的是( )
A、分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面
D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中 1、灼烧操作中需要哪些仪器?操作中有哪些注意要点?2、提供给你淀粉碘化钾试纸,如何利用厨房里的常用物品检验食用盐中是否含有碘元素?课后作业
同课章节目录
- 专题一 物质的分离与提纯
- 课题1 海带中碘元素的分离及检验
- 拓展课题1-1 茶叶中某些元素的鉴定
- 课题2 用纸层析法分离铁离子和铜离子
- 拓展课题1-2 菠菜的叶绿体中色素的提取和分离
- 拓展课题1-3 用粉笔进行层析分离
- 课题3 硝酸钾晶体的制备
- 拓展课题1-4 粗盐提纯
- 专题二 物质性质的研究
- 课题1 铝及其化合物的性质
- 拓展课题2-1 铝热反应
- 课题2 乙醇和苯酚的性质
- 拓展课题2-2 苯酚与甲醛的反应
- 专题三 物质的检验与鉴别
- 课题1 牙膏和火柴中某些成分的检验
- 拓展课题3-1 新装修居室内空气中甲醛浓度的检测
- 拓展课题3-2 汽车尾气成分的检验
- 课题2 亚硝酸钠和食盐的鉴别
- 拓展课题3-3 真假碘盐的鉴别
- 专题四 化学反应条件的控制
- 课题1 硫代硫酸钠与酸反应速率的影响因素
- 拓展课题4-1 “蓝瓶子”实验
- 课题2 催化剂对过氧化氢分解反应速率的影响
- 拓展课题4-2 过氧化氢酶的催化作用
- 拓展课题4-3 蔗糖的燃烧
- 课题3 反应条件对化学平衡的影响
- 拓展课题4-4 淀粉与碘显色现象的探究
- 拓展课题4-5 压强对化学平衡的影响
- 专题五 电化学问题研究
- 课题1 原电池
- 拓展课题5-1 干电池模拟实验
- 课题2 电解与电镀
- 拓展课题5-2 阿伏加德罗常数的测定
- 专题六 物质的定量分析
- 课题1 食醋总酸含量的测定
- 拓展课题6-1 配制并标定氢氧化钠溶液
- 课题2 镀锌铁皮锌镀层厚度的测定
- 拓展课题6-2 水果中维生素C含量的测定
- 专题七 物质的制备与合成
- 课题1 硫酸亚铁铵的制备
- 拓展课题7-1 用制氢废液制备硫酸锌晶体
- 课题2 阿司匹林的合成
- 拓展课题7-2 对氨基苯磺酸的合成
