粤教版九下化学 8.2常见的酸和碱 课件(16张PPT)
文档属性
| 名称 | 粤教版九下化学 8.2常见的酸和碱 课件(16张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 38.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-30 00:00:00 | ||
图片预览






文档简介
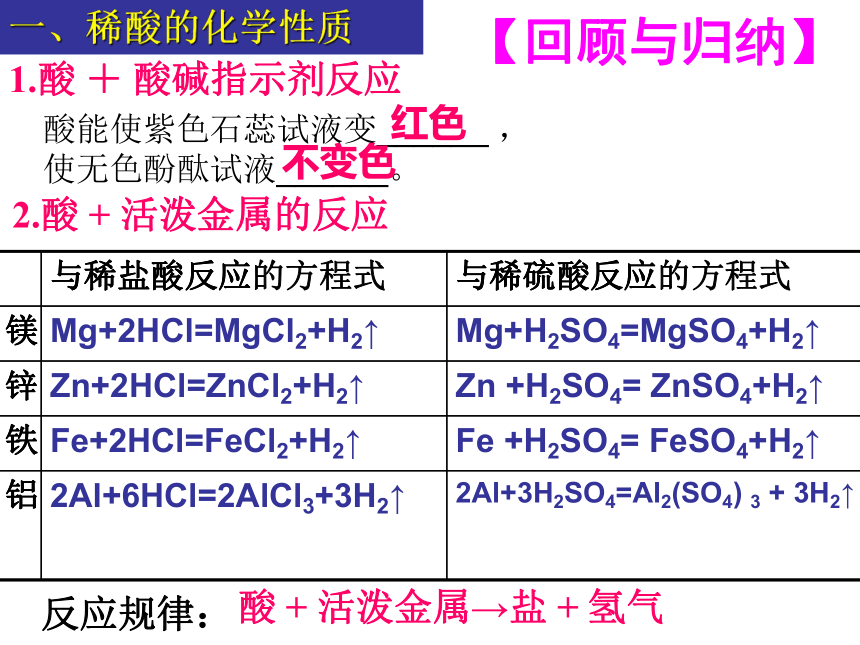
课件16张PPT。酸的化学性质2.酸 + 活泼金属的反应1.酸 + 酸碱指示剂反应酸能使紫色石蕊试液变______?,
使无色酚酞试液______。红色不变色一、稀酸的化学性质反应规律:【回顾与归纳】酸 + 活泼金属→盐 + 氢气 实验与探究合作探究,我会学! 1.实验的中心围绕酸的化学性质展开。
2.实验注意事项:
⑴实验时注意安全。
⑵实验时要按规定取用药品。
3.实验前请同学们清点仪器及药品。
4.整个实验操作要严谨、科学,规范。
5.实验过程中要填好实验现象。
检查药品和仪器是否完备?
生锈的铁钉、氧化铜、稀盐酸、稀硫酸、氢氧化铜、氢氧化钙、鸡蛋壳、硝酸银溶液、硝酸钡溶液、试管、镊子、药匙、酒精灯、试管夹、火柴或打火机。
1.小组汇报实验结果(药品、现象),师生共同总结反应规律。
2.各小组用自己喜欢的方式总结酸的化学性质(框架图、树状图或其它形式)【展示与交流】铁锈逐渐溶解,溶液由无色变为黄色6HCl+Fe2O3=2FeCl3+3H2O
(黄色)3H2SO4+Fe2O3=Fe2(SO4)3+3H2O
(黄色)黑色粉末逐渐溶解,溶液由无色变为蓝色2HCl+CuO=CuCl2+H2O
(蓝色)H2SO4 +CuO=CuSO4+H2O
(蓝色)反应规律:3. 酸 + 金属氧化物的反应酸 + 金属氧化物→ 盐 + 水蓝色固体逐渐溶解,溶液由无色变为蓝色2HCl+Cu(OH)2=CuCl2+2H2OH2SO4+Cu(OH)2=CuSO4+2H2O反应规律:4. 酸 + 碱的反应固体逐渐溶解酸 + 金属氧化物→ 盐 + 水2HCl+Ca(OH)2=CaCl2+2H2OH2SO4+Ca(OH)2=CaSO4+2H2O反应规律:5. 酸 + 盐的反应CaCO3 + 2HCl
=CaCl2 + H2O + CO2↑鸡蛋壳逐渐溶解,冒出大量气泡。生成白色沉淀HCl+AgNO3= HNO3+AgCl ↓H2SO4 + Ba(NO3)2=2HNO3 + BaSO4 ↓酸 + 盐 → 新酸 + 新盐酸+酸碱指示剂+ 活泼金属+金属氧化物+碱+盐能使石蕊溶液变红,
酚酞溶液不变色。→ 盐 + 水→ 盐 + 水→盐 + 氢气
→ 新酸 + 新盐
稀酸的化学性质---酸的通性【反思与释疑】1.由上述反应可看出,酸溶液具有许多共同的性质(通性)原因是什么 。
2.蛋雕工艺品上的文字或图案是怎样刻出的呢?盘 点 收 获
1.今天我们学到了什么知识?
2.今天我们掌握了什么方法?
3.今天我们明白了哪些道理?1.取四朵用石蕊溶液染成紫色的纸花,分别喷洒下列液体,能观察到纸花变红的是( ) A.氢氧化钠溶液 B.稀盐酸
C.蒸馏水 D.食盐水
2.盐酸和稀硫酸常用作金属表面的清洁剂,是利用了它们化学性质中的( )
A.能与金属反应 B.能与金属氧化物反应
C.能使指示剂变色 D.能溶于水
3.衣服上沾了铁锈,直接用水洗很难洗净,要除去白色衣服上的铁锈,你认为比较适宜的液体是( )
A.白醋 B.酱油 C.酒精 D.洗洁精
4.稀盐酸和稀硫酸具有许多相似化学性质的原因是( )
A.它们都是溶液 B.它们都含有酸根离子
C.它们都含有氢元素D.它们的溶液中都含有氢离子
检测提升(相信自己,我能赢!)5.下列化学方程式书写正确的是( )
A.Zn+2HCl=ZnCl+H2?????????????B.Fe+H2SO4=FeSO4+H2
C.Al+2HCl=AlCl2+H2?????????????D.Cu+H2SO4=CuSO4+H2
6.下列物质可由金属与发生置换反应得到的是( )
A.CuCl2 B.Fe2(SO4)3 C.ZnCl2 D.AgCl 7.A、B、C、D、E分别是氧化铁、铁、氧气、一氧化碳、稀盐酸中的一种物质。请回答下列问题:
(1)在图中将一定条件下所有能发生反应的两种物质用“――”连接起来:
(2)A与B反应后的溶液呈黄色,则A与B反应的化学方程式
为 。
(3)A与C能发生置换反应,则C与D反应的实验现象
为 。
(4) A ,B ,C ,D ,E 。
使无色酚酞试液______。红色不变色一、稀酸的化学性质反应规律:【回顾与归纳】酸 + 活泼金属→盐 + 氢气 实验与探究合作探究,我会学! 1.实验的中心围绕酸的化学性质展开。
2.实验注意事项:
⑴实验时注意安全。
⑵实验时要按规定取用药品。
3.实验前请同学们清点仪器及药品。
4.整个实验操作要严谨、科学,规范。
5.实验过程中要填好实验现象。
检查药品和仪器是否完备?
生锈的铁钉、氧化铜、稀盐酸、稀硫酸、氢氧化铜、氢氧化钙、鸡蛋壳、硝酸银溶液、硝酸钡溶液、试管、镊子、药匙、酒精灯、试管夹、火柴或打火机。
1.小组汇报实验结果(药品、现象),师生共同总结反应规律。
2.各小组用自己喜欢的方式总结酸的化学性质(框架图、树状图或其它形式)【展示与交流】铁锈逐渐溶解,溶液由无色变为黄色6HCl+Fe2O3=2FeCl3+3H2O
(黄色)3H2SO4+Fe2O3=Fe2(SO4)3+3H2O
(黄色)黑色粉末逐渐溶解,溶液由无色变为蓝色2HCl+CuO=CuCl2+H2O
(蓝色)H2SO4 +CuO=CuSO4+H2O
(蓝色)反应规律:3. 酸 + 金属氧化物的反应酸 + 金属氧化物→ 盐 + 水蓝色固体逐渐溶解,溶液由无色变为蓝色2HCl+Cu(OH)2=CuCl2+2H2OH2SO4+Cu(OH)2=CuSO4+2H2O反应规律:4. 酸 + 碱的反应固体逐渐溶解酸 + 金属氧化物→ 盐 + 水2HCl+Ca(OH)2=CaCl2+2H2OH2SO4+Ca(OH)2=CaSO4+2H2O反应规律:5. 酸 + 盐的反应CaCO3 + 2HCl
=CaCl2 + H2O + CO2↑鸡蛋壳逐渐溶解,冒出大量气泡。生成白色沉淀HCl+AgNO3= HNO3+AgCl ↓H2SO4 + Ba(NO3)2=2HNO3 + BaSO4 ↓酸 + 盐 → 新酸 + 新盐酸+酸碱指示剂+ 活泼金属+金属氧化物+碱+盐能使石蕊溶液变红,
酚酞溶液不变色。→ 盐 + 水→ 盐 + 水→盐 + 氢气
→ 新酸 + 新盐
稀酸的化学性质---酸的通性【反思与释疑】1.由上述反应可看出,酸溶液具有许多共同的性质(通性)原因是什么 。
2.蛋雕工艺品上的文字或图案是怎样刻出的呢?盘 点 收 获
1.今天我们学到了什么知识?
2.今天我们掌握了什么方法?
3.今天我们明白了哪些道理?1.取四朵用石蕊溶液染成紫色的纸花,分别喷洒下列液体,能观察到纸花变红的是( ) A.氢氧化钠溶液 B.稀盐酸
C.蒸馏水 D.食盐水
2.盐酸和稀硫酸常用作金属表面的清洁剂,是利用了它们化学性质中的( )
A.能与金属反应 B.能与金属氧化物反应
C.能使指示剂变色 D.能溶于水
3.衣服上沾了铁锈,直接用水洗很难洗净,要除去白色衣服上的铁锈,你认为比较适宜的液体是( )
A.白醋 B.酱油 C.酒精 D.洗洁精
4.稀盐酸和稀硫酸具有许多相似化学性质的原因是( )
A.它们都是溶液 B.它们都含有酸根离子
C.它们都含有氢元素D.它们的溶液中都含有氢离子
检测提升(相信自己,我能赢!)5.下列化学方程式书写正确的是( )
A.Zn+2HCl=ZnCl+H2?????????????B.Fe+H2SO4=FeSO4+H2
C.Al+2HCl=AlCl2+H2?????????????D.Cu+H2SO4=CuSO4+H2
6.下列物质可由金属与发生置换反应得到的是( )
A.CuCl2 B.Fe2(SO4)3 C.ZnCl2 D.AgCl 7.A、B、C、D、E分别是氧化铁、铁、氧气、一氧化碳、稀盐酸中的一种物质。请回答下列问题:
(1)在图中将一定条件下所有能发生反应的两种物质用“――”连接起来:
(2)A与B反应后的溶液呈黄色,则A与B反应的化学方程式
为 。
(3)A与C能发生置换反应,则C与D反应的实验现象
为 。
(4) A ,B ,C ,D ,E 。
