粤教版九下化学 8.3酸和碱的反应 课件(20张PPT)
文档属性
| 名称 | 粤教版九下化学 8.3酸和碱的反应 课件(20张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 710.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-05-30 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
复习回顾
酸的化学通性:
⑴能使紫色石蕊变红色,无色酚酞不变色。
⑵酸+较活泼金属→
盐+氢气
⑶酸+金属氧化物→
盐+水
⑷酸+盐→
新酸+新盐
复习回顾
碱的化学通性:
⑴能使紫色石蕊变蓝色,无色酚酞变红色。
⑵碱+非金属氧化物→
⑶碱+盐→
盐+水
新碱+新盐
8.3 酸和碱的反应
中和反应
第八章 常见的酸碱盐
酸、碱各有相似的化学性质,这是什么原因造成的呢?
【实验8—13】溶液的导电性
溶液 蒸馏水 酒精 稀盐酸 稀硫酸 稀烧碱溶液 澄清石灰水
灯泡亮否
否
否
亮
亮
亮
亮
结论:蒸馏水、酒精不导电,而酸溶液和碱溶液能够导电。这说明酸、碱溶液中存在自由移动的带电的粒子。
这些带电的粒子是什么?
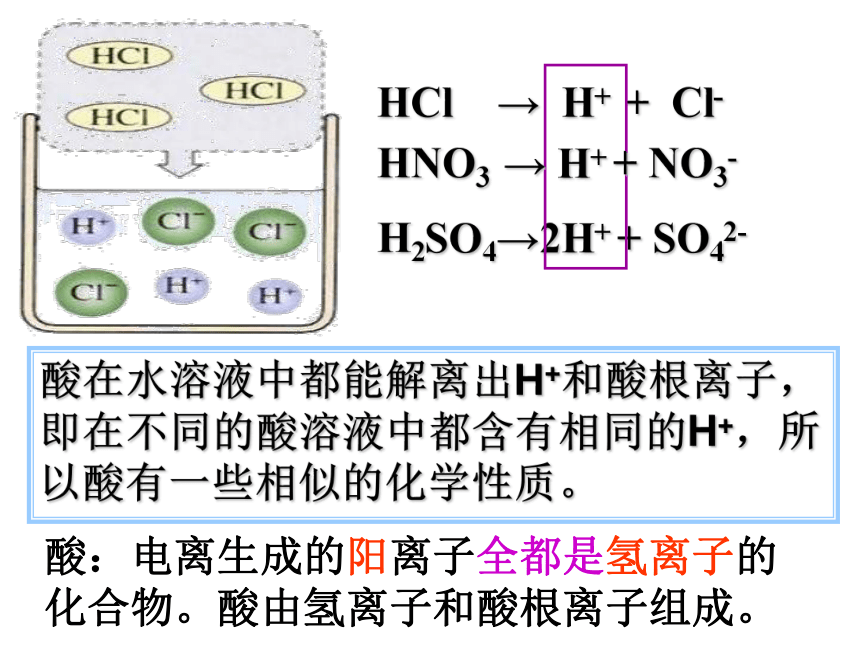
HCl → H+ + Cl-
H2SO4→2H+ + SO42-
酸在水溶液中都能解离出H+和酸根离子,即在不同的酸溶液中都含有相同的H+,所以酸有一些相似的化学性质。
HNO3 → H+ + NO3-
酸:电离生成的阳离子全都是氢离子的化合物。酸由氢离子和酸根离子组成。
NaOH → Na+ + OH-
Ca(OH)2→ Ca2+ + 2OH-
碱在水溶液中都能解离出金属离子和OH- ,即在不同的碱溶液中都含有相同的OH-,所以,碱有一些相似的化学性质。
KOH → K+ + OH-
碱:电离生成的阴离子全都是氢氧根离子的化合物。碱由金属离子和氢氧根离子组成。
同学们有这样的经历吗
蚊子叮咬
蚊虫叮咬时,在蚊子的口器中分泌出一种有机酸--蚁酸,在家庭中可用浓肥皂涂抹可迅速止痒。
情境创设
提出问题:
酸和碱之间是否会发反应
实验验证:
稀盐酸与氢氧化钠溶液直接混合
你能设计出可行的方案证明酸和碱之间发生了反应吗?
自主学习
药品:
NaOH溶液、HCl溶液、酚酞溶液、紫色石蕊溶液
步骤设计:
取3mLNaOH溶液于试管中,滴入2—3滴酚酞溶液,逐滴入稀盐酸,并不断振荡,直到刚好褪色为止;再滴两滴NaOH溶液,振荡,再次滴入适量的稀盐酸,振荡。
操作步骤 观察到的现象
① 取3mLNaOH溶液于试管中,滴入1、2滴酚酞溶液
② 逐渐往NaOH溶液中滴稀盐酸,并不断振荡,
③ 向上述刚好褪色的溶液中再滴两滴NaOH溶液,振荡
④ 再次滴入微量稀盐酸,振荡
现象记录:
溶液由无色变为红色
溶液的红色慢慢褪去,直至无色。
溶液又由无色变为红色
溶液的红色再次褪去。
氢氧化钠与盐酸发生中和反应
解释与结论:指示剂颜色的变化说明碱溶液与滴入的酸溶液发生了化学变化。
盐酸与氢氧化钠反应:
HCl + NaOH = NaCl + H2O
酸
碱
盐
水
讨论:
1. 酚酞在实验中起什么作用?
答:起指示作用。因为NaOH与HCl反应无明显的现象发生,根据酚酞溶液由红色变为无色来判断NaOH和HCl是否反应和是否反应完全。
HCl+NaOH=NaCl+H2O
酸+碱→盐+水
H++OH-=H2O
氢氧化钠与盐酸反应的本质:酸溶液中的氢离子和碱溶液中的氢氧根离子反应生成水的过程。
思考:
如果该用其他酸和碱来进行上述实验,结果会怎样?为什么?
硫酸与氢氧化钾反应:
H2SO4+2NaOH=Na2SO4+2H2O
一、中和反应:
1、定义:
酸跟碱生成盐和水的反应,叫做中和反应。
2、实质:
H++OH-=H2O
3、举例:
HCl+NaOH=NaCl+H2O
H2SO4+2NaOH=Na2SO4+2H2O
2HCl+Ca(OH)2=CaCl2+2H2O
H2SO4+Ca(OH)2=CaSO4+2H2O
写出盐酸、硫酸分别与氢氧化钠、氢氧化钙反应的化学方程式
酸的主要化学性质 碱的主要化学性质
使紫色石蕊溶液( ) 使紫色石蕊溶液( )
无色酚酞溶液( ) 无色酚酞溶液( )
酸+碱→( )+( )
酸+( )氧化物→
( )+( ) 碱+( )氧化物→
( )+( )
酸+盐→( )+( ) 碱+盐→( )+( )
酸+较活泼金属→
( )+( )
变红
变红
变蓝
不变色
盐
水
金属
非金属
盐
盐
新盐
新盐
盐
水
水
新酸
新碱
氢气
二、中和反应在实际中的应用
自主学习
吃碱面时,放点醋,味道会更鲜美。
碱过量的馒头,用放醋的水蒸,
可以降低碱性
1、改变土壤的酸碱性
植物需要在一定酸碱性的土壤中生长,但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长,应怎样去改变酸性土壤?
用熟石灰中和。
2、处理工厂的废水
某硫酸厂排出的废水中含有硫酸等杂质,严重危害当地的生态环境,你会怎样处理这些废水呢?
用碱性物质(例如熟石灰)进行中和处理。
你能写出化学方程式吗?请试一下
Ca(OH)2 + H2 SO4 == CaSO4 + 2H2O
3、用于医药
(1)胃酸的主要成分是 。胃药的主要成分 。
盐酸
氢氧化铝能中和胃酸,你能写出化学方程式吗?
Al(OH)3 + 3HCl = AlCl3 + 3H2O
(2)被蚊虫叮咬后,涂一些含有碱性的物质的药水。
讨论:举出生活中利用中和反应的实例。
自主学习
氢氧化铝
如:凃肥皂水
巩固拓展
1、下列反应中属于中和反应的是( )
A、Zn + 2HCl = ZnCl2 +H2↑
B、CuO + 2HCl = CuCl2+ H2O
C、Ba(OH)2+ H2SO4 = BaSO4 ↓+ 2H2O
D、AgNO3+HCl = AgCl↓ +HNO3
2、下列反应,要借助酸碱指示剂,才能判断二者发生反应的是( )
A、大理石和稀盐酸 B、石灰水和稀盐酸
C、铁锈与稀盐酸 D、镁和稀硫酸
3、下列物质中,不属于盐类的是( )
A、Fe(OH)2 B、AgCl
C、Na2CO3 D、H2SO4
4.小松同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂。为了确定盐酸与氢氧化钠是否恰好完全反应,小松同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。于是他得出“两种物质已恰好完全中和”的结论。
氢氧化钠
稀盐酸
(1)写出该反应的化学方程式: 。
(2)你认为他得出的结论是否正确 ,
理由是 。
(3)为了验证小松同学的结论,你可以选择的试剂是( ) A、紫色石蕊试液 B、稀硫酸
C、铁粉 D、铜片 E、碳酸钠
复习回顾
酸的化学通性:
⑴能使紫色石蕊变红色,无色酚酞不变色。
⑵酸+较活泼金属→
盐+氢气
⑶酸+金属氧化物→
盐+水
⑷酸+盐→
新酸+新盐
复习回顾
碱的化学通性:
⑴能使紫色石蕊变蓝色,无色酚酞变红色。
⑵碱+非金属氧化物→
⑶碱+盐→
盐+水
新碱+新盐
8.3 酸和碱的反应
中和反应
第八章 常见的酸碱盐
酸、碱各有相似的化学性质,这是什么原因造成的呢?
【实验8—13】溶液的导电性
溶液 蒸馏水 酒精 稀盐酸 稀硫酸 稀烧碱溶液 澄清石灰水
灯泡亮否
否
否
亮
亮
亮
亮
结论:蒸馏水、酒精不导电,而酸溶液和碱溶液能够导电。这说明酸、碱溶液中存在自由移动的带电的粒子。
这些带电的粒子是什么?
HCl → H+ + Cl-
H2SO4→2H+ + SO42-
酸在水溶液中都能解离出H+和酸根离子,即在不同的酸溶液中都含有相同的H+,所以酸有一些相似的化学性质。
HNO3 → H+ + NO3-
酸:电离生成的阳离子全都是氢离子的化合物。酸由氢离子和酸根离子组成。
NaOH → Na+ + OH-
Ca(OH)2→ Ca2+ + 2OH-
碱在水溶液中都能解离出金属离子和OH- ,即在不同的碱溶液中都含有相同的OH-,所以,碱有一些相似的化学性质。
KOH → K+ + OH-
碱:电离生成的阴离子全都是氢氧根离子的化合物。碱由金属离子和氢氧根离子组成。
同学们有这样的经历吗
蚊子叮咬
蚊虫叮咬时,在蚊子的口器中分泌出一种有机酸--蚁酸,在家庭中可用浓肥皂涂抹可迅速止痒。
情境创设
提出问题:
酸和碱之间是否会发反应
实验验证:
稀盐酸与氢氧化钠溶液直接混合
你能设计出可行的方案证明酸和碱之间发生了反应吗?
自主学习
药品:
NaOH溶液、HCl溶液、酚酞溶液、紫色石蕊溶液
步骤设计:
取3mLNaOH溶液于试管中,滴入2—3滴酚酞溶液,逐滴入稀盐酸,并不断振荡,直到刚好褪色为止;再滴两滴NaOH溶液,振荡,再次滴入适量的稀盐酸,振荡。
操作步骤 观察到的现象
① 取3mLNaOH溶液于试管中,滴入1、2滴酚酞溶液
② 逐渐往NaOH溶液中滴稀盐酸,并不断振荡,
③ 向上述刚好褪色的溶液中再滴两滴NaOH溶液,振荡
④ 再次滴入微量稀盐酸,振荡
现象记录:
溶液由无色变为红色
溶液的红色慢慢褪去,直至无色。
溶液又由无色变为红色
溶液的红色再次褪去。
氢氧化钠与盐酸发生中和反应
解释与结论:指示剂颜色的变化说明碱溶液与滴入的酸溶液发生了化学变化。
盐酸与氢氧化钠反应:
HCl + NaOH = NaCl + H2O
酸
碱
盐
水
讨论:
1. 酚酞在实验中起什么作用?
答:起指示作用。因为NaOH与HCl反应无明显的现象发生,根据酚酞溶液由红色变为无色来判断NaOH和HCl是否反应和是否反应完全。
HCl+NaOH=NaCl+H2O
酸+碱→盐+水
H++OH-=H2O
氢氧化钠与盐酸反应的本质:酸溶液中的氢离子和碱溶液中的氢氧根离子反应生成水的过程。
思考:
如果该用其他酸和碱来进行上述实验,结果会怎样?为什么?
硫酸与氢氧化钾反应:
H2SO4+2NaOH=Na2SO4+2H2O
一、中和反应:
1、定义:
酸跟碱生成盐和水的反应,叫做中和反应。
2、实质:
H++OH-=H2O
3、举例:
HCl+NaOH=NaCl+H2O
H2SO4+2NaOH=Na2SO4+2H2O
2HCl+Ca(OH)2=CaCl2+2H2O
H2SO4+Ca(OH)2=CaSO4+2H2O
写出盐酸、硫酸分别与氢氧化钠、氢氧化钙反应的化学方程式
酸的主要化学性质 碱的主要化学性质
使紫色石蕊溶液( ) 使紫色石蕊溶液( )
无色酚酞溶液( ) 无色酚酞溶液( )
酸+碱→( )+( )
酸+( )氧化物→
( )+( ) 碱+( )氧化物→
( )+( )
酸+盐→( )+( ) 碱+盐→( )+( )
酸+较活泼金属→
( )+( )
变红
变红
变蓝
不变色
盐
水
金属
非金属
盐
盐
新盐
新盐
盐
水
水
新酸
新碱
氢气
二、中和反应在实际中的应用
自主学习
吃碱面时,放点醋,味道会更鲜美。
碱过量的馒头,用放醋的水蒸,
可以降低碱性
1、改变土壤的酸碱性
植物需要在一定酸碱性的土壤中生长,但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长,应怎样去改变酸性土壤?
用熟石灰中和。
2、处理工厂的废水
某硫酸厂排出的废水中含有硫酸等杂质,严重危害当地的生态环境,你会怎样处理这些废水呢?
用碱性物质(例如熟石灰)进行中和处理。
你能写出化学方程式吗?请试一下
Ca(OH)2 + H2 SO4 == CaSO4 + 2H2O
3、用于医药
(1)胃酸的主要成分是 。胃药的主要成分 。
盐酸
氢氧化铝能中和胃酸,你能写出化学方程式吗?
Al(OH)3 + 3HCl = AlCl3 + 3H2O
(2)被蚊虫叮咬后,涂一些含有碱性的物质的药水。
讨论:举出生活中利用中和反应的实例。
自主学习
氢氧化铝
如:凃肥皂水
巩固拓展
1、下列反应中属于中和反应的是( )
A、Zn + 2HCl = ZnCl2 +H2↑
B、CuO + 2HCl = CuCl2+ H2O
C、Ba(OH)2+ H2SO4 = BaSO4 ↓+ 2H2O
D、AgNO3+HCl = AgCl↓ +HNO3
2、下列反应,要借助酸碱指示剂,才能判断二者发生反应的是( )
A、大理石和稀盐酸 B、石灰水和稀盐酸
C、铁锈与稀盐酸 D、镁和稀硫酸
3、下列物质中,不属于盐类的是( )
A、Fe(OH)2 B、AgCl
C、Na2CO3 D、H2SO4
4.小松同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂。为了确定盐酸与氢氧化钠是否恰好完全反应,小松同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。于是他得出“两种物质已恰好完全中和”的结论。
氢氧化钠
稀盐酸
(1)写出该反应的化学方程式: 。
(2)你认为他得出的结论是否正确 ,
理由是 。
(3)为了验证小松同学的结论,你可以选择的试剂是( ) A、紫色石蕊试液 B、稀硫酸
C、铁粉 D、铜片 E、碳酸钠
