粤教版九下化学 第8章常见的酸碱盐 复习 课件(20张PPT)
文档属性
| 名称 | 粤教版九下化学 第8章常见的酸碱盐 复习 课件(20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 509.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-06-01 00:00:00 | ||
图片预览







文档简介
课件20张PPT。酸碱盐复习课进一步了解复分解反应通过归纳的方式整理出酸碱盐的化学性质总结出常见的沉淀及发生反应的离子对会利用所学知识解决相关问题
学习目标酸碱盐复习
酸碱盐的化学性质
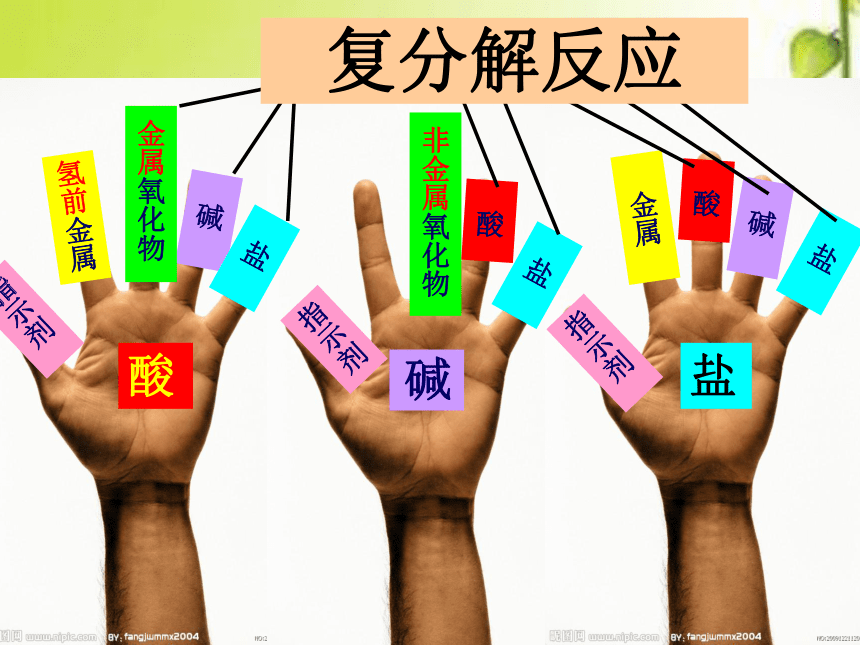
知识梳理1指示剂 碱 金属氧化物氢前金属指示剂 非金属氧化物碱酸 酸指示剂 碱 盐 金属盐 酸 盐 盐
复分解反应
知识梳理2复分解反应1、概念:两种化合物相互交换成分,生成另外两种化合物的反应,叫做复分解反应
AB+CD=AD+CB2、发生复分解反应的条件:生成物中有沉淀或气体或生成水,否则不能发生复分解反应
“一水两气七沉淀”
指示剂 碱 金属氧化物氢前金属指示剂 非金属氧化物碱酸 酸指示剂 碱 盐 金属盐 酸 盐 盐复分解反应复
分
解
反
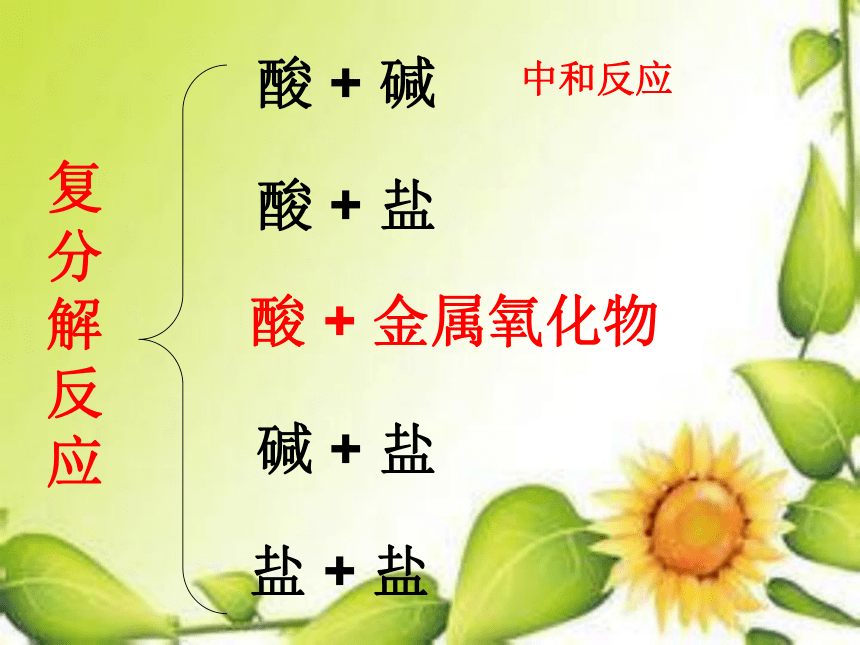
应酸 + 碱酸 + 盐酸 + 金属氧化物碱 + 盐盐 + 盐中和反应
常见的沉淀
“七沉淀”
知识梳理3
蓝色沉淀红褐色沉淀白色沉淀Cu(OH)2Fe(OH)3Mg(OH)2BaSO4AgClCaCO3BaCO3 “ 五白”
发生反应的离子对
产生沉淀的离子组合Cu(OH)2Fe(OH)3Mg(OH)2BaSO4AgClCaCO3BaCO3Cu2+ + OH-Fe3 + + OH-Ba2 + + SO42-Ba2 + + CO32-Ca2 + + CO32-Mg2 + + OH-Ag + + Cl- 产生水和气体的离子组合H+ + OH-H2OH+ + CO32- CO2 + H2ONH4+ + OH-NH3 + H2O温馨提示:在反应中,只要有像上述
“离子对”存在,生成沉淀或水或气体的,
这样的离子就不能大量共存离子共存1.下列各组离子可在同一溶液中大量共存的是( )
A.H+、SO42-、K+、CO32- B.Mg2+、Cl-、OH-、Na+
C.Fe2+、SO42-、H+、Cl- D.Na+、Ba2+、NO3-、SO42-C摸底测试2.能在pH=1的溶液中大量共存,且溶液为无色透明的一组物质是( )
A.FeCl3、CuSO4、NaCl
B.BaCl2、Na2SO4、NaOH
C.CaCl2、Na2CO3、AgNO3
D.K2SO4、NaNO3、NH4ClH+H+H+H+D链接中考1归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应)。(1)为了验证性质①,小红将紫色石蕊溶液滴加到盐酸溶液中,溶液变_____色;
(2)图中A所代表的物质类别是_______;
(3)盐酸的性质③决定了盐酸可用于清除铁锈(主要成分是Fe2O3),该反应的化学方程式是________________________;
(4)为了验证性质⑤,可选用的物质是 ______(填一种即可);红碱Fe2O3 + 6HCl == 2FeCl3+3H2O碳酸钙(5)镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是_____(填序号)。
A.两种金属的形状 B.盐酸的质量分数
C.反应容器的大小 D.温度【易错提醒】
1.根据酸的通性,分析题中已有反应,明确物质A的所属类别;
2.明确哪些量能影响金属与酸反应的速率,那么这些量都需要控制不变。C3.构建知识网络是学习和研究化学常用的科学方法。图18-5是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“—”表示物质之间能够发生化学反应。请按要求回答下列问题。
(1)从物质类别看,“A”物质属于________
(填“氧化物”“酸”“碱”或“盐”,下同);
“B”物质属于________。
(2)从物质组成看,一定由三种元素组成
的是________(填“氧化物”“酸”
“碱”或“盐”)。
(3)举一例用化学方程式表示反应③___
举一例用化学方程式表示反应⑦_____
(4)NH4NO3溶液与NaOH溶液能反应,实质是它们在水中解离出来的NH4+和OH-结合生成了NH3和H2O。结合复分解反应发生的条件,请回答:CaCl2溶液与Na2CO3溶液能反应的实质是它们在水中解离出的__________结合生成了________。
(5)请依据(4)中获得的启示,判断下列各组离子在水溶液中能大量共存的是________(填序号)。A.Ba2+、SO42- B.CO32-、H+
C.H+、OH- D.Na+、NO3-碱酸金属氧化物盐
学习目标酸碱盐复习
酸碱盐的化学性质
知识梳理1指示剂 碱 金属氧化物氢前金属指示剂 非金属氧化物碱酸 酸指示剂 碱 盐 金属盐 酸 盐 盐
复分解反应
知识梳理2复分解反应1、概念:两种化合物相互交换成分,生成另外两种化合物的反应,叫做复分解反应
AB+CD=AD+CB2、发生复分解反应的条件:生成物中有沉淀或气体或生成水,否则不能发生复分解反应
“一水两气七沉淀”
指示剂 碱 金属氧化物氢前金属指示剂 非金属氧化物碱酸 酸指示剂 碱 盐 金属盐 酸 盐 盐复分解反应复
分
解
反
应酸 + 碱酸 + 盐酸 + 金属氧化物碱 + 盐盐 + 盐中和反应
常见的沉淀
“七沉淀”
知识梳理3
蓝色沉淀红褐色沉淀白色沉淀Cu(OH)2Fe(OH)3Mg(OH)2BaSO4AgClCaCO3BaCO3 “ 五白”
发生反应的离子对
产生沉淀的离子组合Cu(OH)2Fe(OH)3Mg(OH)2BaSO4AgClCaCO3BaCO3Cu2+ + OH-Fe3 + + OH-Ba2 + + SO42-Ba2 + + CO32-Ca2 + + CO32-Mg2 + + OH-Ag + + Cl- 产生水和气体的离子组合H+ + OH-H2OH+ + CO32- CO2 + H2ONH4+ + OH-NH3 + H2O温馨提示:在反应中,只要有像上述
“离子对”存在,生成沉淀或水或气体的,
这样的离子就不能大量共存离子共存1.下列各组离子可在同一溶液中大量共存的是( )
A.H+、SO42-、K+、CO32- B.Mg2+、Cl-、OH-、Na+
C.Fe2+、SO42-、H+、Cl- D.Na+、Ba2+、NO3-、SO42-C摸底测试2.能在pH=1的溶液中大量共存,且溶液为无色透明的一组物质是( )
A.FeCl3、CuSO4、NaCl
B.BaCl2、Na2SO4、NaOH
C.CaCl2、Na2CO3、AgNO3
D.K2SO4、NaNO3、NH4ClH+H+H+H+D链接中考1归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应)。(1)为了验证性质①,小红将紫色石蕊溶液滴加到盐酸溶液中,溶液变_____色;
(2)图中A所代表的物质类别是_______;
(3)盐酸的性质③决定了盐酸可用于清除铁锈(主要成分是Fe2O3),该反应的化学方程式是________________________;
(4)为了验证性质⑤,可选用的物质是 ______(填一种即可);红碱Fe2O3 + 6HCl == 2FeCl3+3H2O碳酸钙(5)镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是_____(填序号)。
A.两种金属的形状 B.盐酸的质量分数
C.反应容器的大小 D.温度【易错提醒】
1.根据酸的通性,分析题中已有反应,明确物质A的所属类别;
2.明确哪些量能影响金属与酸反应的速率,那么这些量都需要控制不变。C3.构建知识网络是学习和研究化学常用的科学方法。图18-5是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“—”表示物质之间能够发生化学反应。请按要求回答下列问题。
(1)从物质类别看,“A”物质属于________
(填“氧化物”“酸”“碱”或“盐”,下同);
“B”物质属于________。
(2)从物质组成看,一定由三种元素组成
的是________(填“氧化物”“酸”
“碱”或“盐”)。
(3)举一例用化学方程式表示反应③___
举一例用化学方程式表示反应⑦_____
(4)NH4NO3溶液与NaOH溶液能反应,实质是它们在水中解离出来的NH4+和OH-结合生成了NH3和H2O。结合复分解反应发生的条件,请回答:CaCl2溶液与Na2CO3溶液能反应的实质是它们在水中解离出的__________结合生成了________。
(5)请依据(4)中获得的启示,判断下列各组离子在水溶液中能大量共存的是________(填序号)。A.Ba2+、SO42- B.CO32-、H+
C.H+、OH- D.Na+、NO3-碱酸金属氧化物盐
