2019年鲁教版九年级上册化学解读 第2单元 探秘水世界课件共57张PPT
文档属性
| 名称 | 2019年鲁教版九年级上册化学解读 第2单元 探秘水世界课件共57张PPT |  | |
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-06-04 08:19:26 | ||
图片预览











文档简介
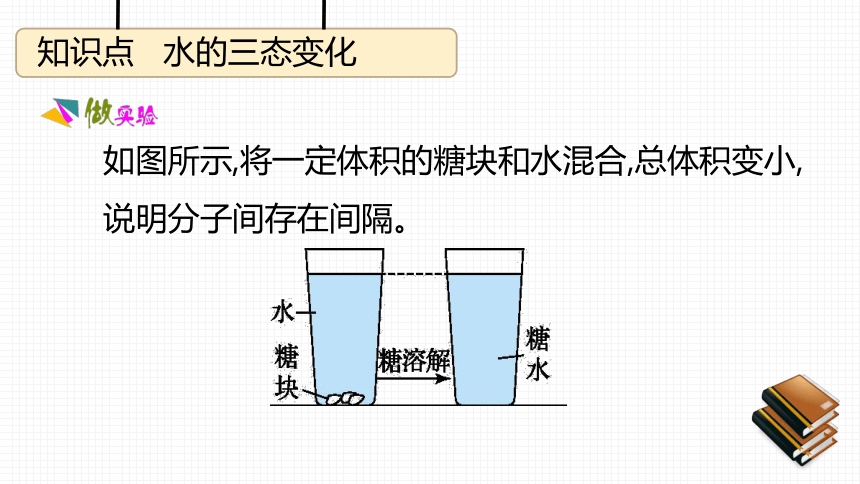
课件57张PPT。学科素养课件第二单元 探秘世界第一节 运动的水分子知识点 水的三态变化如图所示,将一定体积的糖块和水混合,总体积变小,说明分子间存在间隔。知识点 水的三态变化 原子通过作用力相互结合成特定构型的分子,分子聚集构成物质。不同分子构成不同的物质,具有不同的性质。知识点 水的三态变化 一般来说,气态物质分子间的间隔最大,液态次之,固态最小。因为分子之间存在相互作用,分子间的间隔越小,作用力越明显,所以固态时分子只能在固定的位置振动,液态时分子可以比较自由地移动,气态时分子可以自由地移动。知识点 分子及其性质 微观世界中分子的无规则运动是肉眼看不到的,而宏观世界中物体的机械运动则是用肉眼能看到的。知识点 化学的发展历程 按图中装置使有色且密度比空气大的二氧化氮气体放在下瓶,当抽去玻璃片后,看到有色气体扩散到上瓶,下瓶颜色逐渐变浅,这一现象可以证明分子在不断运动。知识点 水的天然循环 (1)水在自然界中有各种形态:云、雾、雨、露、霜、雪、冰、水蒸气等,也就是水在自然界同时以液态、固态和气态存在。雨 (2)水在自然界不断经历着三种状态的循环变化,促使水的三态变化的原因是温度的变化。雪知识点 地球上的水资源 全球淡水资源不仅短缺而且地区分布极不平衡。按地区分布,巴西、俄罗斯、加拿大、中国、美国、印度尼西亚、印度、哥伦比亚和刚果等9个国家的淡水资源占了世界淡水资源的60%。约占世界人口总数40%的80个国家和地区约15亿人口淡水不足,其中26个国家约3亿人极度缺水。更可怕的是,预计到2025年,世界上将会有30亿人面临缺水,40个国家和地区淡水严重不足。知识点 地球上的水资源 过滤操作适用于不溶性固体和液体的分离;若两种固体混合物,一种溶于水,另一种不溶于水,也可以用过滤方法分离。知识点 地球上的水资源 生活中的过滤实例随处可见:纱窗就是最常见的过滤实例,它将草叶、柳絮等挡在了窗户外面,就是过滤。还有筛谷子用的筛子、捉鱼用的网等。知识点 地球上的水资源区分明矾吸附作用与活性炭吸附作用: (1)明矾的吸附性是明矾溶于水后形成胶状物质,将周围的细小粉尘、颗粒“黏”到一起,使细小物质聚集,进而沉降下来。知识点 地球上的水资源 (2)活性炭具有吸附性,是因为活性炭的内部结构是疏松多孔的,可以让一些难溶的微小颗粒或可溶的色素、异味的分子进入到孔隙中去,达到除去杂质的作用。知识点 地球上的水资源活性炭净水器: 入水口在下端是因为能使较大的固体颗粒先沉降,提高净化效果。知识点 地球上的水资源常见的蒸馏装置:知识点5 地球上的水资源水垢的形成原因: 经过沉淀、过滤、吸附等净化处理的水,大部分不溶性杂质被除去了,水中还溶有可溶性钙和镁的化合物,在加热或长久放置时,这些化合物会生成沉淀(水垢)。知识点 地球上的水资源 软水的硬度低,对婴儿身体负担较轻,作为冲泡奶粉的用水被人们所看好。奶粉因为本身含有蛋白质和矿物等营养成分,加入高硬度的硬水冲泡会加重对婴儿身体的负担。婴儿的内脏还未发育完全,矿物成分过量摄入可能会引起消化不良,所以矿物成分含量较低的软水更适合冲泡奶粉。知识点 纯净物和混合物混合物和纯净物的区别: (1)混合物可以看作是由几种纯净物混合而成的,混合物的形成过程中发生的是物理变化。由于混合物的组成一般不固定,所以往往不能用化学式表示。 (2)纯净物只由一种物质组成,有固定的组成,可以用化学式表示。知识点 纯净物和混合物 新鲜、洁净、清洁、混合等词语不是判断物质是否纯净的依据。如洁净的空气属于混合物,冰水混合物是纯净物。知识点 自来水生产过程天然水 天然水指的是自然界中的河水、湖水、井水、海水等,一般在这样的水质中都会存在较多的难溶性杂质,如泥、沙等,使水呈浑浊状或者存在一些可溶性的杂质,使水质呈现出不同的颜色。知识点 自来水生产过程在净水流程中,投药杀菌消毒与其他过程变化类型是否相同? 不相同。自来水的净化过程中,沉淀、吸附、过滤,只是利用明矾和活性炭的吸附性将杂质和异味除掉,此过程中没有新物质生成,属于物理变化过程;消毒杀菌则是利用消毒剂的强氧化性与细菌、病毒发生作用,杀死细菌病毒,属于化学变化。第二单元 探秘世界第二节 水分子的变化知识点 水的分解氢气可用于火箭燃料,是未来理想的高能燃料,从能源角度分析,利用电解水的方法获得大量氢气是否可行? 不可行。利用电解水的方法获得氢气的过程中,会消耗大量的电能。在我国,电能的获得大部分来自于火力发电,从而消耗大量的化石燃料,且会造成一系列的环境污染,所以不能用电解水的方法获得大量的氢气。知识点 水的分解水的性质: (1)物理性质:纯水是一种无色、无臭、无味、透明的液体。纯水不易导电。在常压下,水的凝固点(冰点)是0 ℃,沸点是100 ℃,在4 ℃时水的密度为1 g/cm3,此时密度最大。水结冰时体积膨胀,所以冰的密度比水小,能浮在水面上。 (2)化学性质:①水在通电条件下能分解,生成氢气和氧气。②水还能与某些物质发生反应,如水能和二氧化碳反应等(第六单元中会学)。知识点 水的分解检验氢气纯度的方法(1)操作方法(如图):①用拇指堵住集满氢气的试管口;②靠近火焰,移开拇指点火。(2)结论:①若点燃时,发出尖锐的爆鸣声,说明气体不纯,这样的氢气不能进行点燃;②若点燃时,有轻微的爆鸣声,说明气体较纯净,可以被点燃。知识点 水的分解氢气的用途:(1)由于氢气是密度最小的气体,可用于探空气球。知识点 水的分解①氢气作为新型燃料的优点:热值高、无污染、原料丰富。②目前还不能普遍使用的原因是:制取成本较高,难以保存和运输。③现在比较成熟制取氢气的方法是:在光照和某些特殊物质(能加快反应速率,但本身在反应前后质量不变)的作用下,使水迅速分解生成氢气和氧气。知识点 水的分解 为了保证安全,点燃任何可燃性的气体(如氢气、一氧化碳、甲烷等)之前都应检验纯度。知识点 物质的物理性质和化学性质(1)溶解性 溶解性是物质在形成溶液时的一种物理性质。它是指物质在一种特定溶剂里溶解能力大小的一种属性。(2)延展性 延展性是物质的物理属性,指可锤炼、可延展的程度。物体在外力作用下能延伸成细丝而不断裂的性质叫延性,在外力(锤击或滚轧)作用下能碾成薄片而不破裂的性质叫展性。知识点 物质的物理性质和化学性质 判断某种叙述是指物质的“性质”还是“变化”时,首先要准确把握它们的区别和联系,若叙述中“能”“难”“易”“会”“就”等词语,往往指性质;若叙述中有“已经”“了”“在”等词语,往往指物质的变化。第二单元 走进化学世界第三节:原子的构成知识点 原子的结构以碳原子为例描述原子的构成: 构成碳原子的粒子有6个质子、6个中子和6个电子。其中6个质子和6个中子构成了原子核,作为原子的中心,而6个电子在核外一定空间内绕核做高速运动。知识点 原子的结构 现代科学研究发现,质子和中子等微粒也有内部结构,它们是由一种叫作“夸克”的更小的微粒构成知识点 原子的结构分子一定比原子大吗? 分子不一定比原子大。但分子一定比构成它的原子大,对于其他原子则要视情况而定。知识点 原子质量的计量 碳原子有多种,它们的质子数都是6,但中子数不同,有6、7、8等,这里所说的一种碳原子是指含有6个质子和6个中子的碳原子,简称碳12,其质量的1/12约为1.66×10-27kg,近似等于1个质子或1个中子的实际质量。知识点 原子质量的计量 在各粒子之间的等量关系中,等式“核内质子数=核电荷数=原子序数(原子序数是指元素在元素周期表中的序号,数值上等于原子的核电荷数)”是恒成立的,当它们与核外电子数相等时,只有在原子中成立(即该等号不适用于离子,因为原子在变成相应的离子时,核外电子是有得失的);当它们与“相对原子质量-核内中子数”相等时,是根据相对原子质量的计算公式,通过变形而近似得来的。知识点 原子质量的计量 贝采利乌斯是第一位把原子量测得比较精确的化学家。他在1814~1826年的12年里连续发表了三张原子量表,所列元素多达49种。知识点 原子中的电子 在原子中,电子层并不是真实存在的,只是科学家为了研究方便进行的一种人为规定,是理想上的假设而已。知识点 原子中的电子 电子在原子核外排布时,要尽可能使电子的能量最低。比如说,我们站在地面上,不会觉得有什么危险;如果我们站在20层楼的顶上,再往下看时我们心理会感到害怕。这是因为物体在越高处具有的势能越大,物体总有从高处往低处运动的趋势,就像自由落体一样,我们从来没有见过物体会自动从地面上升到空中,物体要从地面到空中,必须要有外力的作用。电子本身就是一种物质,也具有同样的性质。知识点 离子(1)符号的意义①Na:表示钠元素或一个钠原子。②Na+:一个钠离子。2Na+:两个钠离子。(2)数字的意义mRn+ 或mRn-:n表示一个离子所带电荷的数值,m表示离子的个数。知识点 原子质量的计量 (1)电荷数和正负号的书写位置和语言习惯对应,如:一个镁离子带两个单位的正电荷,先写“2”,后写“+”。 (2)离子符号前的数字只决定离子的个数,元素符号右上角的数字永远是一个离子所带电荷的数值。第二单元 走进化学世界第四节:元 素知识点 元 素 同一种元素可以存在于不同的物质中,如氧气、二氧化碳中都含有氧元素;同一种元素可以形成多种物质,如氧气、臭氧(O3)都是由氧元素组成的物质。知识点 元 素元素的简单分类:知识点 多种多样的物质及其组成与构成物质的构成: (1)由分子构成的物质,有三种说法(以二氧化碳为例):①二氧化碳是由氧元素和碳元素组成的。 ②二氧化碳是由二氧化碳分子构成的。 ③每个二氧化碳分子是由2个氧原子和1个碳原子构成的。 (2)由原子(或离子)直接构成的物质(如汞、食盐),有两种说法:①汞是由汞元素组成的;食盐是由钠元素和氯元素组成的。②汞是由汞原子构成的;食盐是由钠离子和氯离子构成的。知识点 元素符号 有些元素的元素符号可采用形象的方法记忆。例如,钨元素(W),可以联想白炽灯内的钨丝,酷似“W”形;硫元素(S),可以联想起弯弯曲曲的小溪中的流水,形如“S”状;氧元素(O),可以联想圆圆的太阳形状;钾元素(K),可以联想到剪指甲时张开的剪刀的形状。知识点 元素周期表简介 俄国化学家门捷列夫最早发现并提出了元素周期表。每一周期开头的都是金属元素(第一周期除外),靠近尾部的是非金属元素,结尾是稀有气体元素,这种规律性的变化正是“周期性”的具体体现,它反映了元素之间的内在联系。知识点 元素周期表简介 2017年5月9日,经过公众提议、两岸协商、专家研讨和学界征询等程序,中国科学院、国家语言文字工作委员会、全国科学技术名词审定委员会在京联合发布了113号、115号、117号和118号4个新合成元素的中文名称, ,依次为“ (nǐ)、“镆”(mò)、 (tián)、 (ào)。 这4个新元素的英文名称和元素符号,已在2016年11月30日由负责管理元素符号的国际化学组织“国际纯粹与应用化学联合会”(IUPAC)正式发布,加上之前的114号和116号元素,元素周期表中的第7周期被全部填满。第二单元 走进化学世界到实验去:化学实验基本技能训练(二)实验全面解读 托盘天平的精确度是0.1 g,若要更准确称量一定质量的物质,可使用分析天平,能精确称量到0.0001 g。实验全面解读 当使用天平时,用到游码,药品和砝码位置放反,会使称量药品质量偏小。理由是:正常放置时,药品的质量=砝码质量+游码示数,放反后,则变成:药品的质量=砝码质量-游码示数。实验全面解读 量筒上的刻度是指温度在20 ℃时的液体体积。温度升高,量筒发生热膨胀,容积会增大。由此可知,量筒是不能加热的,也不能用于量取过热的液体,更不能在量筒中进行化学反应或配制溶液。实验全面解读(1)要量出一杯水的体积。方法:
①选择大小合适的量筒。即选用体积略大于一杯水体积的量筒。
②将烧杯中的水倒入量筒中。
③将量筒放平,平视凹液面的最低点,读数即为这杯水的体积。若俯视,读数偏高;若仰视,则读数偏低。
(2)要量取80mL的水。方法:
①选择100mL的量筒。
②向量筒中倾倒水至接近80mL刻度线时,改用胶头滴管滴加水至视线与凹液面的最低点在同一水平线上,所量取水的体积即为80mL。若俯视读数,则实际量偏少;若仰视读数,则实际量偏多。实验全面解读 1.在使用铁架台固定、装配或连接装置时,操作顺序是从下到上,从左到右,而拆卸时的顺序,却正好相反,这也是实验的基本原则。 2.在装配或连接多个相对独立的装置时,还要考虑到单个装置的功能和实验的目的等。实验全面解读检查气密性的其他方法:A B实验全面解读洗涤玻璃仪器时的工具——洗瓶: 洗瓶是化学实验室中用于装清洗溶液的一种容器,洗瓶是用以喷注细股水流达到冲洗试剂、沉淀以及洗涤器皿的一种盛水容器。主要用于清洗仪器、设备、装置等。谢 谢
①选择大小合适的量筒。即选用体积略大于一杯水体积的量筒。
②将烧杯中的水倒入量筒中。
③将量筒放平,平视凹液面的最低点,读数即为这杯水的体积。若俯视,读数偏高;若仰视,则读数偏低。
(2)要量取80mL的水。方法:
①选择100mL的量筒。
②向量筒中倾倒水至接近80mL刻度线时,改用胶头滴管滴加水至视线与凹液面的最低点在同一水平线上,所量取水的体积即为80mL。若俯视读数,则实际量偏少;若仰视读数,则实际量偏多。实验全面解读 1.在使用铁架台固定、装配或连接装置时,操作顺序是从下到上,从左到右,而拆卸时的顺序,却正好相反,这也是实验的基本原则。 2.在装配或连接多个相对独立的装置时,还要考虑到单个装置的功能和实验的目的等。实验全面解读检查气密性的其他方法:A B实验全面解读洗涤玻璃仪器时的工具——洗瓶: 洗瓶是化学实验室中用于装清洗溶液的一种容器,洗瓶是用以喷注细股水流达到冲洗试剂、沉淀以及洗涤器皿的一种盛水容器。主要用于清洗仪器、设备、装置等。谢 谢
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
