人教版高中化学必修2第三章《 有机化合物》单元检测题(含答案)
文档属性
| 名称 | 人教版高中化学必修2第三章《 有机化合物》单元检测题(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 162.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-06-05 00:00:00 | ||
图片预览


文档简介
《有机化合物》单元检测题
一、单选题
1.把体积相同的甲烷和氯气充入一个集气瓶中,光照一段时间后,发现气体的黄绿色变浅,集气瓶壁上有淡黄绿色液滴,此时集气瓶内的物质最多可能有( )
A.4种 B.5种 C.6种 D.7种
2.对于下列实验事实的解释,不合理的是( )
选项 实验事实 解释
A 加热蒸干MgSO4溶液能得到MgSO4固体;加热蒸干MgCl2溶液得不到MgCl2固体 H2SO4不易挥发,HCl易挥发
B 电解CuCl2溶液阴极得到Cu;电解NaCl溶液,阴极得不到Na 得电子能力:Cu2+>Na+>H+
C 浓HNO3能氧化NO;稀HNO3不能氧化NO HNO3浓度越大,氧化性越强
D 钠与水反应剧烈;钠与乙醇反应平缓 羟基中氢的活泼性:H2O> C2H5OH
A.A B.B C.C D.D
3.高粱酿酒属于以下哪种利用方式( )
A.直接燃烧 B.生物热化学转化 C.生物化学转化 D.热化学转化
4.关于有机化合物下列说法正确的是( )
A.直链烷烃正戊烷的所有碳原子在一条直线上
B.分子式为C5H10O2的有机物能与NaHCO3溶液反应放出CO2的同分异构体有4种
C.甲烷中混有乙烯,可直接将混合物通入酸性KMnO4中除去乙烯得到纯净的甲烷
D.甲苯和液溴在FeBr3作催化剂的条件下可发生取代反应生成4种一溴代物
5.既可用来鉴别乙烯和甲烷,又可用来除去甲烷中混有的乙烯的方法是( )
A.慢慢通入水中 B.催化加氢
C.慢慢地通入溴水中 D.慢慢地通入酸性高锰酸钾溶液中
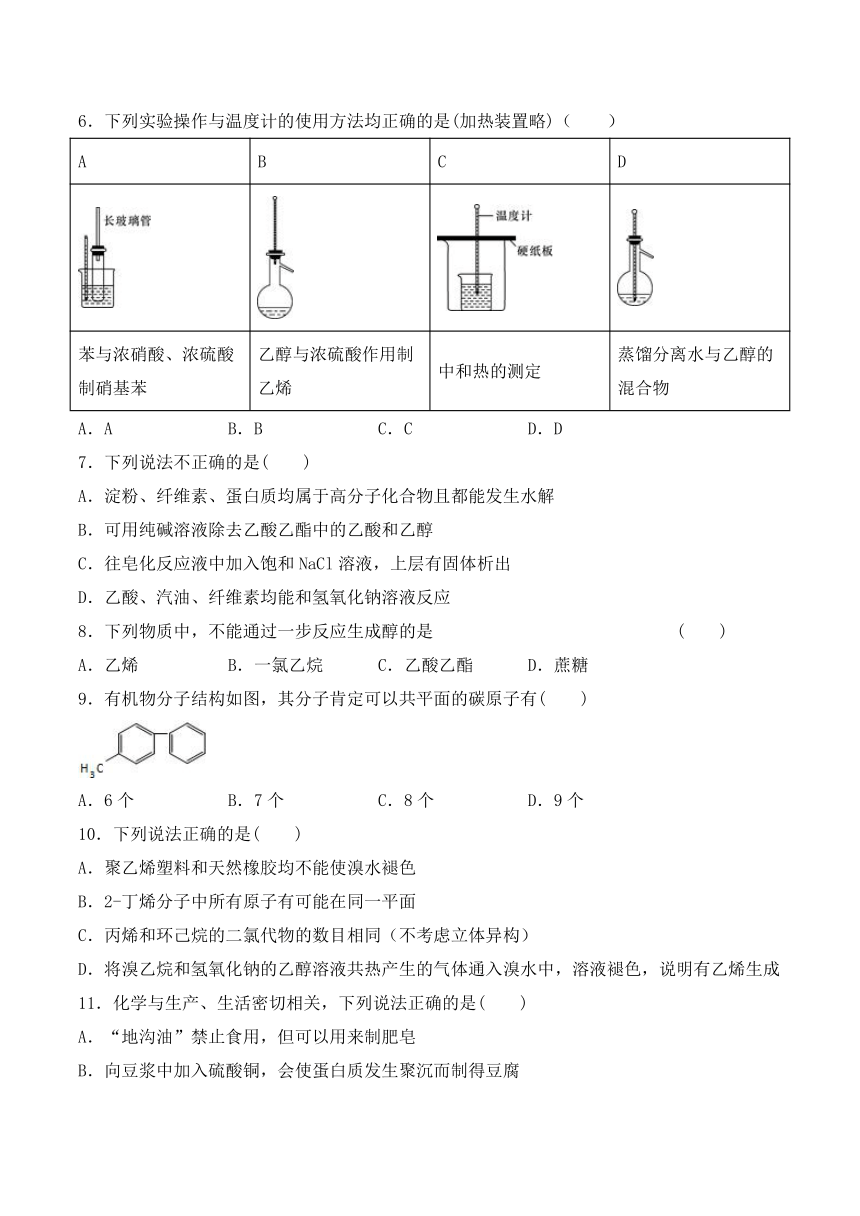
6.下列实验操作与温度计的使用方法均正确的是(加热装置略)( )
A B C D
苯与浓硝酸、浓硫酸制硝基苯 乙醇与浓硫酸作用制乙烯 中和热的测定 蒸馏分离水与乙醇的混合物
A.A B.B C.C D.D
7.下列说法不正确的是( )
A.淀粉、纤维素、蛋白质均属于高分子化合物且都能发生水解
B.可用纯碱溶液除去乙酸乙酯中的乙酸和乙醇
C.往皂化反应液中加入饱和NaCl溶液,上层有固体析出
D.乙酸、汽油、纤维素均能和氢氧化钠溶液反应
8.下列物质中,不能通过一步反应生成醇的是 ( )
A.乙烯 B.一氯乙烷 C.乙酸乙酯 D.蔗糖
9.有机物分子结构如图,其分子肯定可以共平面的碳原子有( )
A.6个 B.7个 C.8个 D.9个
10.下列说法正确的是( )
A.聚乙烯塑料和天然橡胶均不能使溴水褪色
B.2-丁烯分子中所有原子有可能在同一平面
C.丙烯和环己烷的二氯代物的数目相同(不考虑立体异构)
D.将溴乙烷和氢氧化钠的乙醇溶液共热产生的气体通入溴水中,溶液褪色,说明有乙烯生成
11.化学与生产、生活密切相关,下列说法正确的是( )
A.“地沟油”禁止食用,但可以用来制肥皂
B.向豆浆中加入硫酸铜,会使蛋白质发生聚沉而制得豆腐
C.纤维素在人体内可水解为葡萄糖,故可做人类的营养物质
D.合成纤维、人造纤维及碳纤维都属于有机高分子材料
12.苯乙烯是重要的化工原料。下列有关苯乙烯的说法错误的是( )
A.与液溴混合后加入铁粉可发生取代反应
B.与氯化氢反应可以生成氯代苯乙烯
C.能使酸性高锰酸钾溶液褪色
D.在催化剂存在下可以制得聚苯乙烯
13.下列关于物质性质的比较,不正确的是( )
A.沸点:C2H5OH>CH3CH3 B.水的电离程度:100℃>25℃
C.溶解度:AgI>AgCl D.完全燃烧放出的热量:1mol C>1mol CO
14.关于蔗糖的说法中错误的是( )
A.蔗糖是最重要的二糖,它的相对分子质量是葡萄糖相对分子质量的两倍
B.纯净的蔗糖溶液中加入银氨溶液微热,不发生银镜反应
C.在蔗糖与稀硫酸共热后的溶液中滴加银氨溶液,用水浴加热,看不到银镜生成
D.在蔗糖里加入浓硫酸,可观察到颜色变黑,并有泡沫出现
15.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实不能说明上述观点的是( )
A.乙酸分子中羟基上的氢原子较乙醇中羟基上的氢原子更活泼
B.苯酚能和氢氧化钠溶液反应,而乙醇不能和氢氧化钠溶液反应
C.甲苯的硝化反应较苯更容易
D.乙烯能发生加成反应,而乙烷不能发生加成反应
二、实验题
16.下面为甲、乙、丙三位同学制取乙酸乙酯的实验过程。
(实验目的)制取乙酸乙酯。
(实验原理)甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯。
1.(装置设计)甲、乙、丙三位同学分别设计了下列三套实验装置:
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,不应选择的装置是____(填“甲”或“乙”)。丙同学装置中的球形干燥管,除起冷凝作用外,另一重要作用是______。
2.(实验步骤)
(1)按选择的装置组装仪器,在试管中先加入amLCH3CH218OH(密度为ρg/cm-3)和过量的冰醋酸(CH3COOH),并边振荡边缓缓加入2mL浓H2SO4;
(2)将试管固定在铁架台上;
(3)在试管②中加入适量的饱和Na2CO3溶液;
(4)用酒精灯对试管①加热;
(5)当观察到试管②中有明显现象时认为反应基本完成。
(问题讨论)
a.按步骤(1)装好实验装置,加入药品前还应______。
b.在(5)中,当观察到试管②中有______现象时认为反应基本完成。
c.分离试管②中的混合物可以得到产品及回收未反应的乙酸和乙醇,实验操作流程如下:
在上述实验操作流程中,所涉及的①②③三次分离操作分别是:______。
d.已知在酸与醇的酯化反应中,反应的原理是酸失去羟基,醇失去氢原子结合成水。请写出试管①中生成乙酸乙酯反应的化学方程式(注明反应条件)_____________。
最后得到纯净的乙酸乙酯bg,求本实验中乙酸乙酯的产率:______(用a、b、ρ表示)。
三、推断题
17.物质M是一种酰胺类局麻药,某研究小组以A、E两种烃为有机原料,按以下路线合成M
已知:①;②;
③。
请回答:
(1)化合物G的结构简式为______。
(2)下列说法不正确的是_________。
A.A→B为氧化反应
B.化合物G能与浓盐酸反应形成盐
C.化合物H与NaOH溶液反应最多消耗2molNaOH
D.局麻药M的分子式为C14H20N2O
(3)写出D+G→H的化学方程式:____________。
(4)写出满足下列条件的化合物F的所有同分异构体的结构简式________。
ⅰ.能与FeCl3溶液发生显色反应
ⅱ.能发生银镜反应
ⅲ.苯环上只有两个取代基且苯环上只有2种不同环境的氢原子
(5)该小组成员还提出另一种合成M的方案:化合物C与二乙胺[HN(CH2CH3)2]反应制取化合物X,X与G经一步反应即可制得药物M。请设计以烃A为原料制备化合物X的合成路线___________________________(用流程图表示,无机试剂任选)。
18.下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
族 周期 IA 0
1 ① ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧
(1)④、⑤、⑥的离子半径由大到小的顺序为__________________。(用离子符号)
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_______________ 。(用化学式)
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______________。
(4)由表中①④两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________ _。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中①②两种元素可以组成多种烃,若原子也按1:1组成的常见液态化合物是重要的化工原料,也是常见的有机溶剂,写出该物质与硝酸发生反应的化学方程式: _______________。
(6)⑥的单质在⑤的最高价氧化物对应水化物中反应的离子方程式为:________________。
四、计算题
19.在①CH4、②C2H2、③C2H4、④C2H6、⑤苯中
(1)能使酸性高锰酸钾溶液褪色的是__________。(填序号,下同)
(2)相同物质的量,在氧气中完全燃烧时消耗氧气最多的是________;
(3)相同质量,在氧气中完全燃烧时消耗氧气最多的是____,耗氧量、生成CO2和水都相等的是___________。
参考答案
1.D 2.B 3.C 4.B 5.C 6.A 7.D 8.D 9.D 10.D 11.A 12.B 13.C 14.A 15.D
16.甲 防倒吸 检查装置的气密性 油状液体不再增多时(大量油状液体生成时也可) 分液、蒸馏、蒸馏 CH3CH218OH+CH3COOHCH3CO18OCH2CH3+H2O 24b/45aρ或0.53b/aρ
17. AD ClCH2COCl++HCl 、、、
18.O2->Na+>Al3+ HNO3>H2CO3>H2SiO3 (或) ab +HNO3+H2O 2Al+2OH-+2H2O=2AlO2-+3H2↑
19.②③ ⑤ ① ②⑤
一、单选题
1.把体积相同的甲烷和氯气充入一个集气瓶中,光照一段时间后,发现气体的黄绿色变浅,集气瓶壁上有淡黄绿色液滴,此时集气瓶内的物质最多可能有( )
A.4种 B.5种 C.6种 D.7种
2.对于下列实验事实的解释,不合理的是( )
选项 实验事实 解释
A 加热蒸干MgSO4溶液能得到MgSO4固体;加热蒸干MgCl2溶液得不到MgCl2固体 H2SO4不易挥发,HCl易挥发
B 电解CuCl2溶液阴极得到Cu;电解NaCl溶液,阴极得不到Na 得电子能力:Cu2+>Na+>H+
C 浓HNO3能氧化NO;稀HNO3不能氧化NO HNO3浓度越大,氧化性越强
D 钠与水反应剧烈;钠与乙醇反应平缓 羟基中氢的活泼性:H2O> C2H5OH
A.A B.B C.C D.D
3.高粱酿酒属于以下哪种利用方式( )
A.直接燃烧 B.生物热化学转化 C.生物化学转化 D.热化学转化
4.关于有机化合物下列说法正确的是( )
A.直链烷烃正戊烷的所有碳原子在一条直线上
B.分子式为C5H10O2的有机物能与NaHCO3溶液反应放出CO2的同分异构体有4种
C.甲烷中混有乙烯,可直接将混合物通入酸性KMnO4中除去乙烯得到纯净的甲烷
D.甲苯和液溴在FeBr3作催化剂的条件下可发生取代反应生成4种一溴代物
5.既可用来鉴别乙烯和甲烷,又可用来除去甲烷中混有的乙烯的方法是( )
A.慢慢通入水中 B.催化加氢
C.慢慢地通入溴水中 D.慢慢地通入酸性高锰酸钾溶液中
6.下列实验操作与温度计的使用方法均正确的是(加热装置略)( )
A B C D
苯与浓硝酸、浓硫酸制硝基苯 乙醇与浓硫酸作用制乙烯 中和热的测定 蒸馏分离水与乙醇的混合物
A.A B.B C.C D.D
7.下列说法不正确的是( )
A.淀粉、纤维素、蛋白质均属于高分子化合物且都能发生水解
B.可用纯碱溶液除去乙酸乙酯中的乙酸和乙醇
C.往皂化反应液中加入饱和NaCl溶液,上层有固体析出
D.乙酸、汽油、纤维素均能和氢氧化钠溶液反应
8.下列物质中,不能通过一步反应生成醇的是 ( )
A.乙烯 B.一氯乙烷 C.乙酸乙酯 D.蔗糖
9.有机物分子结构如图,其分子肯定可以共平面的碳原子有( )
A.6个 B.7个 C.8个 D.9个
10.下列说法正确的是( )
A.聚乙烯塑料和天然橡胶均不能使溴水褪色
B.2-丁烯分子中所有原子有可能在同一平面
C.丙烯和环己烷的二氯代物的数目相同(不考虑立体异构)
D.将溴乙烷和氢氧化钠的乙醇溶液共热产生的气体通入溴水中,溶液褪色,说明有乙烯生成
11.化学与生产、生活密切相关,下列说法正确的是( )
A.“地沟油”禁止食用,但可以用来制肥皂
B.向豆浆中加入硫酸铜,会使蛋白质发生聚沉而制得豆腐
C.纤维素在人体内可水解为葡萄糖,故可做人类的营养物质
D.合成纤维、人造纤维及碳纤维都属于有机高分子材料
12.苯乙烯是重要的化工原料。下列有关苯乙烯的说法错误的是( )
A.与液溴混合后加入铁粉可发生取代反应
B.与氯化氢反应可以生成氯代苯乙烯
C.能使酸性高锰酸钾溶液褪色
D.在催化剂存在下可以制得聚苯乙烯
13.下列关于物质性质的比较,不正确的是( )
A.沸点:C2H5OH>CH3CH3 B.水的电离程度:100℃>25℃
C.溶解度:AgI>AgCl D.完全燃烧放出的热量:1mol C>1mol CO
14.关于蔗糖的说法中错误的是( )
A.蔗糖是最重要的二糖,它的相对分子质量是葡萄糖相对分子质量的两倍
B.纯净的蔗糖溶液中加入银氨溶液微热,不发生银镜反应
C.在蔗糖与稀硫酸共热后的溶液中滴加银氨溶液,用水浴加热,看不到银镜生成
D.在蔗糖里加入浓硫酸,可观察到颜色变黑,并有泡沫出现
15.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实不能说明上述观点的是( )
A.乙酸分子中羟基上的氢原子较乙醇中羟基上的氢原子更活泼
B.苯酚能和氢氧化钠溶液反应,而乙醇不能和氢氧化钠溶液反应
C.甲苯的硝化反应较苯更容易
D.乙烯能发生加成反应,而乙烷不能发生加成反应
二、实验题
16.下面为甲、乙、丙三位同学制取乙酸乙酯的实验过程。
(实验目的)制取乙酸乙酯。
(实验原理)甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯。
1.(装置设计)甲、乙、丙三位同学分别设计了下列三套实验装置:
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,不应选择的装置是____(填“甲”或“乙”)。丙同学装置中的球形干燥管,除起冷凝作用外,另一重要作用是______。
2.(实验步骤)
(1)按选择的装置组装仪器,在试管中先加入amLCH3CH218OH(密度为ρg/cm-3)和过量的冰醋酸(CH3COOH),并边振荡边缓缓加入2mL浓H2SO4;
(2)将试管固定在铁架台上;
(3)在试管②中加入适量的饱和Na2CO3溶液;
(4)用酒精灯对试管①加热;
(5)当观察到试管②中有明显现象时认为反应基本完成。
(问题讨论)
a.按步骤(1)装好实验装置,加入药品前还应______。
b.在(5)中,当观察到试管②中有______现象时认为反应基本完成。
c.分离试管②中的混合物可以得到产品及回收未反应的乙酸和乙醇,实验操作流程如下:
在上述实验操作流程中,所涉及的①②③三次分离操作分别是:______。
d.已知在酸与醇的酯化反应中,反应的原理是酸失去羟基,醇失去氢原子结合成水。请写出试管①中生成乙酸乙酯反应的化学方程式(注明反应条件)_____________。
最后得到纯净的乙酸乙酯bg,求本实验中乙酸乙酯的产率:______(用a、b、ρ表示)。
三、推断题
17.物质M是一种酰胺类局麻药,某研究小组以A、E两种烃为有机原料,按以下路线合成M
已知:①;②;
③。
请回答:
(1)化合物G的结构简式为______。
(2)下列说法不正确的是_________。
A.A→B为氧化反应
B.化合物G能与浓盐酸反应形成盐
C.化合物H与NaOH溶液反应最多消耗2molNaOH
D.局麻药M的分子式为C14H20N2O
(3)写出D+G→H的化学方程式:____________。
(4)写出满足下列条件的化合物F的所有同分异构体的结构简式________。
ⅰ.能与FeCl3溶液发生显色反应
ⅱ.能发生银镜反应
ⅲ.苯环上只有两个取代基且苯环上只有2种不同环境的氢原子
(5)该小组成员还提出另一种合成M的方案:化合物C与二乙胺[HN(CH2CH3)2]反应制取化合物X,X与G经一步反应即可制得药物M。请设计以烃A为原料制备化合物X的合成路线___________________________(用流程图表示,无机试剂任选)。
18.下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
族 周期 IA 0
1 ① ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧
(1)④、⑤、⑥的离子半径由大到小的顺序为__________________。(用离子符号)
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_______________ 。(用化学式)
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______________。
(4)由表中①④两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________ _。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中①②两种元素可以组成多种烃,若原子也按1:1组成的常见液态化合物是重要的化工原料,也是常见的有机溶剂,写出该物质与硝酸发生反应的化学方程式: _______________。
(6)⑥的单质在⑤的最高价氧化物对应水化物中反应的离子方程式为:________________。
四、计算题
19.在①CH4、②C2H2、③C2H4、④C2H6、⑤苯中
(1)能使酸性高锰酸钾溶液褪色的是__________。(填序号,下同)
(2)相同物质的量,在氧气中完全燃烧时消耗氧气最多的是________;
(3)相同质量,在氧气中完全燃烧时消耗氧气最多的是____,耗氧量、生成CO2和水都相等的是___________。
参考答案
1.D 2.B 3.C 4.B 5.C 6.A 7.D 8.D 9.D 10.D 11.A 12.B 13.C 14.A 15.D
16.甲 防倒吸 检查装置的气密性 油状液体不再增多时(大量油状液体生成时也可) 分液、蒸馏、蒸馏 CH3CH218OH+CH3COOHCH3CO18OCH2CH3+H2O 24b/45aρ或0.53b/aρ
17. AD ClCH2COCl++HCl 、、、
18.O2->Na+>Al3+ HNO3>H2CO3>H2SiO3 (或) ab +HNO3+H2O 2Al+2OH-+2H2O=2AlO2-+3H2↑
19.②③ ⑤ ① ②⑤
