人教新版第7章《燃料及其利用》同步训练(word版有答案)
文档属性
| 名称 | 人教新版第7章《燃料及其利用》同步训练(word版有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 180.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-06-10 00:00:00 | ||
图片预览

文档简介
2019年第7章《燃料及其利用》同步训练
附相对原子质量:H-1;C-12;O-16;S-32;Ca-40
一、选择题:(每题只有一个正确答案,共20分)
1、2018年11月12日,我国大型科学装置“人造太阳”取得重大突破,实现加热功率超过10兆瓦,等离子体储能增加到300千焦,等离子体中心电子温度首次达到1亿度。相比于核裂变,“人造太阳”产生的核聚变可以释放更大的能量,而且不会产生放射性废料,属于清洁能源。下列说法不正确的是( )
A.有利于治理雾霾污染
B.可以减少酸雨的形成
C.可以减少白色污染
D.可以减少化石能源的使用分
2、2019年4月15日傍晚,巴黎圣母院失火,文化损失惨重令人痛心。日常生活中的下列灭火方法不正确的是( )
A.电器着火直接用水灭火
B.图书档案着火用液态二氧化碳灭火器灭火
C.锅内的油着火用锅盖盖灭
D.酒精洒出着火用湿抹布盖灭
3、我市今年扩大了烟花爆竹的禁放区域。如图表示“禁止燃放烟花爆竹”标志的是( )
4、小东发现野营篝火的火焰很小,于是就将木柴架空了些,他这样做主要目的是( )
A.方便添加木柴 B.使木柴与空气充分接触
C.降低木柴的着火点 D.为了升高木柴的温度
5、如图是探究燃烧条件的实验装置图,下列说法中错误的是( )
A.铜片的作用是传递热量
B.A.热水的作用是提供热量和隔绝空气
C.铜片上红磷不燃烧是因为红磷不是可燃物
D.热水中白磷不燃烧是因为没有与氧气接触
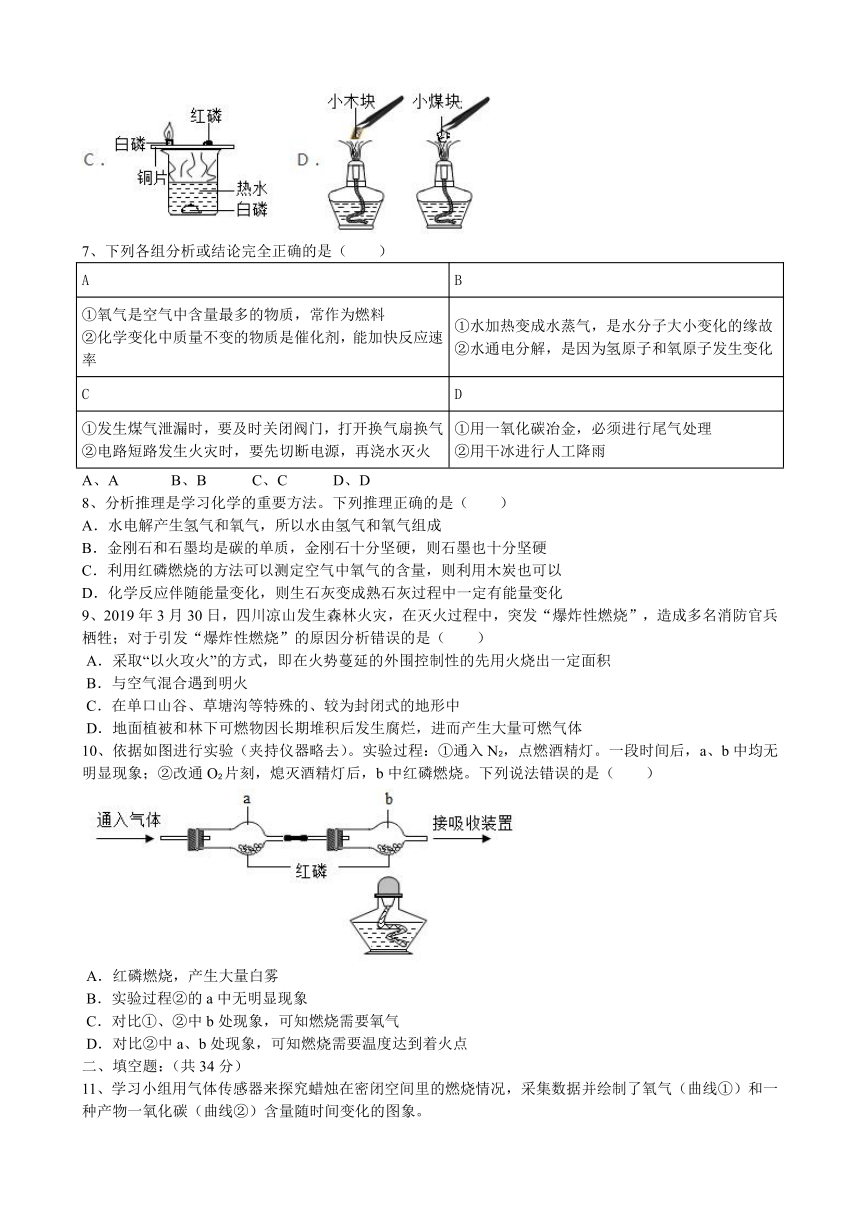
6、下列探究燃烧条件的实验中,只能得出“燃烧需要氧气”结论的是( )
7、下列各组分析或结论完全正确的是( )
A
B
①氧气是空气中含量最多的物质,常作为燃料 ②化学变化中质量不变的物质是催化剂,能加快反应速率
①水加热变成水蒸气,是水分子大小变化的缘故 ②水通电分解,是因为氢原子和氧原子发生变化
C
D
①发生煤气泄漏时,要及时关闭阀门,打开换气扇换气 ②电路短路发生火灾时,要先切断电源,再浇水灭火
①用一氧化碳冶金,必须进行尾气处理 ②用干冰进行人工降雨
A、A B、B C、C D、D
8、分析推理是学习化学的重要方法。下列推理正确的是( )
A.水电解产生氢气和氧气,所以水由氢气和氧气组成
B.金刚石和石墨均是碳的单质,金刚石十分坚硬,则石墨也十分坚硬
C.利用红磷燃烧的方法可以测定空气中氧气的含量,则利用木炭也可以
D.化学反应伴随能量变化,则生石灰变成熟石灰过程中一定有能量变化
9、2019年3月30日,四川凉山发生森林火灾,在灭火过程中,突发“爆炸性燃烧”,造成多名消防官兵栖牲;对于引发“爆炸性燃烧”的原因分析错误的是( )
A.采取“以火攻火”的方式,即在火势蔓延的外围控制性的先用火烧出一定面积
B.与空气混合遇到明火
C.在单口山谷、草塘沟等特殊的、较为封闭式的地形中
D.地面植被和林下可燃物因长期堆积后发生腐烂,进而产生大量可燃气体
10、依据如图进行实验(夹持仪器略去)。实验过程:①通入N2,点燃酒精灯。一段时间后,a、b中均无明显现象;②改通O2片刻,熄灭酒精灯后,b中红磷燃烧。下列说法错误的是( )
A.红磷燃烧,产生大量白雾
B.实验过程②的a中无明显现象
C.对比①、②中b处现象,可知燃烧需要氧气
D.对比②中a、b处现象,可知燃烧需要温度达到着火点
二、填空题:(共34分)
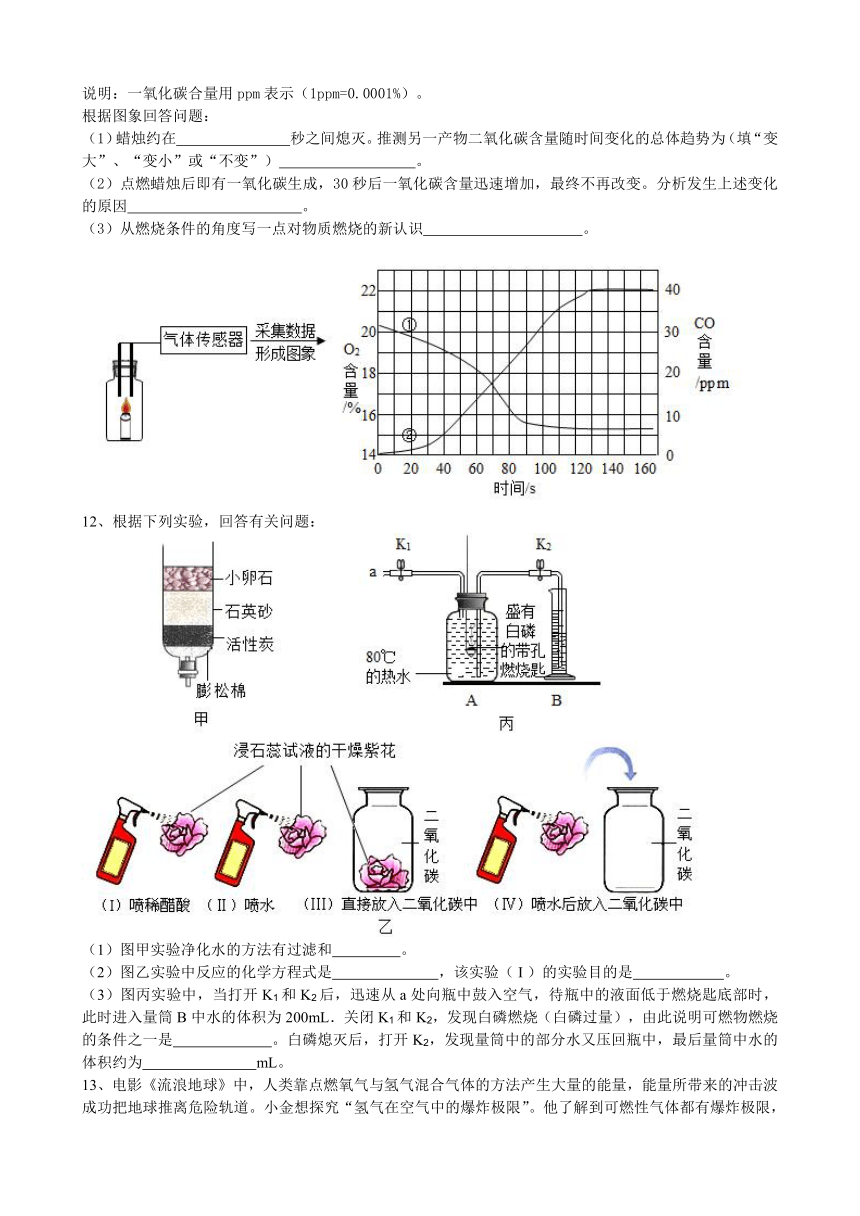
11、学习小组用气体传感器来探究蜡烛在密闭空间里的燃烧情况,采集数据并绘制了氧气(曲线①)和一种产物一氧化碳(曲线②)含量随时间变化的图象。 说明:一氧化碳合量用ppm表示(1ppm=0.0001%)。 根据图象回答问题: (1)蜡烛约在 秒之间熄灭。推测另一产物二氧化碳含量随时间变化的总体趋势为(填“变大”、“变小”或“不变”) 。 (2)点燃蜡烛后即有一氧化碳生成,30秒后一氧化碳含量迅速增加,最终不再改变。分析发生上述变化的原因 。 (3)从燃烧条件的角度写一点对物质燃烧的新认识 。
12、根据下列实验,回答有关问题:
(1)图甲实验净化水的方法有过滤和 。 (2)图乙实验中反应的化学方程式是 ,该实验(?I?)的实验目的是 。 (3)图丙实验中,当打开K1和K2后,迅速从a处向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,此时进入量筒B中水的体积为200mL.关闭K1和K2,发现白磷燃烧(白磷过量),由此说明可燃物燃烧的条件之一是 。白磷熄灭后,打开K2,发现量筒中的部分水又压回瓶中,最后量筒中水的体积约为 mL。
13、电影《流浪地球》中,人类靠点燃氧气与氢气混合气体的方法产生大量的能量,能量所带来的冲击波成功把地球推离危险轨道。小金想探究“氢气在空气中的爆炸极限”。他了解到可燃性气体都有爆炸极限,低于爆炸下限时不爆炸也不着火,高于爆炸上限时不会爆炸会燃烧。他在老师指导下设计并完成了如下实验:
步骤1:利用实验室制取氢气类似的装置,如图甲,用矿泉水瓶收集体积分数分别是5%~100%的氢气若干瓶; 步骤2:将瓶子倒扣后打开瓶塞,架在火柴梗上,如图乙,用另一根火柴点燃氢气,实验现象如表:
H2体积分数/%
5
10
20
30
40
50
60
70
80
90
点燃时的现象
不燃不爆
弱 爆炸
强 爆炸
强 爆炸
强 爆炸
强 爆炸
强 爆炸
弱 爆炸
安静燃烧
安静燃烧
(1)步骤1中收集一瓶体积分数为50%氢气的方法是 ; (2)根据实验现象,氢气在空气中的爆炸极限是 ; (3)小金觉得上述结论的范围还可以更加精确,下一步操作是 。
14、氢能为21世纪最清洁的能源,也是重要的化工原料。 (1)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为 。 (2)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
写出反应I中,发生反应的化学方程式: 。该反应 置换反应(属于或者不属于)。 (3)氢化镁(MgH2)是一种贮氢合金,当它与H2O混合时释放出氢气,同时生成一种碱,该反应的化学方程式是 。
15、蜡烛在密闭装置中燃烧至熄灭,装置中究竟有没有氧气剩余? 某兴趣小组设计了如图所示的实验,请回答下列问题:
(1)图1中气球的作用是 ,集气瓶底部铺一薄层细沙的目的是 。 (2)热水提供的热量就能引燃白磷,主要利用白磷 的性质。 (3)写出能验证蜡烛中含有碳元素的一个化学方程式为 。 (4)通过观察图1和图2的实验现象,可以得出相同情况下蜡烛或白磷在密闭装置中燃烧至熄灭,装置中 (填“蜡烛”或“白磷”)燃烧后氧气剩余较多。 (5)若用蜡烛燃烧测定空气中氧气的含量会导致测量结果偏小的原因可能是: (写出一条即可)。 (6)进一步探究各物质在密闭装置中燃烧至熄灭,用手持技术定量检测氧气的剩余量,结果如图所示:
①用上述三种物质测定空气中的氧气含量时,利用哪种物质燃烧使得实验结果更准确? (填物质名称)。 ②上述三种物质同时在同一个密闭容器中燃烧,哪一种物质燃烧时间最长? 。导致这种现象的可能原因是 。
三、计算题:(共6分)
16、工业上用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙)。主要的反应为 2CaCO3+2SO2+O2=2CaSO4+2CO2, (1)碳酸钙中钙元素的质量分数为 。 (2)吸收32t二氧化硫能获得含80%硫酸钙的石膏多少吨?
参考答案
一、选择题:
1
2
3
4
5
6
7
8
9
10
C
A
B
B
C
B
D
D
A
A
二、填空题:
11、答案
解:(1)由图象可知,氧气的浓度在90~100秒之前时不再改变,说明蜡烛约在90~100秒之间熄灭;蜡烛燃烧还会生成二氧化碳,所以二氧化碳含量随时间变化的总体趋势增大;故填:90~100;增大; (2)因为点燃蜡烛,焰心和内焰处的石蜡蒸气无法与氧气充分接触而发生不充分燃烧,30秒后,氧气含量迅速降低,更多的石蜡蒸气燃烧不充分生成一氧化碳,氧气含量降低到一定程度后,蜡烛熄灭,反应停止,所以点燃蜡烛后即有一氧化碳生成,30秒后一氧化碳含量迅速增加,最终不再改变;故填:点燃蜡烛,焰心和内焰处的石蜡蒸气无法与氧气充分接触而发生不充分燃烧,30秒后,氧气含量迅速降低,更多的石蜡蒸气燃烧不充分生成一氧化碳,氧气含量降低到一定程度后,蜡烛熄灭,反应停止; (3)由图象数据可知,物质燃烧需要氧气达到一定浓度才能发生;故填:物质燃烧需要氧气达到一定浓度才能发生。
12、解:(1)图中纱布、小卵石、石英砂可以起过滤作用,活性炭具有吸附性,可以吸附色素和异味,甲实验净化水的方法是过滤和吸附;故填:吸附; (2)二氧化碳与水反应生成碳酸,化学方程式为H2O+CO2═H2CO3,实验(I)的目的是证明酸能使石蕊试液变红色,实验对照;故填:CO2+H2O=H2CO3;证明酸能使石蕊试液变红色,实验对照; (3)图丙实验中,当打开K1和K2后,迅速从a处向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,此时进入量筒B中水的体积为200mL.关闭K1和K2,发现白磷燃烧(白磷过量),由此说明可燃物燃烧的条件之一是与氧气接触;实验中进入量筒B中水的体积为200mL,即A瓶内空气的体积为200mL,因为氧气约占空气体积的五分之一,所以足量的白磷燃烧后消耗氧气的体积为:40mL,白磷熄灭后,打开K2,发现量筒中的部分水(40mL)又压回瓶中,最后量筒中水的体积约为200mL-40mL=160mL;故填:与氧气接触;160。
13、解:(1)收集一瓶体积分数为50%氢气的方法是往瓶子内先装一半水,然后用排水法将水排出;故填:往瓶子内先装一半水,然后用排水法将水排出; (2)根据实验现象与数据可知,氢气在空气中的爆炸极限是10%-70%;故填:10%-70%; (3)若将爆炸范围测定的更精确,可进行如下操作取氢气体积分数在5%-10%,70%-80%区间以1%为梯度做点燃实验,观察是否会爆炸。故填:取氢气体积分数在5%-10%,70%-80%区间以1%为梯度做点燃实验,观察是否会爆炸。
14、解:(1)由质量守恒定律可知,化学反应前后,原子的种类与数目保持不变,反应前:1个钙原子、1个硅原子、3个氧原子、6个氢原子、6个氟原子;反应后:1个硅原子、4个氟原子、6个氢原子、3个氧原子,所以X中含有1个钙原子和2个氟原子,其化学式为CaF2; 故填:CaF2; (2)由图可知,反应I为二氧化硫、水与碘发生反应生成硫酸和HI,化学方程式为:SO2+2H2O+I2=H2SO4+2HI;置换反应是单质与化合物反应生成单质与化合物,故该反应不属于置换反应; 故填:SO2+I2+2H2O=H2SO4+2HI;不属于; (3)氢化镁(MgH2)是一种贮氢合金,当它与H2O混合时释放出氢气,同时生成一种碱,该反应的化学方程式是:MgH2+2H2O=Mg(OH)2+2H2↑; 故填:MgH2+2H2O=Mg(OH)2+2H2↑。
15、解:(1)图1中蜡烛燃烧产生二氧化并放热,白磷燃烧也放热,瓶内气体会急剧膨胀,气球的作用就是缓冲气体压力;集气瓶底部铺一薄层细沙的目的是防止 生成的高温五氧化二磷炸裂瓶底; (2)白磷的着火点很低,有热水就可以引燃; (3)白磷燃烧的化学方程式为4P+5O22P2O5 (4)通过观察图1与图2中蜡烛的位置较高以及实验现象,可以得出相同情况下蜡烛或白磷在密闭装置中燃烧至熄灭,蜡烛燃烧后剩余的氧气较多; (5)蜡烛与氧气反应生成的是气体,会占据空间,水进入装置内不到其容积的五分之一; ①用上述三种物质测定空气中的氧气含量时,由表中的数据可知,白磷消耗的氧气多,剩余的氧气的量少,所以,利用白磷质燃烧使得实验结果更准确; ②上述三种物质同时在同一个密闭容器中燃烧,白磷燃烧时间最长,由表中的数据可知,导致这种现象的可能原因是在氧气的浓度较低时白磷还能与氧气反应。 故答案为:(1)缓冲气体压力;防止生成的高温五氧化二磷炸裂瓶底; (2)着火点低; (3)4P+5O22P2O5; (4)蜡烛; (5)蜡烛燃烧后生成二氧化碳气体; (6)①白磷;②在氧气的浓度较低时白磷还能与氧气反应。
三、计算题:
16、解:(1)碳酸钙中钙元素的质量分数为:
(2)设吸收32t二氧化硫能获得硫酸钙的质量为x。 2CaCO3+2SO2+O2=2CaSO4+2CO2 ?????????????? 128?????????? 272 ????????????????32t???????????? x
则,解得x=68t 故吸收32t二氧化硫能获得含80%硫酸钙的石膏的质量为:68t÷80%=85t。
附相对原子质量:H-1;C-12;O-16;S-32;Ca-40
一、选择题:(每题只有一个正确答案,共20分)
1、2018年11月12日,我国大型科学装置“人造太阳”取得重大突破,实现加热功率超过10兆瓦,等离子体储能增加到300千焦,等离子体中心电子温度首次达到1亿度。相比于核裂变,“人造太阳”产生的核聚变可以释放更大的能量,而且不会产生放射性废料,属于清洁能源。下列说法不正确的是( )
A.有利于治理雾霾污染
B.可以减少酸雨的形成
C.可以减少白色污染
D.可以减少化石能源的使用分
2、2019年4月15日傍晚,巴黎圣母院失火,文化损失惨重令人痛心。日常生活中的下列灭火方法不正确的是( )
A.电器着火直接用水灭火
B.图书档案着火用液态二氧化碳灭火器灭火
C.锅内的油着火用锅盖盖灭
D.酒精洒出着火用湿抹布盖灭
3、我市今年扩大了烟花爆竹的禁放区域。如图表示“禁止燃放烟花爆竹”标志的是( )
4、小东发现野营篝火的火焰很小,于是就将木柴架空了些,他这样做主要目的是( )
A.方便添加木柴 B.使木柴与空气充分接触
C.降低木柴的着火点 D.为了升高木柴的温度
5、如图是探究燃烧条件的实验装置图,下列说法中错误的是( )
A.铜片的作用是传递热量
B.A.热水的作用是提供热量和隔绝空气
C.铜片上红磷不燃烧是因为红磷不是可燃物
D.热水中白磷不燃烧是因为没有与氧气接触
6、下列探究燃烧条件的实验中,只能得出“燃烧需要氧气”结论的是( )
7、下列各组分析或结论完全正确的是( )
A
B
①氧气是空气中含量最多的物质,常作为燃料 ②化学变化中质量不变的物质是催化剂,能加快反应速率
①水加热变成水蒸气,是水分子大小变化的缘故 ②水通电分解,是因为氢原子和氧原子发生变化
C
D
①发生煤气泄漏时,要及时关闭阀门,打开换气扇换气 ②电路短路发生火灾时,要先切断电源,再浇水灭火
①用一氧化碳冶金,必须进行尾气处理 ②用干冰进行人工降雨
A、A B、B C、C D、D
8、分析推理是学习化学的重要方法。下列推理正确的是( )
A.水电解产生氢气和氧气,所以水由氢气和氧气组成
B.金刚石和石墨均是碳的单质,金刚石十分坚硬,则石墨也十分坚硬
C.利用红磷燃烧的方法可以测定空气中氧气的含量,则利用木炭也可以
D.化学反应伴随能量变化,则生石灰变成熟石灰过程中一定有能量变化
9、2019年3月30日,四川凉山发生森林火灾,在灭火过程中,突发“爆炸性燃烧”,造成多名消防官兵栖牲;对于引发“爆炸性燃烧”的原因分析错误的是( )
A.采取“以火攻火”的方式,即在火势蔓延的外围控制性的先用火烧出一定面积
B.与空气混合遇到明火
C.在单口山谷、草塘沟等特殊的、较为封闭式的地形中
D.地面植被和林下可燃物因长期堆积后发生腐烂,进而产生大量可燃气体
10、依据如图进行实验(夹持仪器略去)。实验过程:①通入N2,点燃酒精灯。一段时间后,a、b中均无明显现象;②改通O2片刻,熄灭酒精灯后,b中红磷燃烧。下列说法错误的是( )
A.红磷燃烧,产生大量白雾
B.实验过程②的a中无明显现象
C.对比①、②中b处现象,可知燃烧需要氧气
D.对比②中a、b处现象,可知燃烧需要温度达到着火点
二、填空题:(共34分)
11、学习小组用气体传感器来探究蜡烛在密闭空间里的燃烧情况,采集数据并绘制了氧气(曲线①)和一种产物一氧化碳(曲线②)含量随时间变化的图象。 说明:一氧化碳合量用ppm表示(1ppm=0.0001%)。 根据图象回答问题: (1)蜡烛约在 秒之间熄灭。推测另一产物二氧化碳含量随时间变化的总体趋势为(填“变大”、“变小”或“不变”) 。 (2)点燃蜡烛后即有一氧化碳生成,30秒后一氧化碳含量迅速增加,最终不再改变。分析发生上述变化的原因 。 (3)从燃烧条件的角度写一点对物质燃烧的新认识 。
12、根据下列实验,回答有关问题:
(1)图甲实验净化水的方法有过滤和 。 (2)图乙实验中反应的化学方程式是 ,该实验(?I?)的实验目的是 。 (3)图丙实验中,当打开K1和K2后,迅速从a处向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,此时进入量筒B中水的体积为200mL.关闭K1和K2,发现白磷燃烧(白磷过量),由此说明可燃物燃烧的条件之一是 。白磷熄灭后,打开K2,发现量筒中的部分水又压回瓶中,最后量筒中水的体积约为 mL。
13、电影《流浪地球》中,人类靠点燃氧气与氢气混合气体的方法产生大量的能量,能量所带来的冲击波成功把地球推离危险轨道。小金想探究“氢气在空气中的爆炸极限”。他了解到可燃性气体都有爆炸极限,低于爆炸下限时不爆炸也不着火,高于爆炸上限时不会爆炸会燃烧。他在老师指导下设计并完成了如下实验:
步骤1:利用实验室制取氢气类似的装置,如图甲,用矿泉水瓶收集体积分数分别是5%~100%的氢气若干瓶; 步骤2:将瓶子倒扣后打开瓶塞,架在火柴梗上,如图乙,用另一根火柴点燃氢气,实验现象如表:
H2体积分数/%
5
10
20
30
40
50
60
70
80
90
点燃时的现象
不燃不爆
弱 爆炸
强 爆炸
强 爆炸
强 爆炸
强 爆炸
强 爆炸
弱 爆炸
安静燃烧
安静燃烧
(1)步骤1中收集一瓶体积分数为50%氢气的方法是 ; (2)根据实验现象,氢气在空气中的爆炸极限是 ; (3)小金觉得上述结论的范围还可以更加精确,下一步操作是 。
14、氢能为21世纪最清洁的能源,也是重要的化工原料。 (1)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为 。 (2)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
写出反应I中,发生反应的化学方程式: 。该反应 置换反应(属于或者不属于)。 (3)氢化镁(MgH2)是一种贮氢合金,当它与H2O混合时释放出氢气,同时生成一种碱,该反应的化学方程式是 。
15、蜡烛在密闭装置中燃烧至熄灭,装置中究竟有没有氧气剩余? 某兴趣小组设计了如图所示的实验,请回答下列问题:
(1)图1中气球的作用是 ,集气瓶底部铺一薄层细沙的目的是 。 (2)热水提供的热量就能引燃白磷,主要利用白磷 的性质。 (3)写出能验证蜡烛中含有碳元素的一个化学方程式为 。 (4)通过观察图1和图2的实验现象,可以得出相同情况下蜡烛或白磷在密闭装置中燃烧至熄灭,装置中 (填“蜡烛”或“白磷”)燃烧后氧气剩余较多。 (5)若用蜡烛燃烧测定空气中氧气的含量会导致测量结果偏小的原因可能是: (写出一条即可)。 (6)进一步探究各物质在密闭装置中燃烧至熄灭,用手持技术定量检测氧气的剩余量,结果如图所示:
①用上述三种物质测定空气中的氧气含量时,利用哪种物质燃烧使得实验结果更准确? (填物质名称)。 ②上述三种物质同时在同一个密闭容器中燃烧,哪一种物质燃烧时间最长? 。导致这种现象的可能原因是 。
三、计算题:(共6分)
16、工业上用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙)。主要的反应为 2CaCO3+2SO2+O2=2CaSO4+2CO2, (1)碳酸钙中钙元素的质量分数为 。 (2)吸收32t二氧化硫能获得含80%硫酸钙的石膏多少吨?
参考答案
一、选择题:
1
2
3
4
5
6
7
8
9
10
C
A
B
B
C
B
D
D
A
A
二、填空题:
11、答案
解:(1)由图象可知,氧气的浓度在90~100秒之前时不再改变,说明蜡烛约在90~100秒之间熄灭;蜡烛燃烧还会生成二氧化碳,所以二氧化碳含量随时间变化的总体趋势增大;故填:90~100;增大; (2)因为点燃蜡烛,焰心和内焰处的石蜡蒸气无法与氧气充分接触而发生不充分燃烧,30秒后,氧气含量迅速降低,更多的石蜡蒸气燃烧不充分生成一氧化碳,氧气含量降低到一定程度后,蜡烛熄灭,反应停止,所以点燃蜡烛后即有一氧化碳生成,30秒后一氧化碳含量迅速增加,最终不再改变;故填:点燃蜡烛,焰心和内焰处的石蜡蒸气无法与氧气充分接触而发生不充分燃烧,30秒后,氧气含量迅速降低,更多的石蜡蒸气燃烧不充分生成一氧化碳,氧气含量降低到一定程度后,蜡烛熄灭,反应停止; (3)由图象数据可知,物质燃烧需要氧气达到一定浓度才能发生;故填:物质燃烧需要氧气达到一定浓度才能发生。
12、解:(1)图中纱布、小卵石、石英砂可以起过滤作用,活性炭具有吸附性,可以吸附色素和异味,甲实验净化水的方法是过滤和吸附;故填:吸附; (2)二氧化碳与水反应生成碳酸,化学方程式为H2O+CO2═H2CO3,实验(I)的目的是证明酸能使石蕊试液变红色,实验对照;故填:CO2+H2O=H2CO3;证明酸能使石蕊试液变红色,实验对照; (3)图丙实验中,当打开K1和K2后,迅速从a处向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,此时进入量筒B中水的体积为200mL.关闭K1和K2,发现白磷燃烧(白磷过量),由此说明可燃物燃烧的条件之一是与氧气接触;实验中进入量筒B中水的体积为200mL,即A瓶内空气的体积为200mL,因为氧气约占空气体积的五分之一,所以足量的白磷燃烧后消耗氧气的体积为:40mL,白磷熄灭后,打开K2,发现量筒中的部分水(40mL)又压回瓶中,最后量筒中水的体积约为200mL-40mL=160mL;故填:与氧气接触;160。
13、解:(1)收集一瓶体积分数为50%氢气的方法是往瓶子内先装一半水,然后用排水法将水排出;故填:往瓶子内先装一半水,然后用排水法将水排出; (2)根据实验现象与数据可知,氢气在空气中的爆炸极限是10%-70%;故填:10%-70%; (3)若将爆炸范围测定的更精确,可进行如下操作取氢气体积分数在5%-10%,70%-80%区间以1%为梯度做点燃实验,观察是否会爆炸。故填:取氢气体积分数在5%-10%,70%-80%区间以1%为梯度做点燃实验,观察是否会爆炸。
14、解:(1)由质量守恒定律可知,化学反应前后,原子的种类与数目保持不变,反应前:1个钙原子、1个硅原子、3个氧原子、6个氢原子、6个氟原子;反应后:1个硅原子、4个氟原子、6个氢原子、3个氧原子,所以X中含有1个钙原子和2个氟原子,其化学式为CaF2; 故填:CaF2; (2)由图可知,反应I为二氧化硫、水与碘发生反应生成硫酸和HI,化学方程式为:SO2+2H2O+I2=H2SO4+2HI;置换反应是单质与化合物反应生成单质与化合物,故该反应不属于置换反应; 故填:SO2+I2+2H2O=H2SO4+2HI;不属于; (3)氢化镁(MgH2)是一种贮氢合金,当它与H2O混合时释放出氢气,同时生成一种碱,该反应的化学方程式是:MgH2+2H2O=Mg(OH)2+2H2↑; 故填:MgH2+2H2O=Mg(OH)2+2H2↑。
15、解:(1)图1中蜡烛燃烧产生二氧化并放热,白磷燃烧也放热,瓶内气体会急剧膨胀,气球的作用就是缓冲气体压力;集气瓶底部铺一薄层细沙的目的是防止 生成的高温五氧化二磷炸裂瓶底; (2)白磷的着火点很低,有热水就可以引燃; (3)白磷燃烧的化学方程式为4P+5O22P2O5 (4)通过观察图1与图2中蜡烛的位置较高以及实验现象,可以得出相同情况下蜡烛或白磷在密闭装置中燃烧至熄灭,蜡烛燃烧后剩余的氧气较多; (5)蜡烛与氧气反应生成的是气体,会占据空间,水进入装置内不到其容积的五分之一; ①用上述三种物质测定空气中的氧气含量时,由表中的数据可知,白磷消耗的氧气多,剩余的氧气的量少,所以,利用白磷质燃烧使得实验结果更准确; ②上述三种物质同时在同一个密闭容器中燃烧,白磷燃烧时间最长,由表中的数据可知,导致这种现象的可能原因是在氧气的浓度较低时白磷还能与氧气反应。 故答案为:(1)缓冲气体压力;防止生成的高温五氧化二磷炸裂瓶底; (2)着火点低; (3)4P+5O22P2O5; (4)蜡烛; (5)蜡烛燃烧后生成二氧化碳气体; (6)①白磷;②在氧气的浓度较低时白磷还能与氧气反应。
三、计算题:
16、解:(1)碳酸钙中钙元素的质量分数为:
(2)设吸收32t二氧化硫能获得硫酸钙的质量为x。 2CaCO3+2SO2+O2=2CaSO4+2CO2 ?????????????? 128?????????? 272 ????????????????32t???????????? x
则,解得x=68t 故吸收32t二氧化硫能获得含80%硫酸钙的石膏的质量为:68t÷80%=85t。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
