人教版(五四)八年级化学 5.化学方程式 单元练习(含解析)
文档属性
| 名称 | 人教版(五四)八年级化学 5.化学方程式 单元练习(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 157.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-06-24 00:00:00 | ||
图片预览



文档简介
人教版(五四)八年级化学跟踪训练 5.化学方程式
一、单选题
1.用“○”和“●”表示不同元素的原子,下列微观示意图能表示化合物的是(?? )
A.???????????????????????????????????????????B.?? C.????????????????????????????????????????????D.?
2.一根蘸有浓盐酸的玻璃棒与另一根蘸有浓氨水的玻璃棒靠近时(未接触),产生大量白烟,其反应的微观示意图如下。下列说法错误的是 (?? )
A.?反应前后原子的种类和个数不变?????????????????????????B.?两根玻璃棒未接触就反应,说明分子是在不停运动的 C.?反应产生的白烟是氯化铵固体小颗粒??????????????????D.?产生白烟的化学方程式为:NH3+HCl=NH3Cl
3.如图是某化学反应的微观模型,“ ”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是(?? )
A.?该反应一定是氧化反应???????????????????????????????????????B.?反应物和生成物中只有一种单质 C.?反应中共有两种元素参与????????????????????????????????????D.?参加反应的两种物质分子个数之比为2:3
4.图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子。下列说法 正确的是(?? )
A.?反应后的物质一定是氧化物????????????????????????????????B.?反应前后各元素的化合价都没有改变 C.?该反应属于化合反应???????????????????????????????????????????D.?该反应中分子和原子的种类均没有改变
5.在加压条件下,25m3的石油气(含丙烷、丁烷等气体)可以装入0.024m3的钢瓶中,由此可以说明的是(?? )
A.?分子的质量很小????????????B.?分子由原子构成????????????C.?分子之间有间隔????????????D.?分子在不断地运动
6.H2、O2和N2组成的混合气体20g,经点燃充分反应后生成18g水,则剩余的气体不可能是(????)
A.?N2和H2?????????????????????????B.?N2和O2?????????????????????????C.?N2 、H2和O2?????????????????????????D.?只有2gN2
7.点燃20克含有O2、H2、N2的混合气体,充分反应后生成18克水,则剩余气体不可能是( )
A.?2克N2???????????B.?O2、N2的混合气体???????C.?H2、N2的混合气体???????????D.?O2、H2、N2的混合气体
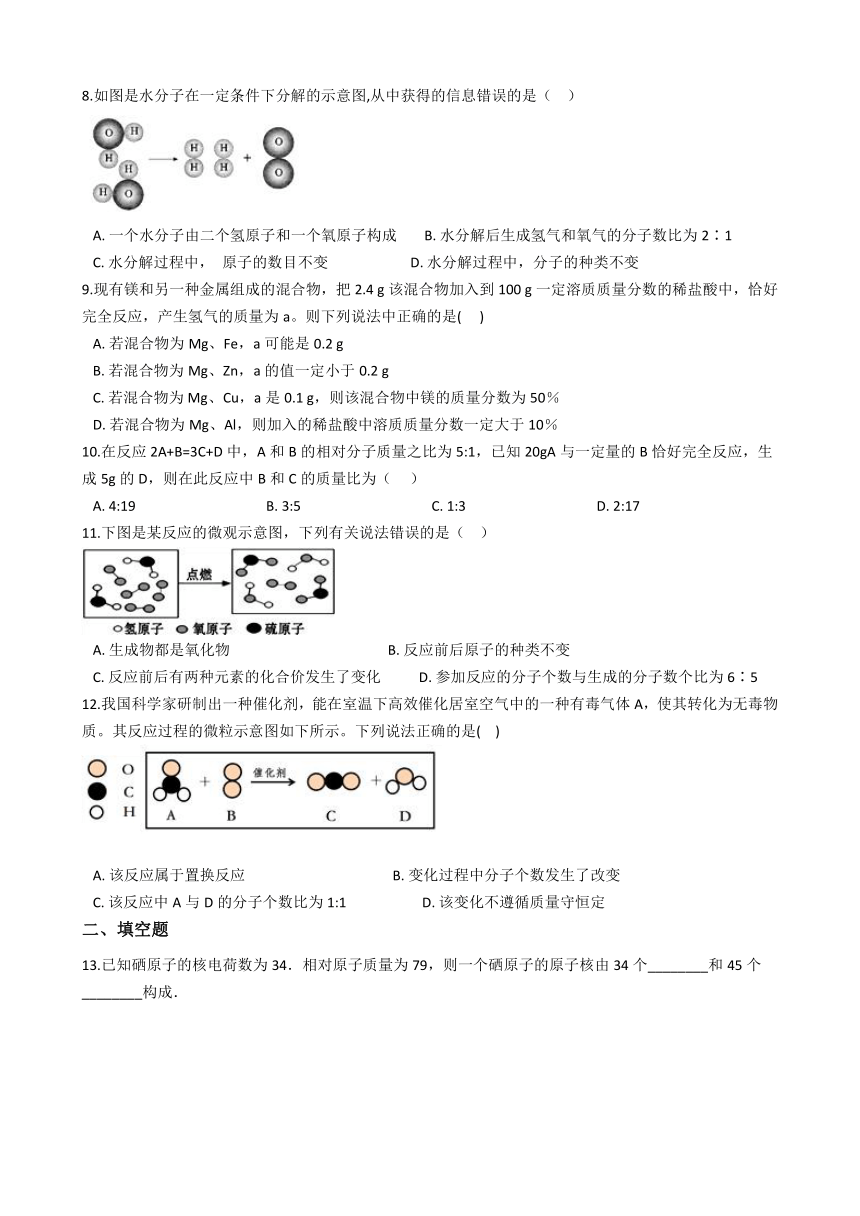
8.如图是水分子在一定条件下分解的示意图,从中获得的信息错误的是(?? )
A.?一个水分子由二个氢原子和一个氧原子构成????????B.?水分解后生成氢气和氧气的分子数比为2∶1 C.?水分解过程中, 原子的数目不变????????????????????????D.?水分解过程中,分子的种类不变
9.现有镁和另一种金属组成的混合物,把2.4 g该混合物加入到100 g一定溶质质量分数的稀盐酸中,恰好完全反应,产生氢气的质量为a。则下列说法中正确的是(??? )
A.?若混合物为Mg、Fe,a可能是0.2 g B.?若混合物为Mg、Zn,a的值一定小于0.2 g C.?若混合物为Mg、Cu,a是0.1 g,则该混合物中镁的质量分数为50% D.?若混合物为Mg、Al,则加入的稀盐酸中溶质质量分数一定大于10%
10.在反应2A+B=3C+D中,A和B的相对分子质量之比为5:1,已知20gA与一定量的B恰好完全反应,生成5g的D,则在此反应中B和C的质量比为(??? )
A.?4:19??????????????????????????????????????B.?3:5??????????????????????????????????????C.?1:3??????????????????????????????????????D.?2:17
11.下图是某反应的微观示意图,下列有关说法错误的是(?? )
A.?生成物都是氧化物??????????????????????????????????????????????B.?反应前后原子的种类不变 C.?反应前后有两种元素的化合价发生了变化???????????D.?参加反应的分子个数与生成的分子数个比为6∶5
12.我国科学家研制出一种催化剂,能在室温下高效催化居室空气中的一种有毒气体A,使其转化为无毒物质。其反应过程的微粒示意图如下所示。下列说法正确的是(?? )
A.?该反应属于置换反应???????????????????????????????????????????B.?变化过程中分子个数发生了改变 C.?该反应中A与D的分子个数比为1:1??????????????????????D.?该变化不遵循质量守恒定
二、填空题
13.已知硒原子的核电荷数为34.相对原子质量为79,则一个硒原子的原子核由34个________和45个________构成.
14.如图是某个化学反应前后各种物质微观模拟图,图中“ ”“ ”表示不同元素的原子。根据图示判断,该反应属于________反应
15.镁在空气中燃烧生成氧化镁,此反应中Mg、O2、MgO的质量比为________.
三、解答题
16.家用漂白剂的有效成分是次氯酸钠(NaClO),其制备反应的化学方程式是:Cl2+2NaOH═NaCl+NaClO+H2O.若要制备149kg的次氯酸钠,则理论上需要氢氧化钠的质量是多少?
四、综合题
17.随着科学的发展,新能源的开发不断取得突破。清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下图(图中的微粒恰 好完全反应)所示。请根据微观示意图回答以下问题。
(1)丁的化学式为________,该反应的化学方程式为________。
(2)下列说法正确的是______(填写字母序号)。
A.?反应前后原子数目发生改变?????????????????????????????????B.?该反应属于复分解反应 C.?甲是单质,乙、丙、丁均为化合物??????????????????????D.?该反应体现了无机物在一定条件下可以转化为有机物
18. 用电石(主要成分为CaC2)与水反应可制取乙炔,最终还可得到电石渣.某电石渣中含氢氧化钙92.5%,其余为杂质,此电石渣可用于处理电镀厂排出的酸性废水.请完成:
(1)乙炔(C2H2)是生产聚氯乙烯的重要原料.聚氯乙烯属于________材料(填合金或有机合成或无机非金属或复合).
(2)100kg上述电石渣中氢氧化钙的质量为________kg.
(3)用上述电石渣处理含硫酸196kg的酸性废水(假设电石渣中的杂质、废水中其他成分均不参加反应),求至少需要这种电石渣的质量(写出计算过程及结果)
答案解析部分
一、单选题
1.【答案】B
【解析】【解答】A、A中有两种分子,是混合物,A不符合题意;
B、B中只有一种分子,且是由两种元素组成的物质,是化合物,B符合题意;
C、C中由一种分子组成,这种物质是由一种元素组成的,是单质,C不符合题意;
D、该图中是混合物,D不符合题意。
故答案为: B。
【分析】模型题主要是根据模型写出物质的化学式,再结合相关定义进行判断。
2.【答案】 D
【解析】【解答】A.根据化学微观反应示意图可知,反应前后原子的种类和个数不变,故A不符合题意,
B.两根玻璃棒未接触就反应,说明分子是在不停运动的,故B不符合题意;
C.反应产生的白烟是氯化铵固体小颗粒,故C不符合题意;
D.产生白烟的化学方程式为:NH3+HCl=NH4Cl,
故答案为:D。
【分析】此类题目应先根据题目提示,书写出负的化学方程式,然后根据化学方程式做答;此题的化学方程式为:NH3+HCl=NH4Cl
3.【答案】 C
【解析】【解答】A、物质与氧气的反应属于氧化反应;不确定反应物是否有氧气,不能确定是否是氧化反应,错误;A不符合题意; B、由一种元素组成的纯净物叫单质;所以两种反应物都是单质,错误;B不符合题意; C,元素是同类原子的总称,由图可知,反应中共有两种元素参与,正确;C符合题意; D. 化学反应前后原子的种类、个数不变,所以参加反应的两种物质分子个数之比为1:3,错误。D不符合题意; 故答案为:C
【分析】根据图例写出每个微粒所代表的物质化学式,然后根据化学式判断每个物质所属的物质类别,根据题意写出反应的化学方程式,要把前后相同大的微粒划去,然后根据方程式的意义分析逐步解答;依据图例正确书写各物质的化学式是解题的关键;化学反应前后原子的种类个数没有改变;由两种或两种以上物质生成一种物质的反应叫化合反应;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物;
4.【答案】 C
【解析】【解答】A、二种元素组成其中一种是氧元素的为氧化物,图中无法确定是否含有氧元素,A不符合题意; B、元素在单质中化合价为0,在化合价中一定不为0,由此,两种元素的化合价都一定改变了,B不符合题意; C、由图是两种微粒生成了一种,即两种物质生成了一种,属于化合反应,C符合题意; D、化学反应中原子种类不变,但分子种类一定改变,D不符合题意。 故答案为:C。
【分析】模型题关键是根据模型写出物质的化学方程式,再根据化学方程式吉祥相关计算即可。
5.【答案】 C
【解析】【解答】解:25m3的石油气(含丙烷、丁烷等气体)可以装入0.024m3的钢瓶中,说明分子之间有间隔,并且间隔较大.
故选C
【分析】微观粒子的特征:质量和体积都很小;微粒与微粒之间有间隙;都是不断运动的.
6.【答案】 C
【解析】
【分析】根据氢气和氧气反应会生成水进行分析;
【解答】所谓充分反应就是能够反应的不能同时剩余. A、氢气过量后会剩余氢气,氮气不会和氢气、氧气反应,可能; B、氧气过量后会剩余氧气,氮气不会和氢气、氧气反应,可能; C、氢气和氧气会生成水,不会同时剩余,不可能; D、氮气的化学性质稳定,不会与氢气、氧气反应,可能. 故选C.
【点评】在解此类题时,首先分析题中气体的性质,然后结合选项中的气体进行分析
7.【答案】 D
【解析】【解答】解:A、如果氢气和氧气恰好完全反应,则剩余气体是氮气,故A正确;
B、如果氧气过量,则剩余气体是氮气和氧气,故B正确;
C、如果氢气过量,则剩余气体是氮气和氢气,故C正确;
D、氢气和氧气不可能同时剩余,即剩余气体不可能是H2、O2和N2 , 故D错误.
故选:D.
【分析】根据氢气和氧气反应生成水,在点燃条件下,氮气不能和氢气、氧气反应.所以该题中的三种气体具有可燃性的气体只有H2 , 所以对混合气体点燃,完全反应后剩余气体中氢气和氧气不可能同时存在进行分析.
8.【答案】 D
【解析】【解答】A.由图可见,一个水分子是由2个氢原子和1个氧原子构成的,A选项不符合题意;
B.由图可知,水分解后,产生氢气和氧气的分子数比值为2:1,B选项不符合题意;
C.由图可知,反应前有6个原子,反应后有6个原子,原子数目没有改变,C选项不符合题意;
D.由图可知,反应前有水分子,反应后有氢分子和氧分子,分子种类发生改变,D选项符合题意。
故答案为:D
【分析】水分解过程中,水分子发生了改变,生成了氢分子和氧分子.化学反应前后原子的种类没有改变.一个水分子是由二个氢原子和一个氧原子构成的.水分解后生成氢气和氧气的分子数比为2:1。
9.【答案】 D
【解析】【解答】根据极值法计算,假设合金中镁的质量为2.4g,利用镁和稀盐酸反应的方程式可得生成氢气质量为0.2g,同理计算出2.4g铝与稀盐酸反应生成氢气的质量大于0.2g,2.4g锌、2.4g铁与相同的稀盐酸反应生成的氢气小于0.2g A? 若混合物为Mg、Fe,a一定小于0.2g,A不符合题意 B 若混合物为Mg、Zn, a的值一定小于0.2 g,B符合题意 C 若混合物为Mg、Cu, a是0.1 g,则该混合物中镁的质量分数大于50% ,C不符合题意 D当粉末是镁、铝合金时,因相同质量的铝消耗盐酸的质量比镁的大,2.4g镁消耗盐酸7.3g,所以合金为镁铝合金时,所需盐酸的质量分数一定大于7.3%,不符合题意
故答案为:B
【分析】因为金属与酸反应生成氢气的质量=金属的质量,所以等质量的镁与盐酸反应生成的氢气的质量大于锌、铁,而小于铝,据此分析解答
10.【答案】 D
【解析】【解答】解:令A与B的相对分子质量为5和1,设恰好与A反应的B的质量为x,则:
2A+
B=3C+D
10
1
20g
x
?
解得x═2g,则由20g A与2g B恰好完全反应,生成5g D,生成C的质量为:20g+2g-5g═17g
则在此反应中B和C的质量比为:2g:17g═2:17。
故答案为:D。
【分析】根据方程式中质量定比关系计算参加反应的的B的质量,再根据质量守恒定律计算C的质量,进而计算B和C的质量比
11.【答案】 D
【解析】【解答】依据反应前后物质的分子结构可知反应物是氧气和硫化氢,生成物是水和二氧化硫,则反应方程式为3O2+2H2S 2H2O+2SO2;
A、根据化学方程式可知生成物是水和二氧化硫,都属于氧化物,不符合题意;
B、由图示或化学方程式可知,化学反应前后原子的种类不变,不符合题意;
C、由方程式可知氧元素由0变成了-2价,硫元素由-2价变成了+4价,氢元素的化合价不变,有两种元素的化合价发生了改变,不符合题意;
D、由化学方程式可知,参加反应的两种分子的个数之比为3:2,符合题意。
故答案为:D。
【分析】有关微观模拟图的题目在解答时,要根据反应前后各微粒的构成确定反应物和生成物,或写出反应方程式,或直接判断参加反应和生成的微粒的个数,要注意反应后有反应物剩余的微观图,不能误以为反应后物质都是生成物。
12.【答案】 C
【解析】【解答】A、由一种单质和一种化合物生成另一种化合物和另一种化合物的反应叫置换反应,该反应的两种生成物都是化合物,不可能是置换反应;A不符合题意 B、由质量守恒定律可知反应前后原子的种类个数不变,所以该反应中分子个数没有发生改变,B不符合题意 C. 由题中信息可知,该反应中A与D的分子个数比为1:1? ,C符合题意 ? D. 所有化学变化中原子的种类个数都不变,都遵循质量守恒定律。D不符合题意 故答案为:C
【分析】A由一种单质和一种化合物生成另一种化合物和另一种化合物的反应叫置换反应结合微观图可解答 ?????????? B、C根据图示写出方程式可解答 ????????? D 所有化学变化都遵循质量守恒定律
二、填空题
13.【答案】质子 ;中子
【解析】【解答】因为原子中:核电荷数=核内质子数,由题意硒原子的核电荷数为34,故一个硒原子的原子核含有34个质子;根据相对原子质量=质子数+中子数,由题意该原子的相对原子质量为79,则中子数=79-34=45.
【分析】根据原子中:核电荷数=核内质子数、相对原子质量=质子数+中子数,结合题意进行分析解答.
14.【答案】化合反应
【解析】【解答】反应前后将具有相同两个分子删掉,因为它们没加反应,反应物有两种分子子反应生成物有一种物质,所以是化合反应。 故答案为:化合反应。 【分析】微粒模型题关键是根据模型写出其物质的化学式。
15.【答案】3:2:5
【解析】【解答】解:镁和氧气反应的化学方程式为:
2Mg+
O2
2MgO
48
32
80
在此反应中镁、氧气和氧化镁的质量关系48:32:80=3:2:5. 故答案为:3:2:5. 【分析】首先正确写出镁和氧气反应的化学方程式,利用各物质之间的质量比等于相对分子质量和的比,进行分析解答即可.
三、解答题
16.【答案】 解:设需要NaOH的质量为x.
Cl2+2NaOH═NaCl+NaClO+H2O 80????????? 74.5 x?????????? 149 kg
?? x=160 kg
答:需要NaOH 160 kg.
【解析】【分析】根据氯气与氢氧化钠溶液反应的化学方程式和NaClO的质量,列出比例式,就可计算出参加反应的NaOH的质量.
四、综合题
17.【答案】(1)H2O;3H2+CO2 CH4O+H2O (或3H2+CO2 CH3OH+H2O) (2)C,D
【解析】【解答】(1)根据反应的微观示意图及质量守恒定律分析解答;(2)根据反应的化学方程式分析解答。由题目信息和质量守恒定律可知,该反应的方程式为:二氧化碳和氢气在催化剂作用下反应生成甲醇和水的化学方程式为3H2+CO2 CH4O+H2O (或3H2+CO2 CH3OH+H2O)。(1)由上述反应可知,丁的化学式为H2O,该反应的化学方程式为3H2+CO2 CH4O+H2O (或3H2+CO2 CH3OH+H2O);(2)A、由上述反应可知,化学反应前后原子数目没有发生改变,错误;
B、由上述反应可知,该反应不属于复分解反应,错误;
C、由微粒的构成可知,甲是单质,乙、丙、丁均为化合物,正确;
D、由上述反应物质的变化可知,该反应体现了无机物可以转化为有机物,正确。
故答案为:CD。
【分析】有关微观模拟图的题目在解答时,要根据反应前后各微粒的构成确定反应物和生成物,或写出反应方程式,或直接判断参加反应和生成的微粒的个数,要注意反应后有反应物剩余的微观图,不能误以为反应后物质都是生成物。
18.【答案】(1)有机合成
(2)92.5
(3)设至少需要电石渣的质量为x
Ca(OH)2+H2SO4═CaSO4+2H2O 74??????? ?? ? 98
x×92.5%? ? ? 196kg
解得:x=160kg
答:需要电石渣160kg
【解析】【解答】解:(1)有机合成材料主要包括塑料、合成纤维、合成橡胶,聚氯乙烯属于有机合成材料.故答案为:有机合成.(2)100kg上述电石渣中氢氧化钙的质量为100kg×92.5%=92.5kg.故答案为:92.5.
3)设至少需要电石渣的质量为x
Ca(OH)2+H2SO4═CaSO4+2H2O 74??????? ?? ? 98
x×92.5%? ? ? 196kg
解得:x=160kg
答:需要电石渣160kg
【分析】(1)有机合成材料是指由人工合成的有机高分子材料制得的材料,主要包括塑料、合成纤维、合成橡胶.(2)根据题意,某电石渣中含氢氧化钙92.5%,其余为杂质,由电石渣的质量,计算出电石渣中氢氧化钙的质量即可.(3)由酸性废水中硫酸的质量,根据反应的化学方程式计算出至少需要电石渣的质量即可.
一、单选题
1.用“○”和“●”表示不同元素的原子,下列微观示意图能表示化合物的是(?? )
A.???????????????????????????????????????????B.?? C.????????????????????????????????????????????D.?
2.一根蘸有浓盐酸的玻璃棒与另一根蘸有浓氨水的玻璃棒靠近时(未接触),产生大量白烟,其反应的微观示意图如下。下列说法错误的是 (?? )
A.?反应前后原子的种类和个数不变?????????????????????????B.?两根玻璃棒未接触就反应,说明分子是在不停运动的 C.?反应产生的白烟是氯化铵固体小颗粒??????????????????D.?产生白烟的化学方程式为:NH3+HCl=NH3Cl
3.如图是某化学反应的微观模型,“ ”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是(?? )
A.?该反应一定是氧化反应???????????????????????????????????????B.?反应物和生成物中只有一种单质 C.?反应中共有两种元素参与????????????????????????????????????D.?参加反应的两种物质分子个数之比为2:3
4.图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子。下列说法 正确的是(?? )
A.?反应后的物质一定是氧化物????????????????????????????????B.?反应前后各元素的化合价都没有改变 C.?该反应属于化合反应???????????????????????????????????????????D.?该反应中分子和原子的种类均没有改变
5.在加压条件下,25m3的石油气(含丙烷、丁烷等气体)可以装入0.024m3的钢瓶中,由此可以说明的是(?? )
A.?分子的质量很小????????????B.?分子由原子构成????????????C.?分子之间有间隔????????????D.?分子在不断地运动
6.H2、O2和N2组成的混合气体20g,经点燃充分反应后生成18g水,则剩余的气体不可能是(????)
A.?N2和H2?????????????????????????B.?N2和O2?????????????????????????C.?N2 、H2和O2?????????????????????????D.?只有2gN2
7.点燃20克含有O2、H2、N2的混合气体,充分反应后生成18克水,则剩余气体不可能是( )
A.?2克N2???????????B.?O2、N2的混合气体???????C.?H2、N2的混合气体???????????D.?O2、H2、N2的混合气体
8.如图是水分子在一定条件下分解的示意图,从中获得的信息错误的是(?? )
A.?一个水分子由二个氢原子和一个氧原子构成????????B.?水分解后生成氢气和氧气的分子数比为2∶1 C.?水分解过程中, 原子的数目不变????????????????????????D.?水分解过程中,分子的种类不变
9.现有镁和另一种金属组成的混合物,把2.4 g该混合物加入到100 g一定溶质质量分数的稀盐酸中,恰好完全反应,产生氢气的质量为a。则下列说法中正确的是(??? )
A.?若混合物为Mg、Fe,a可能是0.2 g B.?若混合物为Mg、Zn,a的值一定小于0.2 g C.?若混合物为Mg、Cu,a是0.1 g,则该混合物中镁的质量分数为50% D.?若混合物为Mg、Al,则加入的稀盐酸中溶质质量分数一定大于10%
10.在反应2A+B=3C+D中,A和B的相对分子质量之比为5:1,已知20gA与一定量的B恰好完全反应,生成5g的D,则在此反应中B和C的质量比为(??? )
A.?4:19??????????????????????????????????????B.?3:5??????????????????????????????????????C.?1:3??????????????????????????????????????D.?2:17
11.下图是某反应的微观示意图,下列有关说法错误的是(?? )
A.?生成物都是氧化物??????????????????????????????????????????????B.?反应前后原子的种类不变 C.?反应前后有两种元素的化合价发生了变化???????????D.?参加反应的分子个数与生成的分子数个比为6∶5
12.我国科学家研制出一种催化剂,能在室温下高效催化居室空气中的一种有毒气体A,使其转化为无毒物质。其反应过程的微粒示意图如下所示。下列说法正确的是(?? )
A.?该反应属于置换反应???????????????????????????????????????????B.?变化过程中分子个数发生了改变 C.?该反应中A与D的分子个数比为1:1??????????????????????D.?该变化不遵循质量守恒定
二、填空题
13.已知硒原子的核电荷数为34.相对原子质量为79,则一个硒原子的原子核由34个________和45个________构成.
14.如图是某个化学反应前后各种物质微观模拟图,图中“ ”“ ”表示不同元素的原子。根据图示判断,该反应属于________反应
15.镁在空气中燃烧生成氧化镁,此反应中Mg、O2、MgO的质量比为________.
三、解答题
16.家用漂白剂的有效成分是次氯酸钠(NaClO),其制备反应的化学方程式是:Cl2+2NaOH═NaCl+NaClO+H2O.若要制备149kg的次氯酸钠,则理论上需要氢氧化钠的质量是多少?
四、综合题
17.随着科学的发展,新能源的开发不断取得突破。清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下图(图中的微粒恰 好完全反应)所示。请根据微观示意图回答以下问题。
(1)丁的化学式为________,该反应的化学方程式为________。
(2)下列说法正确的是______(填写字母序号)。
A.?反应前后原子数目发生改变?????????????????????????????????B.?该反应属于复分解反应 C.?甲是单质,乙、丙、丁均为化合物??????????????????????D.?该反应体现了无机物在一定条件下可以转化为有机物
18. 用电石(主要成分为CaC2)与水反应可制取乙炔,最终还可得到电石渣.某电石渣中含氢氧化钙92.5%,其余为杂质,此电石渣可用于处理电镀厂排出的酸性废水.请完成:
(1)乙炔(C2H2)是生产聚氯乙烯的重要原料.聚氯乙烯属于________材料(填合金或有机合成或无机非金属或复合).
(2)100kg上述电石渣中氢氧化钙的质量为________kg.
(3)用上述电石渣处理含硫酸196kg的酸性废水(假设电石渣中的杂质、废水中其他成分均不参加反应),求至少需要这种电石渣的质量(写出计算过程及结果)
答案解析部分
一、单选题
1.【答案】B
【解析】【解答】A、A中有两种分子,是混合物,A不符合题意;
B、B中只有一种分子,且是由两种元素组成的物质,是化合物,B符合题意;
C、C中由一种分子组成,这种物质是由一种元素组成的,是单质,C不符合题意;
D、该图中是混合物,D不符合题意。
故答案为: B。
【分析】模型题主要是根据模型写出物质的化学式,再结合相关定义进行判断。
2.【答案】 D
【解析】【解答】A.根据化学微观反应示意图可知,反应前后原子的种类和个数不变,故A不符合题意,
B.两根玻璃棒未接触就反应,说明分子是在不停运动的,故B不符合题意;
C.反应产生的白烟是氯化铵固体小颗粒,故C不符合题意;
D.产生白烟的化学方程式为:NH3+HCl=NH4Cl,
故答案为:D。
【分析】此类题目应先根据题目提示,书写出负的化学方程式,然后根据化学方程式做答;此题的化学方程式为:NH3+HCl=NH4Cl
3.【答案】 C
【解析】【解答】A、物质与氧气的反应属于氧化反应;不确定反应物是否有氧气,不能确定是否是氧化反应,错误;A不符合题意; B、由一种元素组成的纯净物叫单质;所以两种反应物都是单质,错误;B不符合题意; C,元素是同类原子的总称,由图可知,反应中共有两种元素参与,正确;C符合题意; D. 化学反应前后原子的种类、个数不变,所以参加反应的两种物质分子个数之比为1:3,错误。D不符合题意; 故答案为:C
【分析】根据图例写出每个微粒所代表的物质化学式,然后根据化学式判断每个物质所属的物质类别,根据题意写出反应的化学方程式,要把前后相同大的微粒划去,然后根据方程式的意义分析逐步解答;依据图例正确书写各物质的化学式是解题的关键;化学反应前后原子的种类个数没有改变;由两种或两种以上物质生成一种物质的反应叫化合反应;由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物;
4.【答案】 C
【解析】【解答】A、二种元素组成其中一种是氧元素的为氧化物,图中无法确定是否含有氧元素,A不符合题意; B、元素在单质中化合价为0,在化合价中一定不为0,由此,两种元素的化合价都一定改变了,B不符合题意; C、由图是两种微粒生成了一种,即两种物质生成了一种,属于化合反应,C符合题意; D、化学反应中原子种类不变,但分子种类一定改变,D不符合题意。 故答案为:C。
【分析】模型题关键是根据模型写出物质的化学方程式,再根据化学方程式吉祥相关计算即可。
5.【答案】 C
【解析】【解答】解:25m3的石油气(含丙烷、丁烷等气体)可以装入0.024m3的钢瓶中,说明分子之间有间隔,并且间隔较大.
故选C
【分析】微观粒子的特征:质量和体积都很小;微粒与微粒之间有间隙;都是不断运动的.
6.【答案】 C
【解析】
【分析】根据氢气和氧气反应会生成水进行分析;
【解答】所谓充分反应就是能够反应的不能同时剩余. A、氢气过量后会剩余氢气,氮气不会和氢气、氧气反应,可能; B、氧气过量后会剩余氧气,氮气不会和氢气、氧气反应,可能; C、氢气和氧气会生成水,不会同时剩余,不可能; D、氮气的化学性质稳定,不会与氢气、氧气反应,可能. 故选C.
【点评】在解此类题时,首先分析题中气体的性质,然后结合选项中的气体进行分析
7.【答案】 D
【解析】【解答】解:A、如果氢气和氧气恰好完全反应,则剩余气体是氮气,故A正确;
B、如果氧气过量,则剩余气体是氮气和氧气,故B正确;
C、如果氢气过量,则剩余气体是氮气和氢气,故C正确;
D、氢气和氧气不可能同时剩余,即剩余气体不可能是H2、O2和N2 , 故D错误.
故选:D.
【分析】根据氢气和氧气反应生成水,在点燃条件下,氮气不能和氢气、氧气反应.所以该题中的三种气体具有可燃性的气体只有H2 , 所以对混合气体点燃,完全反应后剩余气体中氢气和氧气不可能同时存在进行分析.
8.【答案】 D
【解析】【解答】A.由图可见,一个水分子是由2个氢原子和1个氧原子构成的,A选项不符合题意;
B.由图可知,水分解后,产生氢气和氧气的分子数比值为2:1,B选项不符合题意;
C.由图可知,反应前有6个原子,反应后有6个原子,原子数目没有改变,C选项不符合题意;
D.由图可知,反应前有水分子,反应后有氢分子和氧分子,分子种类发生改变,D选项符合题意。
故答案为:D
【分析】水分解过程中,水分子发生了改变,生成了氢分子和氧分子.化学反应前后原子的种类没有改变.一个水分子是由二个氢原子和一个氧原子构成的.水分解后生成氢气和氧气的分子数比为2:1。
9.【答案】 D
【解析】【解答】根据极值法计算,假设合金中镁的质量为2.4g,利用镁和稀盐酸反应的方程式可得生成氢气质量为0.2g,同理计算出2.4g铝与稀盐酸反应生成氢气的质量大于0.2g,2.4g锌、2.4g铁与相同的稀盐酸反应生成的氢气小于0.2g A? 若混合物为Mg、Fe,a一定小于0.2g,A不符合题意 B 若混合物为Mg、Zn, a的值一定小于0.2 g,B符合题意 C 若混合物为Mg、Cu, a是0.1 g,则该混合物中镁的质量分数大于50% ,C不符合题意 D当粉末是镁、铝合金时,因相同质量的铝消耗盐酸的质量比镁的大,2.4g镁消耗盐酸7.3g,所以合金为镁铝合金时,所需盐酸的质量分数一定大于7.3%,不符合题意
故答案为:B
【分析】因为金属与酸反应生成氢气的质量=金属的质量,所以等质量的镁与盐酸反应生成的氢气的质量大于锌、铁,而小于铝,据此分析解答
10.【答案】 D
【解析】【解答】解:令A与B的相对分子质量为5和1,设恰好与A反应的B的质量为x,则:
2A+
B=3C+D
10
1
20g
x
?
解得x═2g,则由20g A与2g B恰好完全反应,生成5g D,生成C的质量为:20g+2g-5g═17g
则在此反应中B和C的质量比为:2g:17g═2:17。
故答案为:D。
【分析】根据方程式中质量定比关系计算参加反应的的B的质量,再根据质量守恒定律计算C的质量,进而计算B和C的质量比
11.【答案】 D
【解析】【解答】依据反应前后物质的分子结构可知反应物是氧气和硫化氢,生成物是水和二氧化硫,则反应方程式为3O2+2H2S 2H2O+2SO2;
A、根据化学方程式可知生成物是水和二氧化硫,都属于氧化物,不符合题意;
B、由图示或化学方程式可知,化学反应前后原子的种类不变,不符合题意;
C、由方程式可知氧元素由0变成了-2价,硫元素由-2价变成了+4价,氢元素的化合价不变,有两种元素的化合价发生了改变,不符合题意;
D、由化学方程式可知,参加反应的两种分子的个数之比为3:2,符合题意。
故答案为:D。
【分析】有关微观模拟图的题目在解答时,要根据反应前后各微粒的构成确定反应物和生成物,或写出反应方程式,或直接判断参加反应和生成的微粒的个数,要注意反应后有反应物剩余的微观图,不能误以为反应后物质都是生成物。
12.【答案】 C
【解析】【解答】A、由一种单质和一种化合物生成另一种化合物和另一种化合物的反应叫置换反应,该反应的两种生成物都是化合物,不可能是置换反应;A不符合题意 B、由质量守恒定律可知反应前后原子的种类个数不变,所以该反应中分子个数没有发生改变,B不符合题意 C. 由题中信息可知,该反应中A与D的分子个数比为1:1? ,C符合题意 ? D. 所有化学变化中原子的种类个数都不变,都遵循质量守恒定律。D不符合题意 故答案为:C
【分析】A由一种单质和一种化合物生成另一种化合物和另一种化合物的反应叫置换反应结合微观图可解答 ?????????? B、C根据图示写出方程式可解答 ????????? D 所有化学变化都遵循质量守恒定律
二、填空题
13.【答案】质子 ;中子
【解析】【解答】因为原子中:核电荷数=核内质子数,由题意硒原子的核电荷数为34,故一个硒原子的原子核含有34个质子;根据相对原子质量=质子数+中子数,由题意该原子的相对原子质量为79,则中子数=79-34=45.
【分析】根据原子中:核电荷数=核内质子数、相对原子质量=质子数+中子数,结合题意进行分析解答.
14.【答案】化合反应
【解析】【解答】反应前后将具有相同两个分子删掉,因为它们没加反应,反应物有两种分子子反应生成物有一种物质,所以是化合反应。 故答案为:化合反应。 【分析】微粒模型题关键是根据模型写出其物质的化学式。
15.【答案】3:2:5
【解析】【解答】解:镁和氧气反应的化学方程式为:
2Mg+
O2
2MgO
48
32
80
在此反应中镁、氧气和氧化镁的质量关系48:32:80=3:2:5. 故答案为:3:2:5. 【分析】首先正确写出镁和氧气反应的化学方程式,利用各物质之间的质量比等于相对分子质量和的比,进行分析解答即可.
三、解答题
16.【答案】 解:设需要NaOH的质量为x.
Cl2+2NaOH═NaCl+NaClO+H2O 80????????? 74.5 x?????????? 149 kg
?? x=160 kg
答:需要NaOH 160 kg.
【解析】【分析】根据氯气与氢氧化钠溶液反应的化学方程式和NaClO的质量,列出比例式,就可计算出参加反应的NaOH的质量.
四、综合题
17.【答案】(1)H2O;3H2+CO2 CH4O+H2O (或3H2+CO2 CH3OH+H2O) (2)C,D
【解析】【解答】(1)根据反应的微观示意图及质量守恒定律分析解答;(2)根据反应的化学方程式分析解答。由题目信息和质量守恒定律可知,该反应的方程式为:二氧化碳和氢气在催化剂作用下反应生成甲醇和水的化学方程式为3H2+CO2 CH4O+H2O (或3H2+CO2 CH3OH+H2O)。(1)由上述反应可知,丁的化学式为H2O,该反应的化学方程式为3H2+CO2 CH4O+H2O (或3H2+CO2 CH3OH+H2O);(2)A、由上述反应可知,化学反应前后原子数目没有发生改变,错误;
B、由上述反应可知,该反应不属于复分解反应,错误;
C、由微粒的构成可知,甲是单质,乙、丙、丁均为化合物,正确;
D、由上述反应物质的变化可知,该反应体现了无机物可以转化为有机物,正确。
故答案为:CD。
【分析】有关微观模拟图的题目在解答时,要根据反应前后各微粒的构成确定反应物和生成物,或写出反应方程式,或直接判断参加反应和生成的微粒的个数,要注意反应后有反应物剩余的微观图,不能误以为反应后物质都是生成物。
18.【答案】(1)有机合成
(2)92.5
(3)设至少需要电石渣的质量为x
Ca(OH)2+H2SO4═CaSO4+2H2O 74??????? ?? ? 98
x×92.5%? ? ? 196kg
解得:x=160kg
答:需要电石渣160kg
【解析】【解答】解:(1)有机合成材料主要包括塑料、合成纤维、合成橡胶,聚氯乙烯属于有机合成材料.故答案为:有机合成.(2)100kg上述电石渣中氢氧化钙的质量为100kg×92.5%=92.5kg.故答案为:92.5.
3)设至少需要电石渣的质量为x
Ca(OH)2+H2SO4═CaSO4+2H2O 74??????? ?? ? 98
x×92.5%? ? ? 196kg
解得:x=160kg
答:需要电石渣160kg
【分析】(1)有机合成材料是指由人工合成的有机高分子材料制得的材料,主要包括塑料、合成纤维、合成橡胶.(2)根据题意,某电石渣中含氢氧化钙92.5%,其余为杂质,由电石渣的质量,计算出电石渣中氢氧化钙的质量即可.(3)由酸性废水中硫酸的质量,根据反应的化学方程式计算出至少需要电石渣的质量即可.
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
