人教版(五四)九年级化学 3.2酸和碱的中和反应 同步练习(含解析)
文档属性
| 名称 | 人教版(五四)九年级化学 3.2酸和碱的中和反应 同步练习(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 121.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-06-25 00:00:00 | ||
图片预览


文档简介
人教版(五四)九年级化学跟踪训练 3.2酸和碱的中和反应
一、单选题
1.生活中一些食物的近似pH如下,其中显碱性的食物是( )
A.?柠檬汁(2.0~3.0)?????????????B.?苹果汁(2.9~3.3)?????????????C.?牛奶(6.3~6.6)?????????????D.?鸡蛋清(7.6~8.0)
2.下列关于碳和碳的氧化物的说法,正确的是(??? )
A.?碳在空气中不充分燃烧,生成二氧化碳???????????????
B.?CO与CO2的组成元素相同,所以它们的化学性质也相同 C.?水墨画可长时间保存不变色是因为碳的化学性质在常温下不活泼??????????
D.?空气中二氧化碳的过量排放会导致“酸雨”
3.生活中常见物质,pH小于7的是(?? )
A.?食醋??????????????????????????????????B.?食盐水??????????????????????????????????C.?糖水??????????????????????????????????D.?肥皂水
4.某学生在检验某溶液是否显酸性时,取出少量该溶液进行如下实验,其中错误的做法是( )
A.?滴入紫色的石蕊试液???????????????????B.?用嘴品尝?????????????????C.?滴入Na2CO3溶液?????????????????D.?加入锌粒
5.生活中常见的物质pH大于7的是(? )
A.?蔗糖溶液????????????????????????????????B.?肥皂水????????????????????????????????C.?食醋????????????????????????????????D.?食盐水
6.人若长期食用“镉大米”(镉含量超标)会引起痛痛病。研究表明水稻对镉的吸收率与土壤的pH有紧密关系(如图所示),下列物质中可用于改良土壤结构,降低水稻对镉吸收率的是(?? )
A.?氯化钾???????????????????????B.?烧碱?????????????????????C.?熟石灰???????????????????????D.?硫酸亚铁(水溶液显酸性)
7. 图示为某些物品对应的pH范围,其中显弱碱性的是( )
A.?小苏打????????????????????????????????????B.?杨梅???????????????????????????????????C.?栗子???????????????????????????????????D.?菠萝
8. 你遇到过很多酸性或碱性物质.一些食物的近似pH如下,其中显碱性的物质是(? )
A.?食醋,pH为2~3????????????????????????????????????????????????B.?厕所清洁剂,pH为1~2 C.?橘子,pH为3~4????????????????????????????????????????????????D.?炉具清洁剂,pH为12~13
9.下列说法正确的是(?? )
A.?波尔多液中的二种成份都属于盐????????????????????????B.?用KClO3及双氧水制O2时,加入的MnO2作用不相同 C.?高炉炼铁中所需的高温和CO的生成都与焦炭有关????????D.?酸碱中和反应生成盐和水,生成盐和水的反应一定是中和反应
10.形成酸雨的主要气体是( )
A.?CO2??????????????????????????????????????B.?SO2??????????????????????????????????????C.?CO??????????????????????????????????????D.?O3
二、填空题
11.在清洗餐具时常加入少量洗涤剂,这是因为洗涤剂具有________功能;碱性洗发水易去油污,但对头发有损坏,于是人们通常用洗发水洗净头发后,再用护发素护理,由此可知护发素的pH________?7。(填“>”、“<”或“=”)
12.SO2 和 NO2都能溶于雨水形成酸雨而污染环境.为减少酸雨的产生,有下列措施:①少用煤作燃料;②把工厂的烟囱建高;③燃料脱硫;④开发新能源.其中有效的措施是 ??????(填序号).
A.?①②④????????????????????????????????B.?①②③????????????????????????????????C.?②③④????????????????????????????????D.?①③④
13. 根据下表中的信息填空:
物质
氨水
苹果汁
牛奶
鸡蛋清
pH
8.5﹣10.5
2.9﹣3.3
6.3﹣6.6
7.6﹣8.0
(1)其中酸性最强的是________; (2)鸡蛋清是________性; (3)若向一支盛有氨水的试管中滴稀盐酸,则试管中液体的PH会________(填“变大”“变小”或不变).
三、解答题
14. 如图是某大理石雕像分别摄于1908年和1969年的两幅图片,雕像被严重腐蚀的主要原因是什么?请就如何解决这一问题提出你的建议. ?
四、综合题
15.按照如图所示进行中和反应实验。
(1)反应的化学方程式为________。
(2)向烧杯中逐滴滴入盐酸至过量,在这个过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是________。
(3)实验后溶液pH ________(填“小于”“等于”或“大于”)7。
16.向滴有几滴酚酞的氢氧化钠溶液中滴加稀盐酸至恰好完全反应.
(1)上述过程的实验现象为________.
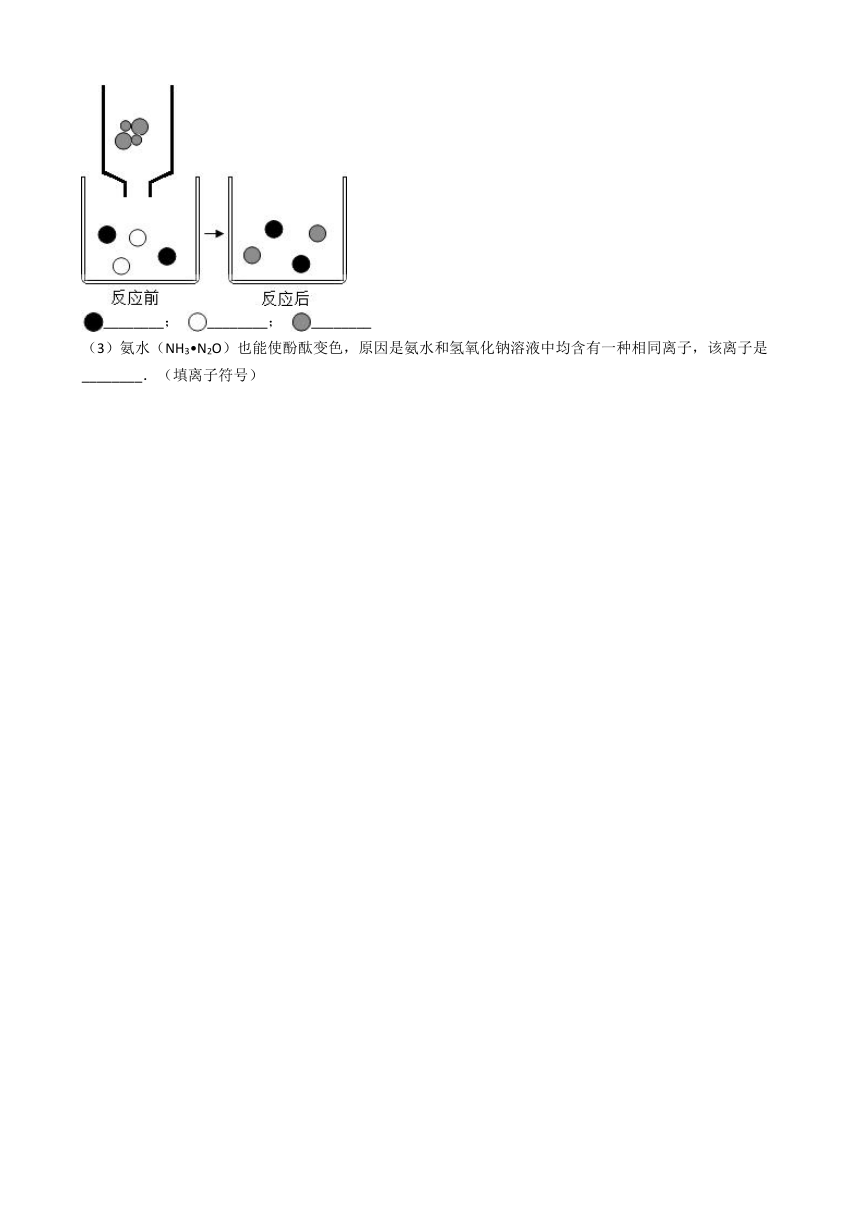
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子.(填离子符号)
________; ________; ________
(3)氨水(NH3?N2O)也能使酚酞变色,原因是氨水和氢氧化钠溶液中均含有一种相同离子,该离子是________.(填离子符号)
答案解析部分
一、单选题
1.【答案】 D
【解析】【解答】鸡蛋清的pH为7.6~8.0,大于7,显碱性。 故答案为:D
【分析】碱性:pH大于7,中性pH=7,酸性;pH小于7
2.【答案】 C
【解析】【解答】A、碳在空气中不充分燃烧,生成一氧化碳,不符合题意;
B、CO和CO2的组成元素相同,但由于它们分子的构成不同,它们的化学性质不同,不符合题意;
C. 水墨画可长时间保存不变色是因为碳的化学性质在常温下不活泼,符合题意;
D、空气中二氧化碳的过量排放会导致“温室效应”增强,不符合题意。
故答案为:C。
【分析】本题主要考查碳的化学性质,考生需要掌握单质碳常温下的稳定性强,完全燃烧(氧气充足),生成CO2,不完全燃烧? (氧气不充足),生成CO,二氧化碳多对环境的影响。
3.【答案】 A
【解析】【解答】pH小于7的物质为酸性物质,食醋为酸,A符合题意。 故答案为:A。【分析】本题主要考查溶液的酸碱性与pH之间的关系,pH小于7,显酸性,大于7显碱性。等于7显中性。
4.【答案】 B
【解析】【解答】解:
A、取少量该无色溶液置于试管中,向其中滴加紫色石蕊试液,若紫色石蕊试液变成红色,则证明该无色溶液具有酸性,故对;
B、根据取用药品的“三不原则”:不能用手拿药品;不能把鼻孔凑近容器口去闻药品的气味;不得品尝任何药品的味道,故错;
C、取少量该无色溶液置于试管中,向其中滴加碳酸钠溶液,若有大量气泡产生,则证明该无色溶液具有酸性,故对;
D、取少量该无色溶液置于试管中,向其中加入锌粒,若有大量气泡产生,则证明该无色溶液具有酸性,故对.
答案:B
【分析】A、根据酸的化学性质解答,酸性溶液能使紫色石蕊试液变红解答;
B、根据实验室取用药品的原则解答;
C、根据酸能与碳酸钠溶液产生二氧化碳解答;
D、根据酸能与活泼金属反应产生氢气解答.
5.【答案】 B
【解析】【解答】解:A、蔗糖溶液是蔗糖溶于水,显中性,pH等于7;
B、肥皂水显碱性,pH大于7;
C、食醋是醋酸的溶液显酸性,pH小于7,
D、食盐属于盐,溶于水显中性,pH等于7,
故选B.
【分析】当溶液的pH等于7时,呈中性.当溶液的pH大于7时,呈碱性.当溶液的pH小于7时,呈酸性.
6.【答案】 C
【解析】【解答】解:A.根据上述分析可知,土壤pH=7.6左右时,水稻对镉的吸收率几乎不变即最小,而氯化钾呈中性,故不符合题意;
B.根据上述分析可知,土壤pH=7.6左右时,水稻对镉的吸收率几乎不变即最小,而烧碱是氢氧化钠俗称,属于强碱,腐蚀性强,不能用来改良土壤结构,故不符合题意;
C.根据上述分析可知,土壤pH=7.6左右时,水稻对镉的吸收率几乎不变即最小,而熟石灰呈弱碱性,故符合题意;
D.根据上述分析可知,土壤pH=7.6左右时,水稻对镉的吸收率几乎不变即最小,而硫酸亚铁水溶液显酸性,故不符合题意。
故答案为:C。
【分析】根据图像可知,水的PH越大,水稻对镉的吸收越少,也就是水稻生长在碱性环境中吸收的镉会减少。烧碱和熟石灰都呈碱性,根据植物生长需要的PH环境、烧碱和熟石灰碱性的强弱、价格及自然资源,可用于改良土壤结构,降低水稻对镉吸收率的是熟石灰。
7.【答案】 C
【解析】【解答】杨梅、菠萝的pH小于7时,呈酸性,栗子、小苏打的pH大于7时,呈碱性,并且栗子的pH更接近于7,碱性弱.
故选:C.
【分析】当溶液的pH等于7时,呈中性;当溶液的pH大于7时,呈碱性;当溶液的pH小于7时,呈酸性.当溶液的pH大于7时,随着pH的减小碱性减弱.
8.【答案】 D
【解析】【解答】解:A、食醋的pH为2~3小于7,显酸性,故选项错误.
B、厕所清洁剂的pH为1~2,小于7,显酸性,故选项错误.
C、橘子的pH为3~4,小于7,显酸性,故选项错误.
D、炉具清洁剂的pH为12~13,大于7,显碱性,故选项正确.
故选:D.
【分析】当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;进行分析判断.本题难度不大,掌握溶液的酸碱性和溶液pH大小之间的关系是正确解答此类题的关键.
9.【答案】 C
【解析】【解答】A、波尔多液中的二种成份分别是硫酸铜和氢氧化钙,其中硫酸铜属于盐,氢氧化钙属于碱,故错误;A不符合题意;
B、用KClO3及双氧水制O2时,加入的MnO2作用相同,故错误;B不符合题意;
C、高炉炼铁中所需的高温和CO的生成都与焦炭有关,正确;C符合题意;
D、 酸碱中和反应生成盐和水,生成盐和水的反应不一定是中和反应,故错误;D不符合题意.
故答案为:C.
【分析】本题主要考查盐的概念、催化剂的作用、炼铁的原理及中和反应的判断.
10.【答案】 B
【解析】A、二氧化碳是大气的成分之一,含量过多会形成温室效应,与水反应生成的碳酸酸性很弱不会形成酸雨,故错误; B、二氧化硫能和水反应生成亚硫酸,当雨水的pH<5.6时就形成酸雨.故正确; C、一氧化碳虽有毒,但不与水反应,不会形成酸雨,故错误; D、臭氧是一种氧的单质,能阻挡紫外线,但不是形成酸雨的气体,故错误. 故选B.
二、填空题
11.【答案】乳化;<
【解析】【解答】洗涤剂能对油污起乳化作用,故答案为:乳化; 碱性洗发水对头发有损坏,用护发素护理,因而护发素呈酸性,故答案为:<。 【分析】此题从生活实际出发,考查了洗涤剂能清洗餐具上的油污,考查了碱性洗发水对头发有损坏,故洗完头发后,用酸性护发素护理.要联系生活实际,从化学中走入生活,从生活中走入化学。
12.【答案】D
【解析】【解答】解:减少用煤作燃料、将燃料脱硫、开发新能源等措施可以减少二氧化硫、氮氧化物的产生,有利于防止酸雨的产生;把工厂的烟囱建高仍然能生成二氧化硫和氮氧化物,不能防止酸雨的产生.
故选:D.
【分析】化石燃料燃烧能生成大量的二氧化硫和氮氧化物,这些物质和水反应能生成显酸性的物质,达到一定程度时会形成酸雨.
13.【答案】苹果汁;碱;变小
【解析】【解答】(1)当溶液的pH<7时,随着pH的减小酸性增强,上述液体中,苹果汁的pH最小,酸性最强,故填:苹果汁; (2)鸡蛋清是的pH范围是7.6﹣8.0,大于7,显碱性,故填:碱; (3)氨水的pH范围是8.5﹣10.5,显碱性,盐酸显酸性,因此向一支盛有氨水的试管中滴稀盐酸,则试管中液体的pH会变小,故填:变小. 【分析】当溶液的pH等于7时,呈中性;当溶液的pH大于7时,呈碱性;当溶液的pH小于7时,呈酸性;当溶液的pH<7时,随着pH的减小酸性增强.酸碱能发生中和反应,据此解答.
三、解答题
14.【答案】酸雨;工厂废气处理后排放.
【解析】【解答】雕像的严重腐蚀反映出最主要的环境污染问题是酸雨; 酸雨分为硝酸型酸雨和硫酸型酸雨,煤的燃烧生成二氧化硫引起的是硫酸型酸雨,汽车尾气的排放产生二氧化氮引起的是硝酸型酸雨.减少酸雨的形成,也就是尽量减少酸性气体的排放,如:①限制含硫煤的使用②化工厂尾气经处理达标后排放③使用绿色能源④汽车尾气经处理后排放等. 故答为:酸雨;工厂废气处理后排放. 【分析】雕像的严重腐蚀反映出最主要的环境污染问题是酸雨;然后根据酸雨的形成及危害提出解决的建议.
四、综合题
15.【答案】(1)NaOH + HCl= NaCl+ H2O (2)溶液由红色变无色 (3)小于
【解析】【解答】 (1)氢氧化钠与盐酸反应生成氯化钠和水,反应的化学方程式为NaOH + HCl= NaCl+ H2O;(2)向烧杯中逐滴滴入盐酸至过量,在这个过程中,pH值逐渐降低,会由碱性变为中性,到最后盐酸过量时变为酸性,酚酞在碱性时为红色,碱性和中性为无色,所以盐酸与氢氧化钠发生了化学反应的实验现象是溶液由红色变无色;(3)实验过程中滴入盐酸过量实验后溶液呈酸性,溶液的pH小于7。 【分析】牢记稀盐酸滴加到氢氧化钠溶液中的曲线变化和氢氧化钠滴加到稀盐酸中的曲边变化的比较是解题的关键。
16.【答案】(1)溶液由红色变为无色 (2)Na+;OH﹣;Cl﹣ (3)OH﹣
【解析】【解答】解:(1)氢氧化钠与盐酸反应生成氯化钠和水,方程式为:NaOH+HCl=NaCl+H2O;氯化钠呈中性,盐酸过量,使反应后溶液呈酸性,中性或酸性溶液不能使酚酞变色.(2)反应前,溶液中含有大量的氢离子、氯离子,钠离子、氢氧根离子,反应后,溶液中含有大量的氯离子、钠离子;故三种离子分别为:Na+、OH﹣、Cl﹣;(3)氨水(NH3?H2O)也能使酚酞变色,原因是氨水和氢氧化钠溶液中均含有一种相同离子,该离子是OH﹣
答案:(1)溶液由红色变为无色;(2)Na+、OH﹣、Cl﹣;(3)OH﹣ .
【分析】(1)根据氢氧化钠溶液显碱性,结合酚酞溶液遇酸性、中性溶液不变色,遇碱性溶液变红色,进行分析解答;(2)根据反应的实质,可以知道溶液里面粒子的变化情况;(3)根据碱性溶液能使酚酞变红色解答.
一、单选题
1.生活中一些食物的近似pH如下,其中显碱性的食物是( )
A.?柠檬汁(2.0~3.0)?????????????B.?苹果汁(2.9~3.3)?????????????C.?牛奶(6.3~6.6)?????????????D.?鸡蛋清(7.6~8.0)
2.下列关于碳和碳的氧化物的说法,正确的是(??? )
A.?碳在空气中不充分燃烧,生成二氧化碳???????????????
B.?CO与CO2的组成元素相同,所以它们的化学性质也相同 C.?水墨画可长时间保存不变色是因为碳的化学性质在常温下不活泼??????????
D.?空气中二氧化碳的过量排放会导致“酸雨”
3.生活中常见物质,pH小于7的是(?? )
A.?食醋??????????????????????????????????B.?食盐水??????????????????????????????????C.?糖水??????????????????????????????????D.?肥皂水
4.某学生在检验某溶液是否显酸性时,取出少量该溶液进行如下实验,其中错误的做法是( )
A.?滴入紫色的石蕊试液???????????????????B.?用嘴品尝?????????????????C.?滴入Na2CO3溶液?????????????????D.?加入锌粒
5.生活中常见的物质pH大于7的是(? )
A.?蔗糖溶液????????????????????????????????B.?肥皂水????????????????????????????????C.?食醋????????????????????????????????D.?食盐水
6.人若长期食用“镉大米”(镉含量超标)会引起痛痛病。研究表明水稻对镉的吸收率与土壤的pH有紧密关系(如图所示),下列物质中可用于改良土壤结构,降低水稻对镉吸收率的是(?? )
A.?氯化钾???????????????????????B.?烧碱?????????????????????C.?熟石灰???????????????????????D.?硫酸亚铁(水溶液显酸性)
7. 图示为某些物品对应的pH范围,其中显弱碱性的是( )
A.?小苏打????????????????????????????????????B.?杨梅???????????????????????????????????C.?栗子???????????????????????????????????D.?菠萝
8. 你遇到过很多酸性或碱性物质.一些食物的近似pH如下,其中显碱性的物质是(? )
A.?食醋,pH为2~3????????????????????????????????????????????????B.?厕所清洁剂,pH为1~2 C.?橘子,pH为3~4????????????????????????????????????????????????D.?炉具清洁剂,pH为12~13
9.下列说法正确的是(?? )
A.?波尔多液中的二种成份都属于盐????????????????????????B.?用KClO3及双氧水制O2时,加入的MnO2作用不相同 C.?高炉炼铁中所需的高温和CO的生成都与焦炭有关????????D.?酸碱中和反应生成盐和水,生成盐和水的反应一定是中和反应
10.形成酸雨的主要气体是( )
A.?CO2??????????????????????????????????????B.?SO2??????????????????????????????????????C.?CO??????????????????????????????????????D.?O3
二、填空题
11.在清洗餐具时常加入少量洗涤剂,这是因为洗涤剂具有________功能;碱性洗发水易去油污,但对头发有损坏,于是人们通常用洗发水洗净头发后,再用护发素护理,由此可知护发素的pH________?7。(填“>”、“<”或“=”)
12.SO2 和 NO2都能溶于雨水形成酸雨而污染环境.为减少酸雨的产生,有下列措施:①少用煤作燃料;②把工厂的烟囱建高;③燃料脱硫;④开发新能源.其中有效的措施是 ??????(填序号).
A.?①②④????????????????????????????????B.?①②③????????????????????????????????C.?②③④????????????????????????????????D.?①③④
13. 根据下表中的信息填空:
物质
氨水
苹果汁
牛奶
鸡蛋清
pH
8.5﹣10.5
2.9﹣3.3
6.3﹣6.6
7.6﹣8.0
(1)其中酸性最强的是________; (2)鸡蛋清是________性; (3)若向一支盛有氨水的试管中滴稀盐酸,则试管中液体的PH会________(填“变大”“变小”或不变).
三、解答题
14. 如图是某大理石雕像分别摄于1908年和1969年的两幅图片,雕像被严重腐蚀的主要原因是什么?请就如何解决这一问题提出你的建议. ?
四、综合题
15.按照如图所示进行中和反应实验。
(1)反应的化学方程式为________。
(2)向烧杯中逐滴滴入盐酸至过量,在这个过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是________。
(3)实验后溶液pH ________(填“小于”“等于”或“大于”)7。
16.向滴有几滴酚酞的氢氧化钠溶液中滴加稀盐酸至恰好完全反应.
(1)上述过程的实验现象为________.
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子.(填离子符号)
________; ________; ________
(3)氨水(NH3?N2O)也能使酚酞变色,原因是氨水和氢氧化钠溶液中均含有一种相同离子,该离子是________.(填离子符号)
答案解析部分
一、单选题
1.【答案】 D
【解析】【解答】鸡蛋清的pH为7.6~8.0,大于7,显碱性。 故答案为:D
【分析】碱性:pH大于7,中性pH=7,酸性;pH小于7
2.【答案】 C
【解析】【解答】A、碳在空气中不充分燃烧,生成一氧化碳,不符合题意;
B、CO和CO2的组成元素相同,但由于它们分子的构成不同,它们的化学性质不同,不符合题意;
C. 水墨画可长时间保存不变色是因为碳的化学性质在常温下不活泼,符合题意;
D、空气中二氧化碳的过量排放会导致“温室效应”增强,不符合题意。
故答案为:C。
【分析】本题主要考查碳的化学性质,考生需要掌握单质碳常温下的稳定性强,完全燃烧(氧气充足),生成CO2,不完全燃烧? (氧气不充足),生成CO,二氧化碳多对环境的影响。
3.【答案】 A
【解析】【解答】pH小于7的物质为酸性物质,食醋为酸,A符合题意。 故答案为:A。【分析】本题主要考查溶液的酸碱性与pH之间的关系,pH小于7,显酸性,大于7显碱性。等于7显中性。
4.【答案】 B
【解析】【解答】解:
A、取少量该无色溶液置于试管中,向其中滴加紫色石蕊试液,若紫色石蕊试液变成红色,则证明该无色溶液具有酸性,故对;
B、根据取用药品的“三不原则”:不能用手拿药品;不能把鼻孔凑近容器口去闻药品的气味;不得品尝任何药品的味道,故错;
C、取少量该无色溶液置于试管中,向其中滴加碳酸钠溶液,若有大量气泡产生,则证明该无色溶液具有酸性,故对;
D、取少量该无色溶液置于试管中,向其中加入锌粒,若有大量气泡产生,则证明该无色溶液具有酸性,故对.
答案:B
【分析】A、根据酸的化学性质解答,酸性溶液能使紫色石蕊试液变红解答;
B、根据实验室取用药品的原则解答;
C、根据酸能与碳酸钠溶液产生二氧化碳解答;
D、根据酸能与活泼金属反应产生氢气解答.
5.【答案】 B
【解析】【解答】解:A、蔗糖溶液是蔗糖溶于水,显中性,pH等于7;
B、肥皂水显碱性,pH大于7;
C、食醋是醋酸的溶液显酸性,pH小于7,
D、食盐属于盐,溶于水显中性,pH等于7,
故选B.
【分析】当溶液的pH等于7时,呈中性.当溶液的pH大于7时,呈碱性.当溶液的pH小于7时,呈酸性.
6.【答案】 C
【解析】【解答】解:A.根据上述分析可知,土壤pH=7.6左右时,水稻对镉的吸收率几乎不变即最小,而氯化钾呈中性,故不符合题意;
B.根据上述分析可知,土壤pH=7.6左右时,水稻对镉的吸收率几乎不变即最小,而烧碱是氢氧化钠俗称,属于强碱,腐蚀性强,不能用来改良土壤结构,故不符合题意;
C.根据上述分析可知,土壤pH=7.6左右时,水稻对镉的吸收率几乎不变即最小,而熟石灰呈弱碱性,故符合题意;
D.根据上述分析可知,土壤pH=7.6左右时,水稻对镉的吸收率几乎不变即最小,而硫酸亚铁水溶液显酸性,故不符合题意。
故答案为:C。
【分析】根据图像可知,水的PH越大,水稻对镉的吸收越少,也就是水稻生长在碱性环境中吸收的镉会减少。烧碱和熟石灰都呈碱性,根据植物生长需要的PH环境、烧碱和熟石灰碱性的强弱、价格及自然资源,可用于改良土壤结构,降低水稻对镉吸收率的是熟石灰。
7.【答案】 C
【解析】【解答】杨梅、菠萝的pH小于7时,呈酸性,栗子、小苏打的pH大于7时,呈碱性,并且栗子的pH更接近于7,碱性弱.
故选:C.
【分析】当溶液的pH等于7时,呈中性;当溶液的pH大于7时,呈碱性;当溶液的pH小于7时,呈酸性.当溶液的pH大于7时,随着pH的减小碱性减弱.
8.【答案】 D
【解析】【解答】解:A、食醋的pH为2~3小于7,显酸性,故选项错误.
B、厕所清洁剂的pH为1~2,小于7,显酸性,故选项错误.
C、橘子的pH为3~4,小于7,显酸性,故选项错误.
D、炉具清洁剂的pH为12~13,大于7,显碱性,故选项正确.
故选:D.
【分析】当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;进行分析判断.本题难度不大,掌握溶液的酸碱性和溶液pH大小之间的关系是正确解答此类题的关键.
9.【答案】 C
【解析】【解答】A、波尔多液中的二种成份分别是硫酸铜和氢氧化钙,其中硫酸铜属于盐,氢氧化钙属于碱,故错误;A不符合题意;
B、用KClO3及双氧水制O2时,加入的MnO2作用相同,故错误;B不符合题意;
C、高炉炼铁中所需的高温和CO的生成都与焦炭有关,正确;C符合题意;
D、 酸碱中和反应生成盐和水,生成盐和水的反应不一定是中和反应,故错误;D不符合题意.
故答案为:C.
【分析】本题主要考查盐的概念、催化剂的作用、炼铁的原理及中和反应的判断.
10.【答案】 B
【解析】A、二氧化碳是大气的成分之一,含量过多会形成温室效应,与水反应生成的碳酸酸性很弱不会形成酸雨,故错误; B、二氧化硫能和水反应生成亚硫酸,当雨水的pH<5.6时就形成酸雨.故正确; C、一氧化碳虽有毒,但不与水反应,不会形成酸雨,故错误; D、臭氧是一种氧的单质,能阻挡紫外线,但不是形成酸雨的气体,故错误. 故选B.
二、填空题
11.【答案】乳化;<
【解析】【解答】洗涤剂能对油污起乳化作用,故答案为:乳化; 碱性洗发水对头发有损坏,用护发素护理,因而护发素呈酸性,故答案为:<。 【分析】此题从生活实际出发,考查了洗涤剂能清洗餐具上的油污,考查了碱性洗发水对头发有损坏,故洗完头发后,用酸性护发素护理.要联系生活实际,从化学中走入生活,从生活中走入化学。
12.【答案】D
【解析】【解答】解:减少用煤作燃料、将燃料脱硫、开发新能源等措施可以减少二氧化硫、氮氧化物的产生,有利于防止酸雨的产生;把工厂的烟囱建高仍然能生成二氧化硫和氮氧化物,不能防止酸雨的产生.
故选:D.
【分析】化石燃料燃烧能生成大量的二氧化硫和氮氧化物,这些物质和水反应能生成显酸性的物质,达到一定程度时会形成酸雨.
13.【答案】苹果汁;碱;变小
【解析】【解答】(1)当溶液的pH<7时,随着pH的减小酸性增强,上述液体中,苹果汁的pH最小,酸性最强,故填:苹果汁; (2)鸡蛋清是的pH范围是7.6﹣8.0,大于7,显碱性,故填:碱; (3)氨水的pH范围是8.5﹣10.5,显碱性,盐酸显酸性,因此向一支盛有氨水的试管中滴稀盐酸,则试管中液体的pH会变小,故填:变小. 【分析】当溶液的pH等于7时,呈中性;当溶液的pH大于7时,呈碱性;当溶液的pH小于7时,呈酸性;当溶液的pH<7时,随着pH的减小酸性增强.酸碱能发生中和反应,据此解答.
三、解答题
14.【答案】酸雨;工厂废气处理后排放.
【解析】【解答】雕像的严重腐蚀反映出最主要的环境污染问题是酸雨; 酸雨分为硝酸型酸雨和硫酸型酸雨,煤的燃烧生成二氧化硫引起的是硫酸型酸雨,汽车尾气的排放产生二氧化氮引起的是硝酸型酸雨.减少酸雨的形成,也就是尽量减少酸性气体的排放,如:①限制含硫煤的使用②化工厂尾气经处理达标后排放③使用绿色能源④汽车尾气经处理后排放等. 故答为:酸雨;工厂废气处理后排放. 【分析】雕像的严重腐蚀反映出最主要的环境污染问题是酸雨;然后根据酸雨的形成及危害提出解决的建议.
四、综合题
15.【答案】(1)NaOH + HCl= NaCl+ H2O (2)溶液由红色变无色 (3)小于
【解析】【解答】 (1)氢氧化钠与盐酸反应生成氯化钠和水,反应的化学方程式为NaOH + HCl= NaCl+ H2O;(2)向烧杯中逐滴滴入盐酸至过量,在这个过程中,pH值逐渐降低,会由碱性变为中性,到最后盐酸过量时变为酸性,酚酞在碱性时为红色,碱性和中性为无色,所以盐酸与氢氧化钠发生了化学反应的实验现象是溶液由红色变无色;(3)实验过程中滴入盐酸过量实验后溶液呈酸性,溶液的pH小于7。 【分析】牢记稀盐酸滴加到氢氧化钠溶液中的曲线变化和氢氧化钠滴加到稀盐酸中的曲边变化的比较是解题的关键。
16.【答案】(1)溶液由红色变为无色 (2)Na+;OH﹣;Cl﹣ (3)OH﹣
【解析】【解答】解:(1)氢氧化钠与盐酸反应生成氯化钠和水,方程式为:NaOH+HCl=NaCl+H2O;氯化钠呈中性,盐酸过量,使反应后溶液呈酸性,中性或酸性溶液不能使酚酞变色.(2)反应前,溶液中含有大量的氢离子、氯离子,钠离子、氢氧根离子,反应后,溶液中含有大量的氯离子、钠离子;故三种离子分别为:Na+、OH﹣、Cl﹣;(3)氨水(NH3?H2O)也能使酚酞变色,原因是氨水和氢氧化钠溶液中均含有一种相同离子,该离子是OH﹣
答案:(1)溶液由红色变为无色;(2)Na+、OH﹣、Cl﹣;(3)OH﹣ .
【分析】(1)根据氢氧化钠溶液显碱性,结合酚酞溶液遇酸性、中性溶液不变色,遇碱性溶液变红色,进行分析解答;(2)根据反应的实质,可以知道溶液里面粒子的变化情况;(3)根据碱性溶液能使酚酞变红色解答.
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
