鲁教版(五四)八年级化学 5.2化学反应的表示 同步练习(含解析)
文档属性
| 名称 | 鲁教版(五四)八年级化学 5.2化学反应的表示 同步练习(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 111.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-06-25 00:00:00 | ||
图片预览



文档简介
鲁教版(五四)八年级 化学跟踪训练 5.2化学反应的表示
一、单选题
1.下列化学方程式书写正确的是(?? )
A.?CH4 +2O2?? 2H2O + CO2??????????????????????B.?P+ O2?? P2O5 C.?S+O2 SO2↑????????????????????????????????????????????D.?4Fe+3O2?? 2Fe2O3
2. 下列反应的化学方程式不正确的是( )
A.?用胃舒平【主要成分是Al(OH)3】治疗胃酸过多症:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O B.?用熟石灰处理硫酸厂排放的污水:Ca(OH)2+H2SO4═CaSO4+2H2O C.?用烧碱溶液处理炼铜厂用黄铜矿(CuFeS2)、辉铜矿(Cu2S)炼铜排出的废气中的二氧化硫:SO2+2NaOH═Na2SO3+H2O D.??新使用的铝桶或铝壶,浸水部分变黑:2Al+Fe2(SO4)3═Al2(SO4)3+2Fe
3.下列书写完全正确的化学方程式是 ()
A.?Fe+ CuSO4 = FeSO4 + Cu↓?????????????????????????????B.?Na2CO3 + HCl =NaCl + H2O + CO2↑ C.?3C+ 2Fe2O34Fe + 3CO2↑?????????????????????????D.?Mg + O2 MgO2
4.用化学方程式解释生活中的现象,其中方程式书写正确的是(?? )
A.?用熟石灰处理工厂硫酸废水:CaO+H2SO4═CaSO4+H2O B.?铝在空气中易形成氧化铝:Al+O2═AlO C.?用石灰水刷墙,墙表面变白变硬:CaO+CO2═CaCO3 D.?用硫酸铜配制波尔多液,不用铁桶的原因:Fe+CuSO4═FeSO4+Cu
5.已知 2NaClO3+H2SO4+SO2=2X+2NaHSO4 由此可知X物质的化学式为( ???)
A.?ClO2???????????????????????????????????B.?NaCl???????????????????????????????????C.?NaClO???????????????????????????????????D.?Cl2O
6.下列化学方程式书写正确的是(?? )
A.?2H2O2 2H2+O2???????????????????????????????????????B.?4Fe+3O2 ?2Fe2O3 C.?P4+5O2 2P2O5???????????????????????????????????????D.?2H2+O2 2H2O
7.下列化学方程式,书写正确的是(?? )
A.?4Fe+ 3O2 ?2Fe2O3?????????????????????????????????B.?2C + O2 ?2CO↑ C.?P+ O2 P2O5????????????????????????????????????????????D.?H2CO3=CO2↑+H2O
8. 下列指定反应的化学方程式正确的是( )
A.?铁丝在氧气中燃烧:4Fe+3O2?2Fe2O3 B.?铝片溶于稀硫酸:Al+H2SO4═AlSO4+H2↑ C.?铜绿的形成:2Cu+O2+H2O+CO2═Cu2(OH)2CO3 D.?过氧化钠与二氧化碳反应生成纯碱和氧气:Na2O2+CO2═Na2CO3+O2
9.同学们对某化学反应的共识如下:①反应在点燃条件下进行②属于化合反应③各物质的分子个数比为2:1:2④各物质的质量比为7:4:11.符合以上要求的反应是(? )
A.?石蜡在空气中燃烧生成水和二氧化碳??????????????????B.?碳在空气中燃烧生成二氧化碳 C.?一氧化碳在空气中燃烧生成二氧化碳??????????????????D.?氢气在空气中燃烧生成水
10.4Al+3O22Al2O3这一反应中,Al、O2、Al2O3三种物质之间的质量比为( )
A.?4:3:2????????????????????????B.?27:24:51????????????????????????C.?27:32:102????????????????????????D.?无法确定
二、填空题
11.?初中化学常见的七种物质A-G,所属物质类别和组成元素的种类如下表。
物质分类
?????单质
化合物
元素种类
金属
非金属
两种
三种
物质代号
A、B
C、D
E、F
G
其中A、B均能与C反应,A与C反应的生成物所含两种元素的质量比是3︰2;B与C反应的生成物组成元素与E相同;C与D反应的生成物常温下为液态,其组成元素与F相同;A、B均能与G溶液反应,且反应后所得溶液的质量均增加。请回答: (1)C的一种用途是________?;E的化学式是________?;F所含的元素是________?。 (2)写出反应的化学方程式:① B+C________?;② C+D________?;③ A+G________?。
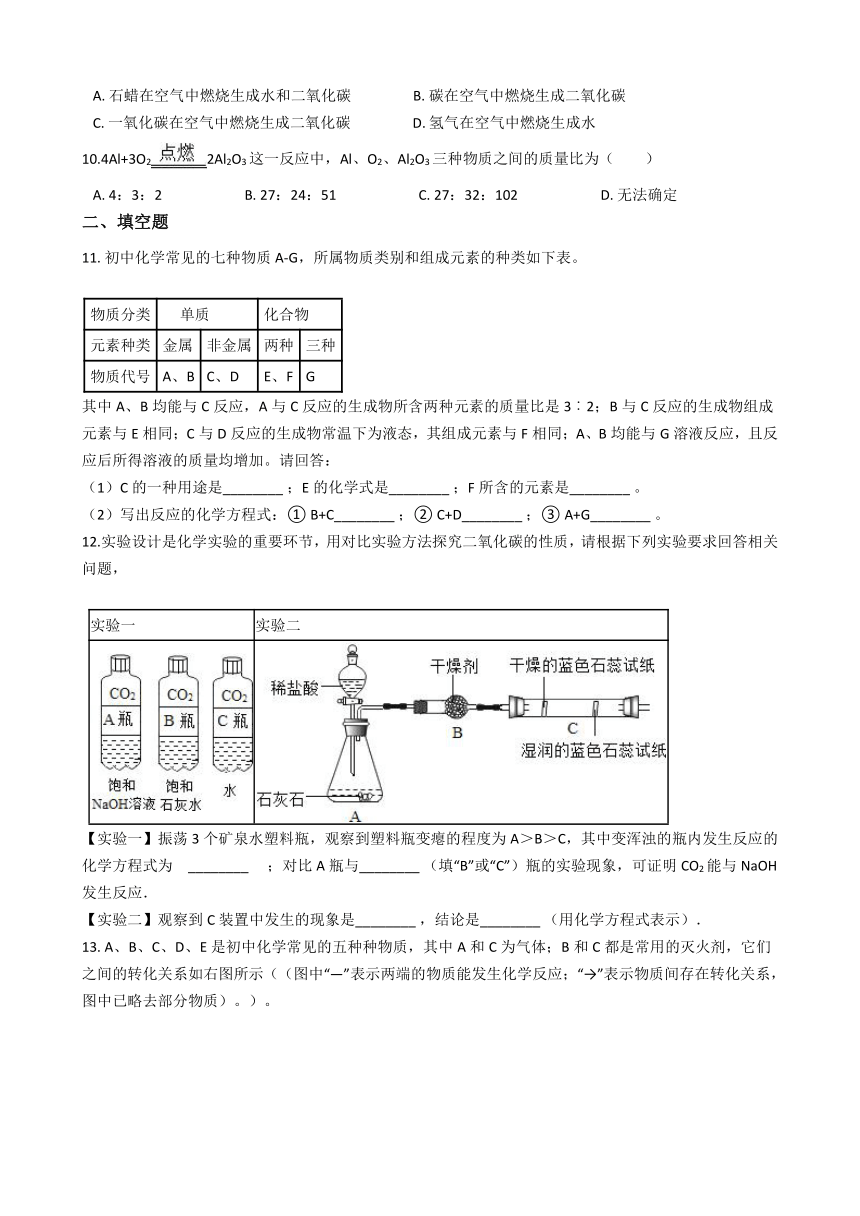
12.实验设计是化学实验的重要环节,用对比实验方法探究二氧化碳的性质,请根据下列实验要求回答相关问题,
实验一
实验二
【实验一】振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为 ________? ;对比A瓶与________?(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
【实验二】观察到C装置中发生的现象是________?,结论是________?(用化学方程式表示).
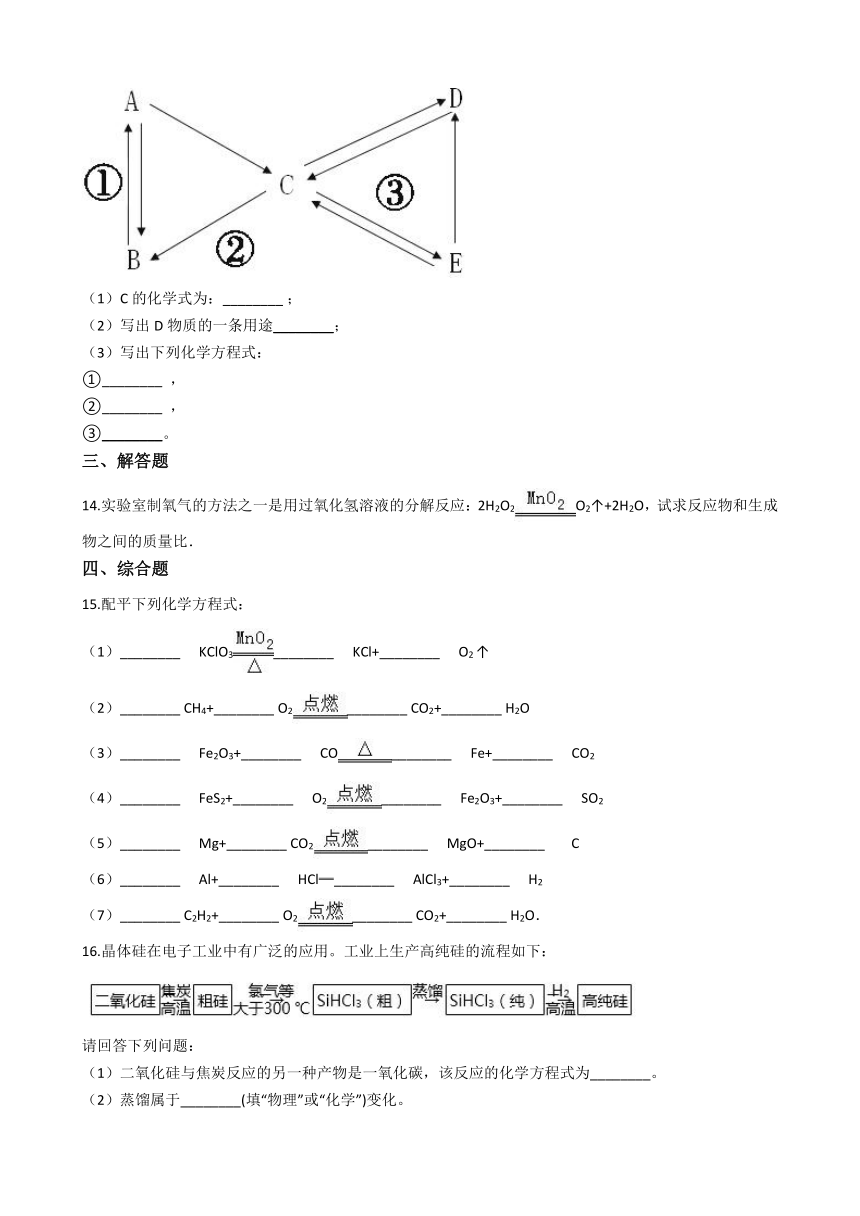
13.?A、B、C、D、E是初中化学常见的五种种物质,其中A和C为气体;B和C都是常用的灭火剂,它们之间的转化关系如右图所示((图中“—”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质)。)。 (1)C的化学式为:________?; (2)写出D物质的一条用途________; (3)写出下列化学方程式: ①________ , ②________ , ③________。
三、解答题
14.实验室制氧气的方法之一是用过氧化氢溶液的分解反应:2H2O2O2↑+2H2O,试求反应物和生成物之间的质量比.
四、综合题
15.配平下列化学方程式:
(1)________? KClO3________? KCl+________? O2 ↑
(2)________?CH4+________?O2________?CO2+________?H2O
(3)________? Fe2O3+________? CO________? Fe+________? CO2
(4)________? FeS2+________? O2________? Fe2O3+________? SO2
(5)________? Mg+________?CO2________? MgO+________? C
(6)________? Al+________? HCl═________? AlCl3+________? H2
(7)________?C2H2+________?O2________?CO2+________?H2O.
16.晶体硅在电子工业中有广泛的应用。工业上生产高纯硅的流程如下:
请回答下列问题:
(1)二氧化硅与焦炭反应的另一种产物是一氧化碳,该反应的化学方程式为________。
(2)蒸馏属于________(填“物理”或“化学”)变化。
(3)完成由下列纯SiHCl3制取高纯硅的化学方程式:
________SiHCl3+________H2 ________Si+________。
答案解析部分
一、单选题
1.【答案】 D
【解析】【解答】A、甲烷和氧气反应生成水和二氧化碳,反应方程式为:CH4 +2O2 2H2O + CO2 , 故A正确;A不符合题意; B、磷和氧气反应生成五氧化二磷,该反应方程式未配平,正确的为:4P+5O2 2P2O5 , 故B错误;B不符合题意; C、硫和氧气反应生成二氧化硫,反应方程式为:S+O2 SO2 , 故C错误;C不符合题意; D、铁和氧气反应生成四氧化三铁,反应方程式为:3Fe+2O2 Fe3O4 , 故D错误;故选D。D符合题意; 【分析】书写化学方程式要遵守的原则:① 必须以客观事实为基础; ② 必须遵守质量守恒定律。 化学方程式时常出现的错误:不尊重科学实验,随意臆造化学式或事实上不存在的化学反应。不遵守质量守恒定律、没有配平或计量数不是最简比。化学式书写错误。写错或漏写反应条件。错标或漏标“↑”(气体生成符号)、“↓”(沉淀符号)。“↑”:如果在反应物中没有气体,而生成物中有气体,那么应该在生成气体的化学式后面标“↑”
2.【答案】 A
【解析】【解答】解:A、氢氧化铝与胃液中的盐酸反应生成氯化铝和水,正确的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O;
B、该化学方程式书写完全正确;
C、二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,正确的化学方程式为SO2+2NaOH═Na2SO3+H2O;
D、该化学方程式书写完全正确.
故选:A.
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
3.【答案】 C
【解析】
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
【解答】A、该化学方程式中反应物中铁是固体,铜的后面不需要标注↓,正确的化学方程式应为:Fe+CuSO4═FeSO4+Cu. B、该化学方程式没有配平,正确的化学方程式应为Na2CO3+2HCl═2NaCl+H2O+CO2↑. C、该化学方程式书写完全正确. D、该化学方程式氧化镁的化学式书写错误,正确的化学方程式应为。
故选C.
【点评】本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断,化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.
4.【答案】D
【解析】【解答】解:A、熟石灰是氢氧化钙的俗称,CaO的俗称生石灰,故选项错误;
B、铝在空气中易形成氧化铝反应的化学方程式为:4Al+3O2═2Al2O3;故选项错误;
C、石灰水是氢氧化钙的水溶液,与空气中的二氧化碳反应生成碳酸钙和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O,故选项错误;
D、铁能置换硫酸铜中的铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;故不能用铁桶配制波尔多液,故选项正确;
故选D
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确;若化学方程式书写正确,再判断是否属于基本反应类型.
5.【答案】 A
【解析】由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2NaClO3+H2SO4+SO2═2X+2NaHSO4 , 反应前钠、氯、氧、氢、硫原子个数分别为2、2、6、10、2、2,反应后的生成物中钠、氯、氧、氢、硫原子个数分别为2、0、8、2、2,根据反应前后原子种类、数目不变,则,2X分子中含有2个氯原子和4个氧原子,则每个X分子由1个氯原子和2个氧原子构成,则物质X的化学式为ClO2。
故答案为:A。
【分析】本题有两种结题思路,一种是质量守恒定律,反应前后原子数目是不变的,通过等式左右两边的原子数目,判断答案为A,另一种是通过化学方程式的配平来解答
6.【答案】 D
【解析】【解答】解:A、水通电分解生成氢气和氧气,过氧化氢分解生成水和氧气,选项化学方程式书写错误,故A不符合题意;
B、铁在氧气中燃烧生成四氧化三铁,正确的化学方程式为3Fe+2O2 Fe3O4 , 故B不符合题意;
C、磷在空气中燃烧生成五氧化二磷,正确的化学方程式为:4P+5O2 2P2O5,故C不符合题意;
D、该化学方程式书写完全正确,故D符合题意.
故答案为:D.
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
7.【答案】 D
【解析】【解答】A、铁在氧气中燃烧生成四氧化三铁,正确的化学方程式为:3Fe+2O2Fe3O4 . A不符合题意; B、该化学方程式中反应物中氧气是气体,一氧化碳后面不需要标注↑,正确的化学方程式为:2C+O2?2CO.B不符合题意; C、该化学方程式缺乏反应条件,正确的化学方程式应为:2H2+O22H2O.C不符合题意; D、该化学方程式书写完全正确.D符合题意. 故答案为:D.
【分析】判断一个化学反应方程式是否正确,需要考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.据此判断即可.
8.【答案】 C
【解析】【解答】A、铁在氧气中燃烧的化学方程式为:3Fe+2O2?Fe3O4 , 该选项书写不正确;
B、铝和稀硫酸反应的化学方程式为:2Al+3H2SO4═Al2(SO4)3+3H2↑,该选项书写不正确;
C、铜绿形成的化学方程式为:2Cu+O2+H2O+CO2═Cu2(OH)2CO3 , 该选项书写正确;
D、过氧化钠和二氧化碳反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2 , 该选项书写不正确.
故选:C.
【分析】A、铁在氧气中燃烧生成四氧化三铁;
B、铝和稀硫酸反应生成硫酸铝和氢气;
C、铜和水、氧气、二氧化碳反应生成碱式碳酸铜;
D、根据反应物、生成物、反应条件及其质量守恒定律可以书写化学方程式.
9.【答案】 C
【解析】【解答】解:A.石蜡与氧气在点燃的条件下反应生成水和二氧化碳,生成物是两种,不符合“多变一”的特征,不属于化合反应,故错误;
B.碳与氧气在点燃的条件下反应生成二氧化碳,反应的方程式为:C+O2 ?CO2 , 不符合各物质的分子个数比为2:1:2,故错误;
C.一氧化碳在空气中燃烧生成二氧化碳,反应的化学方程式为:2CO+O2 ?2CO2 , 该反应符合反应条件是点燃;属于化合反应;各物质的分子个数比为2:1:2;一氧化碳、氧气与二氧化碳的质量比为:56:32:88=7:4:11,故正确;
D.反应的方程式为2H2+O2 ?2H2O,该反应反应条件是点燃,各物质的分子个数比为2:1:2,该反应是化合反应;各物质的质量比(2×2):32:(18×2)=1:8:9,故错误.
故选C.
【分析】由题意,该反应在点燃条件下进行,各物质的分子个数比为2:1:2,该反应是化合反应,各物质的质量比7:4:11;据此结合选项中的化学方程式进行分析判断.
10.【答案】 B
【解析】【解答】解:4A1+3O2═2Al2O3
108??? 96???? 204
在此反应中铝、氧气和氧化铝的质量关系108:96:204=27:24:51或108:96:204=9:8:17.
故选:B.
【分析】首先由反应的化学方程式,利用各物质之间的质量比等于相对分子质量和的比进行计算.
二、填空题
11.【答案】 供给呼吸(炼钢、支持燃烧等) ;Fe2O3 ;氢和氧 ;3 Fe + 2 O2?Fe3O4??? ;2H2 + O2 2H2O ;Mg + H2SO4 = MgSO4 + H2↑?????????????????????????????????????
【解析】【解答】由于A-G是初中化学常见的七种物质,而根据题意可知,金属单质A、B均能与非金属单质C反应,结合所学知识可推测C为O2 , 又由于A与C反应的生成物所含两种元素的质量比是3:2=24:16,故可推测A为金属Mg;由于非金属单质C(O2)与非金属单质D反应的生成物在常温下为液态,可推测其生成物应为H2O,则可推测D为H2;又因为C与D反应的生成物的组成元素与F相同,故可知F为H2O2;金属单质B与非金属单质C(O2)反应的生成物的组成元素与E(含有两种元素)相同,说明该生成物与E均为同种金属的氧化物,符合条件的常见物质应为Fe3O4和Fe2O3 , 则可推测金属单质B为Fe;由于A(Mg)、B(Fe)均能与G溶液反应,说明G应为稀酸或比Mg、Fe不活泼的金属的盐溶液,又因为它们反应后所得溶液的质量均增加,可知G应为稀酸,由于G是由三种元素组成,可推测其为稀硫酸,将以上推测带入原题验证,正确。 【分析】在解此类题时,要学会根据学过的知识先进行有针对性的猜想、假设,然后沿着假设进行推导,只要各步都满足,假设就成立,如不满足,可再假设,再验证。
12.【答案】Ca(OH)2+CO2=CaCO3↓+H2O ;C ;干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色 ;CO2+H2O=H2CO3
【解析】【解答】(1)用对比实验方法探究二氧化碳的性质:实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生的反应是:二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,对比A瓶与C瓶的实验现象,可证明CO2能与NaOH发生反应;故答案为:Ca(OH)2+CO2=CaCO3↓+H2O;C;
(2)实验二观察到C装置中发生的现象是:干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色;因为二氧化碳与水反应生成了碳酸;故答案为:干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色;CO2+H2O=H2CO3 .
【分析】二氧化碳的化学性质有:既不能燃烧也不能支持燃烧,也不供给呼吸;能与水反应生成碳酸;能使澄清的石灰水变浑浊.用对比实验方法探究二氧化碳的性质;实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生的反应是:二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,对比A瓶与C瓶的实验现象,可证明CO2能与NaOH发生反应.
13.【答案】CO2 ? ;用于建筑业 ; ;CO2+Ca(OH)2=CaCO3↓+H2O或CO2+2NaOH=Na2CO3+H2O ;CO2+2NaOH=Na2CO3+H2O
【解析】【解答】(1)由已知A和C为气体;B和C都是常用的灭火剂,得知C的化学式为:CO2; (2)反应生成二氧化碳的方法有:点燃一氧化碳或碳酸钙制取二氧化碳,所以D碳酸钙,碳酸钙可用于建筑、雕刻等; (3)已知反应物,生成物,书写化学方程式: ①2H2O?2H2↑+O2↑; ②CO2+Ca(OH)2=CaCO3↓+H2O或CO2+2NaOH=Na2CO3+H2O; ③CO2+2NaOH=Na2CO3+H2O。 【分析】推断物质,要根据物质的性质,通过实验现象的不同来推断,有时合理额联想也很重要。书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。
三、解答题
14.【答案】解:由化学方程式2H2O22H2O+O2↑可知,反应物和生成物的质量比为反应物和生成物的相对分子质量和之比,即过氧化氢、氧气和水的相对分子质量和之比,具体数值为:68:36:32=17:9:8.
故答案为:过氧化氢、氧气和水的质量比为17:9:8.
【解析】【分析】可以根据化学方程式表示的含义方面进行分析、判断,从而得出正确的结论.
四、综合题
15.【答案】(1)2 ;2 ;3
(2)1 ;2 ;1 ;2
(3)1 ;3 ;2 ;3
(4)4 ;11 ;2 ;8
(5)2 ;1 ;2 ;1
(6)2 ;6 ;2 ;3
(7)2 ;5 ;4 ;2
【解析】【解答】(1)本题根据反应前后氧原子数目不变,反应前为3个氧原子,反应后为2个氧原子,最小公倍数为6,故KClO3前系数为2,O2前系数为3,再通过观察确定KCl前系数为3;
(2)本题可利用“定一法”进行配平,把CH4的化学计量数定为1,则O2、CO2、H2O前面的化学计量数分别为:2、1、2;
(3)本题可从得失氧的角度配平,一个CO分子反应中获得一个氧原子变为二氧化碳分子,由于一个Fe2O3分子中氧原子的数目为3个,所以CO与CO2前面的化学计量数都为3,最后配平其它元素的原子,Fe2O3、Fe前面的化学计量数分别为1、2;
(4)本题可利用“定一法”进行配平,把Fe2O3的计量数定为1,则FeS2、O2、SO2前面的化学计量数分别为:2、、4,再同时扩大2倍即可;
(5)本题根据O原子个数前后不相等,利用其最小公倍数为2可知氧化镁的系数为2,再利用镁原子个数前后应相等,则镁的系数为2,配平后CO2、C前面的化学计量数分别为:1、1;
(6)本题可利用“定一法”进行配平,把AlCl3的计量数定为1,则Al、HCl、H2前面的化学计量数分别为:1、3、, 再同时扩大2倍即可;
(7)本题利用奇数配偶法进行配平,H2O前面的化学计量数为2,则C2H2、O2、CO2前面的化学计量数分别为:2、5、4.
故答案为:(1)2、2、3;(2)1、2、1、2;(3)1、3、2、3;(4)4、11、2、8;(5)2、1、2、1;(6)2、6、2、3;(7)2、5、4、2;
【分析】根据质量守恒定律:反应前后各原子的数目不变,选择相应的配平方法(最小公倍数法、定一法、奇数配偶法、观察法等)进行配平即可.
16.【答案】(1)SiO2+2C Si+2CO (2)物理 (3)1;1;1;3HCl
【解析】【解答】(1)二氧化硅和焦炭反应的另一种产物是一氧化碳,结合转化关系可知还有硅,故反应的方程式为SiO2+2C Si+2CO;故答案为:SiO2+2C Si+2CO (2)蒸馏是提纯混合物的一种方法,变化前后物质的种类灭有变,因此属于物理变化;故答案为:物理 (3)根据质量守恒定律反应前后原子种类和原子个数不变,反应后缺少的是3个H和3个Cl.故答案为:3HCl 故答案为:(1)SiO2+2C Si+2CO(2)物理(3)1;1;1;3HCl
【分析】(1)根据信息可得:二氧化硅和碳在高温下生成硅和一氧化碳 (2)结合转化关系分析蒸馏发生的变化 (3)根据质量守恒定律分析解答
一、单选题
1.下列化学方程式书写正确的是(?? )
A.?CH4 +2O2?? 2H2O + CO2??????????????????????B.?P+ O2?? P2O5 C.?S+O2 SO2↑????????????????????????????????????????????D.?4Fe+3O2?? 2Fe2O3
2. 下列反应的化学方程式不正确的是( )
A.?用胃舒平【主要成分是Al(OH)3】治疗胃酸过多症:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O B.?用熟石灰处理硫酸厂排放的污水:Ca(OH)2+H2SO4═CaSO4+2H2O C.?用烧碱溶液处理炼铜厂用黄铜矿(CuFeS2)、辉铜矿(Cu2S)炼铜排出的废气中的二氧化硫:SO2+2NaOH═Na2SO3+H2O D.??新使用的铝桶或铝壶,浸水部分变黑:2Al+Fe2(SO4)3═Al2(SO4)3+2Fe
3.下列书写完全正确的化学方程式是 ()
A.?Fe+ CuSO4 = FeSO4 + Cu↓?????????????????????????????B.?Na2CO3 + HCl =NaCl + H2O + CO2↑ C.?3C+ 2Fe2O34Fe + 3CO2↑?????????????????????????D.?Mg + O2 MgO2
4.用化学方程式解释生活中的现象,其中方程式书写正确的是(?? )
A.?用熟石灰处理工厂硫酸废水:CaO+H2SO4═CaSO4+H2O B.?铝在空气中易形成氧化铝:Al+O2═AlO C.?用石灰水刷墙,墙表面变白变硬:CaO+CO2═CaCO3 D.?用硫酸铜配制波尔多液,不用铁桶的原因:Fe+CuSO4═FeSO4+Cu
5.已知 2NaClO3+H2SO4+SO2=2X+2NaHSO4 由此可知X物质的化学式为( ???)
A.?ClO2???????????????????????????????????B.?NaCl???????????????????????????????????C.?NaClO???????????????????????????????????D.?Cl2O
6.下列化学方程式书写正确的是(?? )
A.?2H2O2 2H2+O2???????????????????????????????????????B.?4Fe+3O2 ?2Fe2O3 C.?P4+5O2 2P2O5???????????????????????????????????????D.?2H2+O2 2H2O
7.下列化学方程式,书写正确的是(?? )
A.?4Fe+ 3O2 ?2Fe2O3?????????????????????????????????B.?2C + O2 ?2CO↑ C.?P+ O2 P2O5????????????????????????????????????????????D.?H2CO3=CO2↑+H2O
8. 下列指定反应的化学方程式正确的是( )
A.?铁丝在氧气中燃烧:4Fe+3O2?2Fe2O3 B.?铝片溶于稀硫酸:Al+H2SO4═AlSO4+H2↑ C.?铜绿的形成:2Cu+O2+H2O+CO2═Cu2(OH)2CO3 D.?过氧化钠与二氧化碳反应生成纯碱和氧气:Na2O2+CO2═Na2CO3+O2
9.同学们对某化学反应的共识如下:①反应在点燃条件下进行②属于化合反应③各物质的分子个数比为2:1:2④各物质的质量比为7:4:11.符合以上要求的反应是(? )
A.?石蜡在空气中燃烧生成水和二氧化碳??????????????????B.?碳在空气中燃烧生成二氧化碳 C.?一氧化碳在空气中燃烧生成二氧化碳??????????????????D.?氢气在空气中燃烧生成水
10.4Al+3O22Al2O3这一反应中,Al、O2、Al2O3三种物质之间的质量比为( )
A.?4:3:2????????????????????????B.?27:24:51????????????????????????C.?27:32:102????????????????????????D.?无法确定
二、填空题
11.?初中化学常见的七种物质A-G,所属物质类别和组成元素的种类如下表。
物质分类
?????单质
化合物
元素种类
金属
非金属
两种
三种
物质代号
A、B
C、D
E、F
G
其中A、B均能与C反应,A与C反应的生成物所含两种元素的质量比是3︰2;B与C反应的生成物组成元素与E相同;C与D反应的生成物常温下为液态,其组成元素与F相同;A、B均能与G溶液反应,且反应后所得溶液的质量均增加。请回答: (1)C的一种用途是________?;E的化学式是________?;F所含的元素是________?。 (2)写出反应的化学方程式:① B+C________?;② C+D________?;③ A+G________?。
12.实验设计是化学实验的重要环节,用对比实验方法探究二氧化碳的性质,请根据下列实验要求回答相关问题,
实验一
实验二
【实验一】振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为 ________? ;对比A瓶与________?(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
【实验二】观察到C装置中发生的现象是________?,结论是________?(用化学方程式表示).
13.?A、B、C、D、E是初中化学常见的五种种物质,其中A和C为气体;B和C都是常用的灭火剂,它们之间的转化关系如右图所示((图中“—”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质)。)。 (1)C的化学式为:________?; (2)写出D物质的一条用途________; (3)写出下列化学方程式: ①________ , ②________ , ③________。
三、解答题
14.实验室制氧气的方法之一是用过氧化氢溶液的分解反应:2H2O2O2↑+2H2O,试求反应物和生成物之间的质量比.
四、综合题
15.配平下列化学方程式:
(1)________? KClO3________? KCl+________? O2 ↑
(2)________?CH4+________?O2________?CO2+________?H2O
(3)________? Fe2O3+________? CO________? Fe+________? CO2
(4)________? FeS2+________? O2________? Fe2O3+________? SO2
(5)________? Mg+________?CO2________? MgO+________? C
(6)________? Al+________? HCl═________? AlCl3+________? H2
(7)________?C2H2+________?O2________?CO2+________?H2O.
16.晶体硅在电子工业中有广泛的应用。工业上生产高纯硅的流程如下:
请回答下列问题:
(1)二氧化硅与焦炭反应的另一种产物是一氧化碳,该反应的化学方程式为________。
(2)蒸馏属于________(填“物理”或“化学”)变化。
(3)完成由下列纯SiHCl3制取高纯硅的化学方程式:
________SiHCl3+________H2 ________Si+________。
答案解析部分
一、单选题
1.【答案】 D
【解析】【解答】A、甲烷和氧气反应生成水和二氧化碳,反应方程式为:CH4 +2O2 2H2O + CO2 , 故A正确;A不符合题意; B、磷和氧气反应生成五氧化二磷,该反应方程式未配平,正确的为:4P+5O2 2P2O5 , 故B错误;B不符合题意; C、硫和氧气反应生成二氧化硫,反应方程式为:S+O2 SO2 , 故C错误;C不符合题意; D、铁和氧气反应生成四氧化三铁,反应方程式为:3Fe+2O2 Fe3O4 , 故D错误;故选D。D符合题意; 【分析】书写化学方程式要遵守的原则:① 必须以客观事实为基础; ② 必须遵守质量守恒定律。 化学方程式时常出现的错误:不尊重科学实验,随意臆造化学式或事实上不存在的化学反应。不遵守质量守恒定律、没有配平或计量数不是最简比。化学式书写错误。写错或漏写反应条件。错标或漏标“↑”(气体生成符号)、“↓”(沉淀符号)。“↑”:如果在反应物中没有气体,而生成物中有气体,那么应该在生成气体的化学式后面标“↑”
2.【答案】 A
【解析】【解答】解:A、氢氧化铝与胃液中的盐酸反应生成氯化铝和水,正确的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O;
B、该化学方程式书写完全正确;
C、二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,正确的化学方程式为SO2+2NaOH═Na2SO3+H2O;
D、该化学方程式书写完全正确.
故选:A.
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
3.【答案】 C
【解析】
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
【解答】A、该化学方程式中反应物中铁是固体,铜的后面不需要标注↓,正确的化学方程式应为:Fe+CuSO4═FeSO4+Cu. B、该化学方程式没有配平,正确的化学方程式应为Na2CO3+2HCl═2NaCl+H2O+CO2↑. C、该化学方程式书写完全正确. D、该化学方程式氧化镁的化学式书写错误,正确的化学方程式应为。
故选C.
【点评】本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断,化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.
4.【答案】D
【解析】【解答】解:A、熟石灰是氢氧化钙的俗称,CaO的俗称生石灰,故选项错误;
B、铝在空气中易形成氧化铝反应的化学方程式为:4Al+3O2═2Al2O3;故选项错误;
C、石灰水是氢氧化钙的水溶液,与空气中的二氧化碳反应生成碳酸钙和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O,故选项错误;
D、铁能置换硫酸铜中的铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;故不能用铁桶配制波尔多液,故选项正确;
故选D
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确;若化学方程式书写正确,再判断是否属于基本反应类型.
5.【答案】 A
【解析】由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2NaClO3+H2SO4+SO2═2X+2NaHSO4 , 反应前钠、氯、氧、氢、硫原子个数分别为2、2、6、10、2、2,反应后的生成物中钠、氯、氧、氢、硫原子个数分别为2、0、8、2、2,根据反应前后原子种类、数目不变,则,2X分子中含有2个氯原子和4个氧原子,则每个X分子由1个氯原子和2个氧原子构成,则物质X的化学式为ClO2。
故答案为:A。
【分析】本题有两种结题思路,一种是质量守恒定律,反应前后原子数目是不变的,通过等式左右两边的原子数目,判断答案为A,另一种是通过化学方程式的配平来解答
6.【答案】 D
【解析】【解答】解:A、水通电分解生成氢气和氧气,过氧化氢分解生成水和氧气,选项化学方程式书写错误,故A不符合题意;
B、铁在氧气中燃烧生成四氧化三铁,正确的化学方程式为3Fe+2O2 Fe3O4 , 故B不符合题意;
C、磷在空气中燃烧生成五氧化二磷,正确的化学方程式为:4P+5O2 2P2O5,故C不符合题意;
D、该化学方程式书写完全正确,故D符合题意.
故答案为:D.
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
7.【答案】 D
【解析】【解答】A、铁在氧气中燃烧生成四氧化三铁,正确的化学方程式为:3Fe+2O2Fe3O4 . A不符合题意; B、该化学方程式中反应物中氧气是气体,一氧化碳后面不需要标注↑,正确的化学方程式为:2C+O2?2CO.B不符合题意; C、该化学方程式缺乏反应条件,正确的化学方程式应为:2H2+O22H2O.C不符合题意; D、该化学方程式书写完全正确.D符合题意. 故答案为:D.
【分析】判断一个化学反应方程式是否正确,需要考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.据此判断即可.
8.【答案】 C
【解析】【解答】A、铁在氧气中燃烧的化学方程式为:3Fe+2O2?Fe3O4 , 该选项书写不正确;
B、铝和稀硫酸反应的化学方程式为:2Al+3H2SO4═Al2(SO4)3+3H2↑,该选项书写不正确;
C、铜绿形成的化学方程式为:2Cu+O2+H2O+CO2═Cu2(OH)2CO3 , 该选项书写正确;
D、过氧化钠和二氧化碳反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2 , 该选项书写不正确.
故选:C.
【分析】A、铁在氧气中燃烧生成四氧化三铁;
B、铝和稀硫酸反应生成硫酸铝和氢气;
C、铜和水、氧气、二氧化碳反应生成碱式碳酸铜;
D、根据反应物、生成物、反应条件及其质量守恒定律可以书写化学方程式.
9.【答案】 C
【解析】【解答】解:A.石蜡与氧气在点燃的条件下反应生成水和二氧化碳,生成物是两种,不符合“多变一”的特征,不属于化合反应,故错误;
B.碳与氧气在点燃的条件下反应生成二氧化碳,反应的方程式为:C+O2 ?CO2 , 不符合各物质的分子个数比为2:1:2,故错误;
C.一氧化碳在空气中燃烧生成二氧化碳,反应的化学方程式为:2CO+O2 ?2CO2 , 该反应符合反应条件是点燃;属于化合反应;各物质的分子个数比为2:1:2;一氧化碳、氧气与二氧化碳的质量比为:56:32:88=7:4:11,故正确;
D.反应的方程式为2H2+O2 ?2H2O,该反应反应条件是点燃,各物质的分子个数比为2:1:2,该反应是化合反应;各物质的质量比(2×2):32:(18×2)=1:8:9,故错误.
故选C.
【分析】由题意,该反应在点燃条件下进行,各物质的分子个数比为2:1:2,该反应是化合反应,各物质的质量比7:4:11;据此结合选项中的化学方程式进行分析判断.
10.【答案】 B
【解析】【解答】解:4A1+3O2═2Al2O3
108??? 96???? 204
在此反应中铝、氧气和氧化铝的质量关系108:96:204=27:24:51或108:96:204=9:8:17.
故选:B.
【分析】首先由反应的化学方程式,利用各物质之间的质量比等于相对分子质量和的比进行计算.
二、填空题
11.【答案】 供给呼吸(炼钢、支持燃烧等) ;Fe2O3 ;氢和氧 ;3 Fe + 2 O2?Fe3O4??? ;2H2 + O2 2H2O ;Mg + H2SO4 = MgSO4 + H2↑?????????????????????????????????????
【解析】【解答】由于A-G是初中化学常见的七种物质,而根据题意可知,金属单质A、B均能与非金属单质C反应,结合所学知识可推测C为O2 , 又由于A与C反应的生成物所含两种元素的质量比是3:2=24:16,故可推测A为金属Mg;由于非金属单质C(O2)与非金属单质D反应的生成物在常温下为液态,可推测其生成物应为H2O,则可推测D为H2;又因为C与D反应的生成物的组成元素与F相同,故可知F为H2O2;金属单质B与非金属单质C(O2)反应的生成物的组成元素与E(含有两种元素)相同,说明该生成物与E均为同种金属的氧化物,符合条件的常见物质应为Fe3O4和Fe2O3 , 则可推测金属单质B为Fe;由于A(Mg)、B(Fe)均能与G溶液反应,说明G应为稀酸或比Mg、Fe不活泼的金属的盐溶液,又因为它们反应后所得溶液的质量均增加,可知G应为稀酸,由于G是由三种元素组成,可推测其为稀硫酸,将以上推测带入原题验证,正确。 【分析】在解此类题时,要学会根据学过的知识先进行有针对性的猜想、假设,然后沿着假设进行推导,只要各步都满足,假设就成立,如不满足,可再假设,再验证。
12.【答案】Ca(OH)2+CO2=CaCO3↓+H2O ;C ;干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色 ;CO2+H2O=H2CO3
【解析】【解答】(1)用对比实验方法探究二氧化碳的性质:实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生的反应是:二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,对比A瓶与C瓶的实验现象,可证明CO2能与NaOH发生反应;故答案为:Ca(OH)2+CO2=CaCO3↓+H2O;C;
(2)实验二观察到C装置中发生的现象是:干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色;因为二氧化碳与水反应生成了碳酸;故答案为:干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色;CO2+H2O=H2CO3 .
【分析】二氧化碳的化学性质有:既不能燃烧也不能支持燃烧,也不供给呼吸;能与水反应生成碳酸;能使澄清的石灰水变浑浊.用对比实验方法探究二氧化碳的性质;实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生的反应是:二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,对比A瓶与C瓶的实验现象,可证明CO2能与NaOH发生反应.
13.【答案】CO2 ? ;用于建筑业 ; ;CO2+Ca(OH)2=CaCO3↓+H2O或CO2+2NaOH=Na2CO3+H2O ;CO2+2NaOH=Na2CO3+H2O
【解析】【解答】(1)由已知A和C为气体;B和C都是常用的灭火剂,得知C的化学式为:CO2; (2)反应生成二氧化碳的方法有:点燃一氧化碳或碳酸钙制取二氧化碳,所以D碳酸钙,碳酸钙可用于建筑、雕刻等; (3)已知反应物,生成物,书写化学方程式: ①2H2O?2H2↑+O2↑; ②CO2+Ca(OH)2=CaCO3↓+H2O或CO2+2NaOH=Na2CO3+H2O; ③CO2+2NaOH=Na2CO3+H2O。 【分析】推断物质,要根据物质的性质,通过实验现象的不同来推断,有时合理额联想也很重要。书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。
三、解答题
14.【答案】解:由化学方程式2H2O22H2O+O2↑可知,反应物和生成物的质量比为反应物和生成物的相对分子质量和之比,即过氧化氢、氧气和水的相对分子质量和之比,具体数值为:68:36:32=17:9:8.
故答案为:过氧化氢、氧气和水的质量比为17:9:8.
【解析】【分析】可以根据化学方程式表示的含义方面进行分析、判断,从而得出正确的结论.
四、综合题
15.【答案】(1)2 ;2 ;3
(2)1 ;2 ;1 ;2
(3)1 ;3 ;2 ;3
(4)4 ;11 ;2 ;8
(5)2 ;1 ;2 ;1
(6)2 ;6 ;2 ;3
(7)2 ;5 ;4 ;2
【解析】【解答】(1)本题根据反应前后氧原子数目不变,反应前为3个氧原子,反应后为2个氧原子,最小公倍数为6,故KClO3前系数为2,O2前系数为3,再通过观察确定KCl前系数为3;
(2)本题可利用“定一法”进行配平,把CH4的化学计量数定为1,则O2、CO2、H2O前面的化学计量数分别为:2、1、2;
(3)本题可从得失氧的角度配平,一个CO分子反应中获得一个氧原子变为二氧化碳分子,由于一个Fe2O3分子中氧原子的数目为3个,所以CO与CO2前面的化学计量数都为3,最后配平其它元素的原子,Fe2O3、Fe前面的化学计量数分别为1、2;
(4)本题可利用“定一法”进行配平,把Fe2O3的计量数定为1,则FeS2、O2、SO2前面的化学计量数分别为:2、、4,再同时扩大2倍即可;
(5)本题根据O原子个数前后不相等,利用其最小公倍数为2可知氧化镁的系数为2,再利用镁原子个数前后应相等,则镁的系数为2,配平后CO2、C前面的化学计量数分别为:1、1;
(6)本题可利用“定一法”进行配平,把AlCl3的计量数定为1,则Al、HCl、H2前面的化学计量数分别为:1、3、, 再同时扩大2倍即可;
(7)本题利用奇数配偶法进行配平,H2O前面的化学计量数为2,则C2H2、O2、CO2前面的化学计量数分别为:2、5、4.
故答案为:(1)2、2、3;(2)1、2、1、2;(3)1、3、2、3;(4)4、11、2、8;(5)2、1、2、1;(6)2、6、2、3;(7)2、5、4、2;
【分析】根据质量守恒定律:反应前后各原子的数目不变,选择相应的配平方法(最小公倍数法、定一法、奇数配偶法、观察法等)进行配平即可.
16.【答案】(1)SiO2+2C Si+2CO (2)物理 (3)1;1;1;3HCl
【解析】【解答】(1)二氧化硅和焦炭反应的另一种产物是一氧化碳,结合转化关系可知还有硅,故反应的方程式为SiO2+2C Si+2CO;故答案为:SiO2+2C Si+2CO (2)蒸馏是提纯混合物的一种方法,变化前后物质的种类灭有变,因此属于物理变化;故答案为:物理 (3)根据质量守恒定律反应前后原子种类和原子个数不变,反应后缺少的是3个H和3个Cl.故答案为:3HCl 故答案为:(1)SiO2+2C Si+2CO(2)物理(3)1;1;1;3HCl
【分析】(1)根据信息可得:二氧化硅和碳在高温下生成硅和一氧化碳 (2)结合转化关系分析蒸馏发生的变化 (3)根据质量守恒定律分析解答
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
