人教版(五四制)九年级化学 第二单元 溶液 单元复习 课件(24张ppt)
文档属性
| 名称 | 人教版(五四制)九年级化学 第二单元 溶液 单元复习 课件(24张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-06-28 00:00:00 | ||
图片预览






文档简介
课件24张PPT。初中化学总复习-溶液■ 了解溶液的概念、组成、会判断溶液;◆学习目标■ 理解固体溶解度、气体溶解度的概念及影响因素;■ 了解溶液的分类:浓溶液、稀溶液与饱和溶液、不饱和溶液;■ 掌握固体溶解度规律及曲线的含义并且会运用;溶 液■ 掌握溶质质量分数的计算方法与溶液的配制方法。一、溶 液◆知识网络溶 液1、概念:3、溶液的组成: 溶质:被溶解的物质(气体、固体、液体)溶剂:能溶解其他物质的物质(水、酒精、汽油等)生活中常见溶液:碘酒 KMnO4溶液 75%的酒精规定:固体溶于液体时 ,液体作溶剂
液体溶于液体时,量多的作溶剂
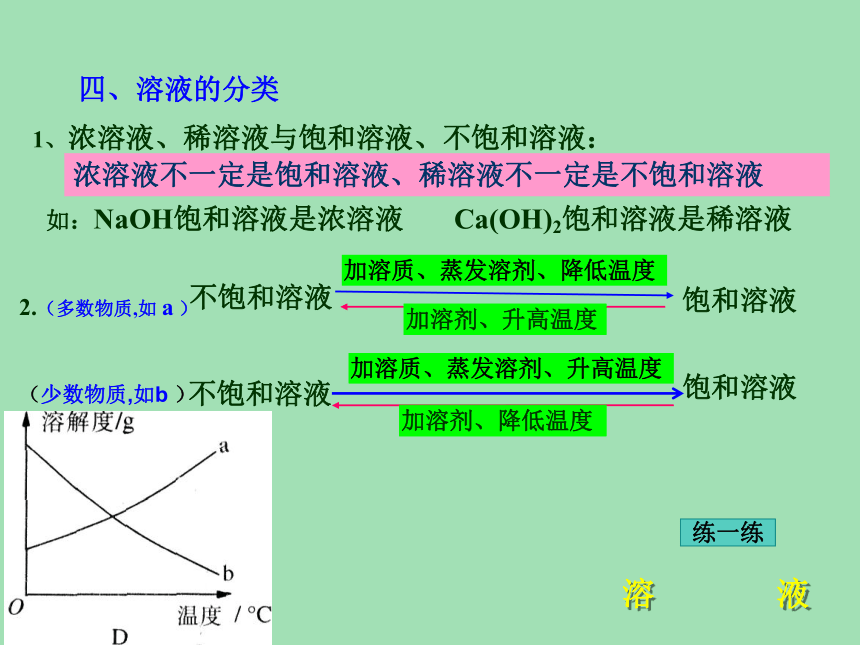
一般有水,无论量多量少水通常作溶剂2、特征:练一练(混合物)均一性、稳定性、混合物由一种或几种物质分散到另一种物质里,形成均一的稳定的混合物。二、溶解时的放热或吸热现象◆知识网络溶 液1、溶解时放热的物质有:3、溶解时温度不变的物质:三、乳化现象洗涤剂具有乳化功能,能乳化油污。2、溶解时吸热的物质:练一练(溶液温度升高)NaOH固体、浓硫酸NH4NO3 (洗涤剂能使植物油在水中分散成无数细小的液滴,而不聚集成大的油珠,从而使油和水不再分层,形成的乳浊液稳定性增强。乳化后形成的细小液滴能随着水流动。)NaCl(溶液温度降低)(温度不变)乳浊液:小液滴分散到液体里形成的混合物叫做乳浊液。四、溶液的分类1、浓溶液、稀溶液与饱和溶液、不饱和溶液: 不饱和溶液饱和溶液加溶剂、升高温度加溶质、蒸发溶剂、降低温度如:NaOH饱和溶液是浓溶液 Ca(OH)2饱和溶液是稀溶液2.(多数物质,如 a )溶 液练一练浓溶液不一定是饱和溶液、稀溶液不一定是不饱和溶液(少数物质,如b )不饱和溶液饱和溶液加溶质、蒸发溶剂、升高温度加溶剂、降低温度五、溶解度1、固体溶解度:(1)四要素: ①一定温度下 ②100g溶剂
③达到饱和状态 ④单位: g
(2)影响因素内因:溶质性质、溶剂性质外因:温度溶 液练一练一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
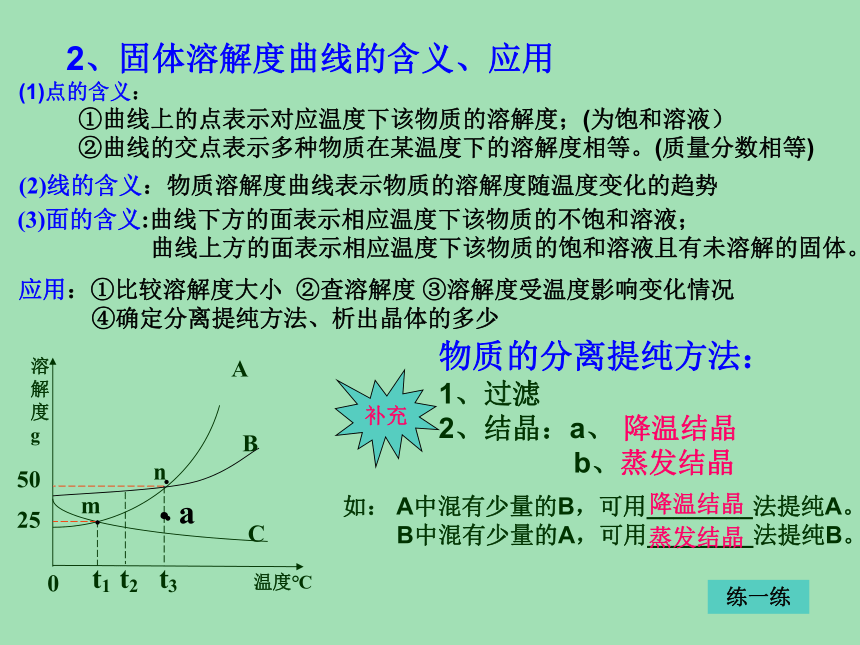
2、固体溶解度曲线的含义、应用应用:①比较溶解度大小 ②查溶解度 ③溶解度受温度影响变化情况
④确定分离提纯方法、析出晶体的多少(1)点的含义:
①曲线上的点表示对应温度下该物质的溶解度;(为饱和溶液)
②曲线的交点表示多种物质在某温度下的溶解度相等。(质量分数相等)25 50 练一练如: A中混有少量的B,可用________法提纯A。
B中混有少量的A,可用________法提纯B。降温结晶蒸发结晶补充(2)线的含义:物质溶解度曲线表示物质的溶解度随温度变化的趋势(3)面的含义:曲线下方的面表示相应温度下该物质的不饱和溶液;
曲线上方的面表示相应温度下该物质的饱和溶液且有未溶解的固体。物质的分离提纯方法:
1、过滤
2、结晶:a、 降温结晶
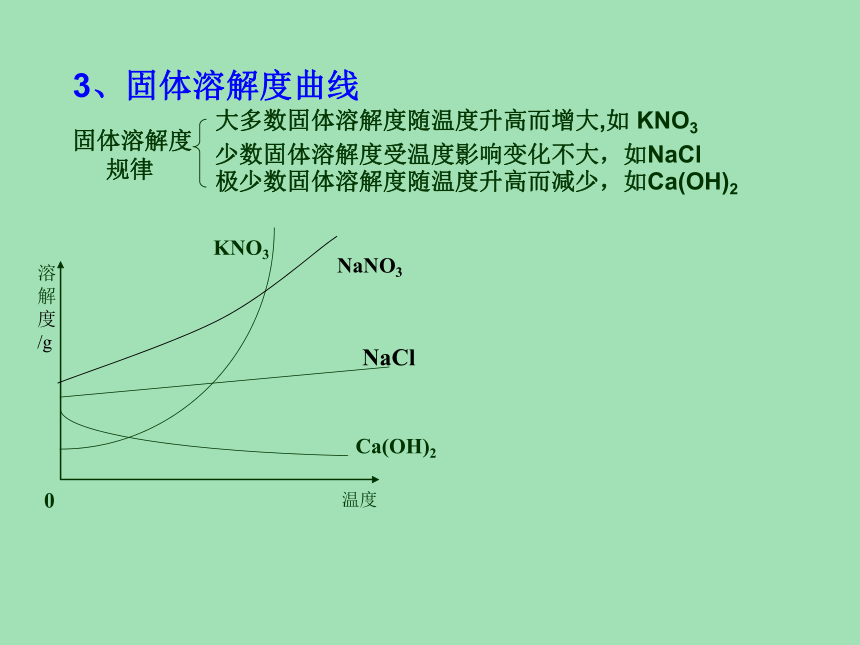
b、蒸发结晶··﹒3、固体溶解度曲线 固体溶解度
规律大多数固体溶解度随温度升高而增大,如 KNO3少数固体溶解度受温度影响变化不大,如NaCl极少数固体溶解度随温度升高而减少,如Ca(OH)2 KNO3 NaCl Ca(OH)2 0 温度 溶
解
度
/g
NaNO34、气体溶解度1)定义:是指该气体在压强为101kPa和一定温度时,
在 1 体积水里达到饱和状态时的气体体积.
2)影响因素内因:气体和水的性质外因:温度和压强3)规律:
气体物质的溶解度随压强减小而减小,
气体物质的溶解度随温度升高而减小。练一练溶 液m溶液 = m溶质 + m溶剂
1、溶质的质量分数=六、溶液的浓度溶质的质量分数=2、饱和溶液中溶质质量分数为:溶解度溶解度 + 100g × 100% 溶 液 练一练 3、溶液稀释的计算依据:
浓溶液中的( )=稀溶液中的( )
4、配制一定溶质质量分数的溶液
(1)用固体配制:
①步骤:( )( )、( )、( )。
②仪器:
(2)用浓溶液稀释(稀释前后,溶质的质量不变)
①步骤:( )、( )、( )。
②仪器:计算称量量取溶解溶质质量溶质质量托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒。计算量取混匀量筒、胶头滴管、烧杯、玻璃棒。溶 液练一练1、下列说法正确的是( )A.凡是均一透明的、稳定的液体就是溶液
B. 高锰酸钾加入水中搅拌所得暗紫色液体不是溶液
C.冰水混合物属于溶液
D.溶液是均一的、稳定的混合物D2、判断下列溶液的溶质、溶剂H2OHClC2H5OH返回你会了吗酒精溶液NaCl溶液盐酸H2OH2O 3.生活中的下列物质,易溶于水而形成溶液的是( )A.面粉B.蔗糖C.植物油 D.铁锈 B4.汽油和洗涤剂都能除油污,原理有何不同?汽油能溶解油污,形成的是溶液;
洗涤剂能乳化油污,形成的是乳浊液。5.向右图试管里的水中加入某种物质后,原来U型管内在同一水平面上的红墨水,右边液面升高了,左边的液面下降了,则加入的物质是( )
A、活性炭 B、生石灰
C、硝酸铵 D、氢氧化钠 BD6、将某物质饱和溶液转变为不饱和溶液最可靠的方法是( )7、下列说法正确的是( )A.升高温度 B. 加入溶质
C. 降低温度 D.加足量的溶剂DA.饱和溶液中溶质的质量一定大于不饱和溶液中溶质的质量。
B. 饱和溶液浓度比不饱和溶液浓度大。
C. 析出晶体的溶液是该温度下这种物质的饱和溶液。
D.一定温度下,同一物质的饱和溶液的溶质质量分数一定比不饱和溶液的溶质质量分数大。C D注:比较饱和溶液和不饱和溶液、浓溶液、稀溶液应
指明一定温度和同一物质的溶液考一考你8、20℃时,氯化钠的溶解度为36g。对这句话理解错
误的是 ( )
A.20℃时,100g水中最多能溶解氯化钠36g
B.20℃时,100g氯化钠饱和溶液中含氯化钠36g
C.20℃时,氯化钠饱和溶液中水与氯化钠的质量
比为100:36
D.20℃时,将36g氯化钠溶解于100g水中,所得溶液
为该温度下氯化钠的饱和溶液B考一考你返回A B C 0 温度 溶解度 t1 t2a 9、右图为A、B、C、三种物质
的溶解度曲线。试回答:t3t4(1)溶解度受温度影响最大的
物质是 ,溶解度随
温度升高而减少的物质是 。(2) ℃时,A、B两种物质的溶解度相等,都为 。(3)t2℃时,三种物质的溶解度由
大到小的顺序为 。(4)n点的含义是 __________________________________ 。(5)相同质量的A.B.C三种饱和溶液,当温度从t4℃降到 t1℃时,溶液中析出晶体最多的物质是 ,没有晶体析出的是_____。 (6)若A中混有少量的B物质,可以采用 的方法提纯A。ACt3 B > A > C AC降温结晶返回考一考你n .t1℃时,A、C两种物质的溶解度相等 a g 10、打开汽水瓶盖时,为什么汽水会自动喷出来?11、喝了汽水以后,为什么常常会打嗝?打开瓶盖,瓶内压强减小,气体的溶解度随压强减小而减小。
气体的溶解度随温度升高而减小。12、根据右图的溶解度曲线,回答下列问题:
(1)20℃时,往50g水中加入20g硝酸钾晶体,充分搅拌
后得到溶液质量为 g。
(2)20℃时,欲配制等质量的两种物质的饱和溶液,所需
水的质量关系是NaCl KNO3 (填写“>”、“<”
或“=”,下同) 。
(3)下面是两同学分别提出的从海水中获取食盐的方法。
甲:蒸发水
乙:冷却热饱和溶液
你认为 (填“甲”或“乙”)
同学的方法合理。 65< 甲返回1、 A、B、C三种固体物质(均不含结晶水)的溶解度曲线如图示,下列说法不正确的是 ( ) A.t1℃,将A、B、C各a g放入100g水中,充分搅拌,所得溶
液溶质质量分数均相等。
B. t2oC时,三种物质的溶液中溶质的质量分数相等。
C.将t3℃时A、B、C的饱和溶液分别降温到t1℃时,所得溶液
中溶质质量分数的关系为:A> B > C。
D.从A与少量C的混合物中提纯A,
可用降温结晶的方法。BC直击中考
2、下图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答问题:
(1)t2℃时,A、B、C三种物质的溶解度大小关系是___________。
(2)t3℃时,将50gA物质加入到50g水中,充分溶解后, 所得溶液是_____
(填“饱和”或 “不饱和”)溶液, 所得溶液质量为__________g。
(3)室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水
中加入一定量的NH4NO3固体并搅拌,试管内可以观察到的现象 _________。
(4)将t1℃时A、B、C的饱和溶液同时升温到t3℃时,所得溶液中溶质质量
分数的大小关系是 _________。
A=B>C饱和B>A>C有晶体析出 90直击中考直击中考3、(佛山市)以下说法正确的是( )
A.溶液一定是均一、无色、稳定的 B.溶液的溶质一定是固体
C.均一、稳定的液体一定是溶液 D.溶液一定是混合物4、(北京市)配制50 g溶质的质量分数为 6%的氯化钠溶液,不需要的仪器是 ( )
A.蒸发皿 B.玻璃棒 C.烧杯 D.量筒
5.(南京市)下列物质加入一定量的水中,能使液体温度明显降低的是 ( )
A.硝酸铵 B.氢氧化钠 C.生石灰 D.氯化钠
6、右图是A、B的溶解度曲线。t2℃时分别将
100gA、B的饱和溶液降温至t1℃,析出固体
质量A _____B(填“>”、“<”或“=”);
把t2℃时150gA的饱和溶液稀释为20%,需加
水______g。 >100DAA7、(2013.泸州市)配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行。请回答下列问题:
(1)用上图所示的序号表示正确配制该溶液的操作顺序为________。
(2)计算配制100g溶质质量分数为5%的氯化钠溶液所需氯化钠____g,
需水______g。
(3)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘
应 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体
C.调节游码 D.添加砝码
(4)用量筒量取水时仰视读数会导致所配溶液溶质质量分数____ 。
(填“偏高”或“偏低”或“不变”)直击中考CBDEAB偏低5958、(黑龙江)甲、乙两种固体的溶解度曲线如图所示.现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯中,再向烧杯中加入一定量的浓硫酸.
(1)10℃时,乙物质的溶解度是________g。
(2)30℃时,甲、乙两种物质的溶解 度大小顺序___________。
(3)烧杯中加入浓硫酸后,试管中固体质量增加的是____ __(选A或B)。除了加浓硫酸外,还可以加__________________(填一种物质名称),也会发生这样的变化.直击中考20甲>乙B氢氧化钠或氧化钙再见
③达到饱和状态 ④单位: g
(2)影响因素内因:溶质性质、溶剂性质外因:温度溶 液练一练一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
2、固体溶解度曲线的含义、应用应用:①比较溶解度大小 ②查溶解度 ③溶解度受温度影响变化情况
④确定分离提纯方法、析出晶体的多少(1)点的含义:
①曲线上的点表示对应温度下该物质的溶解度;(为饱和溶液)
②曲线的交点表示多种物质在某温度下的溶解度相等。(质量分数相等)25 50 练一练如: A中混有少量的B,可用________法提纯A。
B中混有少量的A,可用________法提纯B。降温结晶蒸发结晶补充(2)线的含义:物质溶解度曲线表示物质的溶解度随温度变化的趋势(3)面的含义:曲线下方的面表示相应温度下该物质的不饱和溶液;
曲线上方的面表示相应温度下该物质的饱和溶液且有未溶解的固体。物质的分离提纯方法:
1、过滤
2、结晶:a、 降温结晶
b、蒸发结晶··﹒3、固体溶解度曲线 固体溶解度
规律大多数固体溶解度随温度升高而增大,如 KNO3少数固体溶解度受温度影响变化不大,如NaCl极少数固体溶解度随温度升高而减少,如Ca(OH)2 KNO3 NaCl Ca(OH)2 0 温度 溶
解
度
/g
NaNO34、气体溶解度1)定义:是指该气体在压强为101kPa和一定温度时,
在 1 体积水里达到饱和状态时的气体体积.
2)影响因素内因:气体和水的性质外因:温度和压强3)规律:
气体物质的溶解度随压强减小而减小,
气体物质的溶解度随温度升高而减小。练一练溶 液m溶液 = m溶质 + m溶剂
1、溶质的质量分数=六、溶液的浓度溶质的质量分数=2、饱和溶液中溶质质量分数为:溶解度溶解度 + 100g × 100% 溶 液 练一练 3、溶液稀释的计算依据:
浓溶液中的( )=稀溶液中的( )
4、配制一定溶质质量分数的溶液
(1)用固体配制:
①步骤:( )( )、( )、( )。
②仪器:
(2)用浓溶液稀释(稀释前后,溶质的质量不变)
①步骤:( )、( )、( )。
②仪器:计算称量量取溶解溶质质量溶质质量托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒。计算量取混匀量筒、胶头滴管、烧杯、玻璃棒。溶 液练一练1、下列说法正确的是( )A.凡是均一透明的、稳定的液体就是溶液
B. 高锰酸钾加入水中搅拌所得暗紫色液体不是溶液
C.冰水混合物属于溶液
D.溶液是均一的、稳定的混合物D2、判断下列溶液的溶质、溶剂H2OHClC2H5OH返回你会了吗酒精溶液NaCl溶液盐酸H2OH2O 3.生活中的下列物质,易溶于水而形成溶液的是( )A.面粉B.蔗糖C.植物油 D.铁锈 B4.汽油和洗涤剂都能除油污,原理有何不同?汽油能溶解油污,形成的是溶液;
洗涤剂能乳化油污,形成的是乳浊液。5.向右图试管里的水中加入某种物质后,原来U型管内在同一水平面上的红墨水,右边液面升高了,左边的液面下降了,则加入的物质是( )
A、活性炭 B、生石灰
C、硝酸铵 D、氢氧化钠 BD6、将某物质饱和溶液转变为不饱和溶液最可靠的方法是( )7、下列说法正确的是( )A.升高温度 B. 加入溶质
C. 降低温度 D.加足量的溶剂DA.饱和溶液中溶质的质量一定大于不饱和溶液中溶质的质量。
B. 饱和溶液浓度比不饱和溶液浓度大。
C. 析出晶体的溶液是该温度下这种物质的饱和溶液。
D.一定温度下,同一物质的饱和溶液的溶质质量分数一定比不饱和溶液的溶质质量分数大。C D注:比较饱和溶液和不饱和溶液、浓溶液、稀溶液应
指明一定温度和同一物质的溶液考一考你8、20℃时,氯化钠的溶解度为36g。对这句话理解错
误的是 ( )
A.20℃时,100g水中最多能溶解氯化钠36g
B.20℃时,100g氯化钠饱和溶液中含氯化钠36g
C.20℃时,氯化钠饱和溶液中水与氯化钠的质量
比为100:36
D.20℃时,将36g氯化钠溶解于100g水中,所得溶液
为该温度下氯化钠的饱和溶液B考一考你返回A B C 0 温度 溶解度 t1 t2a 9、右图为A、B、C、三种物质
的溶解度曲线。试回答:t3t4(1)溶解度受温度影响最大的
物质是 ,溶解度随
温度升高而减少的物质是 。(2) ℃时,A、B两种物质的溶解度相等,都为 。(3)t2℃时,三种物质的溶解度由
大到小的顺序为 。(4)n点的含义是 __________________________________ 。(5)相同质量的A.B.C三种饱和溶液,当温度从t4℃降到 t1℃时,溶液中析出晶体最多的物质是 ,没有晶体析出的是_____。 (6)若A中混有少量的B物质,可以采用 的方法提纯A。ACt3 B > A > C AC降温结晶返回考一考你n .t1℃时,A、C两种物质的溶解度相等 a g 10、打开汽水瓶盖时,为什么汽水会自动喷出来?11、喝了汽水以后,为什么常常会打嗝?打开瓶盖,瓶内压强减小,气体的溶解度随压强减小而减小。
气体的溶解度随温度升高而减小。12、根据右图的溶解度曲线,回答下列问题:
(1)20℃时,往50g水中加入20g硝酸钾晶体,充分搅拌
后得到溶液质量为 g。
(2)20℃时,欲配制等质量的两种物质的饱和溶液,所需
水的质量关系是NaCl KNO3 (填写“>”、“<”
或“=”,下同) 。
(3)下面是两同学分别提出的从海水中获取食盐的方法。
甲:蒸发水
乙:冷却热饱和溶液
你认为 (填“甲”或“乙”)
同学的方法合理。 65< 甲返回1、 A、B、C三种固体物质(均不含结晶水)的溶解度曲线如图示,下列说法不正确的是 ( ) A.t1℃,将A、B、C各a g放入100g水中,充分搅拌,所得溶
液溶质质量分数均相等。
B. t2oC时,三种物质的溶液中溶质的质量分数相等。
C.将t3℃时A、B、C的饱和溶液分别降温到t1℃时,所得溶液
中溶质质量分数的关系为:A> B > C。
D.从A与少量C的混合物中提纯A,
可用降温结晶的方法。BC直击中考
2、下图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答问题:
(1)t2℃时,A、B、C三种物质的溶解度大小关系是___________。
(2)t3℃时,将50gA物质加入到50g水中,充分溶解后, 所得溶液是_____
(填“饱和”或 “不饱和”)溶液, 所得溶液质量为__________g。
(3)室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水
中加入一定量的NH4NO3固体并搅拌,试管内可以观察到的现象 _________。
(4)将t1℃时A、B、C的饱和溶液同时升温到t3℃时,所得溶液中溶质质量
分数的大小关系是 _________。
A=B>C饱和B>A>C有晶体析出 90直击中考直击中考3、(佛山市)以下说法正确的是( )
A.溶液一定是均一、无色、稳定的 B.溶液的溶质一定是固体
C.均一、稳定的液体一定是溶液 D.溶液一定是混合物4、(北京市)配制50 g溶质的质量分数为 6%的氯化钠溶液,不需要的仪器是 ( )
A.蒸发皿 B.玻璃棒 C.烧杯 D.量筒
5.(南京市)下列物质加入一定量的水中,能使液体温度明显降低的是 ( )
A.硝酸铵 B.氢氧化钠 C.生石灰 D.氯化钠
6、右图是A、B的溶解度曲线。t2℃时分别将
100gA、B的饱和溶液降温至t1℃,析出固体
质量A _____B(填“>”、“<”或“=”);
把t2℃时150gA的饱和溶液稀释为20%,需加
水______g。 >100DAA7、(2013.泸州市)配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行。请回答下列问题:
(1)用上图所示的序号表示正确配制该溶液的操作顺序为________。
(2)计算配制100g溶质质量分数为5%的氯化钠溶液所需氯化钠____g,
需水______g。
(3)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘
应 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体
C.调节游码 D.添加砝码
(4)用量筒量取水时仰视读数会导致所配溶液溶质质量分数____ 。
(填“偏高”或“偏低”或“不变”)直击中考CBDEAB偏低5958、(黑龙江)甲、乙两种固体的溶解度曲线如图所示.现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯中,再向烧杯中加入一定量的浓硫酸.
(1)10℃时,乙物质的溶解度是________g。
(2)30℃时,甲、乙两种物质的溶解 度大小顺序___________。
(3)烧杯中加入浓硫酸后,试管中固体质量增加的是____ __(选A或B)。除了加浓硫酸外,还可以加__________________(填一种物质名称),也会发生这样的变化.直击中考20甲>乙B氢氧化钠或氧化钙再见
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
