人教版(五四制)九年级化学 1.2 金属的化学性质 课件(21张ppt)
文档属性
| 名称 | 人教版(五四制)九年级化学 1.2 金属的化学性质 课件(21张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-07-01 00:00:00 | ||
图片预览








文档简介
课件21张PPT。课题2 金属的化学性质 你有哪些方法来鉴别这个手镯是真黄金还是假黄金呢?
很多金属能与氧气反应。你学过哪些金属与O2的反应?镁条空气中剧烈燃烧铁丝在空气中不能燃烧
铁在氧气中剧烈燃烧空气中
镁的化学性质比铁活泼化合反应金属与氧气的反应Al+O2=Al O+3-22 3324致密结构因其表面形成致密的氧化物保护膜而有优良的抗腐蚀性能化合反应金属与氧气的反应红色固体变成黑色氧化铜Cu+O2CuO+2-2221用镊子夹持一小块铜片,在酒精灯上加
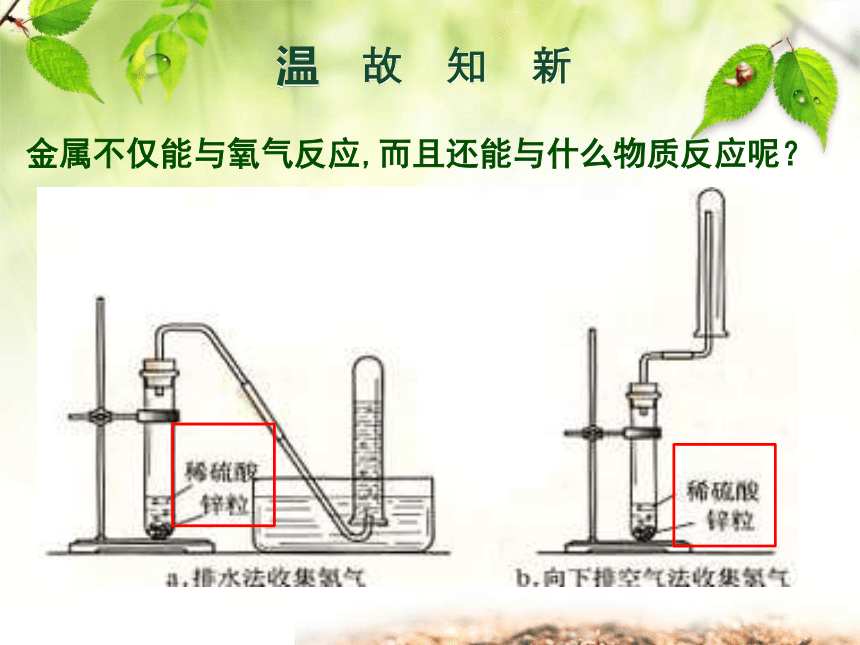
热,观察现象。化合反应金属与氧气的反应金的化学性质 ,即使在 条件下也 O2发生反应。稳定高温不与金属与氧气的反应Mg、Al、Zn> Fe、Cu> Au金属与氧气反应的难易程度或剧烈程度。温 故 知 新金属不仅能与氧气反应,而且还能与什么物质反应呢? 在4只试管里分别放入一小段镁条(已打磨)、四颗锌粒、两根铁丝、一个铜片,再分别加入约5mL稀硫酸或稀盐酸,观察并记录现象,比较反应的剧烈程度。铜放入酸中铁与酸反应锌与酸反应镁与酸反应金属与盐酸、稀硫酸的反应金属与盐酸、稀硫酸的反应剧烈反应,产生大量气泡
放热反应较剧烈,产生大量气泡
放热反应较慢,产生少量气泡。溶液由无色变为浅绿色。无现象Fe2+金属与盐酸、稀硫酸的反应1.能与盐酸、稀硫酸反应的金属是 。
2.不能与盐酸、稀硫酸反应的金属是 。
3.相同条件下,四种金属与酸反应的剧烈程度
> > > 。
4.镁、锌、铁、铜四种金属的活泼性顺序是
> > > 。 Mg Zn FeCu Mg Zn Fe Cu Mg Zn Fe Cu相同条件下,比较金属与酸反应的速率。金属与盐酸、稀硫酸的反应Zn+HCl=ZnCl+22-1+H2↑1121Zn+H2SO4=ZnSO4+2-2+H2↑Mg + 2HCl = MgCl2 + H2↑Mg + H2SO4 = MgSO4 + H2↑Fe + 2HCl = FeCl2 + H2↑Fe + H2SO4 = FeSO4 + H2↑不反应不反应剧烈反应,产生大量气泡
放热反应较剧烈,产生大量气泡
放热反应较慢,产生少量气泡。溶液由无色变为浅绿色。无现象Fe2+金属与盐酸、稀硫酸的反应写出下列方框中物质的类别 单质化合物化合物单质 你有哪些方法来鉴别这个手镯是真黄金还是假黄金呢?
(友情提醒:假黄金实际上就是黄铜,即铜和锌的混合物。)
1.铝有很好的抗腐蚀性能是因为 ( )
A. 化学性质不活泼,在空气中不与氧气反应
B. 常温下不能与氧气反应,在高温时才反应
C. 在空气中铝的表面生成的一层致密的氧化铝薄膜阻止铝进一步氧化
D. 铝不能与酸碱发生反应C2.有元素化合价为+2价的两种金属。取等质量的A、B分别与足量的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示。H2从图示说明的关系,可以得出的正确结论是 ( )
A.与酸反应速率:A 产生氢气质量:A B.与酸反应速率:A 产生氢气质量:A>B
C.与酸反应速率:A>B,产生氢气质量:A>B
D.与酸反应速率:A>B,产生氢气质量:A A. 观察颜色 B. 称量质量 C. 加稀硫酸 D. 磁铁吸引C4.下列反应中,不属于置换反应的是( )A5.我国商代已制造出精美的青铜器,春秋战国时期已会冶铁和炼钢。人类开发利用下列金属单质的时间顺序与金属活动性的强弱有着某种内存联系。由此推断,下列金属中,人类开发利用最晚的是 ( )
A. Al B. Cu C. Fe D. ZnA6.常见的四种金属铝、铜、铁、锌,它们具有的相似的化学性质是 ( )
A.良好的延展性 B.在一定条件下都跟氧气反应
C.良好的导电性 D.都能跟盐酸反应B7.实验室有一包混有铁粉的铜粉,请用以下两种方法除去铜粉中的铁粉(简述操作过程)
(1)物理方法: 。
(2)化学方法: 。 用磁铁吸引加入足量的稀盐酸或稀硫酸中,充分反应后过滤。观察颜色8.铝的利用比铜、铁晚的多,但在100年后,铝的产量早已超过铜,位于铁之后居第二位。三种金属中,常温下在干燥的空气中能与氧气反应的金属所生成的氧化物的化学式是 ,将铁丝浸入稀硫酸溶液中,过一会儿可观察到的现象是
,化学方程式是 。产生少量气泡,溶液由无色变为浅绿色
很多金属能与氧气反应。你学过哪些金属与O2的反应?镁条空气中剧烈燃烧铁丝在空气中不能燃烧
铁在氧气中剧烈燃烧空气中
镁的化学性质比铁活泼化合反应金属与氧气的反应Al+O2=Al O+3-22 3324致密结构因其表面形成致密的氧化物保护膜而有优良的抗腐蚀性能化合反应金属与氧气的反应红色固体变成黑色氧化铜Cu+O2CuO+2-2221用镊子夹持一小块铜片,在酒精灯上加
热,观察现象。化合反应金属与氧气的反应金的化学性质 ,即使在 条件下也 O2发生反应。稳定高温不与金属与氧气的反应Mg、Al、Zn> Fe、Cu> Au金属与氧气反应的难易程度或剧烈程度。温 故 知 新金属不仅能与氧气反应,而且还能与什么物质反应呢? 在4只试管里分别放入一小段镁条(已打磨)、四颗锌粒、两根铁丝、一个铜片,再分别加入约5mL稀硫酸或稀盐酸,观察并记录现象,比较反应的剧烈程度。铜放入酸中铁与酸反应锌与酸反应镁与酸反应金属与盐酸、稀硫酸的反应金属与盐酸、稀硫酸的反应剧烈反应,产生大量气泡
放热反应较剧烈,产生大量气泡
放热反应较慢,产生少量气泡。溶液由无色变为浅绿色。无现象Fe2+金属与盐酸、稀硫酸的反应1.能与盐酸、稀硫酸反应的金属是 。
2.不能与盐酸、稀硫酸反应的金属是 。
3.相同条件下,四种金属与酸反应的剧烈程度
> > > 。
4.镁、锌、铁、铜四种金属的活泼性顺序是
> > > 。 Mg Zn FeCu Mg Zn Fe Cu Mg Zn Fe Cu相同条件下,比较金属与酸反应的速率。金属与盐酸、稀硫酸的反应Zn+HCl=ZnCl+22-1+H2↑1121Zn+H2SO4=ZnSO4+2-2+H2↑Mg + 2HCl = MgCl2 + H2↑Mg + H2SO4 = MgSO4 + H2↑Fe + 2HCl = FeCl2 + H2↑Fe + H2SO4 = FeSO4 + H2↑不反应不反应剧烈反应,产生大量气泡
放热反应较剧烈,产生大量气泡
放热反应较慢,产生少量气泡。溶液由无色变为浅绿色。无现象Fe2+金属与盐酸、稀硫酸的反应写出下列方框中物质的类别 单质化合物化合物单质 你有哪些方法来鉴别这个手镯是真黄金还是假黄金呢?
(友情提醒:假黄金实际上就是黄铜,即铜和锌的混合物。)
1.铝有很好的抗腐蚀性能是因为 ( )
A. 化学性质不活泼,在空气中不与氧气反应
B. 常温下不能与氧气反应,在高温时才反应
C. 在空气中铝的表面生成的一层致密的氧化铝薄膜阻止铝进一步氧化
D. 铝不能与酸碱发生反应C2.有元素化合价为+2价的两种金属。取等质量的A、B分别与足量的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示。H2从图示说明的关系,可以得出的正确结论是 ( )
A.与酸反应速率:A
C.与酸反应速率:A>B,产生氢气质量:A>B
D.与酸反应速率:A>B,产生氢气质量:A
A. Al B. Cu C. Fe D. ZnA6.常见的四种金属铝、铜、铁、锌,它们具有的相似的化学性质是 ( )
A.良好的延展性 B.在一定条件下都跟氧气反应
C.良好的导电性 D.都能跟盐酸反应B7.实验室有一包混有铁粉的铜粉,请用以下两种方法除去铜粉中的铁粉(简述操作过程)
(1)物理方法: 。
(2)化学方法: 。 用磁铁吸引加入足量的稀盐酸或稀硫酸中,充分反应后过滤。观察颜色8.铝的利用比铜、铁晚的多,但在100年后,铝的产量早已超过铜,位于铁之后居第二位。三种金属中,常温下在干燥的空气中能与氧气反应的金属所生成的氧化物的化学式是 ,将铁丝浸入稀硫酸溶液中,过一会儿可观察到的现象是
,化学方程式是 。产生少量气泡,溶液由无色变为浅绿色
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
