人教版(五四制)九年级化学 1.3 金属资源的利用和保护 课件(49张ppt)
文档属性
| 名称 | 人教版(五四制)九年级化学 1.3 金属资源的利用和保护 课件(49张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-07-01 00:00:00 | ||
图片预览









文档简介
课件49张PPT。温故知新1、背诵金属活动性顺序表。
2、金属活动性顺序有哪些应用?
3、金属有哪些化学性质?
4、写出下列化学反应的化学方程式:
(1)镁、锌、铁与盐酸的反应
(2)铁钉与硫酸铜溶液、铜丝与硝酸银溶液的反应。
温故知新1、背诵金属活动性顺序表。 3、金属有哪些化学性质?2、金属活动性顺序有哪些应用?
4、写出下列化学反应的化学方程式:
(1)镁、锌、铁与盐酸的反应
(2)铁钉与硫酸铜溶液、铜丝与硝酸银溶液的反应。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
判断金属的活动性;判断金属与酸的反应;判断金属与盐的反应。
金属与氧气反应,生成金属氧化物;金属与酸反应,生成盐和氢气;
金属与某些盐溶液反应。生成新金属和新盐。
(1)Mg+2HCl=MgCl2+H2↑
Zn+2HCl=ZnCl2+H2 ↑
Fe+2HCl=FeCl2+H2↑、
(2)Fe+CuSO4=FeSO4+Cu
Cu+2AgNO3=Cu(NO3)2+2Ag
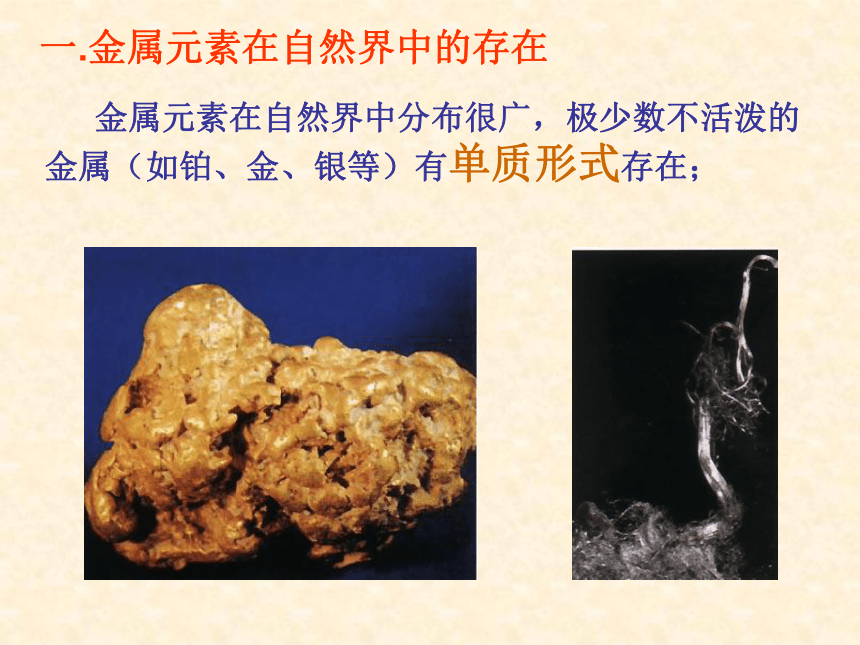
世界跨径最大的斜拉桥———苏通大桥 苏通大桥总长8206米,斜拉桥主孔跨度1088米,列世界第一;主塔高度306米,列世界第一;斜拉索的长度580米,列世界第一。 人类生活离不开金属金属有广泛的用途,对于人类社会起着不可替代的作用!军事与科技也需要大量的金属一.金属元素在自然界中的存在 金属元素在自然界中分布很广,极少数不活泼的金属(如铂、金、银等)有单质形式存在;图5—2 地壳中金属的百分含量 铝
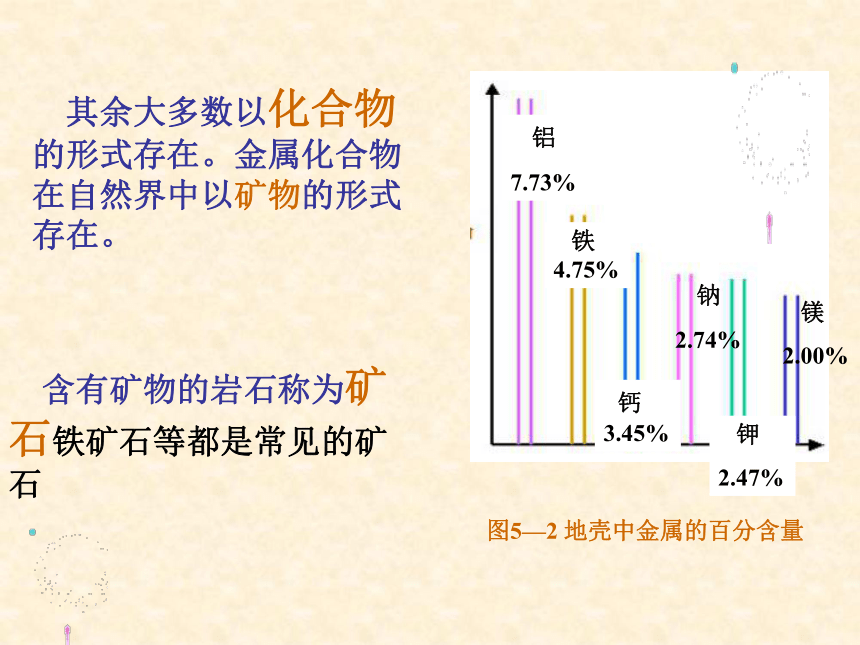
7.73% 铁 4.75% 钙 3.45% 钠
2.74% 钾
2.47% 镁
2.00% 含有矿物的岩石称为矿石铁矿石等都是常见的矿石 其余大多数以化合物的形式存在。金属化合物在自然界中以矿物的形式存在。常见几种金属矿物的成分磁铁矿褐铁矿赤铁矿Fe3O4Fe2O3·XH2OFe2O3 孔雀石
Cu2(OH)2CO3
赤铜矿
Cu2O
赤铁矿黄铁矿菱铁矿铝土矿黄铜矿辉铜矿 我国是世界上已知矿物种类比较齐全的少数国家这一,矿物储量也很丰富,其中钨、钼、钛、锡、锑等储量居世界前列,铜、铝、锰等储量在世界观上也占有重要志地位。 大自然向人类提供了丰富的金属矿物资源,人类每年要提炼数以亿吨计的金属用于工农业生产和其它领域。其中,提取量最大的是铁。二.铁的冶炼现象:红色粉末变成黑色,产生气体使澄清的石灰水变浑浊。一氧化碳还原氧化铁看课本17页[实验8-3]某同学改进CO还原氧化铁实验装置如图1.若先给氧化铁加热,再通CO,后果_____
2.写出A中反应的方程式_____________
3.根据B装置现象可以判断反应是否发生
,则B中试剂为____
4.C装置作用___________
5.C装置收集气体利用_________性质3.一氧化碳还原氧化铁实验
(1)实验装置(如图 8-3-1 所示)(2)实验操作步骤图 8-3-1 ①操作顺序:先通 CO,再加热;实验完毕,先停止加热,
继续通 CO 至试管冷却。
②尾气处理:因 CO 有毒,不能排到空气中,要用酒精灯
将 CO 点燃而除去。实验步骤:
1、检查装置气密性
2、将适量的氧化铁装入试管并固定装置
3、点燃右边酒精灯
4、通入一氧化碳气体
5、点燃酒精喷灯给氧化铁加热
6、待硬质玻璃管内红色物质完全变为黑色时停止加热
7、待玻璃管内固体冷却后停止通入一氧化碳,然后熄灭右边酒精灯
实验前要先通CO将玻璃管中的空气排尽再加热,防止加热时CO与空气混合发生爆炸;实验完毕后,停止加热时要继续通CO至玻璃管内固体冷却,防止高温下的生成物铁与空气接触而被氧化,同时还可防止石灰水倒吸。高炉是个竖直的圆筒形炉子,炉壳用钢板制成,内部用耐火砖作衬里。炼铁的主要原料是铁矿石、焦炭、石灰石和空气。 高温下,用还原剂(主要是一氧化碳)从铁矿石里把铁还原出来 1、原料:黄铁矿 FeS2赤铁矿 Fe2O3菱铁矿 FeCO3磁铁矿 Fe3O42、原理:在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石中还原出来石灰石、铁矿石
焦炭、空气3、设备:高炉化学方程式:70%48.27%46.67%72.41%含铁量铁矿石焦炭热空气炉渣出口生铁出口石灰石高炉炼铁图:补充:炼钢视频:工业上生铁炼钢炼钢和炼铁的比较高温三、有关杂质问题的计算例1、1000t含杂质20%的赤铁矿石中含
氧化铁的质量是多少?氧化铁的质量: 1000t× ( 1- 20% )=800t纯物质的质量=
不纯物质的质量×纯物质的质量分数(纯度)例2、计算多少吨生铁中含铁的质量分数为96%,含铁560t?
生铁的质量: 560t÷96%=583.3t不纯物质的质量=
纯物质的质量÷纯物质的质量分数(纯度)[例题]用1000t 含氧化铁80%的赤铁矿石,理论上可以炼出含杂质4%的生铁多少吨?解:1000t赤铁矿石中含氧化铁的质量为:1000t× 80%=800t
设:800t氧化铁理论上可以炼出铁的质量为 x
Fe2O3 + 3CO = 2Fe + 3CO2
高温
160 112
800t x
x=560t
折合为含杂质4%的生铁的质量为:
560t÷(1-4 %)=583t
答:用1000t 含氧化铁80%的赤铁矿石,理论上可以炼出含杂质4%的生铁583t
诊断补偿,点击中考一、选择题:请将唯一正确答案代量填入下列空格内
1(2006 广州)人类每年从自然界中提取大量的金属铁,下列关于铁的说法正确的是( )
A、炼铁的过程是把单质铁变成氧化铁。 B、钢是很纯的铁。
C、生铁是含少量碳的铁合金。 D、被腐蚀的铁制品属于不可回收的垃圾。
2(2006 益阳)铁是人类生活中重要的一种材料,工业上可用如下化学反应制得铁,
Fe2O3+3CO =2Fe+3CO2,该反应中,发生还原反应的物质是( )
A、Fe2O3 B、CO C、Fe D、CO2
3、做一氧化碳还原氧化铁的实验后,清洗试管壁上留下的黑色物质时可选用的方法是( )
A、用大量水边冲边洗。 B、用试管刷左右、上下猛烈刷。
C、用盐酸或稀硫酸清洗后再用水冲。
D、用肥皂粉清洗后再用水冲洗。
高温CAC诊断补偿,点击中考二、计算题(2006黄冈)
用2000t 含氧化铁80%的赤铁矿石,理论上可以炼出含铁96 %的生铁多少吨?二、计算题(2006黄冈)用2000t 含氧化铁80%的赤铁矿石,理论上可以炼出含铁96 %的生铁多少吨?解:2000t赤铁矿石中含氧化铁的质量为:2000t× 80%=1600t
设:1600t氧化铁理论上可以炼出铁的质量为 x
Fe2O3 + 3CO = 2Fe + 3CO2
160 112
1600t x
x=1120t
折合为含铁96 %的生铁的质量为 1120t÷ 96 %=1166t
答:用2000t 含氧化铁80%的赤铁矿石,理论上可以炼出含铁96 %的生铁1166t
高温梳理整合
本节课你学会了
哪些知识? 据有关资料报导,现在全世界每年被腐蚀而报废的金属设备和材料相当于年产量的20%——40%钢铁的最大的弱点就是容易生绣三.金属资源保护1.金属的腐蚀和防护铁轨的锈蚀铁钉的生锈各种铁制品的锈蚀 为了减少损失,需要探究金属锈蚀的原因、防护的方法和废金属的回收利用金属锈蚀给人类带来了巨大的损失。取3枚洁净无锈的铁钉,分别放入3支试管中进行下面的实验步骤一、在试管1中加入少量的蒸馏水,使铁钉的一半浸没在水中
步骤二、在试管2中注满迅速冷却的沸水塞紧橡皮塞
步骤三、在试管3中加入少量干燥剂(生石灰或无水氯化钙)
再放一团干棉球,把铁钉放在干棉球上,塞紧橡皮塞铁在空气中锈蚀,实际上是铁跟氧气、水等物质相互作用,发生一系列复杂的化学变化,使铁转化为铁的化合物的过程铁锈成分复杂,主要是Fe2O3·XH2O它是一种疏松多孔的物质铁锈 铁锈这种多孔性的物质,能让水分和空气穿过它的空隙,不断向里层渗透,继续跟铁反应,直至铁被完全锈蚀。 在切过咸菜的铁质菜刀同一面上选相近的三处进行下列实验一处:用湿棉球湿润;
一处:用干布檫干
一处:用干布檫干后,涂上一层食油;放置一昼夜,观察菜刀三处表面发生的变化铁铁锈与空气(氧气)接触与水接触怎么防止钢铁生锈呢?在车船的表面喷油漆在机械表面涂防锈油在面盆、杯子、等表面烧涂搪瓷此外,还可以在钢铁表面镀上一层能起保护作用的其他金属。(为什么?)
如:在钢铁表面镀锡、镀锌、和镀铬镀铜?总结:防止钢铁制品生锈的方法: 铝比铁更容易跟氧气和其他物质发生化学反应。铝在空气中与氧气反应,生成的氧化铝形成一层致密而结实的膜覆盖在铝的表面,防止铝继续与氧气反应,从而起来“自我保护”的作用(1)隔绝空气或氧气 (2)隔绝水具体方法:
1.“穿外衣”——加一层保护膜(如:刷油漆、涂油、电镀、致密的氧化膜)
2.“打强心针”——在铁中加入其它金属改变其内部结构,(如:制成不锈钢)①保持钢铁表面的清洁干燥。
②镀金属保护层:如镀锡、镀锌、镀铬等;白铁皮镀锌,马口铁镀锡,
钢圈镀铬、镍。
③涂非金属保护层:如喷涂油漆、涂防锈油、在脸盆、杯子表面烧
涂搪瓷、用橡胶或塑料包在钢铁表面。
④形成氧化膜保护层:枪套上形成四氧化三铁、 锯条上的烤蓝。
⑤在钢铁里加入金属或非金属形成耐腐蚀合金:如不锈钢(加Cr、Ni)防止铁锈蚀的主要措施:2.怎样保护金属资源呢?一.防止金属的腐蚀
二.回收利用废旧金属三.合理有效开采矿物
四.寻找金属的代用品(1)汞与稀盐酸 (2)铝与硫酸铜溶液
(3)银与硫酸锌溶液 (4)锌与硝酸银溶液
(5)钠与稀硫酸1、下列物质能否发生反应?写出能发生反应的化学方程式。2、回答下列问题:
(1)为什么沙漠地区的铁制品锈蚀较慢?
(2)切过咸鱼的刀不经洗净抹干,为什么很快就生锈?
(3)被雨水淋湿的自行车,为什么须先用干布擦净后才
能用带有油的布擦?例:某赤铁矿含Fe2O3 80%,用3000 t这种矿石,可炼出含杂质4%的生铁多少吨?
分析:计算时应注意把反应物和生成物都换算成纯物质的量,再代入化学方程式计算.
解:设3000 t这种矿石,可炼出生铁质量为x,
根据题设:纯Fe2O3质量=3000 t×80%=2400 t
纯Fe质量=x·(1-4%)=x·96%
代入化学方程式中:
Fe2O3+3CO=2Fe+3CO2
160 112
2400 t x·96%
x==1750 t
答:可炼出含杂质4%的生铁1750 t.若赤铁矿石中Fe2O3的质量分数为80%,600 t 这样的赤铁矿可炼出含碳等其他杂质质量分数为7%的生铁多少吨?
解:设可炼出含杂质质量分数为7%的生铁的质量为x
Fe2O3+3CO= 2Fe +3CO2
160 112
600 t×80% x·(1-7%)
x==365 t
答案:可炼出含碳等杂质质量为7%的生铁365 t.
点拨:这类题很容易出错,错误原因主要在于没有理解哪些是不纯物的质量,哪些是纯净物的质量.赤铁矿和生铁都是混合物,而在化学方程式的计算中,所涉及到的都是纯净物的质量,只要牢牢把握住这一点,所有含杂质的计算都可迎刃而解.练习:1、某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,
该厂理论上可以日产Fe98%的生铁多少t?2、冶炼2000t含杂质3%的生铁,需要含90%Fe2O3的赤铁矿
石多少t?4.某钢铁厂每天需消耗5000 t含Fe2O3 76%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁多少吨?
指导建议:首先将不纯物的量转化成纯物质量
Fe2O3质量=5000 t×76%=3800 t
设生铁质量为x,则纯铁质量=98%·x
然后再根据方程式进行计算.
Fe2O3+3CO2Fe+3CO2
160 112
3800 t 98%·x
160∶3800 t=112∶98%·x x=≈2714.3 t冶炼2000 t含杂质3%的生铁,需要含Fe3O4 90%的磁铁矿石多少吨?
指导建议:纯铁质量=2000 t×(1-3%)=1940 t
设磁铁矿石质量为x,则Fe3O4质量为90%·x
反应原理: Fe3O4+4CO3Fe+4CO2
232 168
90%·x 1940 t
232∶90%·x=168∶1940 t
x==2976.7 t
所以磁铁矿质量为2976.7 t.1、245gKClO3完全分解能制得多少O2?若用电解水的方式制等量的O2,则需水几克?
2. 某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,该厂理论上可以日产Fe98%的生铁多少t? 若用含90%Fe3O4的磁铁矿
石来代替,则需含90%Fe3O4的磁铁矿 石多少t?例题:用1000 t含氧化铁80%的赤铁矿石,理论上可以
炼出含铁96%的生铁多少 t ?解:设理论上可以炼出含铁96的生铁的质量为xFe2O3 ------------------2 Fe160 2×561000t×80% x·96%= 583 t答:略。
2、金属活动性顺序有哪些应用?
3、金属有哪些化学性质?
4、写出下列化学反应的化学方程式:
(1)镁、锌、铁与盐酸的反应
(2)铁钉与硫酸铜溶液、铜丝与硝酸银溶液的反应。
温故知新1、背诵金属活动性顺序表。 3、金属有哪些化学性质?2、金属活动性顺序有哪些应用?
4、写出下列化学反应的化学方程式:
(1)镁、锌、铁与盐酸的反应
(2)铁钉与硫酸铜溶液、铜丝与硝酸银溶液的反应。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
判断金属的活动性;判断金属与酸的反应;判断金属与盐的反应。
金属与氧气反应,生成金属氧化物;金属与酸反应,生成盐和氢气;
金属与某些盐溶液反应。生成新金属和新盐。
(1)Mg+2HCl=MgCl2+H2↑
Zn+2HCl=ZnCl2+H2 ↑
Fe+2HCl=FeCl2+H2↑、
(2)Fe+CuSO4=FeSO4+Cu
Cu+2AgNO3=Cu(NO3)2+2Ag
世界跨径最大的斜拉桥———苏通大桥 苏通大桥总长8206米,斜拉桥主孔跨度1088米,列世界第一;主塔高度306米,列世界第一;斜拉索的长度580米,列世界第一。 人类生活离不开金属金属有广泛的用途,对于人类社会起着不可替代的作用!军事与科技也需要大量的金属一.金属元素在自然界中的存在 金属元素在自然界中分布很广,极少数不活泼的金属(如铂、金、银等)有单质形式存在;图5—2 地壳中金属的百分含量 铝
7.73% 铁 4.75% 钙 3.45% 钠
2.74% 钾
2.47% 镁
2.00% 含有矿物的岩石称为矿石铁矿石等都是常见的矿石 其余大多数以化合物的形式存在。金属化合物在自然界中以矿物的形式存在。常见几种金属矿物的成分磁铁矿褐铁矿赤铁矿Fe3O4Fe2O3·XH2OFe2O3 孔雀石
Cu2(OH)2CO3
赤铜矿
Cu2O
赤铁矿黄铁矿菱铁矿铝土矿黄铜矿辉铜矿 我国是世界上已知矿物种类比较齐全的少数国家这一,矿物储量也很丰富,其中钨、钼、钛、锡、锑等储量居世界前列,铜、铝、锰等储量在世界观上也占有重要志地位。 大自然向人类提供了丰富的金属矿物资源,人类每年要提炼数以亿吨计的金属用于工农业生产和其它领域。其中,提取量最大的是铁。二.铁的冶炼现象:红色粉末变成黑色,产生气体使澄清的石灰水变浑浊。一氧化碳还原氧化铁看课本17页[实验8-3]某同学改进CO还原氧化铁实验装置如图1.若先给氧化铁加热,再通CO,后果_____
2.写出A中反应的方程式_____________
3.根据B装置现象可以判断反应是否发生
,则B中试剂为____
4.C装置作用___________
5.C装置收集气体利用_________性质3.一氧化碳还原氧化铁实验
(1)实验装置(如图 8-3-1 所示)(2)实验操作步骤图 8-3-1 ①操作顺序:先通 CO,再加热;实验完毕,先停止加热,
继续通 CO 至试管冷却。
②尾气处理:因 CO 有毒,不能排到空气中,要用酒精灯
将 CO 点燃而除去。实验步骤:
1、检查装置气密性
2、将适量的氧化铁装入试管并固定装置
3、点燃右边酒精灯
4、通入一氧化碳气体
5、点燃酒精喷灯给氧化铁加热
6、待硬质玻璃管内红色物质完全变为黑色时停止加热
7、待玻璃管内固体冷却后停止通入一氧化碳,然后熄灭右边酒精灯
实验前要先通CO将玻璃管中的空气排尽再加热,防止加热时CO与空气混合发生爆炸;实验完毕后,停止加热时要继续通CO至玻璃管内固体冷却,防止高温下的生成物铁与空气接触而被氧化,同时还可防止石灰水倒吸。高炉是个竖直的圆筒形炉子,炉壳用钢板制成,内部用耐火砖作衬里。炼铁的主要原料是铁矿石、焦炭、石灰石和空气。 高温下,用还原剂(主要是一氧化碳)从铁矿石里把铁还原出来 1、原料:黄铁矿 FeS2赤铁矿 Fe2O3菱铁矿 FeCO3磁铁矿 Fe3O42、原理:在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石中还原出来石灰石、铁矿石
焦炭、空气3、设备:高炉化学方程式:70%48.27%46.67%72.41%含铁量铁矿石焦炭热空气炉渣出口生铁出口石灰石高炉炼铁图:补充:炼钢视频:工业上生铁炼钢炼钢和炼铁的比较高温三、有关杂质问题的计算例1、1000t含杂质20%的赤铁矿石中含
氧化铁的质量是多少?氧化铁的质量: 1000t× ( 1- 20% )=800t纯物质的质量=
不纯物质的质量×纯物质的质量分数(纯度)例2、计算多少吨生铁中含铁的质量分数为96%,含铁560t?
生铁的质量: 560t÷96%=583.3t不纯物质的质量=
纯物质的质量÷纯物质的质量分数(纯度)[例题]用1000t 含氧化铁80%的赤铁矿石,理论上可以炼出含杂质4%的生铁多少吨?解:1000t赤铁矿石中含氧化铁的质量为:1000t× 80%=800t
设:800t氧化铁理论上可以炼出铁的质量为 x
Fe2O3 + 3CO = 2Fe + 3CO2
高温
160 112
800t x
x=560t
折合为含杂质4%的生铁的质量为:
560t÷(1-4 %)=583t
答:用1000t 含氧化铁80%的赤铁矿石,理论上可以炼出含杂质4%的生铁583t
诊断补偿,点击中考一、选择题:请将唯一正确答案代量填入下列空格内
1(2006 广州)人类每年从自然界中提取大量的金属铁,下列关于铁的说法正确的是( )
A、炼铁的过程是把单质铁变成氧化铁。 B、钢是很纯的铁。
C、生铁是含少量碳的铁合金。 D、被腐蚀的铁制品属于不可回收的垃圾。
2(2006 益阳)铁是人类生活中重要的一种材料,工业上可用如下化学反应制得铁,
Fe2O3+3CO =2Fe+3CO2,该反应中,发生还原反应的物质是( )
A、Fe2O3 B、CO C、Fe D、CO2
3、做一氧化碳还原氧化铁的实验后,清洗试管壁上留下的黑色物质时可选用的方法是( )
A、用大量水边冲边洗。 B、用试管刷左右、上下猛烈刷。
C、用盐酸或稀硫酸清洗后再用水冲。
D、用肥皂粉清洗后再用水冲洗。
高温CAC诊断补偿,点击中考二、计算题(2006黄冈)
用2000t 含氧化铁80%的赤铁矿石,理论上可以炼出含铁96 %的生铁多少吨?二、计算题(2006黄冈)用2000t 含氧化铁80%的赤铁矿石,理论上可以炼出含铁96 %的生铁多少吨?解:2000t赤铁矿石中含氧化铁的质量为:2000t× 80%=1600t
设:1600t氧化铁理论上可以炼出铁的质量为 x
Fe2O3 + 3CO = 2Fe + 3CO2
160 112
1600t x
x=1120t
折合为含铁96 %的生铁的质量为 1120t÷ 96 %=1166t
答:用2000t 含氧化铁80%的赤铁矿石,理论上可以炼出含铁96 %的生铁1166t
高温梳理整合
本节课你学会了
哪些知识? 据有关资料报导,现在全世界每年被腐蚀而报废的金属设备和材料相当于年产量的20%——40%钢铁的最大的弱点就是容易生绣三.金属资源保护1.金属的腐蚀和防护铁轨的锈蚀铁钉的生锈各种铁制品的锈蚀 为了减少损失,需要探究金属锈蚀的原因、防护的方法和废金属的回收利用金属锈蚀给人类带来了巨大的损失。取3枚洁净无锈的铁钉,分别放入3支试管中进行下面的实验步骤一、在试管1中加入少量的蒸馏水,使铁钉的一半浸没在水中
步骤二、在试管2中注满迅速冷却的沸水塞紧橡皮塞
步骤三、在试管3中加入少量干燥剂(生石灰或无水氯化钙)
再放一团干棉球,把铁钉放在干棉球上,塞紧橡皮塞铁在空气中锈蚀,实际上是铁跟氧气、水等物质相互作用,发生一系列复杂的化学变化,使铁转化为铁的化合物的过程铁锈成分复杂,主要是Fe2O3·XH2O它是一种疏松多孔的物质铁锈 铁锈这种多孔性的物质,能让水分和空气穿过它的空隙,不断向里层渗透,继续跟铁反应,直至铁被完全锈蚀。 在切过咸菜的铁质菜刀同一面上选相近的三处进行下列实验一处:用湿棉球湿润;
一处:用干布檫干
一处:用干布檫干后,涂上一层食油;放置一昼夜,观察菜刀三处表面发生的变化铁铁锈与空气(氧气)接触与水接触怎么防止钢铁生锈呢?在车船的表面喷油漆在机械表面涂防锈油在面盆、杯子、等表面烧涂搪瓷此外,还可以在钢铁表面镀上一层能起保护作用的其他金属。(为什么?)
如:在钢铁表面镀锡、镀锌、和镀铬镀铜?总结:防止钢铁制品生锈的方法: 铝比铁更容易跟氧气和其他物质发生化学反应。铝在空气中与氧气反应,生成的氧化铝形成一层致密而结实的膜覆盖在铝的表面,防止铝继续与氧气反应,从而起来“自我保护”的作用(1)隔绝空气或氧气 (2)隔绝水具体方法:
1.“穿外衣”——加一层保护膜(如:刷油漆、涂油、电镀、致密的氧化膜)
2.“打强心针”——在铁中加入其它金属改变其内部结构,(如:制成不锈钢)①保持钢铁表面的清洁干燥。
②镀金属保护层:如镀锡、镀锌、镀铬等;白铁皮镀锌,马口铁镀锡,
钢圈镀铬、镍。
③涂非金属保护层:如喷涂油漆、涂防锈油、在脸盆、杯子表面烧
涂搪瓷、用橡胶或塑料包在钢铁表面。
④形成氧化膜保护层:枪套上形成四氧化三铁、 锯条上的烤蓝。
⑤在钢铁里加入金属或非金属形成耐腐蚀合金:如不锈钢(加Cr、Ni)防止铁锈蚀的主要措施:2.怎样保护金属资源呢?一.防止金属的腐蚀
二.回收利用废旧金属三.合理有效开采矿物
四.寻找金属的代用品(1)汞与稀盐酸 (2)铝与硫酸铜溶液
(3)银与硫酸锌溶液 (4)锌与硝酸银溶液
(5)钠与稀硫酸1、下列物质能否发生反应?写出能发生反应的化学方程式。2、回答下列问题:
(1)为什么沙漠地区的铁制品锈蚀较慢?
(2)切过咸鱼的刀不经洗净抹干,为什么很快就生锈?
(3)被雨水淋湿的自行车,为什么须先用干布擦净后才
能用带有油的布擦?例:某赤铁矿含Fe2O3 80%,用3000 t这种矿石,可炼出含杂质4%的生铁多少吨?
分析:计算时应注意把反应物和生成物都换算成纯物质的量,再代入化学方程式计算.
解:设3000 t这种矿石,可炼出生铁质量为x,
根据题设:纯Fe2O3质量=3000 t×80%=2400 t
纯Fe质量=x·(1-4%)=x·96%
代入化学方程式中:
Fe2O3+3CO=2Fe+3CO2
160 112
2400 t x·96%
x==1750 t
答:可炼出含杂质4%的生铁1750 t.若赤铁矿石中Fe2O3的质量分数为80%,600 t 这样的赤铁矿可炼出含碳等其他杂质质量分数为7%的生铁多少吨?
解:设可炼出含杂质质量分数为7%的生铁的质量为x
Fe2O3+3CO= 2Fe +3CO2
160 112
600 t×80% x·(1-7%)
x==365 t
答案:可炼出含碳等杂质质量为7%的生铁365 t.
点拨:这类题很容易出错,错误原因主要在于没有理解哪些是不纯物的质量,哪些是纯净物的质量.赤铁矿和生铁都是混合物,而在化学方程式的计算中,所涉及到的都是纯净物的质量,只要牢牢把握住这一点,所有含杂质的计算都可迎刃而解.练习:1、某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,
该厂理论上可以日产Fe98%的生铁多少t?2、冶炼2000t含杂质3%的生铁,需要含90%Fe2O3的赤铁矿
石多少t?4.某钢铁厂每天需消耗5000 t含Fe2O3 76%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁多少吨?
指导建议:首先将不纯物的量转化成纯物质量
Fe2O3质量=5000 t×76%=3800 t
设生铁质量为x,则纯铁质量=98%·x
然后再根据方程式进行计算.
Fe2O3+3CO2Fe+3CO2
160 112
3800 t 98%·x
160∶3800 t=112∶98%·x x=≈2714.3 t冶炼2000 t含杂质3%的生铁,需要含Fe3O4 90%的磁铁矿石多少吨?
指导建议:纯铁质量=2000 t×(1-3%)=1940 t
设磁铁矿石质量为x,则Fe3O4质量为90%·x
反应原理: Fe3O4+4CO3Fe+4CO2
232 168
90%·x 1940 t
232∶90%·x=168∶1940 t
x==2976.7 t
所以磁铁矿质量为2976.7 t.1、245gKClO3完全分解能制得多少O2?若用电解水的方式制等量的O2,则需水几克?
2. 某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,该厂理论上可以日产Fe98%的生铁多少t? 若用含90%Fe3O4的磁铁矿
石来代替,则需含90%Fe3O4的磁铁矿 石多少t?例题:用1000 t含氧化铁80%的赤铁矿石,理论上可以
炼出含铁96%的生铁多少 t ?解:设理论上可以炼出含铁96的生铁的质量为xFe2O3 ------------------2 Fe160 2×561000t×80% x·96%= 583 t答:略。
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
