人教版(五四制)九年级化学 4.1 生活中常见的盐 课件(25张ppt)
文档属性
| 名称 | 人教版(五四制)九年级化学 4.1 生活中常见的盐 课件(25张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-07-01 00:00:00 | ||
图片预览






文档简介
课件25张PPT。氯 化 钠 源自课本氯化钠由 构成,属于 (填“酸、碱或盐”)。 Na+、Cl –盐酸
+
碱酸
+
盐碱
+
盐盐
+
盐知识梳理 回顾酸碱盐的相关知识,搜索有盐生成的反应。
j
j
j
j
j
j
j活动一:比一比、赛一赛 根据以上规律,有哪些反应可以生成NaCl呢?请写出反应的化学方程式。活动一:比一比、赛一赛 2HCl + Na2CO3 == 2NaCl + H2O + CO2 ↑HCl + NaOH == NaCl + H2OCaCl2 + Na2CO3 == CaCO3 ↓ + 2NaCl
……MgCl2 + 2NaOH == Mg(OH)2 ↓ + 2NaCl 根据以上规律,有哪些反应可以生成NaCl呢?请写出反应的化学方程式。氯化钠的制取如何通过海水得到氯化钠呢?海水贮水池 母液海水晒盐 如何通过海水得到氯化钠呢?海水贮水池粗盐(NaCl 、难溶性杂质和可溶性杂质)母液海水晒盐蒸发池结晶池粗盐——去除难溶性杂质实验步骤:加快溶解速率引流使液体均匀受热,防止飞溅把固体转移到纸上粗盐的提纯在蒸发过程中,当蒸发皿中 时,停止加热。出现较多固体Na2CO3 + CaCl2粗盐的提纯NaCl ( CaCl2 、 MgCl2 )——除去某些可溶性杂质 NaOH + MgCl2 Na2CO3 + CaCl2粗盐的提纯NaCl ( CaCl2 、 MgCl2 )——除去某些可溶性杂质 NaOH + MgCl2 某粗盐样品中含有杂质MgCl2、CaCl2.以及泥沙等杂质,某同学设计了以下提纯方案:
?
请回答下列问题:
(1)操作Ⅰ、操作Ⅲ的名称分别是 、 。
(2)滤液B中所含的溶质为 。
(3)向滤液B中滴加稀盐酸,当观察到 现象时,应停止滴加。
(4)所得精盐中NaCl的质量比粗盐样品中多,原因是 。NaCl、NaOH、Na2CO3不再有气泡产生蒸发提纯过程中
有NaCl生成过滤氯化钠的用途关于氯化钠的用途,下列说法错误的是( )D氯化钠对人体的作用具有促生盐酸、帮助消化和增进食欲的作用。对维持细胞内外正常的水分分布和促进细胞内外物质 交换起主要作用。Na+Cl-主要成分NaCl氯化钠的用途 小明在家经常帮助妈妈做家务,在厨房中看到两个装白色固体的瓶子,便问妈妈,白色固体是什么。妈妈说,一瓶是食盐,一瓶是纯碱。你能帮助小明利用简单的方法对它们进行鉴别吗?活动二:食盐和纯碱的鉴别 提供的实验药品: 无色酚酞试液、稀盐酸、
澄清石灰水、CaCl2溶液、AgNO3溶液、稀硝酸。 先小组讨论后动手实验比一比,哪组的方案好、
哪组的方案多。活动三:食盐和纯碱的鉴别 实验室现有A、B两瓶未知溶液(一瓶为NaCl溶液、一瓶为Na2CO3溶液),请利用下列药品设计实验进行鉴别。资料卡片
碳酸银是一种不溶于水但可溶于稀硝酸的白色沉淀。 实验设计:分别取少量的两种待测溶液于试管中,各滴入几滴无色酚酞试液,观察现象。一支试管内无色酚酞试液变红,另一支试管内无明显现象。无色酚酞试液变红的试管中,溶液是Na2CO3溶液,另一种则为NaCl溶液。(示例)1.亚硝酸钠是一种工业用盐,它有毒、有咸味,外形与食盐相似。人误食会引起中毒,危害人体健康,甚至致人死亡。亚硝酸钠的水溶液呈碱性,食盐水呈中性。如果让你来鉴别亚硝酸钠和食盐,你选用什么试剂,如何操作?分别取少量固体放入两支试管中,加水充分溶解,各滴入几滴无色酚酞试液,观察现象。2.氯化钠是在生活中有着非常广泛的用途,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程:
(1)操作①中必须用到的一种仪器是_ ___(填序号)。
? A.研钵?? ?B.量筒?? ?C.烧杯?????D.试管
(2)小刚完成该实验的部分操作过程如图所示,其中有明显错误的是_____ ____。(填字母序号)AA、C(3)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到 ??? 等仪器。该操作中,当看到 时,停止加热。
(4)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是 _________(填序号).
A.食盐没有全部溶解即过滤??
B.蒸发时食盐飞溅剧烈?
C.蒸发后,所得精盐很潮湿?
D.器皿上沾有的精盐没全部转移到称量纸上.蒸发皿有较多固体析出A、B、D3.氯化钠是日常生活的必需品,也是重要的化工原料。粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
(1)欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:
过量的NaOH溶液、 、 ;
过量的BaCl2溶液过量的Na2CO3溶液(B组)(2)在滤液中加盐酸的作用是 ;
(3)用提纯的NaCl配制200g0.9%的生理盐水,需要NaCl的质量为 g。
①配制该溶液时所需要的玻璃仪器有
。
②如果配制后溶液溶质的质量分数低于0.9%,你认为可能的原因是 ?。(任写一个)除去NaOH和Na2CO31.8量筒、胶头滴管、烧杯、玻璃棒量取水时仰视读数实验后,请洗手!友情提醒:谢谢!一份耕耘、一分收获。
祝同学们学习进步!
+
碱酸
+
盐碱
+
盐盐
+
盐知识梳理 回顾酸碱盐的相关知识,搜索有盐生成的反应。
j
j
j
j
j
j
j活动一:比一比、赛一赛 根据以上规律,有哪些反应可以生成NaCl呢?请写出反应的化学方程式。活动一:比一比、赛一赛 2HCl + Na2CO3 == 2NaCl + H2O + CO2 ↑HCl + NaOH == NaCl + H2OCaCl2 + Na2CO3 == CaCO3 ↓ + 2NaCl
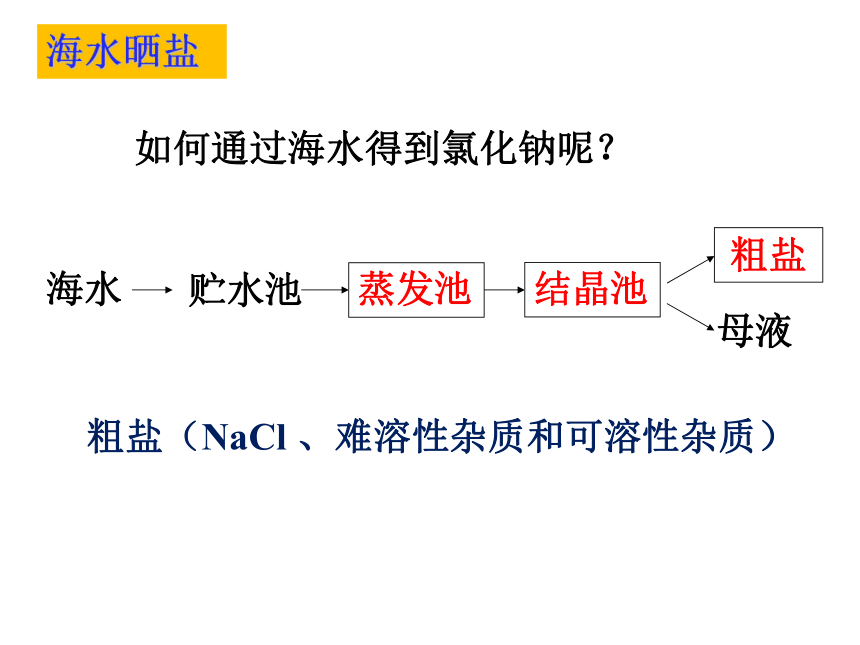
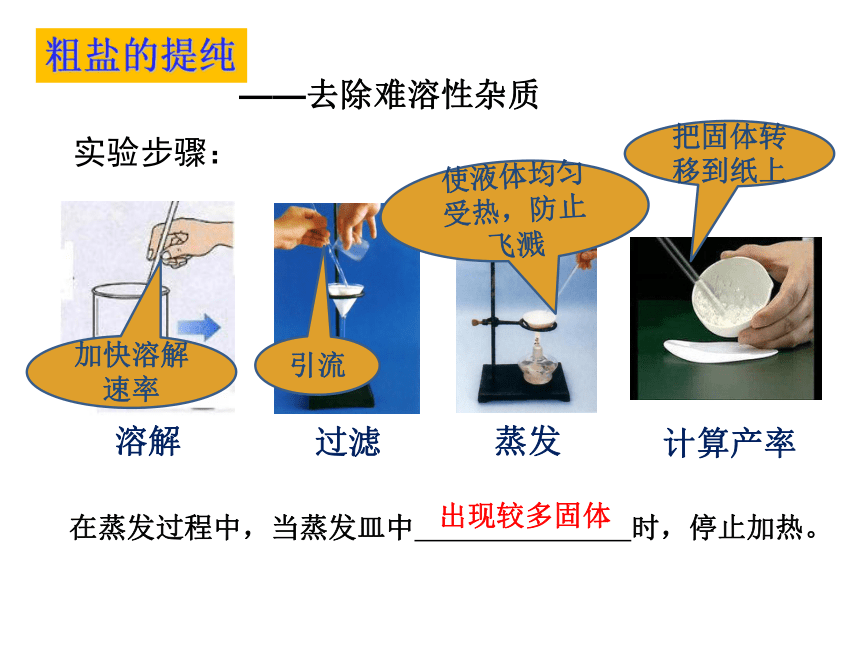
……MgCl2 + 2NaOH == Mg(OH)2 ↓ + 2NaCl 根据以上规律,有哪些反应可以生成NaCl呢?请写出反应的化学方程式。氯化钠的制取如何通过海水得到氯化钠呢?海水贮水池 母液海水晒盐 如何通过海水得到氯化钠呢?海水贮水池粗盐(NaCl 、难溶性杂质和可溶性杂质)母液海水晒盐蒸发池结晶池粗盐——去除难溶性杂质实验步骤:加快溶解速率引流使液体均匀受热,防止飞溅把固体转移到纸上粗盐的提纯在蒸发过程中,当蒸发皿中 时,停止加热。出现较多固体Na2CO3 + CaCl2粗盐的提纯NaCl ( CaCl2 、 MgCl2 )——除去某些可溶性杂质 NaOH + MgCl2 Na2CO3 + CaCl2粗盐的提纯NaCl ( CaCl2 、 MgCl2 )——除去某些可溶性杂质 NaOH + MgCl2 某粗盐样品中含有杂质MgCl2、CaCl2.以及泥沙等杂质,某同学设计了以下提纯方案:
?
请回答下列问题:
(1)操作Ⅰ、操作Ⅲ的名称分别是 、 。
(2)滤液B中所含的溶质为 。
(3)向滤液B中滴加稀盐酸,当观察到 现象时,应停止滴加。
(4)所得精盐中NaCl的质量比粗盐样品中多,原因是 。NaCl、NaOH、Na2CO3不再有气泡产生蒸发提纯过程中
有NaCl生成过滤氯化钠的用途关于氯化钠的用途,下列说法错误的是( )D氯化钠对人体的作用具有促生盐酸、帮助消化和增进食欲的作用。对维持细胞内外正常的水分分布和促进细胞内外物质 交换起主要作用。Na+Cl-主要成分NaCl氯化钠的用途 小明在家经常帮助妈妈做家务,在厨房中看到两个装白色固体的瓶子,便问妈妈,白色固体是什么。妈妈说,一瓶是食盐,一瓶是纯碱。你能帮助小明利用简单的方法对它们进行鉴别吗?活动二:食盐和纯碱的鉴别 提供的实验药品: 无色酚酞试液、稀盐酸、
澄清石灰水、CaCl2溶液、AgNO3溶液、稀硝酸。 先小组讨论后动手实验比一比,哪组的方案好、
哪组的方案多。活动三:食盐和纯碱的鉴别 实验室现有A、B两瓶未知溶液(一瓶为NaCl溶液、一瓶为Na2CO3溶液),请利用下列药品设计实验进行鉴别。资料卡片
碳酸银是一种不溶于水但可溶于稀硝酸的白色沉淀。 实验设计:分别取少量的两种待测溶液于试管中,各滴入几滴无色酚酞试液,观察现象。一支试管内无色酚酞试液变红,另一支试管内无明显现象。无色酚酞试液变红的试管中,溶液是Na2CO3溶液,另一种则为NaCl溶液。(示例)1.亚硝酸钠是一种工业用盐,它有毒、有咸味,外形与食盐相似。人误食会引起中毒,危害人体健康,甚至致人死亡。亚硝酸钠的水溶液呈碱性,食盐水呈中性。如果让你来鉴别亚硝酸钠和食盐,你选用什么试剂,如何操作?分别取少量固体放入两支试管中,加水充分溶解,各滴入几滴无色酚酞试液,观察现象。2.氯化钠是在生活中有着非常广泛的用途,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程:
(1)操作①中必须用到的一种仪器是_ ___(填序号)。
? A.研钵?? ?B.量筒?? ?C.烧杯?????D.试管
(2)小刚完成该实验的部分操作过程如图所示,其中有明显错误的是_____ ____。(填字母序号)AA、C(3)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到 ??? 等仪器。该操作中,当看到 时,停止加热。
(4)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是 _________(填序号).
A.食盐没有全部溶解即过滤??
B.蒸发时食盐飞溅剧烈?
C.蒸发后,所得精盐很潮湿?
D.器皿上沾有的精盐没全部转移到称量纸上.蒸发皿有较多固体析出A、B、D3.氯化钠是日常生活的必需品,也是重要的化工原料。粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
(1)欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:
过量的NaOH溶液、 、 ;
过量的BaCl2溶液过量的Na2CO3溶液(B组)(2)在滤液中加盐酸的作用是 ;
(3)用提纯的NaCl配制200g0.9%的生理盐水,需要NaCl的质量为 g。
①配制该溶液时所需要的玻璃仪器有
。
②如果配制后溶液溶质的质量分数低于0.9%,你认为可能的原因是 ?。(任写一个)除去NaOH和Na2CO31.8量筒、胶头滴管、烧杯、玻璃棒量取水时仰视读数实验后,请洗手!友情提醒:谢谢!一份耕耘、一分收获。
祝同学们学习进步!
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
