【备考2020】2019年浙江中考科学真题分类汇编12:常见物质的性质
文档属性
| 名称 | 【备考2020】2019年浙江中考科学真题分类汇编12:常见物质的性质 | 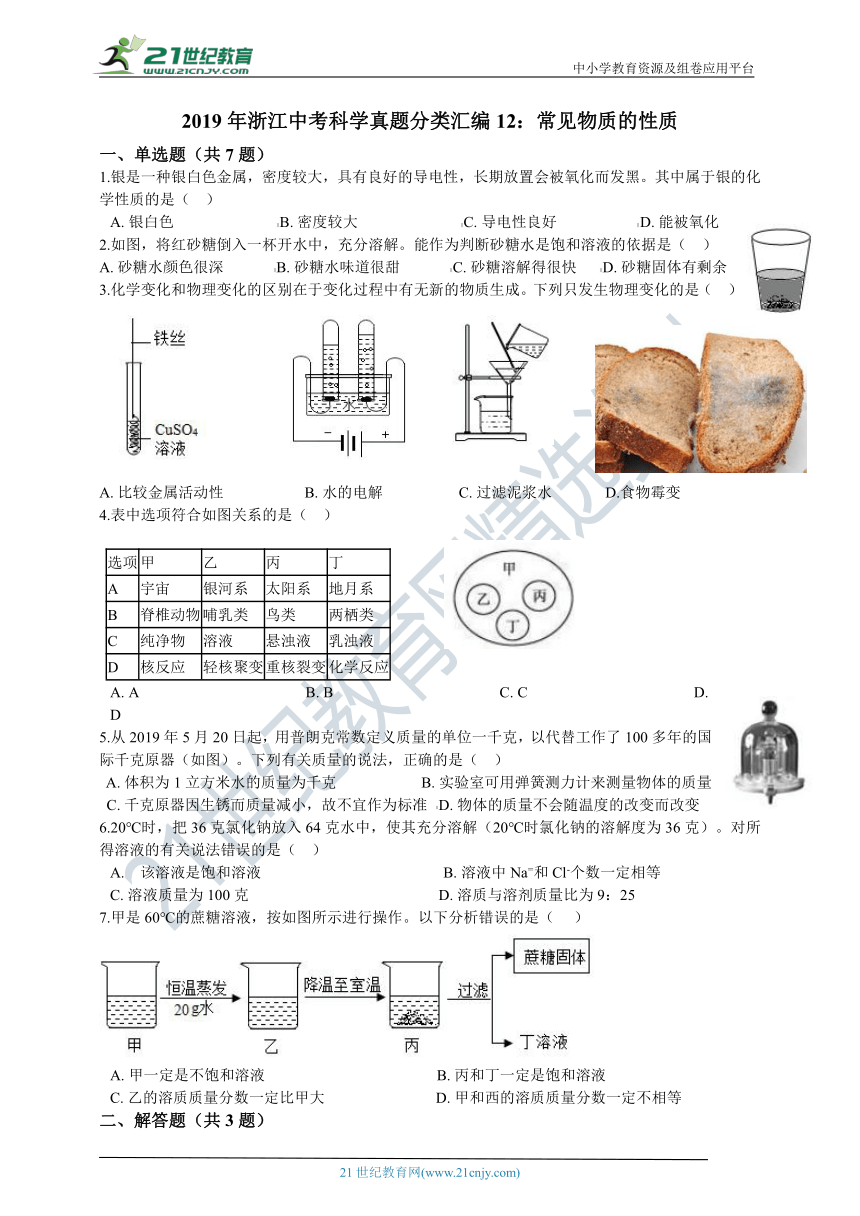 | |
| 格式 | zip | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-07-12 10:18:45 | ||
图片预览



文档简介
2019年浙江中考科学真题分类汇编12:常见物质的性质
一、单选题(共7题)
1.银是一种银白色金属,密度较大,具有良好的导电性,长期放置会被氧化而发黑。其中属于银的化学性质的是(?? )
A.?银白色???????????????????????????B.?密度较大???????????????????????????C.?导电性良好?????????????????????D.?能被氧化
2.如图,将红砂糖倒入一杯开水中,充分溶解。能作为判断砂糖水是饱和溶液的依据是(?? )
A.?砂糖水颜色很深?????????????B.?砂糖水味道很甜?????????????C.?砂糖溶解得很快??????D.?砂糖固体有剩余
3.化学变化和物理变化的区别在于变化过程中有无新的物质生成。下列只发生物理变化的是(?? )
A.?比较金属活动性 ? B.?水的电解 C.?过滤泥浆水 D.食物霉变
4.表中选项符合如图关系的是(?? )
选项
甲
乙
丙
丁
A
宇宙
银河系
太阳系
地月系
B
脊椎动物
哺乳类
鸟类
两栖类
C
纯净物
溶液
悬浊液
乳浊液
D
核反应
轻核聚变
重核裂变
化学反应
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
5.从2019年5月20日起,用普朗克常数定义质量的单位一千克,以代替工作了100多年的国际千克原器(如图)。下列有关质量的说法,正确的是(?? )
A.?体积为1立方米水的质量为千克??????????????? ?B.?实验室可用弹簧测力计来测量物体的质量 C.?千克原器因生锈而质量减小,故不宜作为标准??D.?物体的质量不会随温度的改变而改变
6.20℃时,把36克氯化钠放入64克水中,使其充分溶解(20℃时氯化钠的溶解度为36克)。对所得溶液的有关说法错误的是(?? )
A.?? 该溶液是饱和溶液 B.?溶液中Na=和Cl-个数一定相等 C.?溶液质量为100克 D.?溶质与溶剂质量比为9:25
7.甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是(??? )
A.?甲一定是不饱和溶液??????????????????????????????????????????? B.?丙和丁一定是饱和溶液 C.?乙的溶质质量分数一定比甲大?????????????????????????????D.?甲和西的溶质质量分数一定不相等
二、解答题(共3题)
8.某同学进行硫酸铜晶体(化学式为CuSO4·5H2O)的制备和生长实验,配制了某温度时的硫酸铜热饱和溶液,静置、冷却到室温,观察晶体的生长,如图。
(1)能判断原硫酸铜溶液已饱和的方法是?????? 。
A.?观察颜色,溶液蓝色较深 B.?溶液冷却,有蓝色品体析出 C.?蒸发少量水,有蓝色品体析出 D.?加人硫酸铜晶体,品体质量不变
(2)现称取49克无水硫酸铜溶于水,配成150克某温度时的热饱和溶液,再冷却到室温,共析出50克硫酸铜晶体,请计算该室温时硫酸铜饱和溶液的溶质质量分数。
9.下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
温度/℃
0
10
20
30
40
溶解度/克
13.3
20.9
31.6
45.8
63.9
(1)10℃时,100克水中最多可溶解硝酸钾的质量为________克。
(2)20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为________。
(3)如图是硝酸钾溶液的变化情况,请写出一种可采用的操作方法。(写出计算过程)
10.氯霉素属于广谱抗生素,能杀灭细菌,但摄入过多容易导致血液疾病,所以国家严令禁止在食品中使用。今年,广州市有关部门在抽检中发现,有些不法商贩向黄金贝、花蛤等海产品中添加氯霉素,来延长海鲜的存活期。这种滥用氯霉素的现象引起了市民的警觉。
(1)氯霉素性质稳定,不易分解,这种性质属于________(填“物理”或“化学”)性质。
(2)氯霉素(化学式为C11H12Cl2N2O5)中碳元素和氧元素的质量比为________。 (3)长期使用氯霉素,细菌能对氯霉素产生耐药性。这是氯霉素对细菌进行________的结果。
答案解析部分
一、单选题
1. D
考点:化学性质与物理性质的差别及应用
解析:【分析】物质不需要发生化学变化就能表现出来的性质,如:颜色、状态、气味、密度、硬度、光泽、溶解性、挥发性、导电性、延展性等、熔点、沸点等。 物质在发生化学变化中才能表现出来的性质叫做化学性质,如:可燃性、稳定性、酸性、碱性、氧化性、还原性等、腐蚀性等。 【解答】“银白色”、“密度大”和“导电性”都是银的物理性质,而“能被氧化”是指银和空气中的氧气反应生成氧化银的性质,属于化学性质,故D符合题意。 故选D。
2. D
考点:饱和溶液和不饱和溶液
解析:【分析】在一定温度下,一定剂量的溶剂里面,如果不能继续溶解某种溶质,那么这时的溶液就是饱和溶液;只要能够证明不能再继续溶解某种溶质即可。 【解答】将红砂糖倒入一杯开水中,充分溶解,如果砂糖固体有剩余,说明此时的溶液再也不能溶解砂糖,即这时的砂糖水是饱和溶液,故D正确,而A、B、C错误。 故选D。
3. C
考点:化学变化和物理变化的判别
解析:【分析】根据化学变化物理变化的特点分析,化学变化有新物质生成,物理变化没有新物质生成,判断变化种类就是看变化后有没有新物质生成。 【解答】A、铁与硫酸铜反应会生成新物质铜和硫酸亚铁,发生了化学变化,错误; B、电解水时有新物质氧气和氢气生成,发生了化学变化,错误; C、过滤只是将液体和固体分离,没有新物质生成,发生的只有物理变化,正确; D、食物霉变生成了新物质,发生了化学变化,错误。 故答案为:C。
4. B
考点:宇宙的构成,悬浊液的概念及其与溶液的区别,乳浊液的概念及其与溶液的区别,动物的分类,识别化学反应基本类型
解析:【分析】脊椎动物是指有脊椎骨的动物,是脊索动物的一个亚门。数量最多、结构最复杂,进化地位最高,由软体动物进化而来。形态结构彼此悬殊,生活方式千差万别。脊椎动物一般体形左右对称,全身分为头、躯干、尾三个部分,有比较完善的感觉器官、运动器官和高度分化的神经系统。包括圆口类、鱼类、两栖动物、爬行动物、鸟类和哺乳动物等六大类。 【解答】由图可知,甲包含乙丁丙,乙丙丁之间处于并列关系; A、宇宙包含银河系、太阳系、地月系;银河系包含太阳系、地月系;太阳系包含地月系;故A不符合; B、脊椎动物包含哺乳类、鸟类、两栖类;而哺乳类、鸟类、两栖类之间处于并列关系;故B符合; C、溶液、悬浊液、乳浊液都是混合物,与纯净物并列;故C不符合; D、核反应包含轻核聚变、重核裂变,但不包含化学反应;故D不符合; 故答案为:B。
5. D
考点:质量及其特点
解析:【分析】(1)水的密度会随着状态和温度的变化而变化; (2)弹簧测力计是测力的工具; (3)铁与空气中的氧气和水分发生反应生成铁锈,因此质量会增加; (4)质量是物质本身的一种属性,不随物质形状、状态、位置和温度的变化而变化。 【解答】A.如果水的密度是1g/cm3 , 那么1m3的水质量是1kg;但是水的密度会发生变化,因此1m3的水质量也会发生变化,故A错误; B.实验室用弹簧测力计测量物体的重力,而不是质量,故B错误; C.千克原器因生锈而质量增大,故C错误; D.物体的质量不会随温度的改变而改变,故D正确。 故选D。
6. C
考点:饱和溶液和不饱和溶液,固体溶解度的概念
解析:【分析】根据溶解度定义及溶解度所对应饱和溶液中溶质、溶剂的质量关系分析,一定温度下的饱和溶液溶质和溶剂质量比是定值,为溶解度:100,将物质放入水中溶解,计算所得溶液时先要判断物质是否能全部溶解,没有溶解的物质不算溶质质量。 【解答】A、 20℃时氯化钠的溶解度为36克 ,即100克水中最多溶解36克氯化钠,所以 把36克氯化钠放入64克水中, 氯化钠不能全部溶解,所得溶液为饱和溶液,正确; B、氯化钠中钠离子和氯离子个数比为1:1,则溶液中钠离子和氯离子个数一定相等,正确; C、氯化钠不能全部溶解,所得溶液质量小于100克,错误; D、溶液为饱和溶液,所以溶质与溶剂质量比为36:100=9:25,正确; 故答案为:C。
7. D
考点:饱和溶液和不饱和溶液,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数的变化
解析:【分析】饱和溶液是指在一定温度和压力下,溶剂中所溶解的溶质已达最大量(溶解度)的溶液。即溶质与溶剂接触时,溶解速度与析出速度相等的溶液。溶质的量未达到对应的饱和状态的溶液,称做不饱和溶液。溶质质量分数是指溶液中溶质的质量分数是溶质质量与溶液质量之比。
【解答】A、甲恒温蒸发20g水,依然没有溶质析出,说明甲之前一定是不饱和溶液;故A正确;
B、丙中有晶体析出,说明丙一定是饱和溶液,对丙过滤后形成的丁也是饱和溶液;故B正确;
C、乙是甲蒸发20g水后形成的,溶剂减少而溶质不变,所以乙的溶质质量分数肯定比甲大;故C正确;
D、丙是饱和溶液,而甲是不饱和溶液,但两者的温度不同,所以其溶质质量分数有可能相同;故D错误;
故答案为:D。
二、解答题
8. (1)D (2)解:析出CuSO4溶质的质量为:
=50g× =32g
溶液中剩余CuSO4溶质的质量为:49g-32g=17g
溶液的质量为:150g-50g=100g
溶质质量分数= = =0.17=17%
答:该室温时硫酸钢饱和溶液的溶质质量分数为17%
考点:饱和溶液和不饱和溶液,溶质质量分数的简单计算
解析:【分析】(1)在一种溶液中加入某种溶质,如果溶质的质量不减少,说明溶液已经达到饱和; (2)硫酸铜晶体中含有硫酸铜和水,首先用晶体质量×硫酸铜晶体中硫酸铜的质量分数计算出晶体中硫酸铜的质量,再用前后硫酸铜质量之差计算剩余溶液中硫酸铜的质量;然后用原来溶液质量减去硫酸铜晶体质量计算出声音溶液的质量,最后再计算剩余溶液的溶质质量分数。 【解答】(1)只有在硫酸铜溶液中加入硫酸铜晶体后,晶体的质量不再减少,才能说明硫酸铜溶液已经饱和,故选D。 (2) 析出CuSO4溶质的质量为:
?=50g×??=32g
溶液中剩余CuSO4溶质的质量为:49g-32g=17g
溶液的质量为:150g-50g=100g
溶质质量分数=??=??=0.17=17%
答:该室温时硫酸钢饱和溶液的溶质质量分数为17%
9. (1)20.9 (2)20% (3)解:方法一:设要加入硝酸钾的质量为x。
100克×10%+x=(100克+x)×25%x=20克
答:可向烧杯中加入20克硝酸钾。
方法二:设蒸发水的质量为y。
100克×10%=(100克-y)×25%?? y=60克
答:可蒸发60克水。
考点:固体溶解度的概念,溶质的质量分数的改变方法
解析:【分析】(1)根据溶解度定义分析; (2)根据溶解度判断一定量水中所加物质是否能全部溶解,利用溶质质量分数=溶质质量/溶液质量分析; (3)根据增加溶质质量分数可利用蒸发溶剂或加溶质的方法分析。 【解答】(1) 10℃时,硝酸钾的溶解度为20.9克,则100克水中最多可溶解硝酸钾的质量为 20.9克; (2) 20℃时,硝 酸钾溶解度为31.6克,将10克硝酸钾加入40克水中,只能溶解12.64克,所以将10克硝酸钾加入40克水中能全部溶解, 所得溶液溶质质量分数为 ; 故答案为:(1)20.9;(2)20%;(3)加20克硝酸钾或蒸发60克水。
10. (1)化学 (2)33:20 (3)自然选择
考点:化学性质与物理性质的差别及应用,自然选择学说,有关化学式的计算和推断
解析:【分析】(1)化学性质是经过化学变化表现出来的性质,物理性质是不经过化学变化就表现出来的性质; (2)根据化合物中元素的质量比=各元素的相对原子质量×原子个数之比进行计算; (3)长期使用氯霉素,细菌能对氯霉素产生耐药性,是自然选择的结果。 【解答】(1)氯霉素不易分解属于化学性质; (2)氯霉素中碳元素和氧元素的质量比为:(12×11):(16×5)=33:20; (3)长期使用氯霉素,细菌能对氯霉素产生耐药性,这是氯霉素对细菌进行自然选择的结果; 故答案为:(1)化学;(2)33:20;(3)自然选择。
一、单选题(共7题)
1.银是一种银白色金属,密度较大,具有良好的导电性,长期放置会被氧化而发黑。其中属于银的化学性质的是(?? )
A.?银白色???????????????????????????B.?密度较大???????????????????????????C.?导电性良好?????????????????????D.?能被氧化
2.如图,将红砂糖倒入一杯开水中,充分溶解。能作为判断砂糖水是饱和溶液的依据是(?? )
A.?砂糖水颜色很深?????????????B.?砂糖水味道很甜?????????????C.?砂糖溶解得很快??????D.?砂糖固体有剩余
3.化学变化和物理变化的区别在于变化过程中有无新的物质生成。下列只发生物理变化的是(?? )
A.?比较金属活动性 ? B.?水的电解 C.?过滤泥浆水 D.食物霉变
4.表中选项符合如图关系的是(?? )
选项
甲
乙
丙
丁
A
宇宙
银河系
太阳系
地月系
B
脊椎动物
哺乳类
鸟类
两栖类
C
纯净物
溶液
悬浊液
乳浊液
D
核反应
轻核聚变
重核裂变
化学反应
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
5.从2019年5月20日起,用普朗克常数定义质量的单位一千克,以代替工作了100多年的国际千克原器(如图)。下列有关质量的说法,正确的是(?? )
A.?体积为1立方米水的质量为千克??????????????? ?B.?实验室可用弹簧测力计来测量物体的质量 C.?千克原器因生锈而质量减小,故不宜作为标准??D.?物体的质量不会随温度的改变而改变
6.20℃时,把36克氯化钠放入64克水中,使其充分溶解(20℃时氯化钠的溶解度为36克)。对所得溶液的有关说法错误的是(?? )
A.?? 该溶液是饱和溶液 B.?溶液中Na=和Cl-个数一定相等 C.?溶液质量为100克 D.?溶质与溶剂质量比为9:25
7.甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是(??? )
A.?甲一定是不饱和溶液??????????????????????????????????????????? B.?丙和丁一定是饱和溶液 C.?乙的溶质质量分数一定比甲大?????????????????????????????D.?甲和西的溶质质量分数一定不相等
二、解答题(共3题)
8.某同学进行硫酸铜晶体(化学式为CuSO4·5H2O)的制备和生长实验,配制了某温度时的硫酸铜热饱和溶液,静置、冷却到室温,观察晶体的生长,如图。
(1)能判断原硫酸铜溶液已饱和的方法是?????? 。
A.?观察颜色,溶液蓝色较深 B.?溶液冷却,有蓝色品体析出 C.?蒸发少量水,有蓝色品体析出 D.?加人硫酸铜晶体,品体质量不变
(2)现称取49克无水硫酸铜溶于水,配成150克某温度时的热饱和溶液,再冷却到室温,共析出50克硫酸铜晶体,请计算该室温时硫酸铜饱和溶液的溶质质量分数。
9.下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
温度/℃
0
10
20
30
40
溶解度/克
13.3
20.9
31.6
45.8
63.9
(1)10℃时,100克水中最多可溶解硝酸钾的质量为________克。
(2)20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为________。
(3)如图是硝酸钾溶液的变化情况,请写出一种可采用的操作方法。(写出计算过程)
10.氯霉素属于广谱抗生素,能杀灭细菌,但摄入过多容易导致血液疾病,所以国家严令禁止在食品中使用。今年,广州市有关部门在抽检中发现,有些不法商贩向黄金贝、花蛤等海产品中添加氯霉素,来延长海鲜的存活期。这种滥用氯霉素的现象引起了市民的警觉。
(1)氯霉素性质稳定,不易分解,这种性质属于________(填“物理”或“化学”)性质。
(2)氯霉素(化学式为C11H12Cl2N2O5)中碳元素和氧元素的质量比为________。 (3)长期使用氯霉素,细菌能对氯霉素产生耐药性。这是氯霉素对细菌进行________的结果。
答案解析部分
一、单选题
1. D
考点:化学性质与物理性质的差别及应用
解析:【分析】物质不需要发生化学变化就能表现出来的性质,如:颜色、状态、气味、密度、硬度、光泽、溶解性、挥发性、导电性、延展性等、熔点、沸点等。 物质在发生化学变化中才能表现出来的性质叫做化学性质,如:可燃性、稳定性、酸性、碱性、氧化性、还原性等、腐蚀性等。 【解答】“银白色”、“密度大”和“导电性”都是银的物理性质,而“能被氧化”是指银和空气中的氧气反应生成氧化银的性质,属于化学性质,故D符合题意。 故选D。
2. D
考点:饱和溶液和不饱和溶液
解析:【分析】在一定温度下,一定剂量的溶剂里面,如果不能继续溶解某种溶质,那么这时的溶液就是饱和溶液;只要能够证明不能再继续溶解某种溶质即可。 【解答】将红砂糖倒入一杯开水中,充分溶解,如果砂糖固体有剩余,说明此时的溶液再也不能溶解砂糖,即这时的砂糖水是饱和溶液,故D正确,而A、B、C错误。 故选D。
3. C
考点:化学变化和物理变化的判别
解析:【分析】根据化学变化物理变化的特点分析,化学变化有新物质生成,物理变化没有新物质生成,判断变化种类就是看变化后有没有新物质生成。 【解答】A、铁与硫酸铜反应会生成新物质铜和硫酸亚铁,发生了化学变化,错误; B、电解水时有新物质氧气和氢气生成,发生了化学变化,错误; C、过滤只是将液体和固体分离,没有新物质生成,发生的只有物理变化,正确; D、食物霉变生成了新物质,发生了化学变化,错误。 故答案为:C。
4. B
考点:宇宙的构成,悬浊液的概念及其与溶液的区别,乳浊液的概念及其与溶液的区别,动物的分类,识别化学反应基本类型
解析:【分析】脊椎动物是指有脊椎骨的动物,是脊索动物的一个亚门。数量最多、结构最复杂,进化地位最高,由软体动物进化而来。形态结构彼此悬殊,生活方式千差万别。脊椎动物一般体形左右对称,全身分为头、躯干、尾三个部分,有比较完善的感觉器官、运动器官和高度分化的神经系统。包括圆口类、鱼类、两栖动物、爬行动物、鸟类和哺乳动物等六大类。 【解答】由图可知,甲包含乙丁丙,乙丙丁之间处于并列关系; A、宇宙包含银河系、太阳系、地月系;银河系包含太阳系、地月系;太阳系包含地月系;故A不符合; B、脊椎动物包含哺乳类、鸟类、两栖类;而哺乳类、鸟类、两栖类之间处于并列关系;故B符合; C、溶液、悬浊液、乳浊液都是混合物,与纯净物并列;故C不符合; D、核反应包含轻核聚变、重核裂变,但不包含化学反应;故D不符合; 故答案为:B。
5. D
考点:质量及其特点
解析:【分析】(1)水的密度会随着状态和温度的变化而变化; (2)弹簧测力计是测力的工具; (3)铁与空气中的氧气和水分发生反应生成铁锈,因此质量会增加; (4)质量是物质本身的一种属性,不随物质形状、状态、位置和温度的变化而变化。 【解答】A.如果水的密度是1g/cm3 , 那么1m3的水质量是1kg;但是水的密度会发生变化,因此1m3的水质量也会发生变化,故A错误; B.实验室用弹簧测力计测量物体的重力,而不是质量,故B错误; C.千克原器因生锈而质量增大,故C错误; D.物体的质量不会随温度的改变而改变,故D正确。 故选D。
6. C
考点:饱和溶液和不饱和溶液,固体溶解度的概念
解析:【分析】根据溶解度定义及溶解度所对应饱和溶液中溶质、溶剂的质量关系分析,一定温度下的饱和溶液溶质和溶剂质量比是定值,为溶解度:100,将物质放入水中溶解,计算所得溶液时先要判断物质是否能全部溶解,没有溶解的物质不算溶质质量。 【解答】A、 20℃时氯化钠的溶解度为36克 ,即100克水中最多溶解36克氯化钠,所以 把36克氯化钠放入64克水中, 氯化钠不能全部溶解,所得溶液为饱和溶液,正确; B、氯化钠中钠离子和氯离子个数比为1:1,则溶液中钠离子和氯离子个数一定相等,正确; C、氯化钠不能全部溶解,所得溶液质量小于100克,错误; D、溶液为饱和溶液,所以溶质与溶剂质量比为36:100=9:25,正确; 故答案为:C。
7. D
考点:饱和溶液和不饱和溶液,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数的变化
解析:【分析】饱和溶液是指在一定温度和压力下,溶剂中所溶解的溶质已达最大量(溶解度)的溶液。即溶质与溶剂接触时,溶解速度与析出速度相等的溶液。溶质的量未达到对应的饱和状态的溶液,称做不饱和溶液。溶质质量分数是指溶液中溶质的质量分数是溶质质量与溶液质量之比。
【解答】A、甲恒温蒸发20g水,依然没有溶质析出,说明甲之前一定是不饱和溶液;故A正确;
B、丙中有晶体析出,说明丙一定是饱和溶液,对丙过滤后形成的丁也是饱和溶液;故B正确;
C、乙是甲蒸发20g水后形成的,溶剂减少而溶质不变,所以乙的溶质质量分数肯定比甲大;故C正确;
D、丙是饱和溶液,而甲是不饱和溶液,但两者的温度不同,所以其溶质质量分数有可能相同;故D错误;
故答案为:D。
二、解答题
8. (1)D (2)解:析出CuSO4溶质的质量为:
=50g× =32g
溶液中剩余CuSO4溶质的质量为:49g-32g=17g
溶液的质量为:150g-50g=100g
溶质质量分数= = =0.17=17%
答:该室温时硫酸钢饱和溶液的溶质质量分数为17%
考点:饱和溶液和不饱和溶液,溶质质量分数的简单计算
解析:【分析】(1)在一种溶液中加入某种溶质,如果溶质的质量不减少,说明溶液已经达到饱和; (2)硫酸铜晶体中含有硫酸铜和水,首先用晶体质量×硫酸铜晶体中硫酸铜的质量分数计算出晶体中硫酸铜的质量,再用前后硫酸铜质量之差计算剩余溶液中硫酸铜的质量;然后用原来溶液质量减去硫酸铜晶体质量计算出声音溶液的质量,最后再计算剩余溶液的溶质质量分数。 【解答】(1)只有在硫酸铜溶液中加入硫酸铜晶体后,晶体的质量不再减少,才能说明硫酸铜溶液已经饱和,故选D。 (2) 析出CuSO4溶质的质量为:
?=50g×??=32g
溶液中剩余CuSO4溶质的质量为:49g-32g=17g
溶液的质量为:150g-50g=100g
溶质质量分数=??=??=0.17=17%
答:该室温时硫酸钢饱和溶液的溶质质量分数为17%
9. (1)20.9 (2)20% (3)解:方法一:设要加入硝酸钾的质量为x。
100克×10%+x=(100克+x)×25%x=20克
答:可向烧杯中加入20克硝酸钾。
方法二:设蒸发水的质量为y。
100克×10%=(100克-y)×25%?? y=60克
答:可蒸发60克水。
考点:固体溶解度的概念,溶质的质量分数的改变方法
解析:【分析】(1)根据溶解度定义分析; (2)根据溶解度判断一定量水中所加物质是否能全部溶解,利用溶质质量分数=溶质质量/溶液质量分析; (3)根据增加溶质质量分数可利用蒸发溶剂或加溶质的方法分析。 【解答】(1) 10℃时,硝酸钾的溶解度为20.9克,则100克水中最多可溶解硝酸钾的质量为 20.9克; (2) 20℃时,硝 酸钾溶解度为31.6克,将10克硝酸钾加入40克水中,只能溶解12.64克,所以将10克硝酸钾加入40克水中能全部溶解, 所得溶液溶质质量分数为 ; 故答案为:(1)20.9;(2)20%;(3)加20克硝酸钾或蒸发60克水。
10. (1)化学 (2)33:20 (3)自然选择
考点:化学性质与物理性质的差别及应用,自然选择学说,有关化学式的计算和推断
解析:【分析】(1)化学性质是经过化学变化表现出来的性质,物理性质是不经过化学变化就表现出来的性质; (2)根据化合物中元素的质量比=各元素的相对原子质量×原子个数之比进行计算; (3)长期使用氯霉素,细菌能对氯霉素产生耐药性,是自然选择的结果。 【解答】(1)氯霉素不易分解属于化学性质; (2)氯霉素中碳元素和氧元素的质量比为:(12×11):(16×5)=33:20; (3)长期使用氯霉素,细菌能对氯霉素产生耐药性,这是氯霉素对细菌进行自然选择的结果; 故答案为:(1)化学;(2)33:20;(3)自然选择。
同课章节目录
