沪教版九年级上册化学 3.1.4 离子 课件(21张ppt)
文档属性
| 名称 | 沪教版九年级上册化学 3.1.4 离子 课件(21张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 391.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-07-12 00:00:00 | ||
图片预览







文档简介
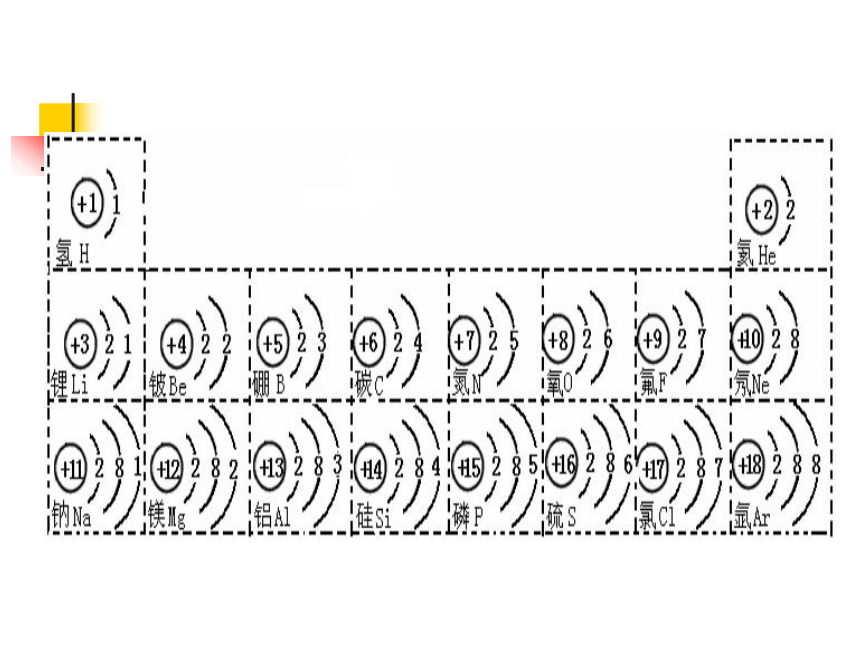
课件21张PPT。构成物质的基本微粒 离子如:干冰由二氧化碳分子构成金刚石由碳原子构成铜由铜原子构成食盐(氯化钠)由钠离子和氯离子构成原子的自述大家好,我是微观粒子的一员:原子。我很小,但我很有能耐,世间的金属和稀有气体等物质都是由我构成的。在我体内,有一个 , 在核外空间作高速运动。羞涩的 和 躲在原子核内,由于质子带 ,中子 ,使得原子核也带上了 ,正好把电子身上的 深深吸引。在化学变化中我还可以通过 变成离子。
原子核核外电子质子中子正电不带电正电负电荷 得失电子原子中电子排布的简单规则:电子排布时,先排满内层再排外层,第一层最多可排2个电子,第二层最多排8个电子,最外层最多可排8个电子。当最外层有2个或者8个电子时,微粒性质稳定。
牛刀小试:请画出黑板上原子的结构示意图。
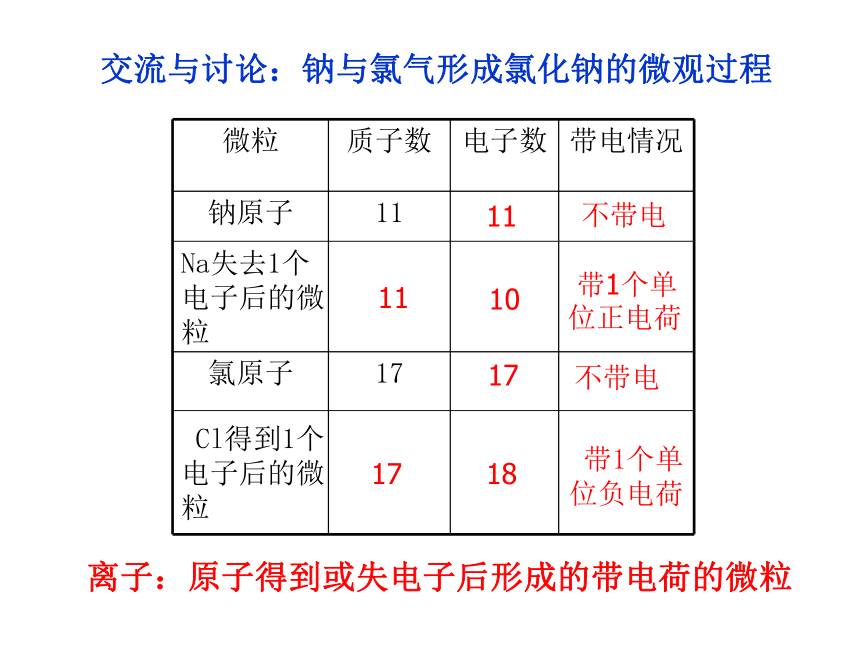
11 带1个单位正电荷 带1个单位负电荷111017不带电1718不带电交流与讨论:钠与氯气形成氯化钠的微观过程Na失去1个电子后的微粒 Cl得到1个电子后的微粒离子:原子得到或失电子后形成的带电荷的微粒 金属钠在氯气中燃烧,每个钠原子失
去1个电子,形成了带 个单位 电荷的钠离子,每个氯原子得到1个电子,形成了带 个单位 电荷的氯离子。带有相反电荷的钠离子(Na+)和氯离子(Cl-)之间 ,构成了氯化钠(NaCl)。正氯化钠的微观形成11负相互作用物质,如二氧化碳、水等物质,如铜、金刚石等 物质,如氯化钠、氧化镁等离子原子分子构成物质的微粒结合失去或得到电子得到或失去电子结合结合分子、原子、离子与物质的关系⑴ 在元素符号的右上角标注离子所带电荷的数目及电性;
⑵ 数字在前,“+”、“-”号在后;
⑶ 离子所带电荷数为1时,1省去不写。离子符号的书写练习:根据下列原子得失电子的情况分别写出它们形成的离子的名称和符号。铝离子
Al3+硫离子
S2-氟离子
F- 硫原子(S) 铝原子(Al) 氟原子(F) 钙原子(Ca)得2个电子失2个电子得1个电子失3个电子钙离子
Ca2+离子符号的意义Mg2+每个镁离子带2个单位的正电荷2表示2个镁离子整体表示镁离子或1个镁离子2个铝离子5个氯离子4Na+Mg2+学完本课,你应该知道...... 1、下列物质不是由离子构成的是( )
A.氯化钙 B. 氧化镁
C.金刚石 D.氯化钠C当堂反馈2、下列有关分子、原子、离子的说法错误的是( )
A.阳离子一定带正电荷,阴离子一定带负电,原子不带电
B.原子中,质子数等于电子数
C.分子、原子、离子都能直接构成物质
D.原子失去了电子就带上了负电荷D3、下列说法中不正确的是( )
A. 原子由原子核和核外电子构成;
B. 原子和离子可以相互转化;
C. 离子中,质子数与电子数不相等;
D. 氯化钠是通过阴、阳离子的静电作用形成的化合物,因此,氯化钠带有一定的电荷。D下列结构示意图中属于阳离子的是( )D4、在原子、中子、电子、质子、原子核、离子(阳离子、阴离子)中, 、 不带电; 、 带负电; 、 、 带正电; 、 可构成物质。 质子 原子核 阳离子电子 阴离子原子 中子原子 离子谢谢!
原子核核外电子质子中子正电不带电正电负电荷 得失电子原子中电子排布的简单规则:电子排布时,先排满内层再排外层,第一层最多可排2个电子,第二层最多排8个电子,最外层最多可排8个电子。当最外层有2个或者8个电子时,微粒性质稳定。
牛刀小试:请画出黑板上原子的结构示意图。
11 带1个单位正电荷 带1个单位负电荷111017不带电1718不带电交流与讨论:钠与氯气形成氯化钠的微观过程Na失去1个电子后的微粒 Cl得到1个电子后的微粒离子:原子得到或失电子后形成的带电荷的微粒 金属钠在氯气中燃烧,每个钠原子失
去1个电子,形成了带 个单位 电荷的钠离子,每个氯原子得到1个电子,形成了带 个单位 电荷的氯离子。带有相反电荷的钠离子(Na+)和氯离子(Cl-)之间 ,构成了氯化钠(NaCl)。正氯化钠的微观形成11负相互作用物质,如二氧化碳、水等物质,如铜、金刚石等 物质,如氯化钠、氧化镁等离子原子分子构成物质的微粒结合失去或得到电子得到或失去电子结合结合分子、原子、离子与物质的关系⑴ 在元素符号的右上角标注离子所带电荷的数目及电性;
⑵ 数字在前,“+”、“-”号在后;
⑶ 离子所带电荷数为1时,1省去不写。离子符号的书写练习:根据下列原子得失电子的情况分别写出它们形成的离子的名称和符号。铝离子
Al3+硫离子
S2-氟离子
F- 硫原子(S) 铝原子(Al) 氟原子(F) 钙原子(Ca)得2个电子失2个电子得1个电子失3个电子钙离子
Ca2+离子符号的意义Mg2+每个镁离子带2个单位的正电荷2表示2个镁离子整体表示镁离子或1个镁离子2个铝离子5个氯离子4Na+Mg2+学完本课,你应该知道...... 1、下列物质不是由离子构成的是( )
A.氯化钙 B. 氧化镁
C.金刚石 D.氯化钠C当堂反馈2、下列有关分子、原子、离子的说法错误的是( )
A.阳离子一定带正电荷,阴离子一定带负电,原子不带电
B.原子中,质子数等于电子数
C.分子、原子、离子都能直接构成物质
D.原子失去了电子就带上了负电荷D3、下列说法中不正确的是( )
A. 原子由原子核和核外电子构成;
B. 原子和离子可以相互转化;
C. 离子中,质子数与电子数不相等;
D. 氯化钠是通过阴、阳离子的静电作用形成的化合物,因此,氯化钠带有一定的电荷。D下列结构示意图中属于阳离子的是( )D4、在原子、中子、电子、质子、原子核、离子(阳离子、阴离子)中, 、 不带电; 、 带负电; 、 、 带正电; 、 可构成物质。 质子 原子核 阳离子电子 阴离子原子 中子原子 离子谢谢!
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
