沪教版九年级上册化学 5.3 金属防护和废金属回收 课件(20张PPT)
文档属性
| 名称 | 沪教版九年级上册化学 5.3 金属防护和废金属回收 课件(20张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 8.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-07-12 17:47:38 | ||
图片预览







文档简介
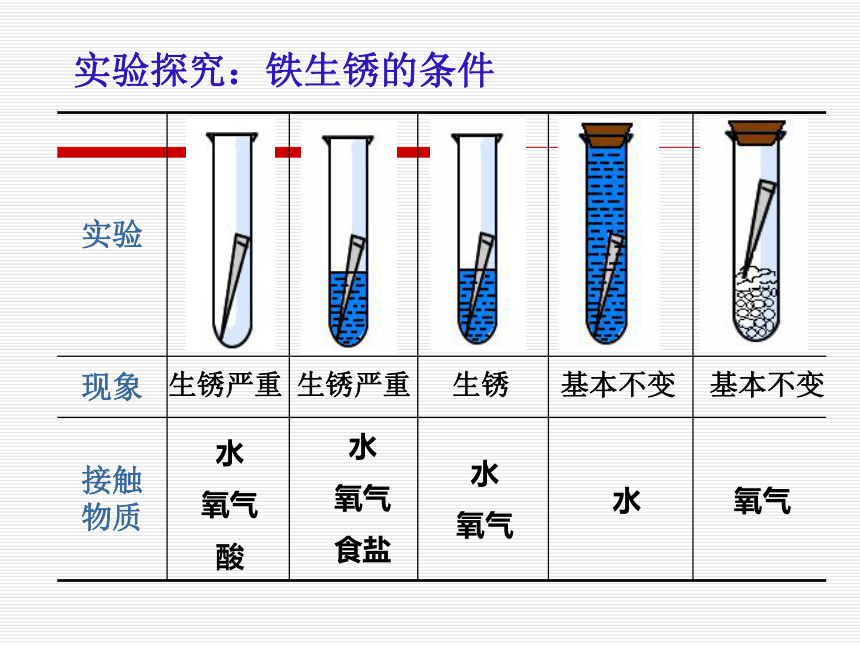
课件20张PPT。5.3 金属防护和废金属回收学习目标1.知道钢铁锈蚀的条件;2.了解防止金属锈蚀的简单方法;3.知道废弃金属对环境的污染, 认识回收金属的重要意义。铁生锈要具备哪些条件?铁生锈可能是因为与空气中的氧气、水以及其他物质反应一、铁生锈条件的探究实验探究:铁生锈的条件水
氧气
酸水
氧气
食盐水
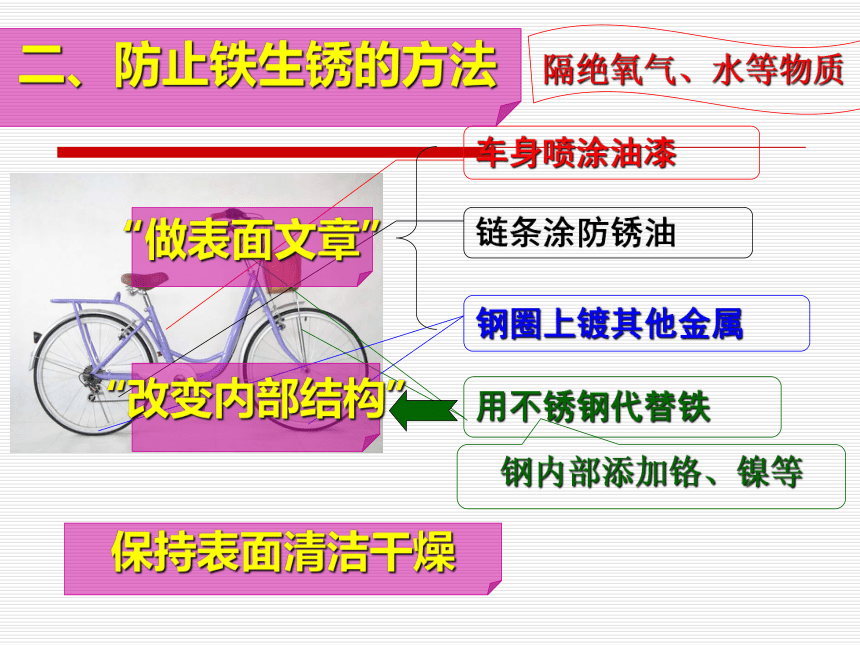
氧气水氧气生锈严重生锈严重生锈基本不变基本不变一周后盐 酸食盐水水蒸馏水干燥剂铁锈疏松多孔,锈“吃”铁铁锈的主要成分是氧化铁栏杆生锈松动 工人失足坠楼 篮球架基生锈倒塌砸到学生 生锈腐蚀易坠落伤人 超龄空调成隐形炸弹汽车生锈危机重重 铁制品生锈造成的危害车身喷涂油漆链条涂防锈油钢圈上镀其他金属隔绝氧气、水等物质用不锈钢代替铁“做表面文章”“改变内部结构”保持表面清洁干燥钢内部添加铬、镍等二、防止铁生锈的方法文具盒钢 尺搪瓷杯回形针三、废金属的回收利用可回收标志1.节约资源
2.保护环境回收废钢铁炼钢 减少冶金渣40%、减少废弃物97%、减少烟灰86%、减轻水污染76%,每生产一吨钢,可以减少投资500-700美元你的收获:一、钢铁制品锈蚀条件的探究
1.铁与氧气、水相互作用而生锈
2.稀酸和食盐溶液能加快铁生锈的速度
二、防止铁制品生锈的方法
1. 覆盖保护层——“做表面文章”
2.改变钢铁内部结构——“改变内部结构”
3.保持表面清洁和干燥
三、废金属的回收利用
1.节约资源
2.保护环境
活学活用1.铝粉漆为什么能防锈?使用前的
一贴热粉末使用后的
一贴热粉末我会做1.在车、船表面刷漆的目的是 ( )
A、增大硬度,防止撞坏 B、防止生锈且美观
C、增大厚度防止磨损 D、改变铁的颜色
2.下列各种情况下,埋在地下的铸铁输气管道被腐蚀
速度最慢的是 ( )
A、在潮湿、疏松、透气的土壤中
B、在呈酸性的潮湿土壤中
C、在干燥、致密、不透气的土壤中
D、在含沙粒较多、潮湿透气的土壤中
3.铝在空气中容易自我保护,写出有关化学方程式:
4Al + 3O2 === 2Al2O3BC我会做4.下列铁制品防锈,适合采用哪一种方法(填序号)。
①锯条;②铁柜;③汽车外壳;④机器上齿轮;
⑤钢制自行车车把
在表面喷涂一层油漆( ) ;在表面涂机油( )
在表面镀其他金属( );
使表面氧化,形成致密的氧化膜 ( )
5.(09福州)人类生活离不开金属。铁是生活中常用
的金属。某“取暖片”中发热剂主要成分有铁粉、活性
炭、氯化钠、水等,其发热是利用铁生锈时会放热 。
①发热剂需接触到空气才会发热,原因是铁要与( ) ( )等物质共同作用才会生锈。
②推测发热剂成分中氯化钠的作用是② ③④⑤ ①氧气水 (加快铁锈蚀放热的速度)我会做 6.小林同学发现铜制眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称铜绿,主要成分是Cu2(OH)2CO3。
[提出问题] 铜是在什么条件下锈蚀的?小林对此进行了探究。
[猜 想] 根据铜锈的化学式,猜想铜生锈可能是铜与 ,
水、 共同作用的结果。
[设计与实验] 借鉴“铁钉锈蚀条件探究”实验,小林设计了“铜片锈蚀条件的探究”实验如右图所示: 氧气二氧化碳我会做(1)实验较长时间后,发现 试管中的光亮铜片最先生锈。
(2)从优化实验的角度,A实验是多余的,他只考虑了水这
个单一条件。C试管中除光亮铜片、蒸馏水外,还有的另
外一种物质为 。
(3)D试管中除光亮铜片外还有的另外两种物质为 ;
从D试管的实验中,获得的结论是 。
[评价与改进] 我认为小林设计的“铜片锈条件的探究”实验不够完
善,要得出正确结论,还要补充的一个实验是(可
图示) 。
[反思与小结] 通过铜片锈蚀条件的探究实验,我获得的启示
是 。
(4)请写出铜在空气中生成铜绿的化学方程式 。BCO2或O2O2和CO2
氧气
酸水
氧气
食盐水
氧气水氧气生锈严重生锈严重生锈基本不变基本不变一周后盐 酸食盐水水蒸馏水干燥剂铁锈疏松多孔,锈“吃”铁铁锈的主要成分是氧化铁栏杆生锈松动 工人失足坠楼 篮球架基生锈倒塌砸到学生 生锈腐蚀易坠落伤人 超龄空调成隐形炸弹汽车生锈危机重重 铁制品生锈造成的危害车身喷涂油漆链条涂防锈油钢圈上镀其他金属隔绝氧气、水等物质用不锈钢代替铁“做表面文章”“改变内部结构”保持表面清洁干燥钢内部添加铬、镍等二、防止铁生锈的方法文具盒钢 尺搪瓷杯回形针三、废金属的回收利用可回收标志1.节约资源
2.保护环境回收废钢铁炼钢 减少冶金渣40%、减少废弃物97%、减少烟灰86%、减轻水污染76%,每生产一吨钢,可以减少投资500-700美元你的收获:一、钢铁制品锈蚀条件的探究
1.铁与氧气、水相互作用而生锈
2.稀酸和食盐溶液能加快铁生锈的速度
二、防止铁制品生锈的方法
1. 覆盖保护层——“做表面文章”
2.改变钢铁内部结构——“改变内部结构”
3.保持表面清洁和干燥
三、废金属的回收利用
1.节约资源
2.保护环境
活学活用1.铝粉漆为什么能防锈?使用前的
一贴热粉末使用后的
一贴热粉末我会做1.在车、船表面刷漆的目的是 ( )
A、增大硬度,防止撞坏 B、防止生锈且美观
C、增大厚度防止磨损 D、改变铁的颜色
2.下列各种情况下,埋在地下的铸铁输气管道被腐蚀
速度最慢的是 ( )
A、在潮湿、疏松、透气的土壤中
B、在呈酸性的潮湿土壤中
C、在干燥、致密、不透气的土壤中
D、在含沙粒较多、潮湿透气的土壤中
3.铝在空气中容易自我保护,写出有关化学方程式:
4Al + 3O2 === 2Al2O3BC我会做4.下列铁制品防锈,适合采用哪一种方法(填序号)。
①锯条;②铁柜;③汽车外壳;④机器上齿轮;
⑤钢制自行车车把
在表面喷涂一层油漆( ) ;在表面涂机油( )
在表面镀其他金属( );
使表面氧化,形成致密的氧化膜 ( )
5.(09福州)人类生活离不开金属。铁是生活中常用
的金属。某“取暖片”中发热剂主要成分有铁粉、活性
炭、氯化钠、水等,其发热是利用铁生锈时会放热 。
①发热剂需接触到空气才会发热,原因是铁要与( ) ( )等物质共同作用才会生锈。
②推测发热剂成分中氯化钠的作用是② ③④⑤ ①氧气水 (加快铁锈蚀放热的速度)我会做 6.小林同学发现铜制眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称铜绿,主要成分是Cu2(OH)2CO3。
[提出问题] 铜是在什么条件下锈蚀的?小林对此进行了探究。
[猜 想] 根据铜锈的化学式,猜想铜生锈可能是铜与 ,
水、 共同作用的结果。
[设计与实验] 借鉴“铁钉锈蚀条件探究”实验,小林设计了“铜片锈蚀条件的探究”实验如右图所示: 氧气二氧化碳我会做(1)实验较长时间后,发现 试管中的光亮铜片最先生锈。
(2)从优化实验的角度,A实验是多余的,他只考虑了水这
个单一条件。C试管中除光亮铜片、蒸馏水外,还有的另
外一种物质为 。
(3)D试管中除光亮铜片外还有的另外两种物质为 ;
从D试管的实验中,获得的结论是 。
[评价与改进] 我认为小林设计的“铜片锈条件的探究”实验不够完
善,要得出正确结论,还要补充的一个实验是(可
图示) 。
[反思与小结] 通过铜片锈蚀条件的探究实验,我获得的启示
是 。
(4)请写出铜在空气中生成铜绿的化学方程式 。BCO2或O2O2和CO2
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
