沪教版九年级上册化学 2.5 基础实验2 二氧化碳的制取与性质 课件(21张PPT)
文档属性
| 名称 | 沪教版九年级上册化学 2.5 基础实验2 二氧化碳的制取与性质 课件(21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 619.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-07-16 00:00:00 | ||
图片预览








文档简介
课件21张PPT。 二氧化碳的实验室制法学习目标:
1、知道气体制取的发生装置及收集装置的选择需考虑的因素,并学会选用制取二氧化碳的仪器
2、了解实验室制二氧化碳的方法、原理、步骤及检验和验满的方法
哪些反应可以产生二氧化碳?生物体的呼吸作用可产生二氧化碳
碳在氧气中燃烧生成二氧化碳;
蜡烛燃烧也可以生成二氧化碳;
铜绿受热分解放出二氧化碳;常温下反应,不消耗能源;装置、操作简单;反应速度适中,便于收集大理石和稀盐酸在常温下反应可产生二氧化碳;
大理石和稀硫酸在常温下反应可产生二氧化碳;
碳酸钠粉末与稀盐酸在常温下反应可产生二氧化碳;
一、实验室制取二氧化碳的化学反应原理1、药品的选择:大理石(石灰石)和稀盐酸探究
实验(太快)(缓慢并逐渐停止)(适中)实验探究:制取二氧化碳最理想的药品!石灰石(主要成分CaCO3)和稀硫酸
碳酸钠粉末和稀盐酸
两者反应生成的硫酸钙是微溶物,覆盖在石灰石表面,阻止反应的进一步进行,产生二氧化碳很少反应速度太快,不利于气体的收集大理石(主要成分CaCO3)和稀盐酸反应速度适中,有利于气体的收集实验室制取二氧化碳的反应原理碳酸钙 + 稀盐酸 → 氯化钙+ 水+二氧化碳CaCO3+HCl → CaCl2+H2O+CO2
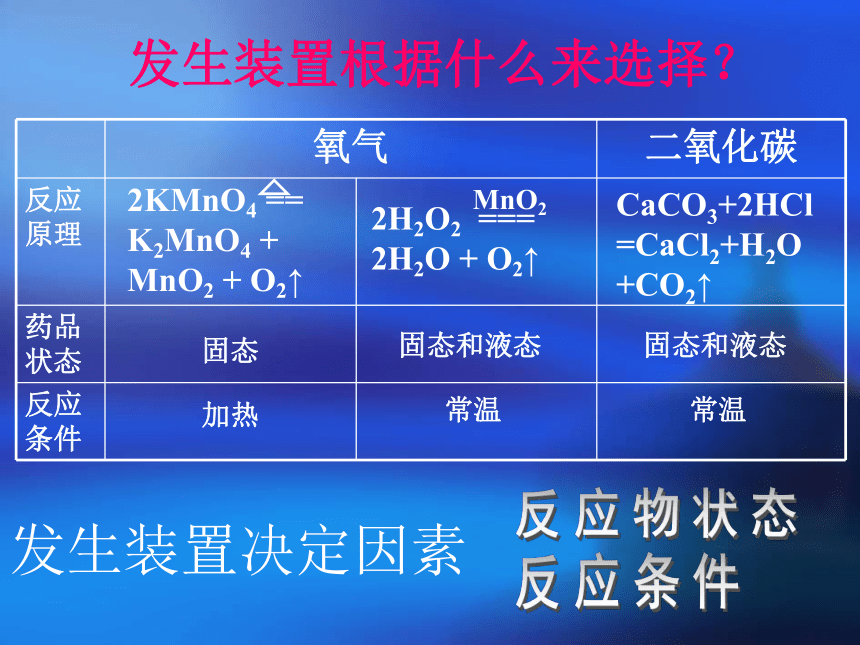
发生装置根据什么来选择?CaCO3+2HCl=CaCl2+H2O+CO2↑ 反应物状态反应条件发生装置决定因素适用于反应物是固体且需加热适用于反应物是(固体+液体)且不需加热实验室制取二氧化碳的装置 发生仪器:
1、长颈漏斗
2、锥形瓶
3、双孔橡皮塞
4、导气管 发生装置(双氧水制取氧气的装置相似)思考:选择收集装置时应以什么为依据?主要应以物理性质两个方面:(1)气体的密度与空气比较(2)气体在水中的溶解性排水法向上排空气法向下排空气法收集方法:向上排空气法(CO2的密度比空气大)不能用排水法(CO2能溶于水且与水发生反应)收集仪器:
1、集气瓶
2、玻璃片实验室里制取二氧化碳的简易装置你能设计出更理想的装置吗?检验方法澄清石灰水
变浑浊验满方法检验和验满放置:盖上玻璃片正放(因为二氧化碳的密度比空气大)实验步骤:检验气密性加入石灰石加入稀盐酸开始反应并收集气体气体的实验室制法要考虑哪些方面?药品选择
反应原理
实验装置
收集方法
检验或验满方法
操作步骤谈一谈:这节课有什么收获?小结:实验室制取二氧化碳1、仪器:锥形瓶(大试管)、长颈漏斗、导气管、集气瓶2、收集方法:向上排空气法3、证明一种无色无味的气体是二氧化碳的方法:加入澄清石灰水变浑浊4、验满方法:燃着木条放在瓶口,熄灭5、CO2暂时存放:正放[练习]1、根据下图所示实验装置进行回答:(1)实验室制取氧气的发生装置可选____,收集装置可选_____;
(2)实验室制取二氧化碳的发生装置可选____,收集装置可选___.
(3)实验室常温可用氧化钙(固)与浓氨水反应制备氨气,已知氨气易溶于水,密度比空气小。则制备氨气的发生装置可选_____收集装置可选_____。A BC、EBCBD2、实验室里制取二氧化碳,应选择的一组药品
是( )
(A)石灰石和稀盐酸 (B)石灰石和浓盐酸
(C) 石灰石和稀硫酸 (D)碳酸钠和稀盐酸 3、可以鉴定一种无色无气味气体是二氧化碳的
方法是( )
(A)用燃着的木条 (B)用澄清的石灰水
(C)可用向上排空气法收集(D)用紫色石蕊试液AB4、长期存放石灰水的试剂瓶壁上有一层白色物
质,这种物质是什么,如何洗去?写出有关的化
学文字表达式。氢氧化钙+二氧化碳 → 碳酸钙+水
1、知道气体制取的发生装置及收集装置的选择需考虑的因素,并学会选用制取二氧化碳的仪器
2、了解实验室制二氧化碳的方法、原理、步骤及检验和验满的方法
哪些反应可以产生二氧化碳?生物体的呼吸作用可产生二氧化碳
碳在氧气中燃烧生成二氧化碳;
蜡烛燃烧也可以生成二氧化碳;
铜绿受热分解放出二氧化碳;常温下反应,不消耗能源;装置、操作简单;反应速度适中,便于收集大理石和稀盐酸在常温下反应可产生二氧化碳;
大理石和稀硫酸在常温下反应可产生二氧化碳;
碳酸钠粉末与稀盐酸在常温下反应可产生二氧化碳;
一、实验室制取二氧化碳的化学反应原理1、药品的选择:大理石(石灰石)和稀盐酸探究
实验(太快)(缓慢并逐渐停止)(适中)实验探究:制取二氧化碳最理想的药品!石灰石(主要成分CaCO3)和稀硫酸
碳酸钠粉末和稀盐酸
两者反应生成的硫酸钙是微溶物,覆盖在石灰石表面,阻止反应的进一步进行,产生二氧化碳很少反应速度太快,不利于气体的收集大理石(主要成分CaCO3)和稀盐酸反应速度适中,有利于气体的收集实验室制取二氧化碳的反应原理碳酸钙 + 稀盐酸 → 氯化钙+ 水+二氧化碳CaCO3+HCl → CaCl2+H2O+CO2
发生装置根据什么来选择?CaCO3+2HCl=CaCl2+H2O+CO2↑ 反应物状态反应条件发生装置决定因素适用于反应物是固体且需加热适用于反应物是(固体+液体)且不需加热实验室制取二氧化碳的装置 发生仪器:
1、长颈漏斗
2、锥形瓶
3、双孔橡皮塞
4、导气管 发生装置(双氧水制取氧气的装置相似)思考:选择收集装置时应以什么为依据?主要应以物理性质两个方面:(1)气体的密度与空气比较(2)气体在水中的溶解性排水法向上排空气法向下排空气法收集方法:向上排空气法(CO2的密度比空气大)不能用排水法(CO2能溶于水且与水发生反应)收集仪器:
1、集气瓶
2、玻璃片实验室里制取二氧化碳的简易装置你能设计出更理想的装置吗?检验方法澄清石灰水
变浑浊验满方法检验和验满放置:盖上玻璃片正放(因为二氧化碳的密度比空气大)实验步骤:检验气密性加入石灰石加入稀盐酸开始反应并收集气体气体的实验室制法要考虑哪些方面?药品选择
反应原理
实验装置
收集方法
检验或验满方法
操作步骤谈一谈:这节课有什么收获?小结:实验室制取二氧化碳1、仪器:锥形瓶(大试管)、长颈漏斗、导气管、集气瓶2、收集方法:向上排空气法3、证明一种无色无味的气体是二氧化碳的方法:加入澄清石灰水变浑浊4、验满方法:燃着木条放在瓶口,熄灭5、CO2暂时存放:正放[练习]1、根据下图所示实验装置进行回答:(1)实验室制取氧气的发生装置可选____,收集装置可选_____;
(2)实验室制取二氧化碳的发生装置可选____,收集装置可选___.
(3)实验室常温可用氧化钙(固)与浓氨水反应制备氨气,已知氨气易溶于水,密度比空气小。则制备氨气的发生装置可选_____收集装置可选_____。A BC、EBCBD2、实验室里制取二氧化碳,应选择的一组药品
是( )
(A)石灰石和稀盐酸 (B)石灰石和浓盐酸
(C) 石灰石和稀硫酸 (D)碳酸钠和稀盐酸 3、可以鉴定一种无色无气味气体是二氧化碳的
方法是( )
(A)用燃着的木条 (B)用澄清的石灰水
(C)可用向上排空气法收集(D)用紫色石蕊试液AB4、长期存放石灰水的试剂瓶壁上有一层白色物
质,这种物质是什么,如何洗去?写出有关的化
学文字表达式。氢氧化钙+二氧化碳 → 碳酸钙+水
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
