4.3 水的组成 教案
图片预览


文档简介
课题3 水的组成
1.能根据水的电解实验知道水的组成。(重点)
2.从组成的不同记住化合物和单质的区别。(难点)
3.了解人类认识物质世界的过程和方法。
【课前预习】
1.你知道水与人的生理、生活和人类生产活动的关系吗?
2.水的物理性质
3.水既普通又宝贵。那么你知道,水究竟是由什么组成的?
【情境导入】通过分组展示对“水既普通又宝贵。那么你知道,水究竟是由什么组成的?”的问题的认识引入新课
知识点1:水的组成
【猜想】
【设计实验】
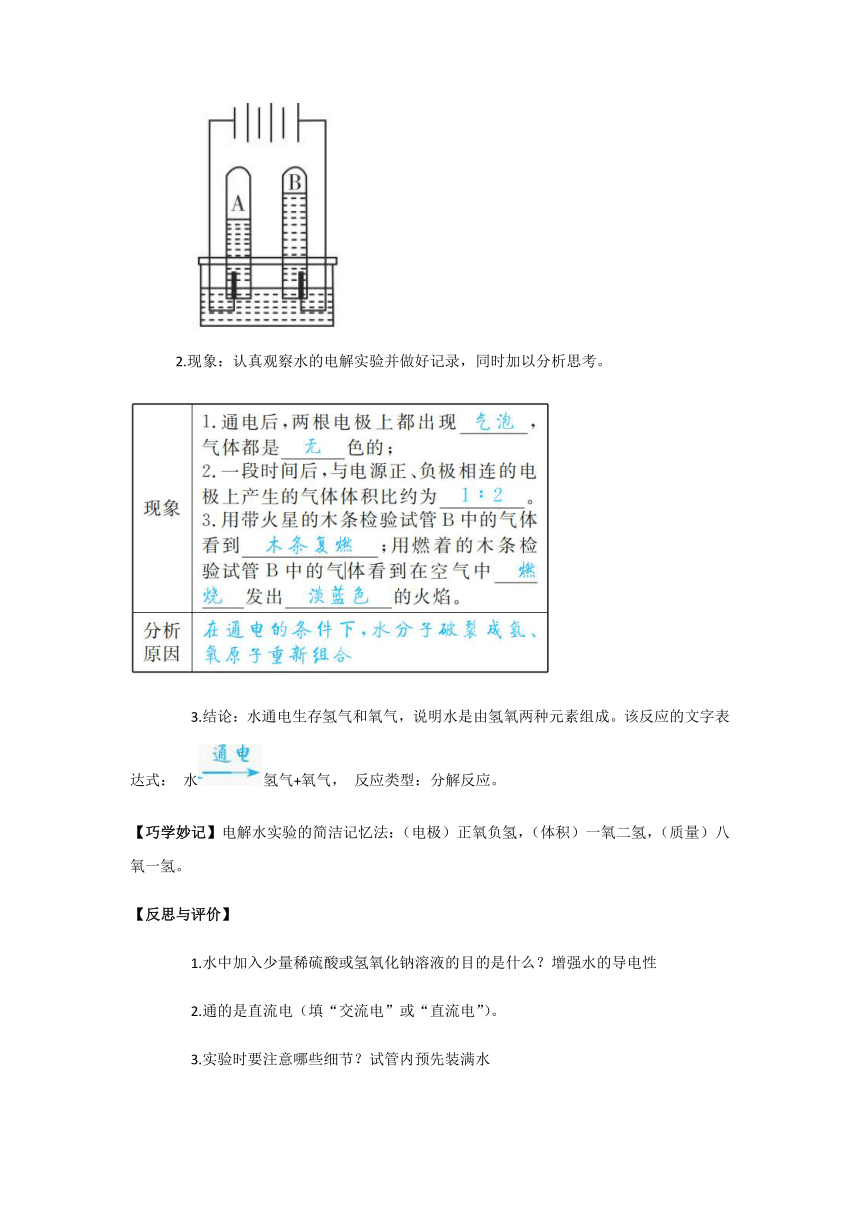
1.装置:如图所示
2.现象:认真观察水的电解实验并做好记录,同时加以分析思考。
3.结论:水通电生存氢气和氧气,说明水是由氢氧两种元素组成。该反应的文字表达式: 水氢气+氧气, 反应类型:分解反应。
【巧学妙记】电解水实验的简洁记忆法:(电极)正氧负氢,(体积)一氧二氢,(质量)八氧一氢。
【反思与评价】
1.水中加入少量稀硫酸或氢氧化钠溶液的目的是什么?增强水的导电性
2.通的是直流电(填“交流电”或“直流电”)。
3.实验时要注意哪些细节?试管内预先装满水
【交流讨论】
1.水的电解实验里,有新物质生成吗?水发生了什么变化?说明水的组成是怎样的?
2.实验操作中试管A、B两试管的气体体积比常大于2∶1原因可能是有部分氧气溶于水
3.从电解水的实验中可见氢气是一种无色的气体,试管A内既有氢气又有水而氢气的体积没有减少,可见氢气是难溶于水水的气体;氢气在空气中燃烧发出淡蓝色的火焰,说明氢气具有可燃性。
4.氢气点燃前一定要验纯,点燃可燃性气体都要验纯。
5.水的沸腾过程与水的分解过程有什么不同?一个是物理变化,一个是化学变化。
6.有人说水可以开发成能源,你是怎样想的?
知识点2:化合物、氧化物、单质
【交流讨论】
1.从上面的实验和发生的化学反应可见,水是由氢(H)、氧(O)两种元素组成。那么二氧化碳(CO2)、高锰酸钾(KMnO4)、五氧化二磷(P2O5)、氢气(H2)、氧化铁(Fe2O3)、氮气(N2)和氧气(O2)分别由几种元素组成的?
2.根据各物质的组成元素特点,把上述物质中的氢气、氮气和氧气等称之为单质;水、二氧化碳、高锰酸钾、五氧化二磷、氧化铁等称之为化合物。试问:什么叫单质?什么叫化合物?
3.上述化合物中二氧化碳(CO2)、五氧化二磷(P2O5)、氧化铁(Fe2O3)又称之为氧化物。试问:它们有又什么共同特点?高锰酸钾(KMnO4)属于氧化物吗?
【阅读】阅读教材P81页内容和“资料”。
1.列表比较化合物和单质:
2.氧化物:由两种元素组成的化合物中,其中一种元素是氧元素。
【思考】
1.由同种元素能否组成混合物?
2.含氧化合物与氧化物有什么区别?
含氧化合物是含有氧元素的化合物,是由两种或两种以上的元素组成的纯净物。如:KClO3、MnO2 等。
教师点拨
氧化物是只含有两种元素的化合物,其中一种元素是氧元素。如:MnO2、CO2、SO2、P2O5等。
【知识归纳】
1.物质的简单分类
2.掌握单质、化合物、氧化物、纯净物、混合物的定义
3.完成下表
【课堂练习】
1.下列有关电解水的说法错误的是(A)
A.水是由氢气和氧气组成的
B.水是由氢元素和氧元素组成
C.自然界中的水大多是混合物
D.水中加入硫酸是为增加导电性
2.下列各组物质中,前者是化合物,后者是单质的是(A)
A.高锰酸钾、氮气
B.洁净的空气、氧气
C.铝、二氧化碳
D.硫粉、氧化镁
3.将下列物质分别按照混合物、纯净物、单质、化合物、氧化物等分类:①空气、②氮气、③水蒸气、④氧化铁、⑤红磷、⑥二氧化锰、⑦氯酸钾、⑧稀有气体,并填充到图中。
4.18世纪末,英国科学家普利斯特里把“易燃空气”(实际为氢气)和空气混合后盛在干燥的玻璃瓶中,点火时混合气体发生爆炸,且玻璃瓶内壁上出现了晶莹的水珠。请写出这一变化的文字表达式氢气+氧气点燃水 ,此反应属于化合(分解反应或化合反应)。
5.用混合物、纯净物、单质、化合物等概念填空。
(1)氧气既属于单质,又属于纯净物。
(2)二氧化锰既属于化合物,又属于纯净物。
本课题通过氢气燃烧生成水和水电解生成氢气及氧气的两个化学实验探究了水的组成,并从微观角度分析了化学反应的实质,使学生能较直观的认识研究物质组成的一般方法和过程,并在此基础上进一步认识了物质的分类。整节课体现了由简单到复杂、由具体到抽象的教学理念,但由于学生对化合物与混合物两个概念的理解不透彻,易混淆,因此在今后的教学过程中应加强训练,使学生明白元素与物质的联系和区别。
1.能根据水的电解实验知道水的组成。(重点)
2.从组成的不同记住化合物和单质的区别。(难点)
3.了解人类认识物质世界的过程和方法。
【课前预习】
1.你知道水与人的生理、生活和人类生产活动的关系吗?
2.水的物理性质
3.水既普通又宝贵。那么你知道,水究竟是由什么组成的?
【情境导入】通过分组展示对“水既普通又宝贵。那么你知道,水究竟是由什么组成的?”的问题的认识引入新课
知识点1:水的组成
【猜想】
【设计实验】
1.装置:如图所示
2.现象:认真观察水的电解实验并做好记录,同时加以分析思考。
3.结论:水通电生存氢气和氧气,说明水是由氢氧两种元素组成。该反应的文字表达式: 水氢气+氧气, 反应类型:分解反应。
【巧学妙记】电解水实验的简洁记忆法:(电极)正氧负氢,(体积)一氧二氢,(质量)八氧一氢。
【反思与评价】
1.水中加入少量稀硫酸或氢氧化钠溶液的目的是什么?增强水的导电性
2.通的是直流电(填“交流电”或“直流电”)。
3.实验时要注意哪些细节?试管内预先装满水
【交流讨论】
1.水的电解实验里,有新物质生成吗?水发生了什么变化?说明水的组成是怎样的?
2.实验操作中试管A、B两试管的气体体积比常大于2∶1原因可能是有部分氧气溶于水
3.从电解水的实验中可见氢气是一种无色的气体,试管A内既有氢气又有水而氢气的体积没有减少,可见氢气是难溶于水水的气体;氢气在空气中燃烧发出淡蓝色的火焰,说明氢气具有可燃性。
4.氢气点燃前一定要验纯,点燃可燃性气体都要验纯。
5.水的沸腾过程与水的分解过程有什么不同?一个是物理变化,一个是化学变化。
6.有人说水可以开发成能源,你是怎样想的?
知识点2:化合物、氧化物、单质
【交流讨论】
1.从上面的实验和发生的化学反应可见,水是由氢(H)、氧(O)两种元素组成。那么二氧化碳(CO2)、高锰酸钾(KMnO4)、五氧化二磷(P2O5)、氢气(H2)、氧化铁(Fe2O3)、氮气(N2)和氧气(O2)分别由几种元素组成的?
2.根据各物质的组成元素特点,把上述物质中的氢气、氮气和氧气等称之为单质;水、二氧化碳、高锰酸钾、五氧化二磷、氧化铁等称之为化合物。试问:什么叫单质?什么叫化合物?
3.上述化合物中二氧化碳(CO2)、五氧化二磷(P2O5)、氧化铁(Fe2O3)又称之为氧化物。试问:它们有又什么共同特点?高锰酸钾(KMnO4)属于氧化物吗?
【阅读】阅读教材P81页内容和“资料”。
1.列表比较化合物和单质:
2.氧化物:由两种元素组成的化合物中,其中一种元素是氧元素。
【思考】
1.由同种元素能否组成混合物?
2.含氧化合物与氧化物有什么区别?
含氧化合物是含有氧元素的化合物,是由两种或两种以上的元素组成的纯净物。如:KClO3、MnO2 等。
教师点拨
氧化物是只含有两种元素的化合物,其中一种元素是氧元素。如:MnO2、CO2、SO2、P2O5等。
【知识归纳】
1.物质的简单分类
2.掌握单质、化合物、氧化物、纯净物、混合物的定义
3.完成下表
【课堂练习】
1.下列有关电解水的说法错误的是(A)
A.水是由氢气和氧气组成的
B.水是由氢元素和氧元素组成
C.自然界中的水大多是混合物
D.水中加入硫酸是为增加导电性
2.下列各组物质中,前者是化合物,后者是单质的是(A)
A.高锰酸钾、氮气
B.洁净的空气、氧气
C.铝、二氧化碳
D.硫粉、氧化镁
3.将下列物质分别按照混合物、纯净物、单质、化合物、氧化物等分类:①空气、②氮气、③水蒸气、④氧化铁、⑤红磷、⑥二氧化锰、⑦氯酸钾、⑧稀有气体,并填充到图中。
4.18世纪末,英国科学家普利斯特里把“易燃空气”(实际为氢气)和空气混合后盛在干燥的玻璃瓶中,点火时混合气体发生爆炸,且玻璃瓶内壁上出现了晶莹的水珠。请写出这一变化的文字表达式氢气+氧气点燃水 ,此反应属于化合(分解反应或化合反应)。
5.用混合物、纯净物、单质、化合物等概念填空。
(1)氧气既属于单质,又属于纯净物。
(2)二氧化锰既属于化合物,又属于纯净物。
本课题通过氢气燃烧生成水和水电解生成氢气及氧气的两个化学实验探究了水的组成,并从微观角度分析了化学反应的实质,使学生能较直观的认识研究物质组成的一般方法和过程,并在此基础上进一步认识了物质的分类。整节课体现了由简单到复杂、由具体到抽象的教学理念,但由于学生对化合物与混合物两个概念的理解不透彻,易混淆,因此在今后的教学过程中应加强训练,使学生明白元素与物质的联系和区别。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
