沪教版九年级上册化学 3.1.2 原子 课件(26张PPT)
文档属性
| 名称 | 沪教版九年级上册化学 3.1.2 原子 课件(26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 164.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-07-20 00:00:00 | ||
图片预览





文档简介
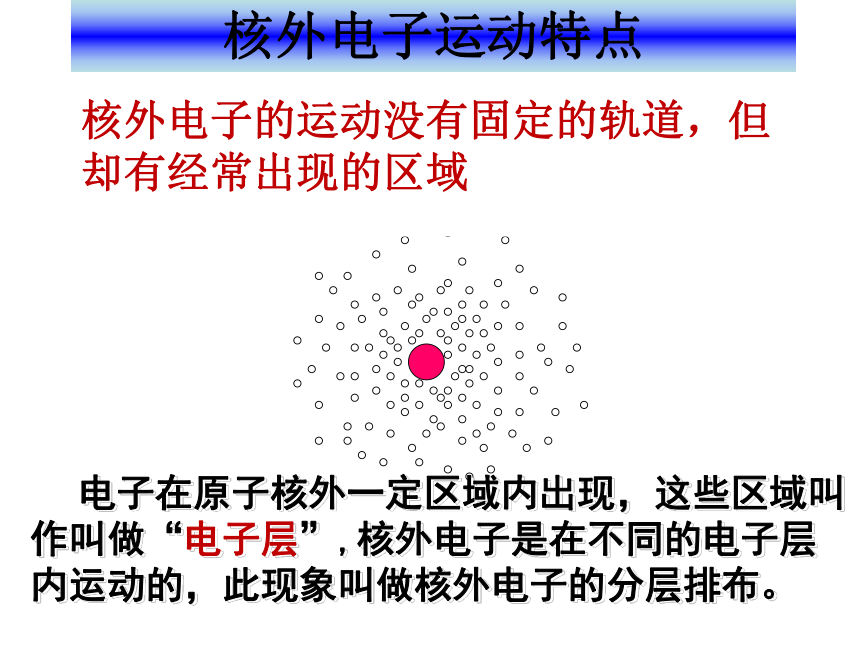
课件26张PPT。原子的结构 离子一、原子的结构核外电子运动特点核外电子的运动没有固定的轨道,但却有经常出现的区域
电子在原子核外一定区域内出现,这些区域叫作叫做“电子层”,核外电子是在不同的电子层内运动的,此现象叫做核外电子的分层排布。核外电子运动特点核外电子的运动没有固定的轨道,但却有经常出现的区域
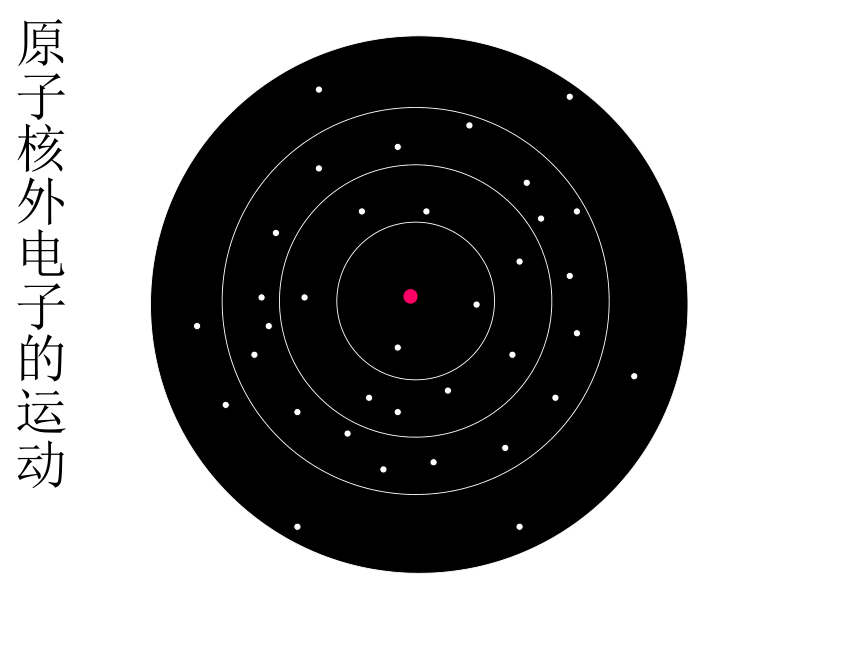
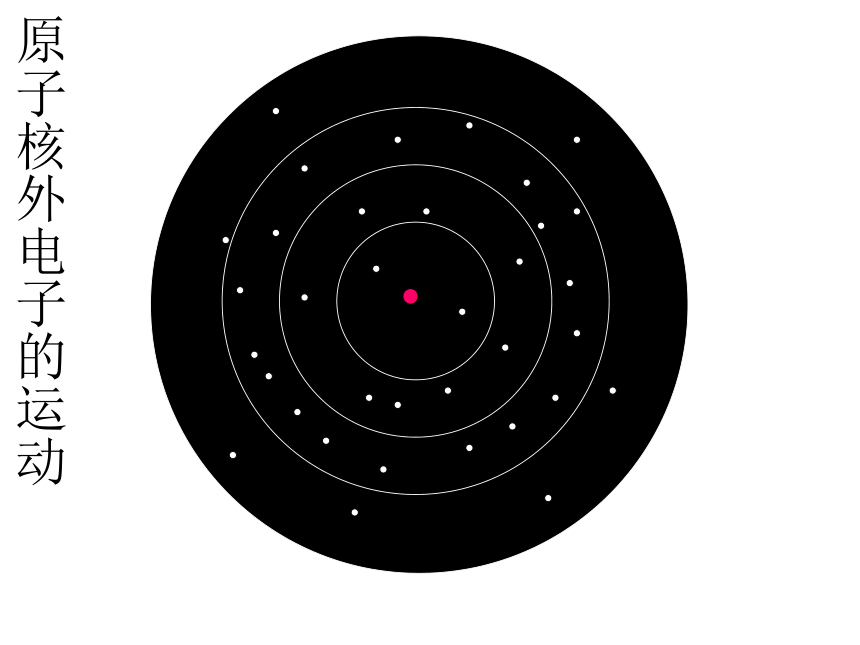
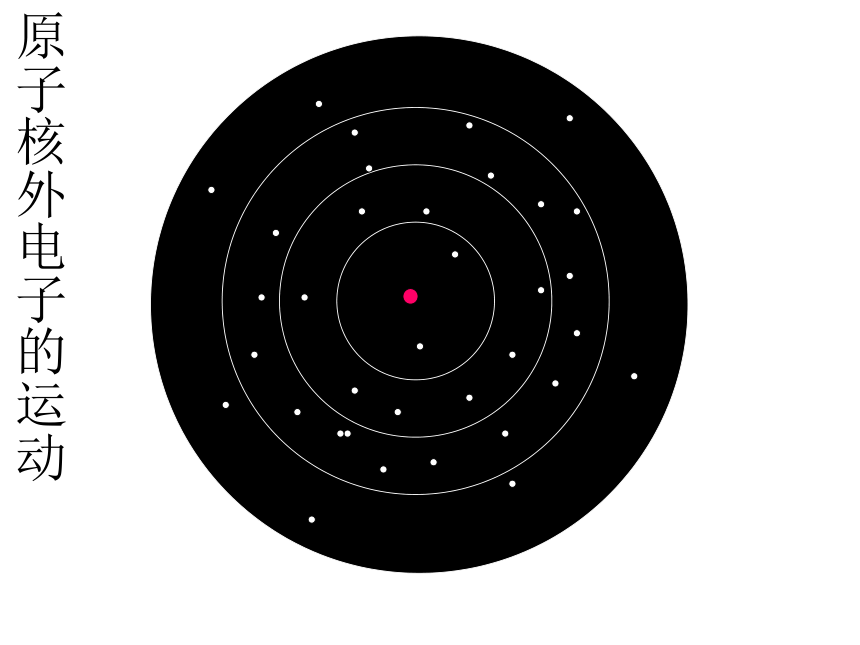
原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动核外电子排布规则原子结构示意图画出氦、氖、氩、钠、镁、铝、氮、氟、硫的原子结构示意图都为 8
(氦为2)稳定一般
少于4不稳定一般
大于4不稳定原子最外层电子数与化学性质的关系密切+11-----------+17-----------------钠原子氯原子质子数=电子数=11质子数=电子数=17不带电不带电NaCl+11+17-----------------钠原子氯原子+17-----------------钠原子氯原子-----------+17-----------------钠原子氯原子+17------------------钠原子氯原子我稳定了我也稳定了,谢谢!钠离子氯离子质子数= 电子数=质子数= 电子数=11101718><带一个单位正电荷带一个单位负电荷Na+Cl-NaCl相互作用形成化合物都为 8
(氦为2)不易
得失稳定一般
少于4易失去不稳定不少于4易得到不稳定原子最外层电子数的关系密切。原子最外层电子数与化学性质的关系密切二、离子的形成1、离子原子得到或失去电子后形成的带电的微粒2、离子分类 阴离子
阳离子3、离子的表示——离子符号(电子数>质子数)(电子数<质子数)Xn±元素符号离子所带电荷数(得失电子数;当n=1时略去不写 )离子带正或负电分子、原子、离子之间的区别和联系分子原子离子
电子在原子核外一定区域内出现,这些区域叫作叫做“电子层”,核外电子是在不同的电子层内运动的,此现象叫做核外电子的分层排布。核外电子运动特点核外电子的运动没有固定的轨道,但却有经常出现的区域
原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动与排布原子核外电子的运动原子核外电子的运动核外电子排布规则原子结构示意图画出氦、氖、氩、钠、镁、铝、氮、氟、硫的原子结构示意图都为 8
(氦为2)稳定一般
少于4不稳定一般
大于4不稳定原子最外层电子数与化学性质的关系密切+11-----------+17-----------------钠原子氯原子质子数=电子数=11质子数=电子数=17不带电不带电NaCl+11+17-----------------钠原子氯原子+17-----------------钠原子氯原子-----------+17-----------------钠原子氯原子+17------------------钠原子氯原子我稳定了我也稳定了,谢谢!钠离子氯离子质子数= 电子数=质子数= 电子数=11101718><带一个单位正电荷带一个单位负电荷Na+Cl-NaCl相互作用形成化合物都为 8
(氦为2)不易
得失稳定一般
少于4易失去不稳定不少于4易得到不稳定原子最外层电子数的关系密切。原子最外层电子数与化学性质的关系密切二、离子的形成1、离子原子得到或失去电子后形成的带电的微粒2、离子分类 阴离子
阳离子3、离子的表示——离子符号(电子数>质子数)(电子数<质子数)Xn±元素符号离子所带电荷数(得失电子数;当n=1时略去不写 )离子带正或负电分子、原子、离子之间的区别和联系分子原子离子
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
