1.6 几种重要的盐(1) 练习
图片预览

文档简介
1.6几种重要的盐(1)
1.近来市场上出现了能补充人体盐分的饮品——盐汽水,你认为盐汽水的成分和普通汽水最大的不同是增加了( )
A.水 B.氯化钠 C.二氧化碳 D.碳酸钙
2.下列有关常见的盐的说法,错误的是( )
A.Na2CO3的俗名叫烧碱 B.CaCO3是大理石的主要成分
C.NaCl通常从海水中提取 D.NaHCO3用于治疗胃酸过多
3.某碳酸钠溶液的pH约为12,分别加入下列试剂,溶液仍然是无色透明的是( )
A.氢氧化钾溶液 B.氯化钙溶液 C.紫色石蕊试液 D.无色酚酞试液
4.碳酸钠俗称“纯碱”.有关它的表述不正确的是( )
A.“纯碱”其实不是碱,它属于盐类 B.可用纯碱代替洗涤灵洗涤餐具表面的油污
C.用纯碱可除去面团发酵产生的酸 D.“冬天捞碱”可说明纯碱的溶解度随温度的变化不大
5.罐头食品能保存较长时间,其原因是( )
A.因为罐头密封,缺氧,细菌、真菌不能繁殖
B.因为罐头内食品已经杀死了细菌、真菌,食品中无菌,外面的细菌、真菌又进不去
C.罐头食品内一定加了防腐剂
D.罐头食品内水分太多,不适宜细菌、真菌的繁殖
6.以下是关于食盐性质的叙述:①易容于水;②其溶液能与稀硫酸反应;③其溶液能与氢氧化钾溶液反应;④其溶液能与硝酸银溶液反应⑤其溶液能与锌反应。其中正确的是( )
A.①④ B.②③ C.②⑤ D.②③⑤
7.如果蔬菜上洒了农药,用碱性溶液或水浸泡,可使残留在蔬菜上的农药毒性降低,因此,买来的蔬菜在食用前最好用稀碱水或清水浸泡一段时间。浸泡蔬菜时可加入适量( )
A.食醋 B.白酒 C.白糖 D.纯碱
8.一天,小影惊奇的发现妈妈蒸馒头时用的不是纯碱,而是小苏打,她好奇的问:“为什么不用纯碱而用小苏打?”妈妈说“面团没发酵,不能用纯碱”。通过查阅资料小影发现小苏打的化学式为NaHCO3,是一种常用的膨松剂,加热可转化为纯碱。下列小影相关的推断不合理的是( )
A.小苏打是膨松剂是因为能产生二氧化碳气体 B.小苏打受热转化为纯碱是分解反应
C.小苏打属于酸 D.小苏打对人体无害
二、填空、实验题
9.测得某溶液中仅含有Na+、Mg2+、Cl?四种离子(不考虑水的电离),其中离子个数比为Na+:Mg2+:Cl?=4:5:8,若设Na+为4n个,则的离子数为 。
10.硝酸银通常贮存在棕色试剂瓶中,它可以发生如下反应:2AgNO32Ag +2□↑+O2↑,据此请你完成下列各题:
(1)□中物质的化学式是 ;
(2)硝酸银通常贮存在棕色试剂瓶中的原因是 。
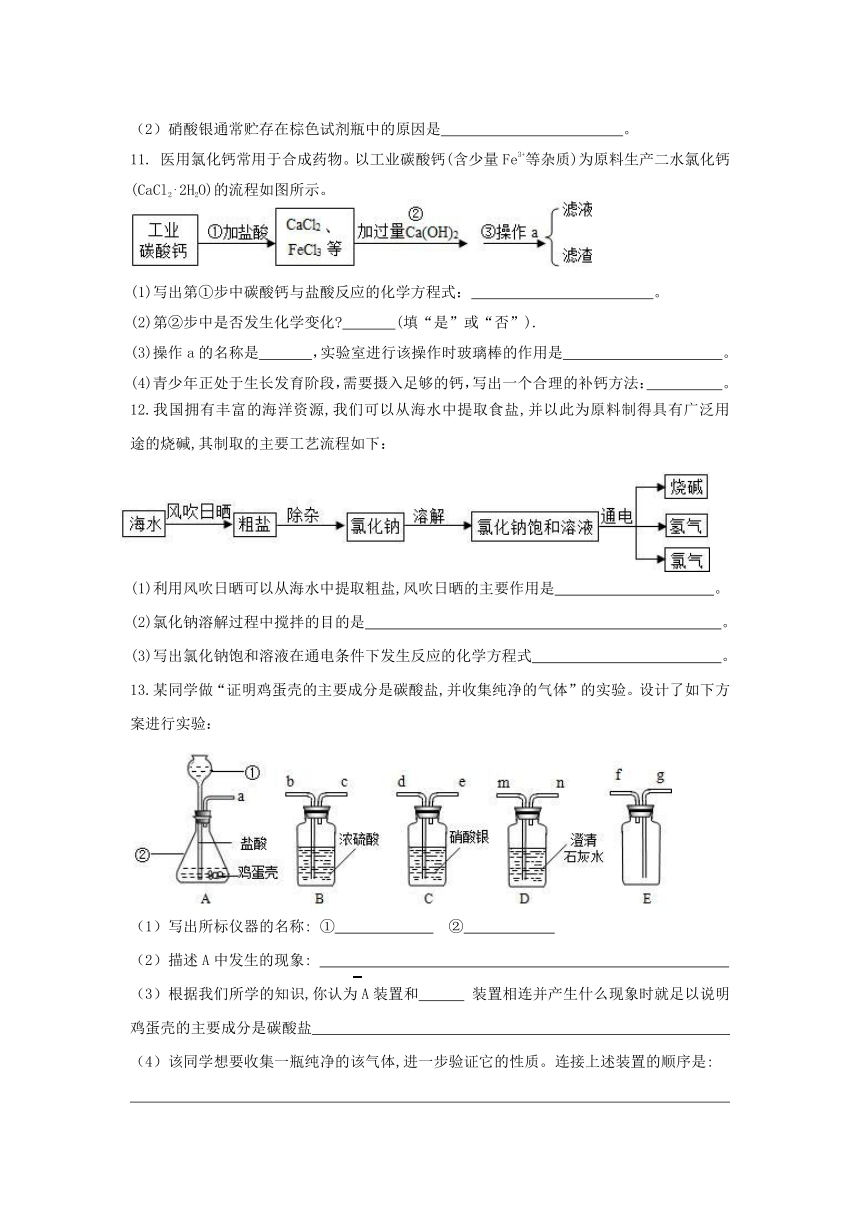
11. 医用氯化钙常用于合成药物。以工业碳酸钙(含少量Fe3+等杂质)为原料生产二水氯化钙(CaCl2?2H2O)的流程如图所示。
(1)写出第①步中碳酸钙与盐酸反应的化学方程式: 。
(2)第②步中是否发生化学变化? (填“是”或“否”).
(3)操作a的名称是 ,实验室进行该操作时玻璃棒的作用是 。
(4)青少年正处于生长发育阶段,需要摄入足够的钙,写出一个合理的补钙方法: 。
12.我国拥有丰富的海洋资源,我们可以从海水中提取食盐,并以此为原料制得具有广泛用 途的烧碱,其制取的主要工艺流程如下:
(1)利用风吹日晒可以从海水中提取粗盐,风吹日晒的主要作用是 。
(2)氯化钠溶解过程中搅拌的目的是 。
(3)写出氯化钠饱和溶液在通电条件下发生反应的化学方程式 。
13.某同学做“证明鸡蛋壳的主要成分是碳酸盐,并收集纯净的气体”的实验。设计了如下方案进行实验:
(1)写出所标仪器的名称: ① ②
(2)描述A中发生的现象:
(3)根据我们所学的知识,你认为A装置和 装置相连并产生什么现象时就足以说明鸡蛋壳的主要成分是碳酸盐
(4)该同学想要收集一瓶纯净的该气体,进一步验证它的性质。连接上述装置的顺序是:
(填写各接口字母) 。 其中,C装置的作用是: 写出有关反应的化学方程式:
(5)写出用A装置还可以制取的日常生活中一种常见气体的化学反应方程式: ,并说出它的一个重要用途 。
14.同学们对实验“煅烧石灰石”展开深入探究。
(1)煅烧石灰石。可观察到石灰石的表面
(2)为证明石灰石已分解,三位同学从其他角度设计方案如下:
①甲同学按图一所示进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式 。
②乙同学按图二所示进行试验,观察到B中液体变 色,A中实验的作用 。
③丙同学取一块石灰石进行煅烧,一段时间后发现固体质量减轻mg(即CO2的质量),证明石灰石已分解。
④大家认为甲同学的方案不合理,请分析原因 。
15. 某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红。碱溶液可以使酚酞溶液变红,是因为碱在水溶液中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞溶液变红呢?他们设计了下图3个实验,请你和他们一起探究。
(1)实验Ⅰ可以证明 。
(2)实验Ⅱ加入蒸馏水的目的是 。
小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是 。
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞溶液变红,向变红后的溶液中再逐渐滴入过量的
CaCl2溶液,红色逐渐消失,同时还观察到产生 现象。由实验Ⅰ、Ⅱ、Ⅲ得出结论:CO32-可以使酚酞溶液变红。
(4)小组同学在与老师交流上述结论时,老师说:“其实Na2CO3溶液能使酚酞溶液变红
也是由于溶液中存在OH-”你认为Na2CO3溶液存在OH-的原因是 。
参考答案
1.B
2.A
3.A
4.D
5.B
6.A
7.D
8.C
9.3
10.(1)NO2?;(2)因为硝酸银见光会分解,装在棕色瓶中可以避光
11.(1) CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)是;(3)过滤;引流;(4)多吃富含钙的食物。
12.(1)促进海水蒸发(2)促进氯化钠溶解(3)2NaCl+2H2O2NaOH+H2↑+Cl2↑
13.(1)长颈漏斗;锥形瓶(2)鸡蛋壳浮在液面上,表面有气泡产生,并渐渐溶解
(3)D;D装置中澄清石灰水变浑浊;Ca(OH)2+CO2=CaCO3↓+H2O
(4)a接d,e接b,c接g;除CO2中混有的HCl气体;AgNO3+HCl=AgCl↓+HNO3
(5)2H2022H2O+O2↑;供给呼吸
14.(1)有气泡产生;
(2)①Ca(OH)2+CO2=CaCO3↓+ H2O;②红;对照试验;④煤气灯中的一氧化碳燃烧会产生二氧化碳,因此使石灰水变浑浊的二氧化碳不一定是碳酸钙分解产生的;
15.(1)Na+ 不会使酚酞溶液变红
(2)探究水分子是否能使酚酞溶液变红;氯化钠溶液中含有水分子(或酚酞溶液中就有水分子)
(3)白色沉淀
(4)Na2CO3与H2O发生反应,使溶液中产生了OH -(合理即可)
1.近来市场上出现了能补充人体盐分的饮品——盐汽水,你认为盐汽水的成分和普通汽水最大的不同是增加了( )
A.水 B.氯化钠 C.二氧化碳 D.碳酸钙
2.下列有关常见的盐的说法,错误的是( )
A.Na2CO3的俗名叫烧碱 B.CaCO3是大理石的主要成分
C.NaCl通常从海水中提取 D.NaHCO3用于治疗胃酸过多
3.某碳酸钠溶液的pH约为12,分别加入下列试剂,溶液仍然是无色透明的是( )
A.氢氧化钾溶液 B.氯化钙溶液 C.紫色石蕊试液 D.无色酚酞试液
4.碳酸钠俗称“纯碱”.有关它的表述不正确的是( )
A.“纯碱”其实不是碱,它属于盐类 B.可用纯碱代替洗涤灵洗涤餐具表面的油污
C.用纯碱可除去面团发酵产生的酸 D.“冬天捞碱”可说明纯碱的溶解度随温度的变化不大
5.罐头食品能保存较长时间,其原因是( )
A.因为罐头密封,缺氧,细菌、真菌不能繁殖
B.因为罐头内食品已经杀死了细菌、真菌,食品中无菌,外面的细菌、真菌又进不去
C.罐头食品内一定加了防腐剂
D.罐头食品内水分太多,不适宜细菌、真菌的繁殖
6.以下是关于食盐性质的叙述:①易容于水;②其溶液能与稀硫酸反应;③其溶液能与氢氧化钾溶液反应;④其溶液能与硝酸银溶液反应⑤其溶液能与锌反应。其中正确的是( )
A.①④ B.②③ C.②⑤ D.②③⑤
7.如果蔬菜上洒了农药,用碱性溶液或水浸泡,可使残留在蔬菜上的农药毒性降低,因此,买来的蔬菜在食用前最好用稀碱水或清水浸泡一段时间。浸泡蔬菜时可加入适量( )
A.食醋 B.白酒 C.白糖 D.纯碱
8.一天,小影惊奇的发现妈妈蒸馒头时用的不是纯碱,而是小苏打,她好奇的问:“为什么不用纯碱而用小苏打?”妈妈说“面团没发酵,不能用纯碱”。通过查阅资料小影发现小苏打的化学式为NaHCO3,是一种常用的膨松剂,加热可转化为纯碱。下列小影相关的推断不合理的是( )
A.小苏打是膨松剂是因为能产生二氧化碳气体 B.小苏打受热转化为纯碱是分解反应
C.小苏打属于酸 D.小苏打对人体无害
二、填空、实验题
9.测得某溶液中仅含有Na+、Mg2+、Cl?四种离子(不考虑水的电离),其中离子个数比为Na+:Mg2+:Cl?=4:5:8,若设Na+为4n个,则的离子数为 。
10.硝酸银通常贮存在棕色试剂瓶中,它可以发生如下反应:2AgNO32Ag +2□↑+O2↑,据此请你完成下列各题:
(1)□中物质的化学式是 ;
(2)硝酸银通常贮存在棕色试剂瓶中的原因是 。
11. 医用氯化钙常用于合成药物。以工业碳酸钙(含少量Fe3+等杂质)为原料生产二水氯化钙(CaCl2?2H2O)的流程如图所示。
(1)写出第①步中碳酸钙与盐酸反应的化学方程式: 。
(2)第②步中是否发生化学变化? (填“是”或“否”).
(3)操作a的名称是 ,实验室进行该操作时玻璃棒的作用是 。
(4)青少年正处于生长发育阶段,需要摄入足够的钙,写出一个合理的补钙方法: 。
12.我国拥有丰富的海洋资源,我们可以从海水中提取食盐,并以此为原料制得具有广泛用 途的烧碱,其制取的主要工艺流程如下:
(1)利用风吹日晒可以从海水中提取粗盐,风吹日晒的主要作用是 。
(2)氯化钠溶解过程中搅拌的目的是 。
(3)写出氯化钠饱和溶液在通电条件下发生反应的化学方程式 。
13.某同学做“证明鸡蛋壳的主要成分是碳酸盐,并收集纯净的气体”的实验。设计了如下方案进行实验:
(1)写出所标仪器的名称: ① ②
(2)描述A中发生的现象:
(3)根据我们所学的知识,你认为A装置和 装置相连并产生什么现象时就足以说明鸡蛋壳的主要成分是碳酸盐
(4)该同学想要收集一瓶纯净的该气体,进一步验证它的性质。连接上述装置的顺序是:
(填写各接口字母) 。 其中,C装置的作用是: 写出有关反应的化学方程式:
(5)写出用A装置还可以制取的日常生活中一种常见气体的化学反应方程式: ,并说出它的一个重要用途 。
14.同学们对实验“煅烧石灰石”展开深入探究。
(1)煅烧石灰石。可观察到石灰石的表面
(2)为证明石灰石已分解,三位同学从其他角度设计方案如下:
①甲同学按图一所示进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式 。
②乙同学按图二所示进行试验,观察到B中液体变 色,A中实验的作用 。
③丙同学取一块石灰石进行煅烧,一段时间后发现固体质量减轻mg(即CO2的质量),证明石灰石已分解。
④大家认为甲同学的方案不合理,请分析原因 。
15. 某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红。碱溶液可以使酚酞溶液变红,是因为碱在水溶液中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞溶液变红呢?他们设计了下图3个实验,请你和他们一起探究。
(1)实验Ⅰ可以证明 。
(2)实验Ⅱ加入蒸馏水的目的是 。
小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是 。
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞溶液变红,向变红后的溶液中再逐渐滴入过量的
CaCl2溶液,红色逐渐消失,同时还观察到产生 现象。由实验Ⅰ、Ⅱ、Ⅲ得出结论:CO32-可以使酚酞溶液变红。
(4)小组同学在与老师交流上述结论时,老师说:“其实Na2CO3溶液能使酚酞溶液变红
也是由于溶液中存在OH-”你认为Na2CO3溶液存在OH-的原因是 。
参考答案
1.B
2.A
3.A
4.D
5.B
6.A
7.D
8.C
9.3
10.(1)NO2?;(2)因为硝酸银见光会分解,装在棕色瓶中可以避光
11.(1) CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)是;(3)过滤;引流;(4)多吃富含钙的食物。
12.(1)促进海水蒸发(2)促进氯化钠溶解(3)2NaCl+2H2O2NaOH+H2↑+Cl2↑
13.(1)长颈漏斗;锥形瓶(2)鸡蛋壳浮在液面上,表面有气泡产生,并渐渐溶解
(3)D;D装置中澄清石灰水变浑浊;Ca(OH)2+CO2=CaCO3↓+H2O
(4)a接d,e接b,c接g;除CO2中混有的HCl气体;AgNO3+HCl=AgCl↓+HNO3
(5)2H2022H2O+O2↑;供给呼吸
14.(1)有气泡产生;
(2)①Ca(OH)2+CO2=CaCO3↓+ H2O;②红;对照试验;④煤气灯中的一氧化碳燃烧会产生二氧化碳,因此使石灰水变浑浊的二氧化碳不一定是碳酸钙分解产生的;
15.(1)Na+ 不会使酚酞溶液变红
(2)探究水分子是否能使酚酞溶液变红;氯化钠溶液中含有水分子(或酚酞溶液中就有水分子)
(3)白色沉淀
(4)Na2CO3与H2O发生反应,使溶液中产生了OH -(合理即可)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
