第5章 金属的冶炼与利用 单元练习(含解析)
文档属性
| 名称 | 第5章 金属的冶炼与利用 单元练习(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 109.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-07-23 00:00:00 | ||
图片预览



文档简介
沪教版九年级上册化学练习 5.金属的冶炼与利用
一、单选题
1.为防止铁制品锈蚀,下列做法不恰当的是(? ?)
A.?车船表面喷漆?????????????B.?铁制品表面镀锌?????????????C.?制成不锈钢?????????????D.?洗涤剂洗去铁表面油膜
2. 下列反应属于置换反应的是(?? )
A.?3Fe+2O2 Fe3O4??????????????????????????????????????B.?CaCO3 CaO+CO2↑ C.?CuSO4+2NaOH=Cu(OH)2↓+Na2SO4??????????D.?C+2CuO 2Cu+CO2
3. 下列物质不属于合金的是(?? )
A.?氧化铁??????????????????????????????????B.?生铁??????????????????????????????????C.?不锈钢??????????????????????????????????D.?青铜
4.下列有关合金的叙述,正确的是(??? ) ①合金中至少含两种金属; ②合金中的元素以化合物形式存在; ③合金中一定含有金属; ④合金一定是混合物; ⑤生铁是含杂质较多的铁合金; ⑥合金的强度和硬度一般比组成它们的纯金属更高,抗腐蚀性能等也更好。
A.?①②③④⑤⑥?????????????????????????????B.?①②?????????????????????????????C.?①③④?????????????????????????????D.?③④⑤⑥
5.稀土铝镁合金新型材料,比普通铝型材轻,比钢铁材料轻,而抗拉性能也达到钢铁材料的要求。稀土铝镁合金新型材料属于()
A.?天然材料???????????????????????????B.?金属材料???????????????????????????C.?复合材料???????????????????????????D.?合成材料
6.下列关于合金的说法正确的是(?? )
A.?合金不属于金属材料???????????????????????????????????????????B.?台金的硬度一般比各成分金属大 C.?合金属于金属单质??????????????????????????????????????????????D.?多数合金的熔点高于组成它的成分金属
7.钢铁是世界上使用最广泛的金属材料.下列有关钢铁说法正确的是(?? )
A.?用硫酸铜可除去铁螺丝表面的铁锈??????????????????????B.?钢铁中只含有金属元素 C.?钢比生铁中碳的含量大???????????????????????????????????????D.?废弃的钢铁制品应该回收再利用
8.在面盆、痰盂等铁制品表面烧制搪瓷的目的是(??)
A.?增大硬度防止撞坏????????B.?增大厚度防止磨损????????C.?防止铁生锈且美观????????D.?美观和杀菌消毒作用
9.下列关于金属的说法中,错误的是 ??
A.?铜有良好的导电性,常用于制作导线 B.?钛合金与人体具有很好的相容性 C.?合金与组成它们的纯金属相比,一般硬度更大,抗腐蚀性能更好 D.?锈蚀后的铁制品没有回收价值
10.正在上海举行的世博会上,中国馆——“东方之冠”给人强烈的视觉冲击,它的主体结构为四根巨型的钢筋混凝土制成的核心筒。其中钢属于(????)
A.?合成材料???????????????????????????B.?天然材料???????????????????????????C.?隐身材料???????????????????????????D.?金属材料
11.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是( )
A.?利用电池外壳的金属材料 B.?防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 C.?不使电池中渗透的电解液腐蚀其它物品 D.?回收其中石墨电极
12.下列有关金属的说法正确的是( )
A.?金属都是固态且均为银白色 B.?自然界中有单质形式存在的金属也有化合物形式存在的金属 C.?生活中使用的金属材料基本都是纯金属 D.?所有的金属均能与氧气发生反应
13.下列关于金属材料的叙述错误的是(?? )
A.?回收利用废旧金属可减少对环境的污染 B.?在铁制品表面刷漆或镀耐腐蚀性金属都可以防止铁制品锈蚀 C.?铝块能制成铝箔是利用了铝的延展性 D.?铝比铁更容易跟氧气和其他物质反应,因而铝的抗腐蚀性能比铁差
二、填空题
14.金属在日常生活中随处可见,研究金属的性质可以更好地利用金属。 (1)铝、铁、铜是常见金属。下列生活用品中,主要利用金属导热性的是________?(填序号)。 (2)“淬火”是金属热处理常用的方法。宝剑淬火过程中,铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,此反应的化学方程式为________?,该反应属于基本反应类型中的________?反应。 (3)将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤。滤液中的溶质一定有________?。 (4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等。下列做法与此结果相符的是________?(填序号)。
A.相同质量的三种金属与足量的稀盐酸反应
B.2.4 g镁、6.5 g锌、5.6 g铁与足量的稀盐酸反应
C.向足量的镁、锌、铁中加入稀盐酸的质量比为2︰3︰2
D.足量的三种金属与等量的稀盐酸反应
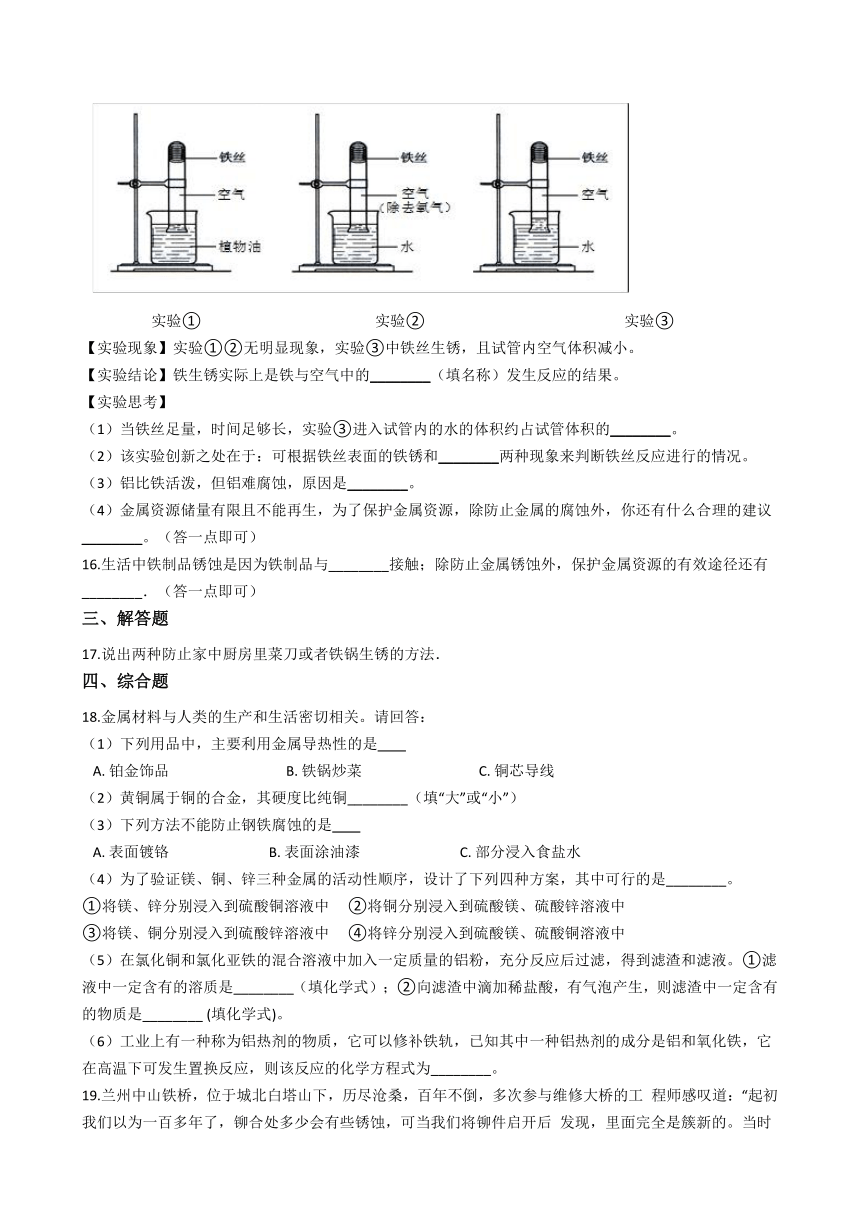
15.在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整。 【实验目的】铁生锈条件的探究。 【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象。 ?????????????????? 实验①???????????? ? ? ? ? ? ? ? ? ? ?? ? 实验②????????????? ? ? ? ? ? ? ? ? ? ? ? ? ?? 实验③ 【实验现象】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小。 【实验结论】铁生锈实际上是铁与空气中的________(填名称)发生反应的结果。 【实验思考】 (1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的________。 (2)该实验创新之处在于:可根据铁丝表面的铁锈和________两种现象来判断铁丝反应进行的情况。 (3)铝比铁活泼,但铝难腐蚀,原因是________。 (4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什么合理的建议________。(答一点即可)
16.生活中铁制品锈蚀是因为铁制品与________接触;除防止金属锈蚀外,保护金属资源的有效途径还有________.(答一点即可)
三、解答题
17.说出两种防止家中厨房里菜刀或者铁锅生锈的方法.
四、综合题
18.金属材料与人类的生产和生活密切相关。请回答:
(1)下列用品中,主要利用金属导热性的是 ??????
A.?铂金饰品??????????????????????????????????B.?铁锅炒菜??????????????????????????????????C.?铜芯导线
(2)黄铜属于铜的合金,其硬度比纯铜________(填“大”或“小”)
(3)下列方法不能防止钢铁腐蚀的是 ??????
A.?表面镀铬?????????????????????????????B.?表面涂油漆?????????????????????????????C.?部分浸入食盐水
(4)为了验证镁、铜、锌三种金属的活动性顺序,设计了下列四种方案,其中可行的是________。
①将镁、锌分别浸入到硫酸铜溶液中??? ②将铜分别浸入到硫酸镁、硫酸锌溶液中
③将镁、铜分别浸入到硫酸锌溶液中??? ④将锌分别浸入到硫酸镁、硫酸铜溶液中
(5)在氯化铜和氯化亚铁的混合溶液中加入一定质量的铝粉,充分反应后过滤,得到滤渣和滤液。①滤液中一定含有的溶质是________(填化学式);②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是________?(填化学式)。
(6)工业上有一种称为铝热剂的物质,它可以修补铁轨,已知其中一种铝热剂的成分是铝和氧化铁,它在高温下可发生置换反应,则该反应的化学方程式为________。
19.兰州中山铁桥,位于城北白塔山下,历尽沧桑,百年不倒,多次参与维修大桥的工 程师感叹道:“起初我们以为一百多年了,铆合处多少会有些锈蚀,可当我们将铆件启开后 发现,里面完全是簇新的。当时使用炭火和锤具等简单工具,能达到如此工艺令人匪夷所 思。”。请同学们结合自己所学的知识回答下列问题。
(1)中山铁桥铆合处簇新如初,说明百年来没有水和________进入其中而造成锈蚀。
(2)我国生产和使用铁器历史悠久,请写出一氧化碳与氧化铁反应的化学方程式________
(3)全世界每年因生锈损失的钢铁,约占世界年产量的四分之一,请你写出一种防止铁制 品锈蚀的方法________。(任填一种)
答案解析部分
一、单选题
1.【答案】 D
【解析】【解答】A、喷漆能使铁与水和氧气隔绝,能防止生锈,A不符合题意;
B、镀一层耐腐蚀的金属能使铁与水和氧气隔绝,能防锈,B不符合题意;
C、制成不锈钢改变了金属的内部结构,能防止铁生锈,C不符合题意;
D、存放在潮湿的空气中铁与水和氧气同时接触,易生锈,D符合题意;
【分析】防止金属生锈的办法主要是隔绝氧气和水,但是在实际生活中还要结合现实情况利用。
2.【答案】D
【解析】【解答】解:A、反应物是两种单质,生成物是一种化合物,不是置换反应,是化合反应;
B、反应物为一种,生成物是两种,不是置换反应,是分解反应;
C、反应物和生成物均是两种化合物,所以不是置换反应,是复分解反应;
D、反应物是一种单质和一种化合物,生成物也是一种单质和一种化合物,所以是置换反应;
故选D.
【分析】根据置换反应的含义进行解答,置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物.
3.【答案】A
【解析】【解答】解:A、氧化铁是氧化物,属于纯净物;
B、生铁是铁碳合金;
C、不锈钢是铁的合金属于混合物;
D、青铜是铜锡合金;
故选A
【分析】根据合金的定义与特点进行解答.合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质.合金概念有三个特点:①一定是混合物;②合金中各成分都是以单质形式存在;③合金中至少有一种金属.
4.【答案】 D
【解析】【解答】①由合金的概念可知,合金中至少含有一种金属,故错误;
②合金中的金属元素以单质形式存在为主,故错误; ③合金中一定含有金属,故正确; ④合金一定是混合物,故正确; ⑤生铁是铁的合金,生铁中含有碳,所以生铁是含杂质较多的铁合金,故正确; ⑥铁和盐酸反应生成氯化亚铁和氢气,所以铁可完全溶解在稀盐酸中,故正确. 故选:D.
【分析】合金是指由一种金属与其它金属或非金属熔合而成的具有金属特性的物质.解答本题要充分理解合金的含义和性质等方面的知识,只有这样才能对相关方面的问题做出正确的判断.
5.【答案】 C
【解析】【解答】A、稀土铝镁合金新型材料是扬州宏福铝业公司研发的,不是天然材料.故A错误; B、稀土铝镁合金新型材料含有稀土,不纯是金属材料.故B错误; C、稀土铝镁合金新型材料属于复合材料.故C正确; D、稀土铝镁合金新型材料中,铝、镁还保持各自的性质,不属于合成材料.故D错误; 故选C. 【分析】稀土铝镁合金新型材料是扬州宏福铝业公司研发的,不是天然材料.铝、镁还保持各自的性质,不属于合成材料.含有稀土,不纯是金属材料.而是属于复合材料.本题考查新型材料的识别.稀土铝镁合金新型材料属于复合材料.
6.【答案】 B
【解析】【分析】A、根据合金的概念,合金中必须有金属,所以合金属于金属材料,故A错误;B、合金的硬度一般比组成合金的各成分硬度高,故B正确;C、合金是金属与金属或金属与非金属的混合物,故C错误;D、合金的熔点比各成分的熔点低,故D错误;故选B。 【点评】根据合金的概念:金属与金属或金属与非金属的混合物。合金的熔点比各成分的熔点低,但硬度比各成分硬度高。
7.【答案】D
【解析】【解答】解:A、铁锈的主要成分是氧化铁,不能与硫酸铜溶液反应,不能用硫酸铜可除去铁螺丝表面的铁锈,故选项说法错误.
B、钢是含碳量为0.03%~2%的铁合金,含有碳等非金属元素,故选项说法错误.
C、生铁和钢都是铁的合金,生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,钢比生铁中碳的含量低,故选项说法错误.
D、废弃的钢铁制品应该回收再利用,能节约金属资源、减少污染,故选项说法正确.
故选:D.
【分析】A、根据铁锈的主要成分是氧化铁,不能与硫酸铜溶液反应,进行分析判断.
B、根据钢是含碳量为0.03%~2%的铁合金,进行分析判断.
C、根据生铁和钢的主要成分,进行分析判断.
D、根据金属回收利用的优点进行分析判断.
8.【答案】 C
【解析】答案C 【分析】防止铁生锈的方法是使铁与氧气和水隔绝,在脸盆等铁制品表面烧制搪瓷,能够隔绝空气和水,不但能防止铁生锈,而且美观. A、在茶缸和脸盆等铁制品表面烧制搪瓷的目的不是为了增大硬度,故选项错误; B、在茶缸和脸盆等铁制品表面烧制搪瓷的目的不是为了增大厚度,故选项错误; C、在茶缸和脸盆等铁制品表面烧制搪瓷不但能防止铁生锈,而且美观,故选项正确; D、在茶缸和脸盆等铁制品表面烧制搪瓷不能杀菌消毒,故选项错误.故选C 考点:本题考查金属锈蚀的条件及其防护 【点评】解答本题要掌握防止铁生锈的方法方面的知识,只有这样才能对问题做出正确的判断
9.【答案】 D
【解析】【解答】A、铜有良好的导电性,常用于制作导线,故A不符合题意;
B、钛合金与人体具有很好的相容性,故B不符合题意;
C、合金与组成它们的纯金属相比,一般硬度更大,熔点低,抗腐蚀性能强,故不C符合题意;
D、锈蚀后的铁制品回收有利于保护金属资源、保护环境、节约金属冶炼的成本,故D符合题意。
故答案为:D。
【分析】A、根据物质的性质决定用途分析,即铜具有良好的导电性,故可以用作导线; B、根据钛合金的性质和用途判断; C、根据合金与组成他的纯金属的不同性质分析; D、根据金属资源的利用和保护来分析;
10.【答案】 D
【解析】【解答】钢为铁的合金,属于金属材料.
故选D.
【分析】金属材料包括金属和合金;合金是指由一种金属与其它金属或非金属熔合而成的具有金属特性的物质.解答本题要掌握材料的分类方法方面的内容,只有这样才能对各种材料进行正确的分类.
11.【答案】 B
【解析】【解答】回收废电池的首要原因是防止废电池中渗漏出的重金属离子对土壤和水源的污染,而对废电池的综合利用是第二位的.
故选B.
【分析】根据废电池进行集中处理的原因:即对环境的污染问题考虑本题.
12.【答案】 B
【解析】【解答】A、大多数金属是银白色的,但铜是紫红色的,金是黄色的.汞在常温下是液态,故A说法错误;
B、自然界中的金属存在有两种形式,游离态(即单质形式存在)和化合态(即以化合物形式存在),故B说法正确;
C、生活中使用的金属材料大多数是合金.故C说法错误;
D、大多数金属在一定条件下能与氧气反应,但金不行.故D说法错误;
故选:B.
【分析】A、根据金属状态和颜色分析判断;
B、根据金属在自然界中的存在状态分析判断;
C、生活中使用的金属材料大多数是合金;
D、根据大多数金属能与氧气反应分析.
13.【答案】 D
【解析】【解答】A.回收利用废旧金属可以减少对环境的污染,A不符合题意
B. 在铁制品表面刷漆或镀耐腐蚀性金属都可以防止铁制品锈蚀 是正确的 ,B不符合题意
C. 铝块能制成铝箔是利用了铝的延展性 是正确的,C不符合题意
D.铝比铁更容易和氧气或其他物质反应,但是铝表面形成的氧化铝是致密的薄膜,能起到保护作用,D符合题意
故答案为:D
【分析】根据已有金属的性质及金属回收利用和腐蚀条件进行分析解答
二、填空题
14.【答案】②? ;3Fe +4H2O(气) Fe3O4 +4H2 ;置换 ;FeSO4、ZnSO4 ;BD
【解析】【解答】(1)题中生活用品中,②铜制火锅主要利用金属导热性; (2)铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,此反应的化学方程式为3Fe +4H2O(气) Fe3O4 +4H2 , 该反应是单质与化合物反应,生成了新的单质和新的化合物,属于基本反应类型中的置换反应。 (3)铁的金属活动性强于铜,但弱与锌,故将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤。滤液中的溶质一定有FeSO4、ZnSO4。 (4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等。则有两种可能性,1、金属都足量,盐酸的量相等,且盐酸全部反应完,因为氢气中的氢元素都来源于盐酸;2、2.4 g镁、6.5 g锌、5.6 g铁(或者镁、锌、铁的质量是2.4、6.5、5.6的相同倍数)与足量的稀盐酸反应,金属全部反应完。选BD。 【分析】一种单质与一种化合物反应,生成了新的单质和新的化合物,属于基本反应类型中的置换反应。
15.【答案】氧气和水蒸气??;1/5;试管内空气体积减小(或试管内液面上升);易生成一层致密的氧化物保护膜,阻止铝不再被氧化;回收利用(有计划合理地开采矿物;废旧金属的回收利用;寻找金属的替代品等合理答案均可)
【解析】【分析】【实验结论】有实验可知,铁生锈实际上是铁与空气中的氧气和水蒸气发生反应的结果。 【实验思考】 (1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的1/5(21%)。 (2)该实验创新之处在于:可根据铁丝表面的铁锈和试管内空气体积减小(或试管内液面上升)两种现象来判断铁丝反应进行的情况。 (3)铝比铁活泼,但铝难腐蚀,原因是铝的表面易生成一层致密的氧化物保护膜,阻止铝不再被氧化。 (4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,我们可以回收利用。(有计划合理地开采矿物;废旧金属的回收利用;寻找金属的替代品等合理答案均可) 【分析】本题综合性较强,难度较大,关键要根据金属锈蚀的原因来分析题意,金属锈蚀是金属和氧气、水等共同作用的结果;金属防锈、金属回收利用对保护金属资源有重大意义。
16.【答案】氧气和水;回收利用废旧金属
【解析】【解答】解:铁在与水和氧气并存时易生锈;保护金属资源可以从金属防锈、回收废旧金属、合理开采金属资源和寻找金属代用品的角度进行,故填:氧气和水,回收利用废旧金属. 【分析】根据已有的知识进行分析,铁在与水和氧气并存时易生锈,保护金属资源可以从金属防锈、回收废旧金属、合理开采金属资源和寻找金属代用品的角度进行.
三、解答题
17.【答案】解:铁锅或菜刀暴露在潮湿的空气中容易生锈,因此使菜刀、铁锅保持干燥或给菜刀、铁锅涂一层植物油,就可以防止铁锅生锈; 故答案为:不用时保持铁锅干燥或涂一层植物油.
【解析】【分析】铁与水和氧气同时接触时容易生锈,使铁制品与水和氧气隔绝,可以防止生锈.
四、综合题
18.【答案】 (1)B (2)大 (3)C (4)③④ (5)AlCl3 ;Cu和Fe (6)2Al+Fe2O3 Al2O3+2Fe
【解析】【解答】(1)在常见的金属材料用品中,铂金饰品,主要利用了其金属光泽;铁锅炒菜,主要利用了导热性;铝导线主要利用金属导电性;(2)黄铜属于铜的合金,其硬度比纯铜大;(3) 表面镀铬 、表面涂油漆 能将金属与氧气、水隔绝,能防止生锈;部分浸入食盐水会加速锈蚀;(4)①镁、锌与硫酸铜反应,可验证镁、锌的活动性都比铜强.但不能验证验证镁、锌两种金属的活动性顺序;②铜与硫酸镁、硫酸锌溶液都不反应,可验证镁、锌的活动性都比铜强.但不能验证验证镁、锌两种金属的活动性顺序;③将镁、铜分别浸入到硫酸锌溶液中,镁与硫酸锌反应,证明镁的活动性比 锌强;铜不与硫酸锌反应,证明铜的活动性比锌弱,可验证镁、铜、锌三种金属的活动性顺序;? ④将锌分别浸入到硫酸镁、硫酸铜溶液中,与硫酸镁溶液不反应,能证明锌的活动性比镁弱;锌与硫酸铜溶液反应,证明锌的活动性比铜强,可验证镁、铜、锌三种金属的活动性顺序;(5)在氯化铜和氯化亚铁的混合溶液中加入一定质量的铝粉,铝先与氯化铜反应生成氯化铝和铜,剩余的铝再与氯化亚铁反应,充分反应后过滤,①滤液中一定含有的溶质是 AlCl3? ;②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是Cu和Fe,可能有锌;(6)铝和氧化铁,它在高温下可发生置换反应,则该反应的化学方程式为2Al+Fe2O3 ?Al2O3+2Fe; 故答案为:B、大、C、③④、AlCl3、Cu和Fe、2Al+Fe2O3 Al2O3+2Fe。
【分析】(1)越左金属活动性就越强,左边的金属可以从右边金属的盐溶液中置换出该金属出来;(2)排在氢左边的金属,可以从酸中置换出氢气;排在氢右边的则不能。
19.【答案】(1)氧气(或空气) (2)3CO+Fe2O3 ?2Fe+3CO2 (3)涂油漆
【解析】【解答】(1)铁与氧气、水接触时易生锈,中山铁桥铆合处簇新如初,说明百年来没有水和氧气进入其中而造成锈蚀;(2)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,化学方程式为:3CO+Fe2O3 ?2Fe+3CO2;(3)铁在与水和氧气同时接触时容易生锈,要防锈可以使铁与水或氧气隔绝,可以在铁表面刷漆、涂油等。
【分析】根据铁生锈是铁与氧气、水的反应分析,所以要防锈就是使铁与氧气和水隔离;根据炼铁原理分析。
一、单选题
1.为防止铁制品锈蚀,下列做法不恰当的是(? ?)
A.?车船表面喷漆?????????????B.?铁制品表面镀锌?????????????C.?制成不锈钢?????????????D.?洗涤剂洗去铁表面油膜
2. 下列反应属于置换反应的是(?? )
A.?3Fe+2O2 Fe3O4??????????????????????????????????????B.?CaCO3 CaO+CO2↑ C.?CuSO4+2NaOH=Cu(OH)2↓+Na2SO4??????????D.?C+2CuO 2Cu+CO2
3. 下列物质不属于合金的是(?? )
A.?氧化铁??????????????????????????????????B.?生铁??????????????????????????????????C.?不锈钢??????????????????????????????????D.?青铜
4.下列有关合金的叙述,正确的是(??? ) ①合金中至少含两种金属; ②合金中的元素以化合物形式存在; ③合金中一定含有金属; ④合金一定是混合物; ⑤生铁是含杂质较多的铁合金; ⑥合金的强度和硬度一般比组成它们的纯金属更高,抗腐蚀性能等也更好。
A.?①②③④⑤⑥?????????????????????????????B.?①②?????????????????????????????C.?①③④?????????????????????????????D.?③④⑤⑥
5.稀土铝镁合金新型材料,比普通铝型材轻,比钢铁材料轻,而抗拉性能也达到钢铁材料的要求。稀土铝镁合金新型材料属于()
A.?天然材料???????????????????????????B.?金属材料???????????????????????????C.?复合材料???????????????????????????D.?合成材料
6.下列关于合金的说法正确的是(?? )
A.?合金不属于金属材料???????????????????????????????????????????B.?台金的硬度一般比各成分金属大 C.?合金属于金属单质??????????????????????????????????????????????D.?多数合金的熔点高于组成它的成分金属
7.钢铁是世界上使用最广泛的金属材料.下列有关钢铁说法正确的是(?? )
A.?用硫酸铜可除去铁螺丝表面的铁锈??????????????????????B.?钢铁中只含有金属元素 C.?钢比生铁中碳的含量大???????????????????????????????????????D.?废弃的钢铁制品应该回收再利用
8.在面盆、痰盂等铁制品表面烧制搪瓷的目的是(??)
A.?增大硬度防止撞坏????????B.?增大厚度防止磨损????????C.?防止铁生锈且美观????????D.?美观和杀菌消毒作用
9.下列关于金属的说法中,错误的是 ??
A.?铜有良好的导电性,常用于制作导线 B.?钛合金与人体具有很好的相容性 C.?合金与组成它们的纯金属相比,一般硬度更大,抗腐蚀性能更好 D.?锈蚀后的铁制品没有回收价值
10.正在上海举行的世博会上,中国馆——“东方之冠”给人强烈的视觉冲击,它的主体结构为四根巨型的钢筋混凝土制成的核心筒。其中钢属于(????)
A.?合成材料???????????????????????????B.?天然材料???????????????????????????C.?隐身材料???????????????????????????D.?金属材料
11.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是( )
A.?利用电池外壳的金属材料 B.?防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 C.?不使电池中渗透的电解液腐蚀其它物品 D.?回收其中石墨电极
12.下列有关金属的说法正确的是( )
A.?金属都是固态且均为银白色 B.?自然界中有单质形式存在的金属也有化合物形式存在的金属 C.?生活中使用的金属材料基本都是纯金属 D.?所有的金属均能与氧气发生反应
13.下列关于金属材料的叙述错误的是(?? )
A.?回收利用废旧金属可减少对环境的污染 B.?在铁制品表面刷漆或镀耐腐蚀性金属都可以防止铁制品锈蚀 C.?铝块能制成铝箔是利用了铝的延展性 D.?铝比铁更容易跟氧气和其他物质反应,因而铝的抗腐蚀性能比铁差
二、填空题
14.金属在日常生活中随处可见,研究金属的性质可以更好地利用金属。 (1)铝、铁、铜是常见金属。下列生活用品中,主要利用金属导热性的是________?(填序号)。 (2)“淬火”是金属热处理常用的方法。宝剑淬火过程中,铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,此反应的化学方程式为________?,该反应属于基本反应类型中的________?反应。 (3)将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤。滤液中的溶质一定有________?。 (4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等。下列做法与此结果相符的是________?(填序号)。
A.相同质量的三种金属与足量的稀盐酸反应
B.2.4 g镁、6.5 g锌、5.6 g铁与足量的稀盐酸反应
C.向足量的镁、锌、铁中加入稀盐酸的质量比为2︰3︰2
D.足量的三种金属与等量的稀盐酸反应
15.在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整。 【实验目的】铁生锈条件的探究。 【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象。 ?????????????????? 实验①???????????? ? ? ? ? ? ? ? ? ? ?? ? 实验②????????????? ? ? ? ? ? ? ? ? ? ? ? ? ?? 实验③ 【实验现象】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小。 【实验结论】铁生锈实际上是铁与空气中的________(填名称)发生反应的结果。 【实验思考】 (1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的________。 (2)该实验创新之处在于:可根据铁丝表面的铁锈和________两种现象来判断铁丝反应进行的情况。 (3)铝比铁活泼,但铝难腐蚀,原因是________。 (4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什么合理的建议________。(答一点即可)
16.生活中铁制品锈蚀是因为铁制品与________接触;除防止金属锈蚀外,保护金属资源的有效途径还有________.(答一点即可)
三、解答题
17.说出两种防止家中厨房里菜刀或者铁锅生锈的方法.
四、综合题
18.金属材料与人类的生产和生活密切相关。请回答:
(1)下列用品中,主要利用金属导热性的是 ??????
A.?铂金饰品??????????????????????????????????B.?铁锅炒菜??????????????????????????????????C.?铜芯导线
(2)黄铜属于铜的合金,其硬度比纯铜________(填“大”或“小”)
(3)下列方法不能防止钢铁腐蚀的是 ??????
A.?表面镀铬?????????????????????????????B.?表面涂油漆?????????????????????????????C.?部分浸入食盐水
(4)为了验证镁、铜、锌三种金属的活动性顺序,设计了下列四种方案,其中可行的是________。
①将镁、锌分别浸入到硫酸铜溶液中??? ②将铜分别浸入到硫酸镁、硫酸锌溶液中
③将镁、铜分别浸入到硫酸锌溶液中??? ④将锌分别浸入到硫酸镁、硫酸铜溶液中
(5)在氯化铜和氯化亚铁的混合溶液中加入一定质量的铝粉,充分反应后过滤,得到滤渣和滤液。①滤液中一定含有的溶质是________(填化学式);②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是________?(填化学式)。
(6)工业上有一种称为铝热剂的物质,它可以修补铁轨,已知其中一种铝热剂的成分是铝和氧化铁,它在高温下可发生置换反应,则该反应的化学方程式为________。
19.兰州中山铁桥,位于城北白塔山下,历尽沧桑,百年不倒,多次参与维修大桥的工 程师感叹道:“起初我们以为一百多年了,铆合处多少会有些锈蚀,可当我们将铆件启开后 发现,里面完全是簇新的。当时使用炭火和锤具等简单工具,能达到如此工艺令人匪夷所 思。”。请同学们结合自己所学的知识回答下列问题。
(1)中山铁桥铆合处簇新如初,说明百年来没有水和________进入其中而造成锈蚀。
(2)我国生产和使用铁器历史悠久,请写出一氧化碳与氧化铁反应的化学方程式________
(3)全世界每年因生锈损失的钢铁,约占世界年产量的四分之一,请你写出一种防止铁制 品锈蚀的方法________。(任填一种)
答案解析部分
一、单选题
1.【答案】 D
【解析】【解答】A、喷漆能使铁与水和氧气隔绝,能防止生锈,A不符合题意;
B、镀一层耐腐蚀的金属能使铁与水和氧气隔绝,能防锈,B不符合题意;
C、制成不锈钢改变了金属的内部结构,能防止铁生锈,C不符合题意;
D、存放在潮湿的空气中铁与水和氧气同时接触,易生锈,D符合题意;
【分析】防止金属生锈的办法主要是隔绝氧气和水,但是在实际生活中还要结合现实情况利用。
2.【答案】D
【解析】【解答】解:A、反应物是两种单质,生成物是一种化合物,不是置换反应,是化合反应;
B、反应物为一种,生成物是两种,不是置换反应,是分解反应;
C、反应物和生成物均是两种化合物,所以不是置换反应,是复分解反应;
D、反应物是一种单质和一种化合物,生成物也是一种单质和一种化合物,所以是置换反应;
故选D.
【分析】根据置换反应的含义进行解答,置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物.
3.【答案】A
【解析】【解答】解:A、氧化铁是氧化物,属于纯净物;
B、生铁是铁碳合金;
C、不锈钢是铁的合金属于混合物;
D、青铜是铜锡合金;
故选A
【分析】根据合金的定义与特点进行解答.合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质.合金概念有三个特点:①一定是混合物;②合金中各成分都是以单质形式存在;③合金中至少有一种金属.
4.【答案】 D
【解析】【解答】①由合金的概念可知,合金中至少含有一种金属,故错误;
②合金中的金属元素以单质形式存在为主,故错误; ③合金中一定含有金属,故正确; ④合金一定是混合物,故正确; ⑤生铁是铁的合金,生铁中含有碳,所以生铁是含杂质较多的铁合金,故正确; ⑥铁和盐酸反应生成氯化亚铁和氢气,所以铁可完全溶解在稀盐酸中,故正确. 故选:D.
【分析】合金是指由一种金属与其它金属或非金属熔合而成的具有金属特性的物质.解答本题要充分理解合金的含义和性质等方面的知识,只有这样才能对相关方面的问题做出正确的判断.
5.【答案】 C
【解析】【解答】A、稀土铝镁合金新型材料是扬州宏福铝业公司研发的,不是天然材料.故A错误; B、稀土铝镁合金新型材料含有稀土,不纯是金属材料.故B错误; C、稀土铝镁合金新型材料属于复合材料.故C正确; D、稀土铝镁合金新型材料中,铝、镁还保持各自的性质,不属于合成材料.故D错误; 故选C. 【分析】稀土铝镁合金新型材料是扬州宏福铝业公司研发的,不是天然材料.铝、镁还保持各自的性质,不属于合成材料.含有稀土,不纯是金属材料.而是属于复合材料.本题考查新型材料的识别.稀土铝镁合金新型材料属于复合材料.
6.【答案】 B
【解析】【分析】A、根据合金的概念,合金中必须有金属,所以合金属于金属材料,故A错误;B、合金的硬度一般比组成合金的各成分硬度高,故B正确;C、合金是金属与金属或金属与非金属的混合物,故C错误;D、合金的熔点比各成分的熔点低,故D错误;故选B。 【点评】根据合金的概念:金属与金属或金属与非金属的混合物。合金的熔点比各成分的熔点低,但硬度比各成分硬度高。
7.【答案】D
【解析】【解答】解:A、铁锈的主要成分是氧化铁,不能与硫酸铜溶液反应,不能用硫酸铜可除去铁螺丝表面的铁锈,故选项说法错误.
B、钢是含碳量为0.03%~2%的铁合金,含有碳等非金属元素,故选项说法错误.
C、生铁和钢都是铁的合金,生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,钢比生铁中碳的含量低,故选项说法错误.
D、废弃的钢铁制品应该回收再利用,能节约金属资源、减少污染,故选项说法正确.
故选:D.
【分析】A、根据铁锈的主要成分是氧化铁,不能与硫酸铜溶液反应,进行分析判断.
B、根据钢是含碳量为0.03%~2%的铁合金,进行分析判断.
C、根据生铁和钢的主要成分,进行分析判断.
D、根据金属回收利用的优点进行分析判断.
8.【答案】 C
【解析】答案C 【分析】防止铁生锈的方法是使铁与氧气和水隔绝,在脸盆等铁制品表面烧制搪瓷,能够隔绝空气和水,不但能防止铁生锈,而且美观. A、在茶缸和脸盆等铁制品表面烧制搪瓷的目的不是为了增大硬度,故选项错误; B、在茶缸和脸盆等铁制品表面烧制搪瓷的目的不是为了增大厚度,故选项错误; C、在茶缸和脸盆等铁制品表面烧制搪瓷不但能防止铁生锈,而且美观,故选项正确; D、在茶缸和脸盆等铁制品表面烧制搪瓷不能杀菌消毒,故选项错误.故选C 考点:本题考查金属锈蚀的条件及其防护 【点评】解答本题要掌握防止铁生锈的方法方面的知识,只有这样才能对问题做出正确的判断
9.【答案】 D
【解析】【解答】A、铜有良好的导电性,常用于制作导线,故A不符合题意;
B、钛合金与人体具有很好的相容性,故B不符合题意;
C、合金与组成它们的纯金属相比,一般硬度更大,熔点低,抗腐蚀性能强,故不C符合题意;
D、锈蚀后的铁制品回收有利于保护金属资源、保护环境、节约金属冶炼的成本,故D符合题意。
故答案为:D。
【分析】A、根据物质的性质决定用途分析,即铜具有良好的导电性,故可以用作导线; B、根据钛合金的性质和用途判断; C、根据合金与组成他的纯金属的不同性质分析; D、根据金属资源的利用和保护来分析;
10.【答案】 D
【解析】【解答】钢为铁的合金,属于金属材料.
故选D.
【分析】金属材料包括金属和合金;合金是指由一种金属与其它金属或非金属熔合而成的具有金属特性的物质.解答本题要掌握材料的分类方法方面的内容,只有这样才能对各种材料进行正确的分类.
11.【答案】 B
【解析】【解答】回收废电池的首要原因是防止废电池中渗漏出的重金属离子对土壤和水源的污染,而对废电池的综合利用是第二位的.
故选B.
【分析】根据废电池进行集中处理的原因:即对环境的污染问题考虑本题.
12.【答案】 B
【解析】【解答】A、大多数金属是银白色的,但铜是紫红色的,金是黄色的.汞在常温下是液态,故A说法错误;
B、自然界中的金属存在有两种形式,游离态(即单质形式存在)和化合态(即以化合物形式存在),故B说法正确;
C、生活中使用的金属材料大多数是合金.故C说法错误;
D、大多数金属在一定条件下能与氧气反应,但金不行.故D说法错误;
故选:B.
【分析】A、根据金属状态和颜色分析判断;
B、根据金属在自然界中的存在状态分析判断;
C、生活中使用的金属材料大多数是合金;
D、根据大多数金属能与氧气反应分析.
13.【答案】 D
【解析】【解答】A.回收利用废旧金属可以减少对环境的污染,A不符合题意
B. 在铁制品表面刷漆或镀耐腐蚀性金属都可以防止铁制品锈蚀 是正确的 ,B不符合题意
C. 铝块能制成铝箔是利用了铝的延展性 是正确的,C不符合题意
D.铝比铁更容易和氧气或其他物质反应,但是铝表面形成的氧化铝是致密的薄膜,能起到保护作用,D符合题意
故答案为:D
【分析】根据已有金属的性质及金属回收利用和腐蚀条件进行分析解答
二、填空题
14.【答案】②? ;3Fe +4H2O(气) Fe3O4 +4H2 ;置换 ;FeSO4、ZnSO4 ;BD
【解析】【解答】(1)题中生活用品中,②铜制火锅主要利用金属导热性; (2)铁在高温下和水蒸气发生反应生成四氧化三铁和另一种气体单质,此反应的化学方程式为3Fe +4H2O(气) Fe3O4 +4H2 , 该反应是单质与化合物反应,生成了新的单质和新的化合物,属于基本反应类型中的置换反应。 (3)铁的金属活动性强于铜,但弱与锌,故将一定量铁粉加入到硫酸锌、硫酸铜的混合液中,充分反应后过滤。滤液中的溶质一定有FeSO4、ZnSO4。 (4)取一定量镁、锌、铁三种金属,分别加入溶质质量分数相等的稀盐酸,充分反应后,生成氢气的质量相等。则有两种可能性,1、金属都足量,盐酸的量相等,且盐酸全部反应完,因为氢气中的氢元素都来源于盐酸;2、2.4 g镁、6.5 g锌、5.6 g铁(或者镁、锌、铁的质量是2.4、6.5、5.6的相同倍数)与足量的稀盐酸反应,金属全部反应完。选BD。 【分析】一种单质与一种化合物反应,生成了新的单质和新的化合物,属于基本反应类型中的置换反应。
15.【答案】氧气和水蒸气??;1/5;试管内空气体积减小(或试管内液面上升);易生成一层致密的氧化物保护膜,阻止铝不再被氧化;回收利用(有计划合理地开采矿物;废旧金属的回收利用;寻找金属的替代品等合理答案均可)
【解析】【分析】【实验结论】有实验可知,铁生锈实际上是铁与空气中的氧气和水蒸气发生反应的结果。 【实验思考】 (1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的1/5(21%)。 (2)该实验创新之处在于:可根据铁丝表面的铁锈和试管内空气体积减小(或试管内液面上升)两种现象来判断铁丝反应进行的情况。 (3)铝比铁活泼,但铝难腐蚀,原因是铝的表面易生成一层致密的氧化物保护膜,阻止铝不再被氧化。 (4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,我们可以回收利用。(有计划合理地开采矿物;废旧金属的回收利用;寻找金属的替代品等合理答案均可) 【分析】本题综合性较强,难度较大,关键要根据金属锈蚀的原因来分析题意,金属锈蚀是金属和氧气、水等共同作用的结果;金属防锈、金属回收利用对保护金属资源有重大意义。
16.【答案】氧气和水;回收利用废旧金属
【解析】【解答】解:铁在与水和氧气并存时易生锈;保护金属资源可以从金属防锈、回收废旧金属、合理开采金属资源和寻找金属代用品的角度进行,故填:氧气和水,回收利用废旧金属. 【分析】根据已有的知识进行分析,铁在与水和氧气并存时易生锈,保护金属资源可以从金属防锈、回收废旧金属、合理开采金属资源和寻找金属代用品的角度进行.
三、解答题
17.【答案】解:铁锅或菜刀暴露在潮湿的空气中容易生锈,因此使菜刀、铁锅保持干燥或给菜刀、铁锅涂一层植物油,就可以防止铁锅生锈; 故答案为:不用时保持铁锅干燥或涂一层植物油.
【解析】【分析】铁与水和氧气同时接触时容易生锈,使铁制品与水和氧气隔绝,可以防止生锈.
四、综合题
18.【答案】 (1)B (2)大 (3)C (4)③④ (5)AlCl3 ;Cu和Fe (6)2Al+Fe2O3 Al2O3+2Fe
【解析】【解答】(1)在常见的金属材料用品中,铂金饰品,主要利用了其金属光泽;铁锅炒菜,主要利用了导热性;铝导线主要利用金属导电性;(2)黄铜属于铜的合金,其硬度比纯铜大;(3) 表面镀铬 、表面涂油漆 能将金属与氧气、水隔绝,能防止生锈;部分浸入食盐水会加速锈蚀;(4)①镁、锌与硫酸铜反应,可验证镁、锌的活动性都比铜强.但不能验证验证镁、锌两种金属的活动性顺序;②铜与硫酸镁、硫酸锌溶液都不反应,可验证镁、锌的活动性都比铜强.但不能验证验证镁、锌两种金属的活动性顺序;③将镁、铜分别浸入到硫酸锌溶液中,镁与硫酸锌反应,证明镁的活动性比 锌强;铜不与硫酸锌反应,证明铜的活动性比锌弱,可验证镁、铜、锌三种金属的活动性顺序;? ④将锌分别浸入到硫酸镁、硫酸铜溶液中,与硫酸镁溶液不反应,能证明锌的活动性比镁弱;锌与硫酸铜溶液反应,证明锌的活动性比铜强,可验证镁、铜、锌三种金属的活动性顺序;(5)在氯化铜和氯化亚铁的混合溶液中加入一定质量的铝粉,铝先与氯化铜反应生成氯化铝和铜,剩余的铝再与氯化亚铁反应,充分反应后过滤,①滤液中一定含有的溶质是 AlCl3? ;②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是Cu和Fe,可能有锌;(6)铝和氧化铁,它在高温下可发生置换反应,则该反应的化学方程式为2Al+Fe2O3 ?Al2O3+2Fe; 故答案为:B、大、C、③④、AlCl3、Cu和Fe、2Al+Fe2O3 Al2O3+2Fe。
【分析】(1)越左金属活动性就越强,左边的金属可以从右边金属的盐溶液中置换出该金属出来;(2)排在氢左边的金属,可以从酸中置换出氢气;排在氢右边的则不能。
19.【答案】(1)氧气(或空气) (2)3CO+Fe2O3 ?2Fe+3CO2 (3)涂油漆
【解析】【解答】(1)铁与氧气、水接触时易生锈,中山铁桥铆合处簇新如初,说明百年来没有水和氧气进入其中而造成锈蚀;(2)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,化学方程式为:3CO+Fe2O3 ?2Fe+3CO2;(3)铁在与水和氧气同时接触时容易生锈,要防锈可以使铁与水或氧气隔绝,可以在铁表面刷漆、涂油等。
【分析】根据铁生锈是铁与氧气、水的反应分析,所以要防锈就是使铁与氧气和水隔离;根据炼铁原理分析。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
