科学八上习题精练——第一章《水和水的溶液》(1.4-1.7)
文档属性
| 名称 | 科学八上习题精练——第一章《水和水的溶液》(1.4-1.7) |  | |
| 格式 | zip | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-07-26 15:21:15 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
第一章《水和水的溶液》(1.4-1.7)
一、选择题
1. 某油漆在不同液体中溶解能力不同(见下表),则20℃时,在相同条件下清洗该油漆污渍,效果最好的是( )
液体种类 水 乙醇 乙醛 汽油
溶解性(20℃) 不溶 可溶 可溶 易溶
A、水 B、乙醇 C、乙醛 D、汽油
2. 关于溶液下列说法正确的是( )
A、饱和溶液一定是浓溶液
B、t℃时,100克某物质的饱和溶液中含该溶质18克,则该物质在t℃时溶解度是18克
C、饱和溶液指一定温度下一定量溶剂中不能继续溶解某种溶质的溶液
D、不饱和溶液加溶剂可以变为饱和溶液
3. (2019·温州)如图,将红砂糖倒入一杯开水中,充分溶解。能作为判断砂糖水是饱和溶液的依据是( )
A、砂糖水颜色很深
B、砂糖水味道很甜
C、砂糖溶解得很快
D、砂糖固体有剩余
4. 人们常用过滤的方法来净化水,如图所示。下列有关说法正确的是( )
A、用过滤法可以将溶解在水中的物质分离
B、滤纸放入漏斗时边缘要稍低于漏斗边缘
C、过滤物也可以沿着漏斗内壁倒入
D、过滤出杂质后所得的滤液属于纯净物
5. 下列实验或现象,与物质的结晶无关的是( )
A、盐田晒盐 B、利用食盐溶液做窗花 C、晶体的“长大” D、配制食盐溶液
6. 江南多雨,许多地方都在建设海绵城市。下列做法不符合海绵城市建设理念的是( )
A、用水泥硬化路面 B、建人工湖泊 C、屋顶种绿色植物 D、加粗雨水管道
7. 日常生活中的许多小事都能保护水资源。下列做法中不合理的是( )
A、用洗脸水浇花 B、用低流量喷头 C、生活污水排放到河里 D、收集雨水作生活用水
8. 阳春三月,骤雨初歇,浙江省浦江县翠湖之畔,柳枝摇曳,远山如黛,一池春水踏着微风,向东奔流而去……(如图)为保护环境,美化家园, 下列措施不可取的是( )
A、加大空气质量检测,改善环境状况
B、生活垃圾分类回收,垃圾资源化
C、全面禁止水晶加工厂生产
D、大力开展五水共治,保护水资源
9.(2019·杭州)如图所示为蒸发氯化钠溶液的实验过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,可以作出的正确判断是( )
A、在①→②过程中,氯化钠的质量分数保持不变
B、在②→③过程中,氯化钠的溶解度不断增大
C、在③→④过程中,水的质量分数不断增大
D、在②→④过程中,氯化钠的质量分数先不变后增大
10.(2019·广州)25℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是( )
编号 ① ② ③ ④
水的质量/g 50 50 50 50
加入固体质量/g 5 10 15 20
现象 固体完全溶解 固体完全溶解 剩余少量固体 剩余较多固体
A、实验①所得溶液质量分数为10%? B、实验说明25℃时该物质的溶解度是20g
C、实验③④所得溶液质量分数相同 D、实验④所得溶液中含溶质20g
11.硝酸钾的溶解度如表,取20℃等质量的两份饱和硝酸钾溶液,第一份溶液升温到 40℃;另一份溶液恒温蒸发10克水。则两份溶液中都不变化的量是( )
A、溶质质量
温度/℃ 20 40
硝酸钾溶解度/g 31.6 63.9
B、溶剂质量
C、溶液质量
D、溶质质量分数
12.在一定温度下,向一定量的氯化钠不饱和溶液中不断加入氯化钠固体,并搅拌。在此过程溶液中溶质的质量分数(b)与加入氯化钠质量(a)的变化关系如下图所示,其中正确的是( )
13.(2019·呼和浩特) 配制70克16%的NaCl溶液,下列操作会使所配溶液溶质质量分数大于16%的是( )
A、称取氯化钠 B、转移氯化钠 C、量取水 D、配好后装瓶
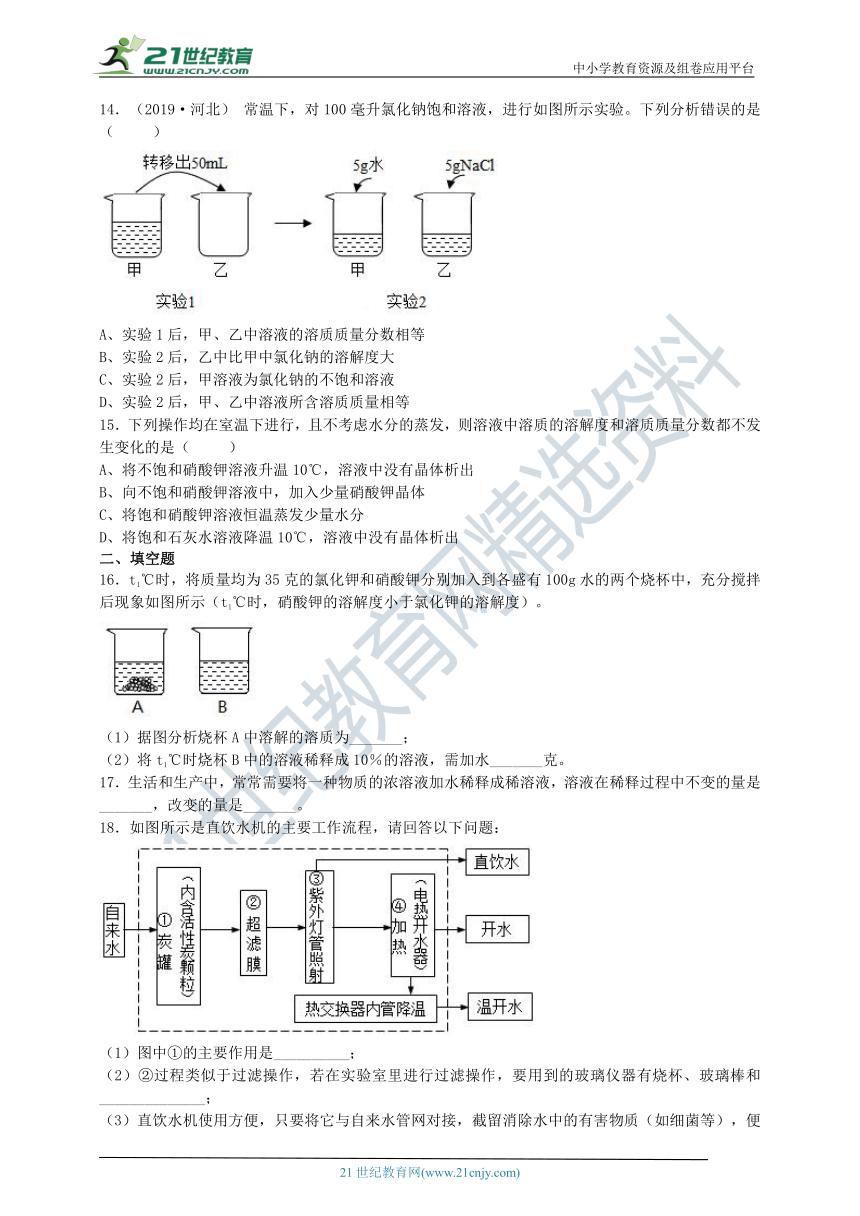
14.(2019·河北) 常温下,对100毫升氯化钠饱和溶液,进行如图所示实验。下列分析错误的是( )
A、实验1后,甲、乙中溶液的溶质质量分数相等
B、实验2后,乙中比甲中氯化钠的溶解度大
C、实验2后,甲溶液为氯化钠的不饱和溶液
D、实验2后,甲、乙中溶液所含溶质质量相等
15.下列操作均在室温下进行,且不考虑水分的蒸发,则溶液中溶质的溶解度和溶质质量分数都不发生变化的是( )
A、将不饱和硝酸钾溶液升温10℃,溶液中没有晶体析出
B、向不饱和硝酸钾溶液中,加入少量硝酸钾晶体
C、将饱和硝酸钾溶液恒温蒸发少量水分
D、将饱和石灰水溶液降温10℃,溶液中没有晶体析出
二、填空题
16.t1℃时,将质量均为35克的氯化钾和硝酸钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图所示(t1℃时,硝酸钾的溶解度小于氯化钾的溶解度)。
(1)据图分析烧杯A中溶解的溶质为_______;
(2)将t1℃时烧杯B中的溶液稀释成10%的溶液,需加水_______克。
17.生活和生产中,常常需要将一种物质的浓溶液加水稀释成稀溶液,溶液在稀释过程中不变的量是_______,改变的量是_______。
18.如图所示是直饮水机的主要工作流程,请回答以下问题:
(1)图中①的主要作用是__________;
(2)②过程类似于过滤操作,若在实验室里进行过滤操作,要用到的玻璃仪器有烧杯、玻璃棒和______________;
(3)直饮水机使用方便,只要将它与自来水管网对接,截留消除水中的有害物质(如细菌等),便得到直饮水,直饮水属于____________(选填“混合物”或“纯净物”)。
19.(2019·宁波)图甲是一种稀释瓶,用户可以根据需求用它以一定体积比对原液进行稀释,图乙是它的7种不同比例的稀释方式。小科用该稀释瓶按1:2的比例稀释原液,原液是密度为1.5g/mL、溶质质量分数为50%的NaOH溶液。稀释过程中,不考虑温度变化和混合前后的体积变化。
(1)当水加到1:1刻度线时,水对稀释瓶底的压强为p1,当水加到1:2的刻度线时,水对稀释瓶底的压强为p2,则p1 p2。(添“>”“<”或“=”)
(2)稀释得到的NaOH溶液的密度为 g/mL,溶质质量分数为 。(计算结果分别精确到0.1g/mL和0.1%)
20.如图是某硫酸试剂瓶标签上的内容:
(1)小妍需要500g18%的稀硫酸进行实验,则她需从该瓶硫酸中取出 g与适量水混合配制。
(2)配制时,所需的玻璃仪器除烧杯、量筒和胶头滴管外,还需要 (填仪器名称)。
(3)在配制过程中,下列情况会引起硫酸溶液的质量分数偏高的是 (选填字母)。
A、用量筒量取硫酸时仰视刻度线 B、配制好后装瓶过程中有少量液体溅出
C、烧杯洗涤后还有少量水就进行配制 D、浓硫酸敞口放置一段时间后再量取
21.某温度下,将40克食盐放到100克水中,充分搅拌后溶解掉36克食盐,得到136克食盐水。据此回答下列问题:
(1)食盐水中溶质是 ,溶剂是 。
(2)得到的溶液中,溶质质量为 ,溶剂质量为 。
(3)将上述溶液等分为四份,则每一份溶质质量为 ,溶剂质量为 。
22.科学兴趣小组进行粗盐提纯实验,过程如图甲所示;并用所得的精盐配制5%NaCl溶液50克,过程如图乙所示。
(1)图甲操作C中玻璃棒的作用是___________。
(2)称量精盐发现天平指针偏左,此时应 ,直至天平再次平衡。
(3)所配制 NaCl 溶液溶质质量分数偏小,其原因可能有 (填字母)。
A、粗盐溶解时不充分 B、过滤时滤纸破损
C、蒸发时溶液飞溅 D、配溶液时称量的精盐仍潮湿
三、实验探究题
23.为研究物质的溶解性与哪些因素有关,某科学兴趣小组同学设计了如下表所示实验方案进行研究:
因素 第1组 第2组
温度/℃ 20 20 20
加入溶剂种类 水 酒精 水
加入溶剂质量/克 20 20 10
加入固体种类 硝酸钾 硝酸钾 硝酸钾
加入固体质量/克 10 10 10
试回答:
(1)实验中物质的溶解性是通过_________________来比较的。
(2)第1组实验中研究的问题是_____________________。
(3)第2组实验中要研究溶解性与溶质种类的关系,请将表格内容填写完整。
24.如图是配制50克质量分数为10%的氯化钠溶液的操作过程示意图,请回答:
(1)请指出上述操作中的错误之处__________;
(2)实验所需氯化钠的质量为____克。称量时,天平调平后,下一步的操作是_________;
(3)下列操作可能导致溶液溶质质量分数小于10%的是(填序号)_______。
①C操作中有固体洒出 ②D操作中有少量水溅出 ③E操作有少量溶液溅出
25.实验室用溶质质量分数为 4%氢氧化钠溶液进行水的电解实验。
步骤一:配制 100g溶质质量分数为 4%的氢氧化钠溶液。
(1)计算所需的氢氧化钠质量为 g;
(2)称量氢氧化钠固体时,若发现指针偏向分度盘的右边,应进行的操作是 。
步骤二:电解水用如图装置进行水电解实验,已知氢氧化钠在水的电解实验中,只起到增强水的导电性作用。
(3)若实验中用4%的氢氧化钠溶液100g,通电一段时间后,氢氧化钠溶液溶质质量分数变为6.25%,则被电解的水的质量为______g。
四、简答题
26.(2019·绍兴)下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
(1)10℃时,100克水中最多可溶解硝酸钾的质量为 克。
(2)20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为 。
(3)如图是硝酸钾溶液的变化情况,请写出一种可采用的操作方法。(写出计算过程)
27.乐清产盐有悠久的历史,盐产品在日常生活、工业生产中有广泛用途。以下流程图反映了制取精盐的过程。
(1)在溶解的操作中,玻璃棒的作用是___________。
(2)在过滤时,若经过两次过滤后滤液仍然浑浊,其原因可能是___________。
(3)实验中,利用阳光、风力进行蒸发。在蒸发阶段,滤液A、溶液B、溶液C的状况依次如下图A、B、C所示,则B烧杯中的溶液________是饱和溶液。(选填“一定”、“不”或”可能”)
28.实验室保存一瓶浓盐酸,瓶上的标签部分内容如图所示,请根据标签上的信息回答下列各问:
(1)这一瓶浓盐酸中溶质的质量是多少克?(结果精确到0.1)
(2)取100克此瓶内的浓盐酸可以稀释成1.85%的稀盐酸多少克?同时加水多少克?
参考答案
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 D C D B D A C C D C
题号 11 12 13 14 15
答案 D C C B C
二、填空题
16.(1)硝酸钾 (2)215
17.溶质质量 溶剂质量(溶液质量、溶质质量分数)
18.(1)吸附 (2)漏斗 (3)混合物
19.(1)< (2)1.2 21.4%
20.(1)100 (2)玻璃棒 (3)A
21.(1)食盐 水 (2)36g 100g (3)9g 25g
22.(1)受热均匀,防止固体飞溅 (2)减少左盘中精盐质量 (3)BD
三、实验探究题
23.(1)溶质不能再继续溶解时所溶解的溶质的质量
(2)物质溶解性与溶剂种类的关系或溶剂种类对物质溶解性的影响
(3)20 水 10 氯化钠 10
24.(1)瓶塞未倒放、砝码和氯化钠位置放反(2)5 左右盘放置相同的纸张 (3)①
25.(1)4 (2)继续往左盘内添加氢氧化钠固体直至天平平衡 (3)36
四、简答题
26.(1)20.9 (2)20%
(3)方法一:设要加入硝酸钾的质量为x
100克×10%+x=(100克+x)×25% x=20克
答:可向烧杯中加入20克硝酸钾。
方法二:设蒸发水的质量为y。
100克×10%=(100克-y)×25% y=60克
答:可蒸发60克水
27.(1)加快粗盐溶解 (2)滤纸破损 (3)可能
28.解:(1)V=500mL=500cm3
浓盐酸中溶质的质量=1.19g/cm3×500cm3×37%≈220.2g
(2)设可以稀释成1.85%的稀盐酸的质量为x
100g×37%=x×1.85%???
x=2000g
水的质量=2000g-100g=1900g
答:(1)这一瓶浓盐酸中溶质的质量是220.2g;
(2)可以稀释成1.85%的稀盐酸2000g,同时加水1900g。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
