8年级升9年级化学专题复习:化学用语和化学计算(无答案)
文档属性
| 名称 | 8年级升9年级化学专题复习:化学用语和化学计算(无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 366.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-07-31 00:00:00 | ||
图片预览

文档简介
8年级升9年级化学专题复习
化学入门知识的复习:化学用语与化学计算
一、构成物质的微粒
学习目标:务必掌握常见物质是由什么微粒构成的。
1、构成物质的微粒之间的关系(逻辑图)
【归纳总结】分子与原子的关系:
离子与原子的关系:
2、常见物质的构成微粒
(1)由原子直接构成的物质有:
①______________________________________;
②__________________________________________;
③____________________________。
(2)由离子构成的物质:目前所学的有_____________。
(3)其他物质(大多数)是由__________构成的:物质一般由分子构成。
3、物质的化学性质是由直接构成物质的微粒保持的。
例题1 (1)水的化学性质是由_____________保持的;氯化钠的化学性质是由______________保持的。
(2)CO有毒,而CO2无毒,原因是它们___________________________。
(3)金刚石和石墨都是由________构成的,所以它们的_________性质相似;而金刚石硬度大、不导电,石墨质软,是导体,说明它们的________性质不同,微观原因是它们___________________________。
变式训练 已知由同种元素组成的不同种单质,互称为同素异形体。例如金刚石和石墨是同素异形体,红磷和白磷也是同素异形体。已知铁有δ-Fe、γ-Fe、α-Fe三种同素异形体(如下图)。三种晶体在不同温度下能发生以下转化。/下列有关说法正确的是( )
A.δ-Fe、γ-Fe、α-Fe之间的相互转化是化学变化
B.δ-Fe、γ-Fe、α-Fe一定不属于同种元素
C.δ-Fe、γ-Fe、α-Fe属于同种物质
D.δ-Fe、γ-Fe、α-Fe三种铁单质的性质都相同
4、元素与原子的区别
比较项目
元素
原子
概念
元素是具有相同核电荷数的同一类原子的总称。
原子是化学变化中的最小微粒。
区别
元素着眼于种类不表示个数,没有数量多少的含义。
原子既表示种类又讲个数,有数量的含义。
使用领域
元素是用来描述物质的宏观组成(习惯上说组成),如:水里含有氢元素和氧元素,水是由氢元素和氧元素组成的。但不能说“水是由二个氢元素和一个氧元素所组成的”。
原子是用来描述物质的微观构成(习惯上说构成),如:一个水分子是由两个氢原子和一个氧原子构成的。但不能说“一个水分子是由氢元素和氧元素所组成。”
联系
元素是同一类原子的总称;原子是构成元素的基本单元。
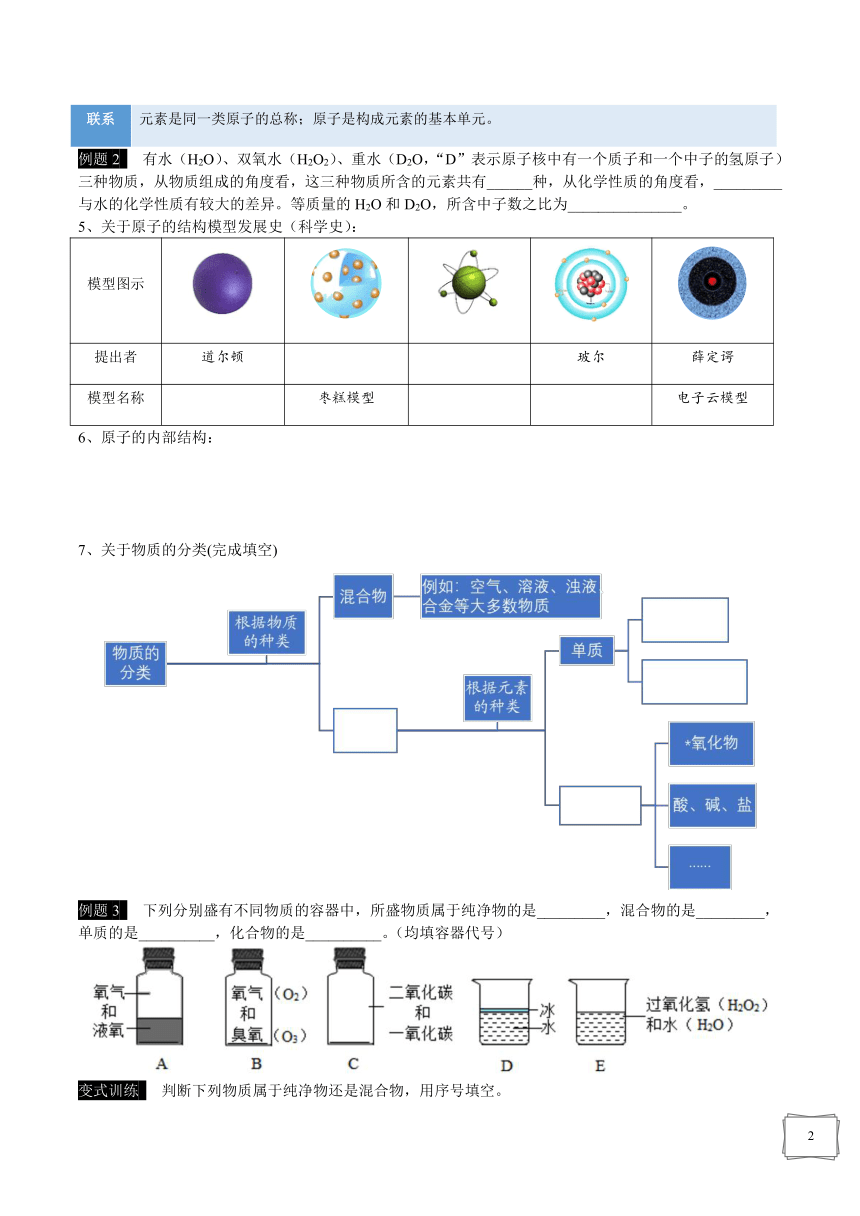
例题2 有水(H2O)、双氧水(H2O2)、重水(D2O,“D”表示原子核中有一个质子和一个中子的氢原子)三种物质,从物质组成的角度看,这三种物质所含的元素共有______种,从化学性质的角度看,_________与水的化学性质有较大的差异。等质量的H2O和D2O,所含中子数之比为_______________。
5、关于原子的结构模型发展史(科学史):
模型图示
/
/
/
/
/
提出者
道尔顿
玻尔
薛定谔
模型名称
枣糕模型
电子云模型
6、原子的内部结构:
7、关于物质的分类(完成填空)
/
例题3 下列分别盛有不同物质的容器中,所盛物质属于纯净物的是_________,混合物的是_________,单质的是__________,化合物的是__________。(均填容器代号)
/
变式训练 判断下列物质属于纯净物还是混合物,用序号填空。
①液氧;②石蜡;③青铜;④干冰;⑤稀有气体;⑥糖水;⑦三氯化磷;⑧水银;⑨医用酒精;⑩水蒸气;?铜矿石;?KMnO4制O2反应完后的剩余固体
(1)其中纯净物是:__________;混合物是:__________。
(2)请写出其中纯净物的化学式______________________________。
例题4 (2018·杭州-1)南京理工大学胡炳成团队用新方法制得了NaN5?3H2O,该化合物中含有N5-等微粒,已知N为7号元素,则下列有关说法正确的是( )
A﹒N5-是一种单质 B﹒1 个N5- 带一个单位的正电荷
C﹒1 个N5-共含有 35 个质子 D﹒1 个N5-中共含有 35 个电子
二、化学用语
1、元素符号(必记):1~20号元素,需要掌握序数、符号和中文名称。常见元素铁、铜、金、银、汞、锌等只需掌握名称与符号对应起来。
2、常见的原子团符号(必记)
名称
符号
化合价
名称
符号
化合价
铵根离子
硝酸根离子
碳酸根离子
硫酸根离子
碳酸氢根离子
氢氧根离子
3、常见元素化合价(口诀,必记)
钾钠银氢正一价
钙镁钡锌正二价
氟氯溴碘(卤)负一价
通常氧是负二价
铜正一二、铝正三
铁有正二和正三
注意:(1)H2O2中氧元素的化合价是________;
(2)氟氯溴碘同为一族,被称为卤族元素,只有在卤化物中,卤族元素才是-1价。
(3)正一价铜是亚铜,正二价铁是亚铁。
例题5 (1)标出下列物质中氯元素的化合价。
NaCl Cl2 HClO KClO3 KClO4
(2)写出下列物质的化学式。
①硫酸铁:__________________; ②氢氧化亚铁:__________________;
③碳酸铵:__________________; ④碳酸氢铵:__________________。
三、化学计算
(一)化学式有关的计算——元素质量比、相对分子质量、质量分数的有关计算
例题6 (2018·金丽-5)如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是( )
A.苯分子由碳、氢两种元素组成
B.苯中氢元素的质量分数小于10%
C.六氯苯中碳氯两种元素的质量比为1∶1
D.六氯苯由6个碳原子和6个氯原子构成
例题7 A、B两种元素的相对原子质量之比为7∶2,它们组成的一种化合物,A、B两种元素的质量比为21∶8,则该化合物的化学式可表示为( )
A. A3B4 B. AB2 C. A2B D. A2B2
例题8 通常状况下某NH4NO3晶体的样品中,测得其中氮元素的质量分数为38%,那么该样品所含的杂质在下列物质中可能是( )
A. NH4Cl B. N2 C. (NH4)2SO4 D. CO(NH2)2
(二)质量守恒定律及化学方程式的书写与计算
例题9 下列关于化学反应“X2+3Y2===2Z”的叙述,错误的是( )
① Z的化学式为XY3
② 若m gX2和n gY2恰好完全反应,则生成(m+n)g Z
③ 若X2和Y2的相对分子质量分别为M和N,则Z的相对分子质量为(M+N)
④ 若a gX2完全反应生成b gZ,则同时消耗(a-b)g Y2
A. ①② B. ①③ C. ②④ D. ③④
例题10 1、(2018·台州-20)草酸固体熔点较低,受热熔化后,迅速分解生成水、一氧化碳和二氧化碳。
(1)草酸(H2C2O4)中,氢、碳氧原子的个数比为 。
(2)写出草酸受热分解的化学方程式: 。
(3)加热分解草酸固体,应选择图中的 装置。
/
2、(2018·宁波-28,改编)丁酸乙脂是无色有菠萝香味的液体,其密度为0. 87g/cm3,难溶于水,可与油类互溶。现取11.6g丁酸乙脂在氧气中完全燃烧,只产生26.4gCO2和10.8gH2O。
(1)根据计算,推断丁酸乙酯中一定含有的元素是______________。
(2)丁酸乙脂中碳元素和氢元素的质量比为 。
例题11 关于混合物的化学方程式的2道经典计算,学会分析图表(数形结合)。
1、某校九年级综合实践活动小组的同学用一定量的溶质质量分数为10%的过氧化氢溶液和二氧化锰来制取氧气,最后所得气体质量与时间的关系如图所示。请计算:
(1) 完全反应后生成氧气的质量是多少?
(2) 所用过氧化氢溶液的质量是多少?
2、我市盛产石灰石,主要成分是CaCO3。某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验。取一定量的石灰石样品研碎和100g溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录数据如下表:(假设反应匀速进行;杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25g。)
反应时间/s
20
40
60
80
100
烧杯和药品质量/g
137.8
135.6
m
134.5
134.5
请计算:
(1) 表中的“m”为________g。
(2) 该石灰石样品中碳酸钙的质量分数。(结果精确至0.1%)
化学入门知识的复习:化学用语与化学计算
一、构成物质的微粒
学习目标:务必掌握常见物质是由什么微粒构成的。
1、构成物质的微粒之间的关系(逻辑图)
【归纳总结】分子与原子的关系:
离子与原子的关系:
2、常见物质的构成微粒
(1)由原子直接构成的物质有:
①______________________________________;
②__________________________________________;
③____________________________。
(2)由离子构成的物质:目前所学的有_____________。
(3)其他物质(大多数)是由__________构成的:物质一般由分子构成。
3、物质的化学性质是由直接构成物质的微粒保持的。
例题1 (1)水的化学性质是由_____________保持的;氯化钠的化学性质是由______________保持的。
(2)CO有毒,而CO2无毒,原因是它们___________________________。
(3)金刚石和石墨都是由________构成的,所以它们的_________性质相似;而金刚石硬度大、不导电,石墨质软,是导体,说明它们的________性质不同,微观原因是它们___________________________。
变式训练 已知由同种元素组成的不同种单质,互称为同素异形体。例如金刚石和石墨是同素异形体,红磷和白磷也是同素异形体。已知铁有δ-Fe、γ-Fe、α-Fe三种同素异形体(如下图)。三种晶体在不同温度下能发生以下转化。/下列有关说法正确的是( )
A.δ-Fe、γ-Fe、α-Fe之间的相互转化是化学变化
B.δ-Fe、γ-Fe、α-Fe一定不属于同种元素
C.δ-Fe、γ-Fe、α-Fe属于同种物质
D.δ-Fe、γ-Fe、α-Fe三种铁单质的性质都相同
4、元素与原子的区别
比较项目
元素
原子
概念
元素是具有相同核电荷数的同一类原子的总称。
原子是化学变化中的最小微粒。
区别
元素着眼于种类不表示个数,没有数量多少的含义。
原子既表示种类又讲个数,有数量的含义。
使用领域
元素是用来描述物质的宏观组成(习惯上说组成),如:水里含有氢元素和氧元素,水是由氢元素和氧元素组成的。但不能说“水是由二个氢元素和一个氧元素所组成的”。
原子是用来描述物质的微观构成(习惯上说构成),如:一个水分子是由两个氢原子和一个氧原子构成的。但不能说“一个水分子是由氢元素和氧元素所组成。”
联系
元素是同一类原子的总称;原子是构成元素的基本单元。
例题2 有水(H2O)、双氧水(H2O2)、重水(D2O,“D”表示原子核中有一个质子和一个中子的氢原子)三种物质,从物质组成的角度看,这三种物质所含的元素共有______种,从化学性质的角度看,_________与水的化学性质有较大的差异。等质量的H2O和D2O,所含中子数之比为_______________。
5、关于原子的结构模型发展史(科学史):
模型图示
/
/
/
/
/
提出者
道尔顿
玻尔
薛定谔
模型名称
枣糕模型
电子云模型
6、原子的内部结构:
7、关于物质的分类(完成填空)
/
例题3 下列分别盛有不同物质的容器中,所盛物质属于纯净物的是_________,混合物的是_________,单质的是__________,化合物的是__________。(均填容器代号)
/
变式训练 判断下列物质属于纯净物还是混合物,用序号填空。
①液氧;②石蜡;③青铜;④干冰;⑤稀有气体;⑥糖水;⑦三氯化磷;⑧水银;⑨医用酒精;⑩水蒸气;?铜矿石;?KMnO4制O2反应完后的剩余固体
(1)其中纯净物是:__________;混合物是:__________。
(2)请写出其中纯净物的化学式______________________________。
例题4 (2018·杭州-1)南京理工大学胡炳成团队用新方法制得了NaN5?3H2O,该化合物中含有N5-等微粒,已知N为7号元素,则下列有关说法正确的是( )
A﹒N5-是一种单质 B﹒1 个N5- 带一个单位的正电荷
C﹒1 个N5-共含有 35 个质子 D﹒1 个N5-中共含有 35 个电子
二、化学用语
1、元素符号(必记):1~20号元素,需要掌握序数、符号和中文名称。常见元素铁、铜、金、银、汞、锌等只需掌握名称与符号对应起来。
2、常见的原子团符号(必记)
名称
符号
化合价
名称
符号
化合价
铵根离子
硝酸根离子
碳酸根离子
硫酸根离子
碳酸氢根离子
氢氧根离子
3、常见元素化合价(口诀,必记)
钾钠银氢正一价
钙镁钡锌正二价
氟氯溴碘(卤)负一价
通常氧是负二价
铜正一二、铝正三
铁有正二和正三
注意:(1)H2O2中氧元素的化合价是________;
(2)氟氯溴碘同为一族,被称为卤族元素,只有在卤化物中,卤族元素才是-1价。
(3)正一价铜是亚铜,正二价铁是亚铁。
例题5 (1)标出下列物质中氯元素的化合价。
NaCl Cl2 HClO KClO3 KClO4
(2)写出下列物质的化学式。
①硫酸铁:__________________; ②氢氧化亚铁:__________________;
③碳酸铵:__________________; ④碳酸氢铵:__________________。
三、化学计算
(一)化学式有关的计算——元素质量比、相对分子质量、质量分数的有关计算
例题6 (2018·金丽-5)如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是( )
A.苯分子由碳、氢两种元素组成
B.苯中氢元素的质量分数小于10%
C.六氯苯中碳氯两种元素的质量比为1∶1
D.六氯苯由6个碳原子和6个氯原子构成
例题7 A、B两种元素的相对原子质量之比为7∶2,它们组成的一种化合物,A、B两种元素的质量比为21∶8,则该化合物的化学式可表示为( )
A. A3B4 B. AB2 C. A2B D. A2B2
例题8 通常状况下某NH4NO3晶体的样品中,测得其中氮元素的质量分数为38%,那么该样品所含的杂质在下列物质中可能是( )
A. NH4Cl B. N2 C. (NH4)2SO4 D. CO(NH2)2
(二)质量守恒定律及化学方程式的书写与计算
例题9 下列关于化学反应“X2+3Y2===2Z”的叙述,错误的是( )
① Z的化学式为XY3
② 若m gX2和n gY2恰好完全反应,则生成(m+n)g Z
③ 若X2和Y2的相对分子质量分别为M和N,则Z的相对分子质量为(M+N)
④ 若a gX2完全反应生成b gZ,则同时消耗(a-b)g Y2
A. ①② B. ①③ C. ②④ D. ③④
例题10 1、(2018·台州-20)草酸固体熔点较低,受热熔化后,迅速分解生成水、一氧化碳和二氧化碳。
(1)草酸(H2C2O4)中,氢、碳氧原子的个数比为 。
(2)写出草酸受热分解的化学方程式: 。
(3)加热分解草酸固体,应选择图中的 装置。
/
2、(2018·宁波-28,改编)丁酸乙脂是无色有菠萝香味的液体,其密度为0. 87g/cm3,难溶于水,可与油类互溶。现取11.6g丁酸乙脂在氧气中完全燃烧,只产生26.4gCO2和10.8gH2O。
(1)根据计算,推断丁酸乙酯中一定含有的元素是______________。
(2)丁酸乙脂中碳元素和氢元素的质量比为 。
例题11 关于混合物的化学方程式的2道经典计算,学会分析图表(数形结合)。
1、某校九年级综合实践活动小组的同学用一定量的溶质质量分数为10%的过氧化氢溶液和二氧化锰来制取氧气,最后所得气体质量与时间的关系如图所示。请计算:
(1) 完全反应后生成氧气的质量是多少?
(2) 所用过氧化氢溶液的质量是多少?
2、我市盛产石灰石,主要成分是CaCO3。某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验。取一定量的石灰石样品研碎和100g溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录数据如下表:(假设反应匀速进行;杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25g。)
反应时间/s
20
40
60
80
100
烧杯和药品质量/g
137.8
135.6
m
134.5
134.5
请计算:
(1) 表中的“m”为________g。
(2) 该石灰石样品中碳酸钙的质量分数。(结果精确至0.1%)
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
