必修一 第一章 第一节 化学实验基本方法(43张)
文档属性
| 名称 | 必修一 第一章 第一节 化学实验基本方法(43张) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-08-06 00:00:00 | ||
图片预览










文档简介
(共43张PPT)
化学必修1
第一章 从实验学化学
化学是什么
化学的作用和地位
1.化学是解决食物短缺问题的主要学科之一
2.化学在能源和资源的合理开发和高效安全利用中起关键作用
3.化学推动材料科学发展
4.化学是提高人类生存质量和生存安全的有效保障
化学学习的方法
重视化学实验
重视学习的过程与方法
注意合作学习及自我评价
做好笔记和复习
高中化学结构
化
学
1
化
学
2
化学与生活
化学与技术
物质结构与性质
化学反应原理
有机化学基础
实 验 化 学
化学在高考中的地位及今后的就业方向
1、高考地位:
6选3不选择化学的同学高二要通过化学学业水平测试
6选3选择化学的同学高考要考化学
2、就业方向
科研及高新技术方向
工农生产、环境、医疗、教育、公务员
等
新闻报道:X年X月X日,陕西富平县薛镇初中初三(1)班学生在上化学实验课时,由于学生操作失误造成意外,8名学生被炸伤。
据富平县薛镇初三(1)班一学生介绍,当天上午,他们班在上化学实验课时,老师要求学生做“高锰酸钾制氧”实验,十余名同学围成一组,开始动起手来。其中一名学生在添加药品时,操作失误,用量过多,造成正在加热的化学试管爆炸破裂,周围8名同学不同程度受了伤。
一、化学实验安全 1、遵守实验室规则 2、了解安全措施 3、掌握正确的操作方法
4、重视并逐步熟悉污染物和废弃物的处理方法
1.遵守实验室规则
(1)实验前预习;
(2)严格按照老师要求做实验,并且实保持安静;
(3)实验结束要清洗仪器,搞好卫生。
2.了解安全措施
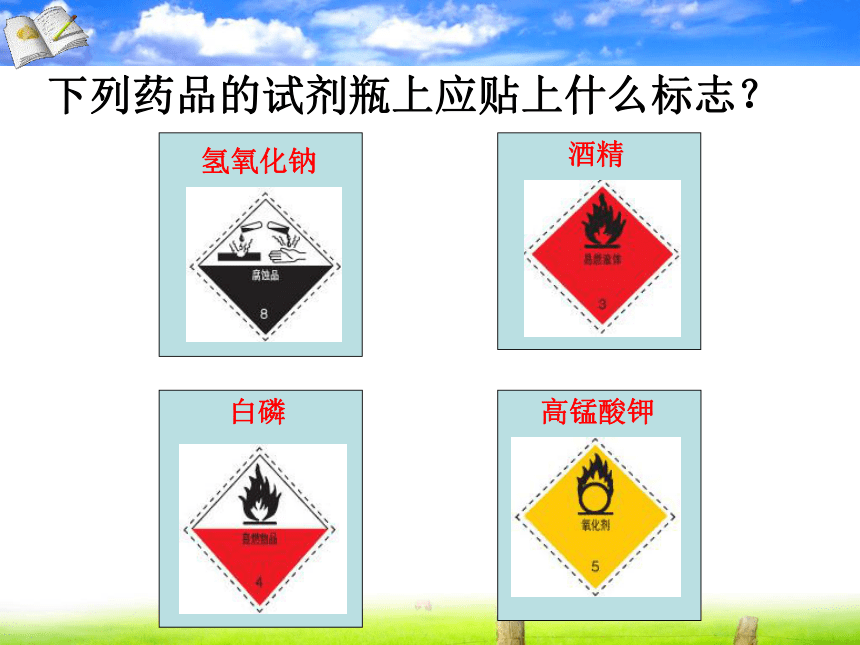
(1)学会识别常用危险化学品的标志;
一些常用危险化学品的标志
下列药品的试剂瓶上应贴上什么标志?
氢氧化钠
酒精
白磷
高锰酸钾
(2)了解实验室一般事故的处理方法
思考与讨论:
1.若不慎将浓硫酸沾在皮肤上,应如何处理?
2.若不慎将浓氢氧化钠沾在手上应如何处理?
3.燃着的酒精洒在实验台上,如何处理?
先用干抹布擦干,然后用大量水冲洗,再用3%-5%的NaHCO3溶液冲洗
立即用大量水冲洗,再涂上硼酸溶液
用湿抹布扑灭
3.掌握正确的操作方法
药品的取用
(1)药品取用三忌。
不能用手 药品,不要把鼻孔凑到容器口去 气体,不得 药品的味道。
(2)药品用量。
无说明,液体取 mL,固体 。
(3)操作步骤。
取粉用 ,试管 ,药匙送管底,试管再竖起。取块状用 夹,试管横放,送入试管中,倾斜往下滑。
接触
闻
1-2
尝
盖满试管底
镊子
横放
药匙/纸槽
(4)液体药品的取用。
简记为:瓶盖 ,标签 ,瓶口挨管口,药液沿壁流。
物质的溶解
浓硫酸的稀释:必须把 沿烧杯壁慢慢注入水中,边加边 。
物质的加热
加热时,受热容器外壁不能有 ,试管加热前要先 。给试管里的固体加热,应将管口 。液体加热,体积不能超过试管容积的 。
浓硫酸
向手心
朝上
1/3
向下倾斜
预热
水
搅拌
酒精灯的使用
托盘天平的使用
遵循左 右 。
4.重视并逐步熟悉污染物和废弃物的处理方法
物
码
二、混合物的分离和提纯
思考与交流(课本P5 ):
淘金者是利用什么方法和性质将金子从沙里分出来?
方法:用水冲洗
利用性质:物质的密度不同
思考与交流(课本P5 ):
铁屑和沙子怎么分离?
方法:用磁铁
利用性质:铁有磁性
过滤
烧杯、铁架台、漏斗、
玻璃棒、滤纸。
★用到的仪器、用品:
“一贴”:滤纸紧贴漏斗内壁,中间无气泡
“二低”:①滤纸的边缘低于漏斗口;
②漏斗里的液体低于滤纸边缘。
“三靠”:①倾倒液体的烧杯尖口要紧靠玻璃棒。
②玻璃棒的一端要靠在三层滤纸的一侧
③漏斗的下端(尖嘴部分)要紧靠烧杯内壁
蒸发
★仪器:
蒸发皿、玻璃棒、酒精灯、三角架(或铁架台带铁圈)
①液体量不超过2/3
②玻璃棒不断搅拌
③剩余少量水或析出较
多量固体时,停止加热
思考1:通过上述操作得到的是比较纯净的氯化钠吗?可能还有什么杂质没有除去?
粗盐中含有的杂质:MgCl2、CaCl2以及一些硫酸盐。
提问:怎样来检验粗盐中可能含的硫酸盐杂质呢?
检验原则:产生明显现象(溶液颜色变化、沉淀、气体)
思考2:能否将检测试剂一次加入全部加待检验试样或配好的试样溶液中?为什么?
不能。防止一次检验失败而需要重作实验时,无试样可用;检验会引入杂质,试样不能做其它用途。
提问:通过上述实验可知粗盐中含有硫酸盐杂质,除了硫酸盐以外,还含有可溶性杂质CaCl2、MgCl2,那么怎样才能将这些杂质除去,而得到纯净的食盐呢?
1.易分:一般将杂质转为沉淀、气体或水,使之易与主要物质分离;
2.过量:除杂试剂过量,完全除尽杂质;
3.不减:不能减少主要物质(一般加入的试剂只与杂质发生反应);
4.无新:即最后结果没有引入新的物质;
5.顺序:加入除杂试剂要考虑顺序。
化学方法除杂的主要原则
除去粗盐中可溶性杂质:
杂? 质 加入的试剂 化学方程式
硫酸盐 BaCl2 BaCl2+Na2SO4=BaSO4↓+2NaCl
MgCl2 NaOH MgCl2+2NaOH=Mg(OH)2↓+2NaCl
CaCl2 Na2CO3 CaCl2+Na2CO3=CaCO3↓+2NaCl
食盐水中Na2SO4、CaCl2等
分离提纯混合物
除去食盐水中的泥沙
NaCl溶液中除去水
过滤
②可溶性杂质
①不溶性杂质
转化法——先沉淀、再过滤
蒸发
③溶质与溶剂的分离
粗盐的提纯
步? 骤 现? 象
? (1)溶解:称取约4 g粗盐加到盛有约12 mL 水的烧杯中,边加边用玻璃棒搅拌,直至粗盐不再溶解为止 ? 固体食盐逐渐溶解而减少,食盐水略显浑浊
? (2)过滤: 将烧杯中的液体沿玻璃棒倒入过滤器中, 过滤器中的液面不能超过滤纸的边缘。 若滤液浑浊,再过滤一次 ? 不溶物留在滤纸上,液体渗过滤纸,沿漏斗颈流入另一个烧杯中
? (3)蒸发:将滤液倒入蒸发皿中,然后用酒精灯加热,同时用玻璃棒不断搅拌溶液,待出现较多固体时停止加热 ? 水分蒸发,逐渐析出固体
蒸馏
定义:将液态物质加热到沸腾变成蒸气,又将蒸气冷凝为液体这两个过程的联合操作。
所用仪器:
酒精灯
蒸馏烧瓶
温度计
冷凝管
牛角管/承接管
锥形瓶
操作要点:
隔网加热冷管倾,上缘下缘两相平。需加碎瓷防暴沸,热气冷水逆向行。
上口出
下口进
①液体量:1/3—2/3
不得将液体全蒸干
先通冷凝水,再加热;先停热,后停冷凝水
其它:
分液
分液漏斗、
铁架台、
烧杯
1.定义:利用溶质在互不相溶的溶剂里溶解度不同,用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来。
萃取
步骤:
1、检漏;2、关闭活塞倒原溶液;3、加萃取剂;
4、用力振荡(注意分液漏斗的操作姿势和双手握法);
5、铁圈上静置,分层为止;
6、分液(打开玻璃塞,便于液体顺利流下。分液时控制活塞)
实验 用CCl4萃取碘水(饱和)
从碘水中萃取碘能否用酒精作为萃取剂?请说明原因
不可以,酒精与水互溶
练一练:
1.下列物质不能用于萃取碘水中的碘的是( )
A.四氯化碳 b.苯 C.汽油 D.酒精
D
2.在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。
答:取一支小试管,打开分液漏斗的活塞,慢慢放出少量液体,往其中加入少量水,如果加水后,试管中的液体不分层,说明分液漏斗中,下层是“水层”,反之,则上层是水层。
除去食盐水中的泥沙
NaCl溶液中除去水
过滤
②溶质与溶剂的分离
①不溶性杂质
蒸发
③沸点不同的两种混合物
海水淡化
蒸馏
④在两种互不相溶的溶剂中溶解度相差很大
⑤互不相溶的两种液态混合物
碘水中提取碘
萃取
分液
四氯化碳和水的混合物、油和水的混合物
混合物的分离与提纯
常见离子检验
SO
4
2-
(硫酸和可溶性硫酸盐)
1、
为什么加入盐酸?是否可以用硫酸或硝酸代替盐酸?
为什么加入稀硝酸?是否可以用硫酸或盐酸代替?
1.下列仪器:
①漏斗;②蒸发皿;③托盘天平;④分液漏斗;⑤蒸馏烧瓶;⑥量筒;⑦燃烧匙。常用于物质分离的是 ( )
A.①②⑤⑥ B.①②④⑤
C.②③⑤⑥ D.③④⑥⑦
B
2.对下列各组物质:
①NaNO3和NaCl; ②CaCl2和CaCO3;
③MnO2和KCl; ④BaSO4和AgCl。
可按照溶解、过滤、蒸发的实验操作顺序,将它们相互分离的是( )
A.只有① B.③④
C.②③ D.②④
C
3.实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯②固定铁圈的位置③放上蒸发皿④加热搅拌⑤停止加热、余热蒸干,其正确的操作顺序是 ( )
A.①②③④ B.①②③④⑤ C.②③①④⑤ D.②①③④⑤
B
4.已知丙酮通常是无色的液体,不溶于水,密度小于1g/ml,沸点约为55 ℃ 。要从水与丙酮的混合物里将丙酮分离出来,下列方法中最合理的是 ( )
A.蒸馏 B.分液 C.过滤 D.蒸发
B
5.下列所采取的分离方法正确的是 ( )
A.由于碘在乙醇中的溶解度大,所以可用乙醇将碘水中的碘萃取出来
B.水的沸点是100℃ ,酒精的沸点是78.5℃ ,所以可用直接加热蒸馏法使含水酒精变为无水酒精
C.可用冷却热的饱和硝酸钾和氯化钠溶液的方法得到纯净的硝酸钾晶体
C
6.用CCl4萃取碘的饱和水溶液中的碘,下列说法中不正确的是 ( )
A.实验使用的主要仪器是分液漏斗
B.碘在四氯化碳中的溶解度比在水中的溶解度大
C.碘的四氯化碳溶液呈紫(红)色
D.分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗口倒出
D
7.下列离子检验的方法正确的是( )
A.某溶液
生产白色沉淀,说明原溶液中有Cl-
B.某溶液
生产白色沉淀,说明原溶液中有SO42-
C.某溶液
生产蓝色沉淀,说明原溶液中有Cu2+
D. 某溶液
生成无色气体,说明原溶液中有CO32-
C
8.某化学课外小组用海带为原料制取少量碘水,现用CCl4,从碘水中萃取碘并用分液漏斗分离两种溶液。其实验可分解为如下各步:
A. 把盛有溶液的分液漏斗放在铁架台的铁圈中;
B. 把50mL碘水和15 mLCCl4加入分液漏斗中,并盖好玻璃塞;
C. 检验分液漏斗活塞和上口的玻璃塞是否漏液:
D. 倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞.把分液漏斗放正;
E. 旋开活塞,用烧杯接收溶液,
F. 从分液漏斗上口倒出上层水溶液,
G. 将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置,分层。
就此实验完成F列填空:
1.正确操作步骤的顺序是(用上述各操作的编号字母填写)
→ → →A→G → →E → F
(2)上述E步骤的操作中应注意------------------------------------------------
上述G步骤操作目的是-----------------------------------------------------------------------------
(3)能选用CCl4,从碘水中萃取碘的原因是-----------------------------------
使漏斗下端管口紧靠烧杯内壁,及时关闭活塞,不要让上层液体流出.
使漏斗内外空气相通,以保证进行E 操作时,漏斗里液体能够流出.
CCl4 和碘不反应,CCl4与水互不相溶,而且碘在CCl4中的溶解度比水中的大很多
C
B
D
H
化学必修1
第一章 从实验学化学
化学是什么
化学的作用和地位
1.化学是解决食物短缺问题的主要学科之一
2.化学在能源和资源的合理开发和高效安全利用中起关键作用
3.化学推动材料科学发展
4.化学是提高人类生存质量和生存安全的有效保障
化学学习的方法
重视化学实验
重视学习的过程与方法
注意合作学习及自我评价
做好笔记和复习
高中化学结构
化
学
1
化
学
2
化学与生活
化学与技术
物质结构与性质
化学反应原理
有机化学基础
实 验 化 学
化学在高考中的地位及今后的就业方向
1、高考地位:
6选3不选择化学的同学高二要通过化学学业水平测试
6选3选择化学的同学高考要考化学
2、就业方向
科研及高新技术方向
工农生产、环境、医疗、教育、公务员
等
新闻报道:X年X月X日,陕西富平县薛镇初中初三(1)班学生在上化学实验课时,由于学生操作失误造成意外,8名学生被炸伤。
据富平县薛镇初三(1)班一学生介绍,当天上午,他们班在上化学实验课时,老师要求学生做“高锰酸钾制氧”实验,十余名同学围成一组,开始动起手来。其中一名学生在添加药品时,操作失误,用量过多,造成正在加热的化学试管爆炸破裂,周围8名同学不同程度受了伤。
一、化学实验安全 1、遵守实验室规则 2、了解安全措施 3、掌握正确的操作方法
4、重视并逐步熟悉污染物和废弃物的处理方法
1.遵守实验室规则
(1)实验前预习;
(2)严格按照老师要求做实验,并且实保持安静;
(3)实验结束要清洗仪器,搞好卫生。
2.了解安全措施
(1)学会识别常用危险化学品的标志;
一些常用危险化学品的标志
下列药品的试剂瓶上应贴上什么标志?
氢氧化钠
酒精
白磷
高锰酸钾
(2)了解实验室一般事故的处理方法
思考与讨论:
1.若不慎将浓硫酸沾在皮肤上,应如何处理?
2.若不慎将浓氢氧化钠沾在手上应如何处理?
3.燃着的酒精洒在实验台上,如何处理?
先用干抹布擦干,然后用大量水冲洗,再用3%-5%的NaHCO3溶液冲洗
立即用大量水冲洗,再涂上硼酸溶液
用湿抹布扑灭
3.掌握正确的操作方法
药品的取用
(1)药品取用三忌。
不能用手 药品,不要把鼻孔凑到容器口去 气体,不得 药品的味道。
(2)药品用量。
无说明,液体取 mL,固体 。
(3)操作步骤。
取粉用 ,试管 ,药匙送管底,试管再竖起。取块状用 夹,试管横放,送入试管中,倾斜往下滑。
接触
闻
1-2
尝
盖满试管底
镊子
横放
药匙/纸槽
(4)液体药品的取用。
简记为:瓶盖 ,标签 ,瓶口挨管口,药液沿壁流。
物质的溶解
浓硫酸的稀释:必须把 沿烧杯壁慢慢注入水中,边加边 。
物质的加热
加热时,受热容器外壁不能有 ,试管加热前要先 。给试管里的固体加热,应将管口 。液体加热,体积不能超过试管容积的 。
浓硫酸
向手心
朝上
1/3
向下倾斜
预热
水
搅拌
酒精灯的使用
托盘天平的使用
遵循左 右 。
4.重视并逐步熟悉污染物和废弃物的处理方法
物
码
二、混合物的分离和提纯
思考与交流(课本P5 ):
淘金者是利用什么方法和性质将金子从沙里分出来?
方法:用水冲洗
利用性质:物质的密度不同
思考与交流(课本P5 ):
铁屑和沙子怎么分离?
方法:用磁铁
利用性质:铁有磁性
过滤
烧杯、铁架台、漏斗、
玻璃棒、滤纸。
★用到的仪器、用品:
“一贴”:滤纸紧贴漏斗内壁,中间无气泡
“二低”:①滤纸的边缘低于漏斗口;
②漏斗里的液体低于滤纸边缘。
“三靠”:①倾倒液体的烧杯尖口要紧靠玻璃棒。
②玻璃棒的一端要靠在三层滤纸的一侧
③漏斗的下端(尖嘴部分)要紧靠烧杯内壁
蒸发
★仪器:
蒸发皿、玻璃棒、酒精灯、三角架(或铁架台带铁圈)
①液体量不超过2/3
②玻璃棒不断搅拌
③剩余少量水或析出较
多量固体时,停止加热
思考1:通过上述操作得到的是比较纯净的氯化钠吗?可能还有什么杂质没有除去?
粗盐中含有的杂质:MgCl2、CaCl2以及一些硫酸盐。
提问:怎样来检验粗盐中可能含的硫酸盐杂质呢?
检验原则:产生明显现象(溶液颜色变化、沉淀、气体)
思考2:能否将检测试剂一次加入全部加待检验试样或配好的试样溶液中?为什么?
不能。防止一次检验失败而需要重作实验时,无试样可用;检验会引入杂质,试样不能做其它用途。
提问:通过上述实验可知粗盐中含有硫酸盐杂质,除了硫酸盐以外,还含有可溶性杂质CaCl2、MgCl2,那么怎样才能将这些杂质除去,而得到纯净的食盐呢?
1.易分:一般将杂质转为沉淀、气体或水,使之易与主要物质分离;
2.过量:除杂试剂过量,完全除尽杂质;
3.不减:不能减少主要物质(一般加入的试剂只与杂质发生反应);
4.无新:即最后结果没有引入新的物质;
5.顺序:加入除杂试剂要考虑顺序。
化学方法除杂的主要原则
除去粗盐中可溶性杂质:
杂? 质 加入的试剂 化学方程式
硫酸盐 BaCl2 BaCl2+Na2SO4=BaSO4↓+2NaCl
MgCl2 NaOH MgCl2+2NaOH=Mg(OH)2↓+2NaCl
CaCl2 Na2CO3 CaCl2+Na2CO3=CaCO3↓+2NaCl
食盐水中Na2SO4、CaCl2等
分离提纯混合物
除去食盐水中的泥沙
NaCl溶液中除去水
过滤
②可溶性杂质
①不溶性杂质
转化法——先沉淀、再过滤
蒸发
③溶质与溶剂的分离
粗盐的提纯
步? 骤 现? 象
? (1)溶解:称取约4 g粗盐加到盛有约12 mL 水的烧杯中,边加边用玻璃棒搅拌,直至粗盐不再溶解为止 ? 固体食盐逐渐溶解而减少,食盐水略显浑浊
? (2)过滤: 将烧杯中的液体沿玻璃棒倒入过滤器中, 过滤器中的液面不能超过滤纸的边缘。 若滤液浑浊,再过滤一次 ? 不溶物留在滤纸上,液体渗过滤纸,沿漏斗颈流入另一个烧杯中
? (3)蒸发:将滤液倒入蒸发皿中,然后用酒精灯加热,同时用玻璃棒不断搅拌溶液,待出现较多固体时停止加热 ? 水分蒸发,逐渐析出固体
蒸馏
定义:将液态物质加热到沸腾变成蒸气,又将蒸气冷凝为液体这两个过程的联合操作。
所用仪器:
酒精灯
蒸馏烧瓶
温度计
冷凝管
牛角管/承接管
锥形瓶
操作要点:
隔网加热冷管倾,上缘下缘两相平。需加碎瓷防暴沸,热气冷水逆向行。
上口出
下口进
①液体量:1/3—2/3
不得将液体全蒸干
先通冷凝水,再加热;先停热,后停冷凝水
其它:
分液
分液漏斗、
铁架台、
烧杯
1.定义:利用溶质在互不相溶的溶剂里溶解度不同,用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来。
萃取
步骤:
1、检漏;2、关闭活塞倒原溶液;3、加萃取剂;
4、用力振荡(注意分液漏斗的操作姿势和双手握法);
5、铁圈上静置,分层为止;
6、分液(打开玻璃塞,便于液体顺利流下。分液时控制活塞)
实验 用CCl4萃取碘水(饱和)
从碘水中萃取碘能否用酒精作为萃取剂?请说明原因
不可以,酒精与水互溶
练一练:
1.下列物质不能用于萃取碘水中的碘的是( )
A.四氯化碳 b.苯 C.汽油 D.酒精
D
2.在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。
答:取一支小试管,打开分液漏斗的活塞,慢慢放出少量液体,往其中加入少量水,如果加水后,试管中的液体不分层,说明分液漏斗中,下层是“水层”,反之,则上层是水层。
除去食盐水中的泥沙
NaCl溶液中除去水
过滤
②溶质与溶剂的分离
①不溶性杂质
蒸发
③沸点不同的两种混合物
海水淡化
蒸馏
④在两种互不相溶的溶剂中溶解度相差很大
⑤互不相溶的两种液态混合物
碘水中提取碘
萃取
分液
四氯化碳和水的混合物、油和水的混合物
混合物的分离与提纯
常见离子检验
SO
4
2-
(硫酸和可溶性硫酸盐)
1、
为什么加入盐酸?是否可以用硫酸或硝酸代替盐酸?
为什么加入稀硝酸?是否可以用硫酸或盐酸代替?
1.下列仪器:
①漏斗;②蒸发皿;③托盘天平;④分液漏斗;⑤蒸馏烧瓶;⑥量筒;⑦燃烧匙。常用于物质分离的是 ( )
A.①②⑤⑥ B.①②④⑤
C.②③⑤⑥ D.③④⑥⑦
B
2.对下列各组物质:
①NaNO3和NaCl; ②CaCl2和CaCO3;
③MnO2和KCl; ④BaSO4和AgCl。
可按照溶解、过滤、蒸发的实验操作顺序,将它们相互分离的是( )
A.只有① B.③④
C.②③ D.②④
C
3.实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯②固定铁圈的位置③放上蒸发皿④加热搅拌⑤停止加热、余热蒸干,其正确的操作顺序是 ( )
A.①②③④ B.①②③④⑤ C.②③①④⑤ D.②①③④⑤
B
4.已知丙酮通常是无色的液体,不溶于水,密度小于1g/ml,沸点约为55 ℃ 。要从水与丙酮的混合物里将丙酮分离出来,下列方法中最合理的是 ( )
A.蒸馏 B.分液 C.过滤 D.蒸发
B
5.下列所采取的分离方法正确的是 ( )
A.由于碘在乙醇中的溶解度大,所以可用乙醇将碘水中的碘萃取出来
B.水的沸点是100℃ ,酒精的沸点是78.5℃ ,所以可用直接加热蒸馏法使含水酒精变为无水酒精
C.可用冷却热的饱和硝酸钾和氯化钠溶液的方法得到纯净的硝酸钾晶体
C
6.用CCl4萃取碘的饱和水溶液中的碘,下列说法中不正确的是 ( )
A.实验使用的主要仪器是分液漏斗
B.碘在四氯化碳中的溶解度比在水中的溶解度大
C.碘的四氯化碳溶液呈紫(红)色
D.分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗口倒出
D
7.下列离子检验的方法正确的是( )
A.某溶液
生产白色沉淀,说明原溶液中有Cl-
B.某溶液
生产白色沉淀,说明原溶液中有SO42-
C.某溶液
生产蓝色沉淀,说明原溶液中有Cu2+
D. 某溶液
生成无色气体,说明原溶液中有CO32-
C
8.某化学课外小组用海带为原料制取少量碘水,现用CCl4,从碘水中萃取碘并用分液漏斗分离两种溶液。其实验可分解为如下各步:
A. 把盛有溶液的分液漏斗放在铁架台的铁圈中;
B. 把50mL碘水和15 mLCCl4加入分液漏斗中,并盖好玻璃塞;
C. 检验分液漏斗活塞和上口的玻璃塞是否漏液:
D. 倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞.把分液漏斗放正;
E. 旋开活塞,用烧杯接收溶液,
F. 从分液漏斗上口倒出上层水溶液,
G. 将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置,分层。
就此实验完成F列填空:
1.正确操作步骤的顺序是(用上述各操作的编号字母填写)
→ → →A→G → →E → F
(2)上述E步骤的操作中应注意------------------------------------------------
上述G步骤操作目的是-----------------------------------------------------------------------------
(3)能选用CCl4,从碘水中萃取碘的原因是-----------------------------------
使漏斗下端管口紧靠烧杯内壁,及时关闭活塞,不要让上层液体流出.
使漏斗内外空气相通,以保证进行E 操作时,漏斗里液体能够流出.
CCl4 和碘不反应,CCl4与水互不相溶,而且碘在CCl4中的溶解度比水中的大很多
C
B
D
H
