4.1 质量守恒定律同步练习
图片预览


文档简介
4.3质量守恒定律—专题(1)
一、选择题
1.下列各项:①物质种类②物质的总质量③元素种类④分子种类⑤分子数目⑥原子种类⑦原子数目,在化学反应前后,肯定没有变化的是( )
A.①②⑥⑦ B.②③④⑥⑦ C.②③⑤⑥⑦ D.②③⑥⑦
2.下列事实不能用质量守恒定律来解释的是 ( )
A 镁带在空气中燃烧后,生成物的质量比镁带质量增加了 B水结成冰
C 煤燃烧后留下的煤灰比煤的质量减轻了 D 用12 g碳作原料可制得44 g二氧化碳
1、下列现象不能用质量守恒定律解释的是 ( )
A.纸燃烧化为灰烬,灰烬的质量比纸的质量小 B.洗衣服晾晒后变轻了
C.铁丝在氧气中燃烧,生成物的质量比铁丝的质量大 D.蜡烛燃烧后质量减小
2、下列“化学反应前后”的叙述不正确的是 ( )
A.物质的质量总和相同 B.元素的种类相同 21世纪教育网
C.物质的分子个数相同 D.原子的个数相同
3、目前有关部门做出决定,司机酒后驾车会受到严惩。交警常用一种“酒精检测仪”检查司机是否酒后驾车。其反应原理为C2H5OH+4CrO3+6H2SO4═2X+2CO2↑+9H2O,反应中红色的CrO3转变为绿色的化合物X,则X的化学式为 21cnjy.com
A.Cr2O3 B.CrSO3 C.Cr2(SO4)3 D.Cr2S3
4.化学反应前后,肯定没有变化的是( )
①原子的数目 ②分子的数目 ③元素的种类 ④物质的总质量 ⑤物质的种类
A.①④ B.①③⑤
C.①③④ D.①②③④⑤
5.我国发射的“嫦娥Ⅰ号”卫星,卫星运载火箭的动力由高氯酸铵(NH4ClO4)分解提供。高氯酸铵分解有可能排入大气的物质是( )
A.H2O B.SO2 C.CO2 D.CO
6、根据质量守恒定律可知:反应2XY+Y2=Z中,Z的化学式为( )
A.XY2 B.X2Y2 C.X2Y4 D.X2Y
7、某物质加热分解产生氧化铜和水。则该物质含有的全部元素是( )
A.Cu、O B.Cu、O、H C.O、H D.Cu、H
8、R在氧气中燃烧的化学方程式为:2R+3O (?http:?/??/?www.21cnjy.com?)2==2CO2+4H2O,则有关R的组成叙述正确的是( )A.只含有碳、氢元素 B.一定含有碳、氢元素,可能含有氧元素
C.一定含有碳、氢、氧元素 D.定含碳、氧元素,可能含有氢元素
9.以下是某两种物质在一定条件下发生化学反应的微观示意图:
(其中和分别表示两种不同的原子)
由图可知,下列说法中正确的是( )
①该反应属于化合反应 ②生成物可能是氧化物 ③反应遵守质量守恒定律 ④反应前后分子和原子种类都不变 ⑤分子在化学变化中可以再分,而原子不能再分
A.①②③⑤ B.①②④⑤
C.①③④⑤ D.①②③④⑤
10.在反应A+B―→C中,1.5 g A与足量B充分反应生成9.5 g C,则参加反应的B的质量为( )
A.3 g B.9.5 g C.8 g D.4 g
11.燃烧法是测定有机物组成的常用方法。某学习小组取一定质量的某有机物在足量氧气中充分燃烧只得到二氧化碳和水。根据质量守恒定律判断该有机物的组成正确的是( )
A.只含有C、H两种元素 B.一定含有C、H两种元素,可能含有O元素
C.含有C、H、O三种元素 D.一定含有C、O两种元素,可能含有H元素
12.下列现象能用质量守恒定律解释的是( )
A.1升芝麻和1升大米混合,总体积小于2升
B.在加压降温的条件下,氧气变为淡蓝色液体 C.水结冰前后质量不变
D.氧化钙与水反应生成氢氧化钙,反应前后物质的总质量不变
二、非选择题
1.某可燃物32 g充分燃烧后,生成44 g CO2和36 g H2O,则可燃物一定含______元素。
2、某化学反应可以用A+B=C+D表示,回答下列问题:
(1)反应前有12gA和8gB,反应后生成10gC,A消耗完全,B剩余2g,则生成D g.
(2)参加化学反应的各物质质量总和为_ _g,反应后生成的各物质质量总和为_____g.
(3) A与B参加反应的质量比为________若24gA完全反应则生成D的质量为 g
3、磷在氧气中完全燃烧生成五氧化二磷。磷、氧气、五氧化二磷的质量比是_______。?
4、若要制取10g铜,?至少需要用____g氧化铜跟过量氢气反应.(保留一位小数)
5、用氢气还原氧化铜,如果氢气的利用率为50%,要得到3.2g铜,需要氢气________g。(保留一位小数)21世纪教育网版权所有
6、12g碳和34g氧气反应后,可得到_______ g二氧化碳.?
7、已知A+B→C+D,现将A、B两种物质各15g,混合后加热,生成16g?C和9g?D测得B已完全反应,则A与B反应物的质量比__________.2·1·c·n·j·y
8、11.2g铁与稀盐酸反应,?生成的气体恰好能跟____g氯气反应生成氯化氢(保留一位小数)?
9、19.5g金属锌与足量的盐酸反应生成的氢气,?全部用来与氧化铜反应,?可还原出____?g铜(保留一位小数)?21教育网
10、用氢气还原氧化铜,如果反应生成了27g水,则剩余固体的质量比原来固体的质量减少________g。?21世纪教育网【来源:21·世纪·教育·网】
?11、在化学反应2A+B=2C+D中,若A的式量为80,B的式量为12,D的式量为?44,则C的式量为_________.21
·4.3质量守恒定律—专题(2) 能力提升
1. 2.3 g某物质在空气中完全燃烧,生成4.4 g二氧化碳和2.7 g水,则该物质中一定含有______元素(填元素符号),其质量比为_________。
2.某物质W在氧气中充分燃烧后,生成了4.4g C02和3.6g H20,消耗氧气的质量为6.4g,下列对w中所含元素的判断正确的是 ( )
A.一定含有C、H元素,不含0元素 D.条件不足,无法判断
B.一定含有C、H元素,可能含有0元素 C.一定含有C、H、0三种元素
3.3.2g某物质在氧气中完全燃烧生成8.8g C02和7.2g H20,关于物质组成的判断有:①一定含有C、H元素②一定含有O元素③可能含有O元素 ④一定不含0元素⑤分子中C、H原子个数比为l:2⑥分子中C、H原子个数比为l: 4。其中正确的 ( )
A.①④⑥ B.①②⑤ C.①③⑤ D.①④⑤
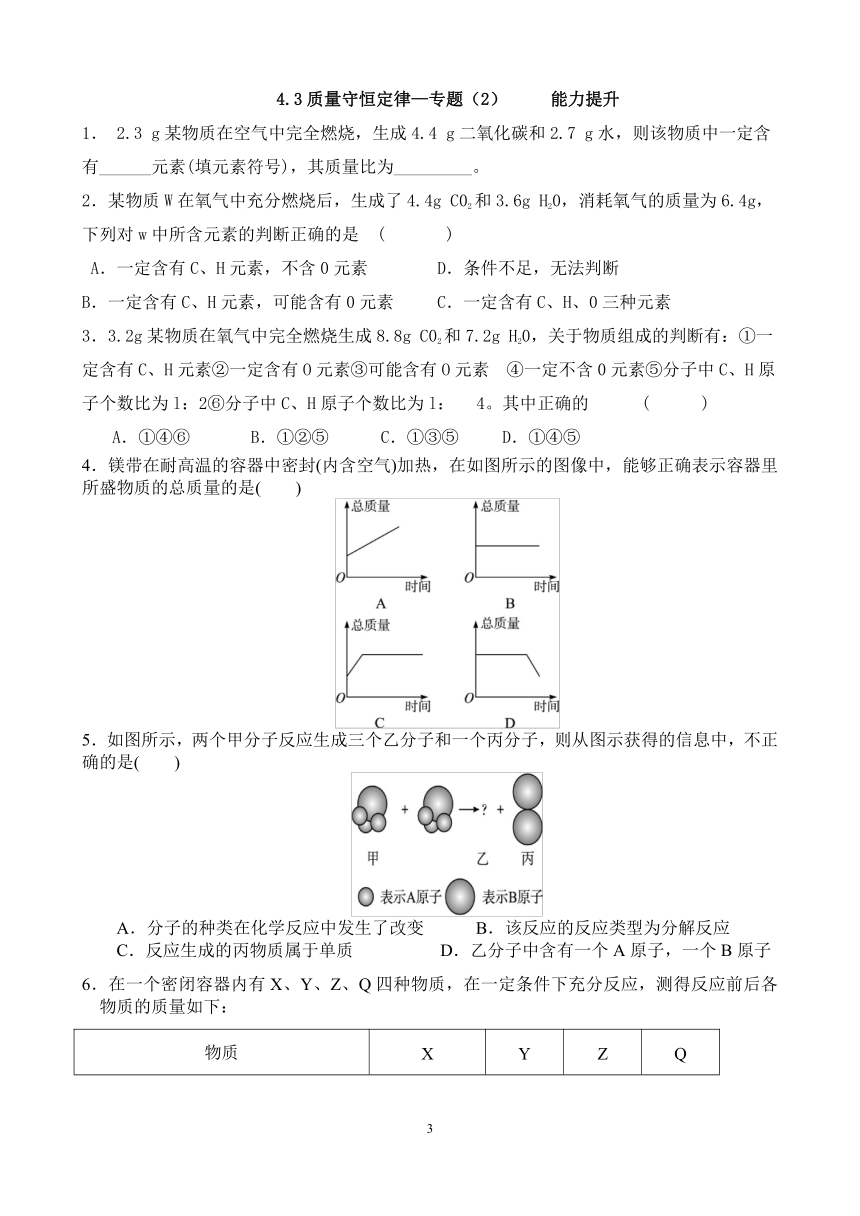
4.镁带在耐高温的容器中密封(内含空气)加热,在如图所示的图像中,能够正确表示容器里所盛物质的总质量的是( )
5.如图所示,两个甲分子反应生成三个乙分子和一个丙分子,则从图示获得的信息中,不正确的是( )
A.分子的种类在化学反应中发生了改变 B.该反应的反应类型为分解反应
C.反应生成的丙物质属于单质 D.乙分子中含有一个A原子,一个B原子
6.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
物质 X Y Z Q
反应前质量/g 2 2 84 5
反应后质量/g 待测 24 0 14
试推断该密闭容器中发生的化学反应基本类型为( )
A.分解反应 B.化合反应 C.置换反应 D.氧化反应
7.在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法错误的是( )
物质 a b c d
反应前质量/g 10 10 10 2
反应后质量/g 待测 2 21 2
A.该反应是化合反应,d可能是催化剂 B.反应后a物质的质量为3 g
C.a、b两种物质中元素种类一定与c物质中元素种类相同 D.b物质可能是单质
8.实验室制取氧气时,在试管中加热一定量高锰酸钾固体,随着反应的发生,纵坐标表示的是( )
A.高锰酸钾的质量 B.氧气的质量
C.锰元素的质量分数 D.固体物质的质量
9.蜡烛(足量)在如下左图密闭的集气瓶内燃烧至熄灭,用仪器测出瓶内氧气含量的变化如下右图所示。下列判断正确的是( )
A.蜡烛燃烧前瓶内只有氧气 B.氧气浓度小于一定值时,蜡烛无法燃烧
C.过程中瓶内物质总质量不断减少 D.蜡烛熄灭后瓶内只剩二氧化碳气体
10.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示:
下列说法正确的是( )
A.丙可能是单质 B.在该反应中丁一定没有参加化学反应
C.该反应是化合反应 D.甲和乙的质量之和一定等于生成丙的质量
11、把A、B、C、D四种纯净物放在密闭容器中,在一定条件下充分反应,反应前后各物质的质量如下表:
物质 A B C D
反应前质量/g 2 24.5 2 1
反应后质量/g 16.9 0 2 未知
回答下列问题:反应后D的质量是_______________g;
C物质可能是_______________(填写“反应物”、“生成物”或“催化剂”);
容器中发生反应的反应类型是__________________(填写基本反应类型)。
12.一定质量的镁条在氧气中完全燃烧后生成氧化镁。固体质量随时间的变化关系如图所示。下列说法不正确的是( )
A.生成MgO的质量:m2 g B.参加反应的Mg的质量:m1 g
C.参加反应的O2的质量:(m2-m1) g
D.参加反应的镁和氧气的质量比:
13、在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表:www.21-cn-jy.com
物质 甲 乙 丙 丁
反应前质量(g) 4 1 42 10
反应后质量(g) 待测 20 6 3121世纪教育网
反应后,甲的“待测”值应为 ( )
A.10 B.8 C.4 D.021世纪教育网
世14.甲、乙、丙、丁四种物质混合后,在一定条件下充分反应,测得反应前后各 物质的质量分数如下表所示。下列说法正确的是 ( )
甲 乙 丙 丁
反应前质量分数% 70 15 6.25 8.75
反应后质量分数% 35 7.5 48.75 8.75
A.丁一定是该反应的催化剂
B.参加反应的甲和乙的质量之和一定等于生成的丙的质量
C.甲一定是化合物,乙一定是单质 D.该反应可能是分解反应。
15.在一密闭容器中加入甲、乙、丙、丁四种物质,在给定条件下发生化学反应, 测得反应前及t1、t2时各物质质量如图所示。下列说法不正确的是 ( )
A.该反应为化合反应 B.丙可能为该反应的催化剂
C.该反应中,乙、丁的质量变化之比为7:5
D.该反应中,甲、乙的质量变化之比为1:4
16.下图所示的四个图像能正确反映对应变化关系的是 ( )
A B C D
A.木炭在密闭的容器内燃烧 B.加热一定量的高锰酸钾制氧气
C.等质量的氯酸钾在有无二氧化锰条件下加热 D.水的电解
4.3质量守恒定律—专题(1)
参考答案
一.选择题
1.B 2.C 3.C 4.C 5.A 6.A 7.B 8.C 9.A 10.C 11.B 12. D
二.非选择题
1.C、H、O 2.(1)8;(2)18(3)2:1、16
3.31:40:70 4.12.5 5.0.2 6.44 7.2:3 8. 14.2 9. 19.2 10.24 11.64
4.3质量守恒定律—专题(2) 能力提升
参考答案
1. C、H、0 12:3:8 22.A 3.D 4.B 5.D 6.D 7.B 8.D 9.B 10.C 11.10.6;催化剂;分解反应。 12.D 13.D 14.B 出15.D 16.A
5.把4 g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示。
? 第一次 第二次 第三次
集气瓶中的氧气的质量(g) 3 4 6
SO2的质量(g) 6 ? ?
剩余S的质量(g) ? ?
请回答下列问题:
(1)第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比是????????????;?
(2)请你通过计算,求出第二次实验生成二氧化硫的质量???? ;?
(3)在表中填写第三次生成的二氧化硫的质量????。
6.加热 mg 高锰酸钾制氧气,反应一段时间后停止加热,试管中残留固体wg,则生成氧气的克数为 ( )
A .等于 m 一 w B.大于 m 一w
C .小于 m 一w D. 不知是否反应完,无法确定生成O2的质量
7.下列关于化学方程式:2H2+O22H2O的读法中不正确的是( )
A. 氢气与氧气在点燃的条件下生成了水 B.两个氢分子加一个氧分子等于两个水分子
C.每4份质量的氢气和32份质量的氧气反应生成36份质量的水
D.每两个氢分子和一个氧分子反应生成两个水分子
2.根据化学方程式4NH3+5O2====4X+6H2O,可推断X的化学式是 ( )
A.NO B.NO2 C.N2O3 D.NH3
5
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
