人教版高中化学必修一第四章第三节硫和氮的氧化物 课件(共23张PPT)
文档属性
| 名称 | 人教版高中化学必修一第四章第三节硫和氮的氧化物 课件(共23张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-08-10 00:00:00 | ||
图片预览








文档简介
(共23张PPT)
问苍天 枯木无言
被污染的树叶
乐山大佛开凿于唐玄宗开元初年(公元713年),为世界第一大石刻弥勒佛,“佛是一座山,山是一尊佛”是其真实写照,请同学们仔细观察,历经千年时间的流逝,是什么物质使大佛鼻翼发黑,佛容暗淡 呢?
1908年 1968年
酸雨横行 雕像何辜
二氧化硫
饮用酸化的地下水危害人类
腐蚀建筑物和工业设备
破坏土壤成分使农作物减产甚至死亡
损坏植物叶面导致森林死亡
破坏露天文物古迹
使湖泊中鱼虾死亡
酸雨的危害:
一. 硫
硫是一种重要的非金属元素,广泛存在于自然界。
1.存在
游离态:
化合态:
火山口附近或地壳的岩层里
硫化物和硫酸盐的形式
2.物理性质:黄色晶体(俗称硫黄),质脆,易研成粉末。 不溶于水,微溶于酒精,易溶于CS2 。
(1)氧化性
S+Fe=FeS
△
2Cu+S=Cu2S
△
既有氧化性又有还原性!
硫在氧气中燃烧
(2)还原性
点燃
S + O2 = SO2
实验现象:S在氧气中燃烧生成明亮的蓝紫色火焰。
3.化学性质:
一. 硫
颜色、气味、状态(通常状况下)
密度
溶解性
熔沸点
易溶于水(常温常压下,1体积水大约能溶解40体积的SO2)
一. 二氧化硫的物理性质
无色、有刺激性气味的有毒
气体
易液化
比空气大
有毒
扇闻
用手轻轻地在瓶口扇动,使极少量的SO2气体飘进鼻孔。
实验探究1:
探究结论:
探究现象:
试管内液面上升
SO2 易溶于水
SO2 是一种无色、有刺激性气味的气体、有毒、 比空气重、易液化、易溶于水的气体。
小结:
将集满SO2的试管倒扣在水中,振荡,观察现象并分析。
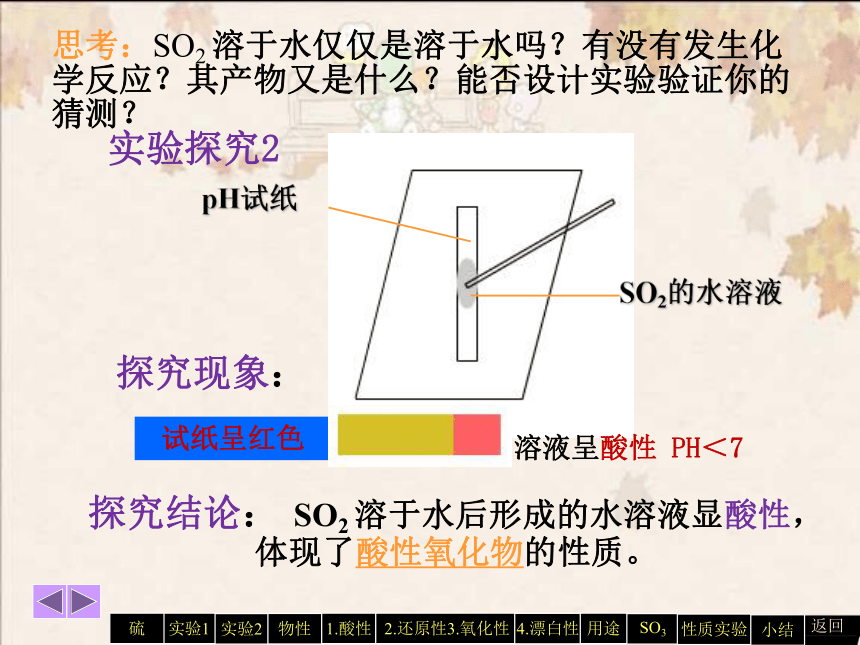
思考:SO2 溶于水仅仅是溶于水吗?有没有发生化学反应?其产物又是什么?能否设计实验验证你的猜测?
实验探究2
pH试纸
SO2的水溶液
探究现象:
溶液呈酸性 PH<7
试纸呈红色
探究结论: SO2 溶于水后形成的水溶液显酸性,体现了酸性氧化物的性质。
亚硫酸
在相同条件下,既能向正反应进行,同时又能向逆反应方向进行的化学反应。
可逆反应:
*亚硫酸是一种弱酸,不稳定
与盐碱反应生成盐和水
与碱性氧化物反生成盐
与H2O反应生成酸
酸性氧化物
二. 二氧化硫的化学性质
(1)酸性氧化物的通性:
①与水反应:
②与CaO反应:
③与NaOH
溶液反应:
④与澄清的石灰水反应:
2NaOH + SO2 = Na2SO3+H2O
NaOH + SO2 = NaHSO3
Ca(OH)2 +SO2 = CaSO3 ↓ + H2O
CaSO3+ H2O+ SO2 = Ca(HSO3)2
SO2+H2O H2SO3 (亚硫酸)
CaO+SO2 = CaSO3
?
【思考】 SO2 与 CO2 怎样区别?
② SO2 + Br2 + 2H2O H2SO4 + 2HBr
①紫红色KMnO4溶液
SO2
溶液褪色(不是SO2的漂白性)
S S S S
-2 0 +4 +6
(2)SO2的还原性(较强):
SO2使溴水橙色褪去(不是漂白性)
SO2 + 2H2S 3S↓+ 2H2O
(3)SO2的氧化性:
二. 二氧化硫的化学性质
③ 2SO2 + O2 2SO3
催化剂
△
既有氧化性又有还原性!
SO3
SO3的物理性质:是无色固体,熔沸点低,易溶于水并放出大量的热。
SO3也是酸性氧化物:
SO3 +CaO = CaSO4
SO3+Ca(OH)2==CaSO4+H2O
(微溶物,量大时有沉淀)
SO3 +H2O = H2SO4
(4)SO2的漂白性:
二. 二氧化硫的化学性质
“黄色”银耳是怎样“变”成“白”的呢?
硫磺熏后的银耳变白
(4)SO2的漂白性:——特性
实验探究3 现象 结论
往装有SO2溶液的试管内滴入2-3滴品红溶液,然后振动试管。
把试管内液体用酒精灯加热
品红溶液褪色
溶液变回红色
SO2有漂白作用
被SO2 漂白不稳定,容易变回原来的颜色
二. 二氧化硫的化学性质
SO2与氯水漂白作用的比较
氯水 SO2 木炭
漂白原理
反应类型
与品红溶液作用
效果
范围
同类漂白物质
SO2跟某些有色物质化合生成不稳定的无色物质
氯水中的HClO有强氧化性,将某些有色物质氧化成无色物质
氧化还原反应
非氧化还原反应
红色褪去加热后不恢复
红色褪去加热后又变红
Na2O2 H2O2 O3
将有色物质的分子吸附在其表面
物理吸附
暂时性
永久性
暂时性
可漂白大多数有色物质,能使紫色石蕊褪色
可漂白某些有色物质,不能使石蕊试液褪色
可吸附某些有色物质的分子
(4)SO2的漂白性:
性质 用途
三. 二氧化硫的用途
①可以漂白纸浆、毛、丝、草编制品等。
漂白性
有毒
②能够杀灭霉菌和细菌,可用作食物和干果的防腐剂。
SO3 + H2O = H2SO4
2SO2 + O2 2 SO3
催化剂
△
③工业上常用来制硫酸
决定
四. SO2的性质实验装置图
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
四. SO2的性质实验装置图
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
四. SO2的性质实验装置图
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
四. SO2的性质实验装置图
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
四. SO2的性质实验装置图
一、物理性质
二、化学性质
1、酸性氧化物的通性
2、还原性
3、氧化性
4、漂白性
三、用途
问苍天 枯木无言
被污染的树叶
乐山大佛开凿于唐玄宗开元初年(公元713年),为世界第一大石刻弥勒佛,“佛是一座山,山是一尊佛”是其真实写照,请同学们仔细观察,历经千年时间的流逝,是什么物质使大佛鼻翼发黑,佛容暗淡 呢?
1908年 1968年
酸雨横行 雕像何辜
二氧化硫
饮用酸化的地下水危害人类
腐蚀建筑物和工业设备
破坏土壤成分使农作物减产甚至死亡
损坏植物叶面导致森林死亡
破坏露天文物古迹
使湖泊中鱼虾死亡
酸雨的危害:
一. 硫
硫是一种重要的非金属元素,广泛存在于自然界。
1.存在
游离态:
化合态:
火山口附近或地壳的岩层里
硫化物和硫酸盐的形式
2.物理性质:黄色晶体(俗称硫黄),质脆,易研成粉末。 不溶于水,微溶于酒精,易溶于CS2 。
(1)氧化性
S+Fe=FeS
△
2Cu+S=Cu2S
△
既有氧化性又有还原性!
硫在氧气中燃烧
(2)还原性
点燃
S + O2 = SO2
实验现象:S在氧气中燃烧生成明亮的蓝紫色火焰。
3.化学性质:
一. 硫
颜色、气味、状态(通常状况下)
密度
溶解性
熔沸点
易溶于水(常温常压下,1体积水大约能溶解40体积的SO2)
一. 二氧化硫的物理性质
无色、有刺激性气味的有毒
气体
易液化
比空气大
有毒
扇闻
用手轻轻地在瓶口扇动,使极少量的SO2气体飘进鼻孔。
实验探究1:
探究结论:
探究现象:
试管内液面上升
SO2 易溶于水
SO2 是一种无色、有刺激性气味的气体、有毒、 比空气重、易液化、易溶于水的气体。
小结:
将集满SO2的试管倒扣在水中,振荡,观察现象并分析。
思考:SO2 溶于水仅仅是溶于水吗?有没有发生化学反应?其产物又是什么?能否设计实验验证你的猜测?
实验探究2
pH试纸
SO2的水溶液
探究现象:
溶液呈酸性 PH<7
试纸呈红色
探究结论: SO2 溶于水后形成的水溶液显酸性,体现了酸性氧化物的性质。
亚硫酸
在相同条件下,既能向正反应进行,同时又能向逆反应方向进行的化学反应。
可逆反应:
*亚硫酸是一种弱酸,不稳定
与盐碱反应生成盐和水
与碱性氧化物反生成盐
与H2O反应生成酸
酸性氧化物
二. 二氧化硫的化学性质
(1)酸性氧化物的通性:
①与水反应:
②与CaO反应:
③与NaOH
溶液反应:
④与澄清的石灰水反应:
2NaOH + SO2 = Na2SO3+H2O
NaOH + SO2 = NaHSO3
Ca(OH)2 +SO2 = CaSO3 ↓ + H2O
CaSO3+ H2O+ SO2 = Ca(HSO3)2
SO2+H2O H2SO3 (亚硫酸)
CaO+SO2 = CaSO3
?
【思考】 SO2 与 CO2 怎样区别?
② SO2 + Br2 + 2H2O H2SO4 + 2HBr
①紫红色KMnO4溶液
SO2
溶液褪色(不是SO2的漂白性)
S S S S
-2 0 +4 +6
(2)SO2的还原性(较强):
SO2使溴水橙色褪去(不是漂白性)
SO2 + 2H2S 3S↓+ 2H2O
(3)SO2的氧化性:
二. 二氧化硫的化学性质
③ 2SO2 + O2 2SO3
催化剂
△
既有氧化性又有还原性!
SO3
SO3的物理性质:是无色固体,熔沸点低,易溶于水并放出大量的热。
SO3也是酸性氧化物:
SO3 +CaO = CaSO4
SO3+Ca(OH)2==CaSO4+H2O
(微溶物,量大时有沉淀)
SO3 +H2O = H2SO4
(4)SO2的漂白性:
二. 二氧化硫的化学性质
“黄色”银耳是怎样“变”成“白”的呢?
硫磺熏后的银耳变白
(4)SO2的漂白性:——特性
实验探究3 现象 结论
往装有SO2溶液的试管内滴入2-3滴品红溶液,然后振动试管。
把试管内液体用酒精灯加热
品红溶液褪色
溶液变回红色
SO2有漂白作用
被SO2 漂白不稳定,容易变回原来的颜色
二. 二氧化硫的化学性质
SO2与氯水漂白作用的比较
氯水 SO2 木炭
漂白原理
反应类型
与品红溶液作用
效果
范围
同类漂白物质
SO2跟某些有色物质化合生成不稳定的无色物质
氯水中的HClO有强氧化性,将某些有色物质氧化成无色物质
氧化还原反应
非氧化还原反应
红色褪去加热后不恢复
红色褪去加热后又变红
Na2O2 H2O2 O3
将有色物质的分子吸附在其表面
物理吸附
暂时性
永久性
暂时性
可漂白大多数有色物质,能使紫色石蕊褪色
可漂白某些有色物质,不能使石蕊试液褪色
可吸附某些有色物质的分子
(4)SO2的漂白性:
性质 用途
三. 二氧化硫的用途
①可以漂白纸浆、毛、丝、草编制品等。
漂白性
有毒
②能够杀灭霉菌和细菌,可用作食物和干果的防腐剂。
SO3 + H2O = H2SO4
2SO2 + O2 2 SO3
催化剂
△
③工业上常用来制硫酸
决定
四. SO2的性质实验装置图
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
四. SO2的性质实验装置图
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
四. SO2的性质实验装置图
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
四. SO2的性质实验装置图
石蕊试液
品红溶液
溴水
氢硫酸
NaOH溶液
四. SO2的性质实验装置图
一、物理性质
二、化学性质
1、酸性氧化物的通性
2、还原性
3、氧化性
4、漂白性
三、用途
