鲁教版(五四制)八上第三单元第三节物质组成的表示 导学案
文档属性
| 名称 | 鲁教版(五四制)八上第三单元第三节物质组成的表示 导学案 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-08-13 00:00:00 | ||
图片预览



文档简介
第三单元 物质构成的奥秘
第三节 物质组成的表示
教材知识全解
知识点一 物质组成的表示
1.定义:用元素符号和数字表示物质组成的式子叫作化学式。任何纯净物都有固定的组成,不同的物质组成不同。因此,只有纯净物才有化学式,且一种纯净物只有一种化学式。
2.化学式表示的意义
化学式表示的意义
举例
宏观
意义
①表示一种物质
②表示该物质是由哪些元素组成的
宏
观
意
义
③由分子构成的物质的化学式可以表示该物质的一个分子
④表示该物质的一个分子是由哪些原子构成的
【知识拓展】 化学符号中各数字所代表的意义主要有以下几种:(1)化学符号前面的数字表示粒子(原子、离子或分子)的数目;(2)化学符号右下角的数字表示一个粒子中某原子或原子团的数目,如“2O2”中两个“2”的含义是不同的,前面的“2”表示2个氧气分子,右下角的“2”表示每个氧气分子由2个氧原子构成。
例1 (2018湖南邵阳中考改编)“塑化剂”是一种工业原料,但不法商家把它添加到饮用品当中,对人的身体造成严重危害。已知“塑化剂”的主要成分是邻苯二甲酸二辛酯,化学式为C24H38O4。下列有关邻苯二甲酸二辛酯的说法中错误的是( )
A.它属于纯净物
B.它是由C、H、O三种元素组成的
C.一个邻苯二甲酸二辛酯分子中共有66个原子
D.苯二甲酸二辛酯是由碳原子、氢原子、氧原子构成的
解析 C24H38O4是由C、H、O三种元素组成的化合物,属于纯净物,A、B项正确;一个C24H38O4分子中共有66个原子,C项正确;邻苯二甲酸二辛酯分子是由碳原子、氢原子、氧原子构成的,D项错误。
答案 D
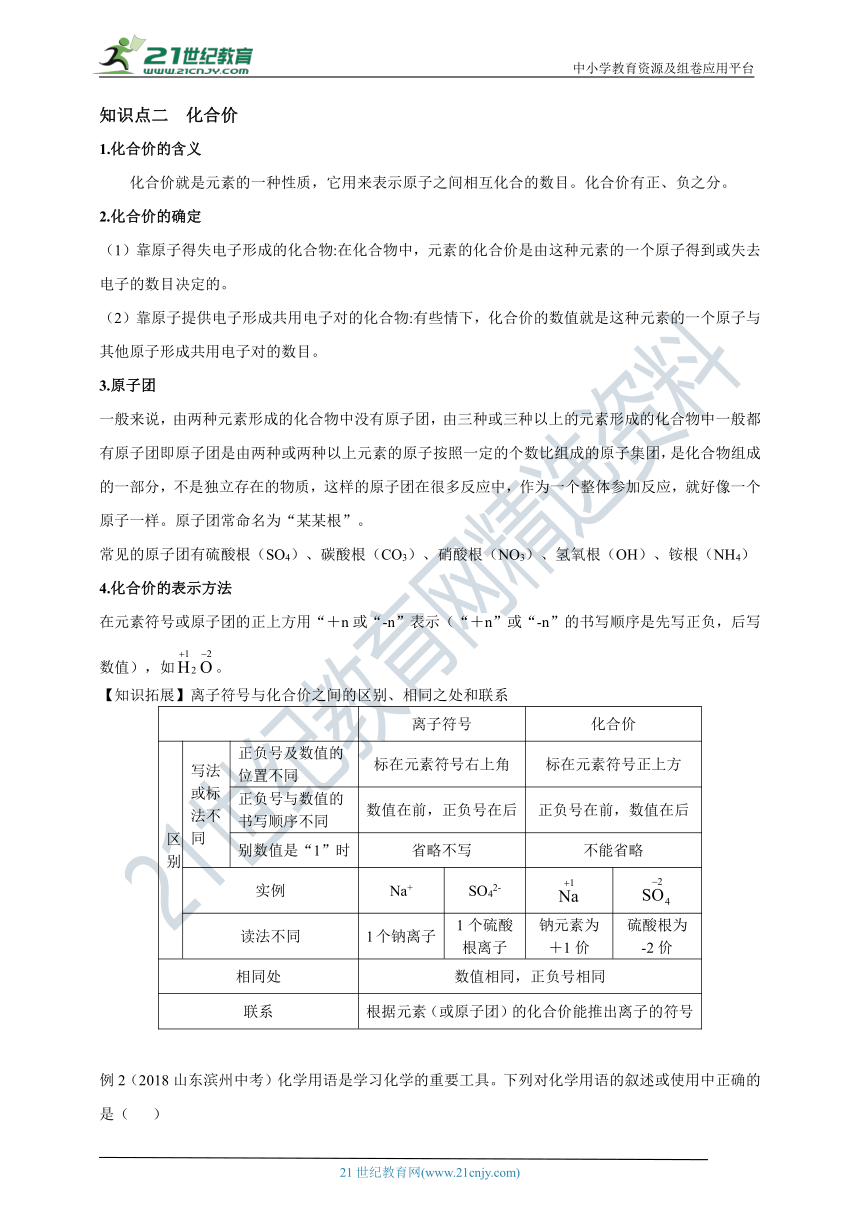
知识点二 化合价
1.化合价的含义
化合价就是元素的一种性质,它用来表示原子之间相互化合的数目。化合价有正、负之分。
2.化合价的确定
(1)靠原子得失电子形成的化合物:在化合物中,元素的化合价是由这种元素的一个原子得到或失去电子的数目决定的。
(2)靠原子提供电子形成共用电子对的化合物:有些情下,化合价的数值就是这种元素的一个原子与其他原子形成共用电子对的数目。
3.原子团
一般来说,由两种元素形成的化合物中没有原子团,由三种或三种以上的元素形成的化合物中一般都有原子团即原子团是由两种或两种以上元素的原子按照一定的个数比组成的原子集团,是化合物组成的一部分,不是独立存在的物质,这样的原子团在很多反应中,作为一个整体参加反应,就好像一个原子一样。原子团常命名为“某某根”。
常见的原子团有硫酸根(SO4)、碳酸根(CO3)、硝酸根(NO3)、氢氧根(OH)、铵根(NH4)
4.化合价的表示方法
在元素符号或原子团的正上方用“+n或“-n”表示(“+n”或“-n”的书写顺序是先写正负,后写数值),如。
【知识拓展】离子符号与化合价之间的区别、相同之处和联系
离子符号
化合价
区别
写法
或标
法不
同
正负号及数值的位置不同
标在元素符号右上角
标在元素符号正上方
正负号与数值的书写顺序不同
数值在前,正负号在后
正负号在前,数值在后
别数值是“1”时
省略不写
不能省略
实例
Na+
SO42-
读法不同
1个钠离子
1个硫酸根离子
钠元素为+1价
硫酸根为-2价
相同处
数值相同,正负号相同
联系
根据元素(或原子团)的化合价能推出离子的符号
例2(2018山东滨州中考)化学用语是学习化学的重要工具。下列对化学用语的叙述或使用中正确的是( )
A.—— NH3中氮元素显-3价 B.4H——4个氢元素
C.镁离子——Mg+2 D.氧化亚铁——Fe3O4
解析 化合价的表示方法为在其化学式中该元素的正上方用正负号和数字表示,正负号在前,数字在后,A正确。4H表示4个原子,元素只讲种类、不讲个数,B项错误。离子的表示方法为在表示该离子的元素符号的右上角,标出该离子所带的正负电荷数,数字在前,正、负号在后。带1个单位电荷时,1要省略。镁离子可表示为Mg2+,C错误。氧化亚铁中铁元素显+2价,氧元素显-2价,其化学式为FeO,D错误。
答案 A
5.化合价规则
(1)化合价有正价和负价之分。
(2)金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价,如MgCl2中Mg为+2价,Cl为-1价;非金属元素和氧元素形成化合物时,非金属元素通常显正价,氧元素通常显 -2价,如SO2中S为+4价,O为 -2价。
(3)一些元素在不同物质中可显示不同的化合价,如KMnO4、K2MnO4中锰元素的化合价分别为+7、+6。
(4)在化合物中,各元素的正负化合价之和为零。
(5)因为化合价是元素的原子在形成化合物时才表现出来的一种性质,所以单质中元素的化合价为零。
(6)原子团不能独立存在,只是化合物的一个组成部分,所以原子团的化合价由其组成元素的化合价的代数和算出,原子团的化合价一定不为零。
例3 下列有关化合价的叙述,正确的是( )
A.化合价是元素与元素间化合时表现出来的性质
B.任何元素都可能显正价和负价
C.一种元素在不同化合物中可能有多种化合价,但在一种物质中只能有一种化合价
D.在原子团中各元素的正负化合价之和为零
解析 化合价是元素在形成化合物时表现出来的一种性质,故A正确。氟无正价,稀有气体元素通常显零价,故B错。有些元素可以在一种物质中显示不同的化合价,如在硝酸铵中铵根中的氮元素显-3价,硝酸根中的氮元素显+5价,故C错。原子团是化合物的一个组成部分,不能独立存在,因此所有的原子团中各元素的正负化合价之和均不为零,故D错。
答案 A
知识点三 化合价与化学式
1.根据化学式求化合价
(1)已知物质的化学式,根据化合物中,各元素的正负化合价之和为零的原则确定元素的化合价。如:
标出已知、未知化合价:;
列出式子求解:(+1)×2+x×1+(-2)×3=0,x=+4
(2)根据化合价原则,判断化学式的正误,如判断化学式KCO3是否正确。
标出元素或原子团的化合价:;
计算正负化合价之和是否为零:(+1)×1+(-2)×1=-1≠0,所以给出的化学式是错误的,正确的为K2CO3。
(3)根据化合价原则,计算原子团中某元素的化合价,如计算中氮元素的化合价和(磷酸二氢根)中磷元素的化合价。
由于带一个单位的正电荷,不是电中性的,因此各元素的化合价之和不为0,而是等于+1。
设氮元素的化合价为x,x+(+1)×4=+1 x=-3
所以在中,氮元素的化合价为-3。同理带一个单位的负电荷,也不是电中性的,因此各元素的正负化合价之和不为零,而是-1。
设磷元素的化合价为y,(+1)×2+y×1+(-2)4=-1 y=+5
所以在中磷元素的化合价为+5。
(4)根据化合价原则,确定物质按化合价排序。如H2S、S、SO2、H2SO4四种物质中均含有硫元素,并且硫元素的化合价在四种物质中分别为-2、0、+4、+6,故这四种物质是按硫元素的化合价由低到高的顺序排列的。
例4 偏钛酸钡(Bax TiO3)因其显著的“压电效应”而广泛地应用于超声波发生装置中。已知偏钛酸钡中钛元素的化合价为+4,则其化学式中x的数值为( )
A.1 B.2 C.3 D.4
解析 钡元素显+2价,钛元素显+4价,氧元素显-2价,根据在化合物中,各元素的正负化合价之和为零,可得:(+2)×x+(+4)+(-2)×3=0,则x=1
答案 A
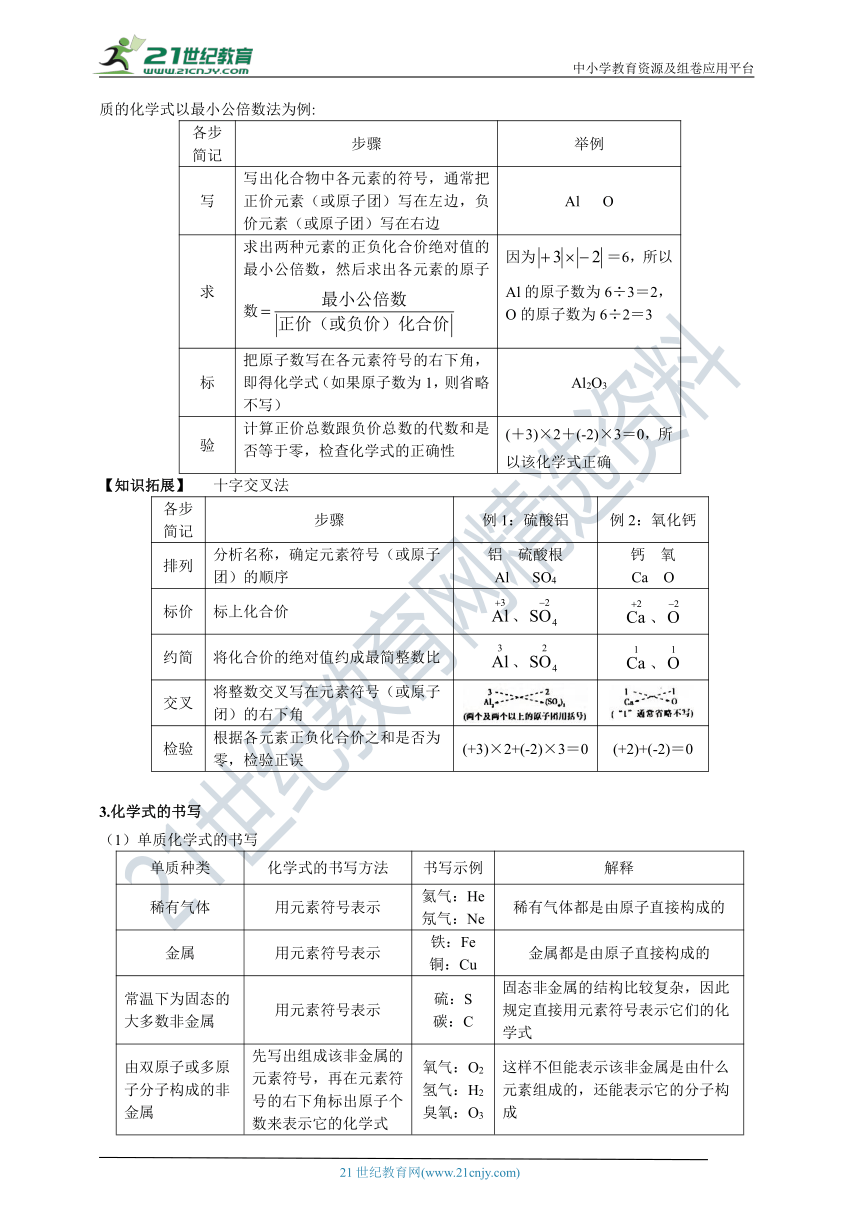
2.根据化合价写化学式
根据在化合物中,各元素的正负化合价之和等于零的原则,已知元素的化合价可以推出实际存在的物质的化学式以最小公倍数法为例:
各步
简记
步骤
举例
写
写出化合物中各元素的符号,通常把正价元素(或原子团)写在左边,负价元素(或原子团)写在右边
Al O
求
求出两种元素的正负化合价绝对值的最小公倍数,然后求出各元素的原子数
因为=6,所以Al的原子数为6÷3=2,O的原子数为6÷2=3
标
把原子数写在各元素符号的右下角,即得化学式(如果原子数为1,则省略不写)
Al2O3
验
计算正价总数跟负价总数的代数和是否等于零,检查化学式的正确性
(+3)×2+(-2)×3=0,所
以该化学式正确
【知识拓展】 十字交叉法
各步
简记
步骤
例1:硫酸铝
例2:氧化钙
排列
分析名称,确定元素符号(或原子团)的顺序
铝 硫酸根
Al SO4
钙 氧
Ca O
标价
标上化合价
、
、
约简
将化合价的绝对值约成最简整数比
、
、
交叉
将整数交叉写在元素符号(或原子闭)的右下角
检验
根据各元素正负化合价之和是否为零,检验正误
(+3)×2+(-2)×3=0
(+2)+(-2)=0
3.化学式的书写
(1)单质化学式的书写
单质种类
化学式的书写方法
书写示例
解释
稀有气体
用元素符号表示
氦气:He
氖气:Ne
稀有气体都是由原子直接构成的
金属
用元素符号表示
铁:Fe
铜:Cu
金属都是由原子直接构成的
常温下为固态的大多数非金属
用元素符号表示
硫:S
碳:C
固态非金属的结构比较复杂,因此规定直接用元素符号表示它们的化学式
由双原子或多原子分子构成的非金属
先写出组成该非金属的元素符号,再在元素符号的右下角标出原子个数来表示它的化学式
氧气:O2
氢气:H2
臭氧:O3
这样不但能表示该非金属是由什么元素组成的,还能表示它的分子构成
(2)化合物化学式的书写
化学式的写法
化学式的读法
氧化物
氧元素符号在后,另一元素符号在前,如CuO,CO2,等
从后向前读作“氧化某",如CuO读作氧化铜;有时需读出原子个数,如Fe3O4,读作“四氧化三铁”
由金属元素和非金属元素(除氧元素外)组成的化合物
非金属元素符号在后,金属元素符号在前,如 K2S、CaCl2,等
从后向前读作“某化某”,如K2S读作“硫化钾”;有时需读出原子个数,如FeCl3,读作“三氯化铁”
【知识拓展】 在读氧化物时,一般读作“几氧化儿某”,数字为1时一般不读;若元素具有可变化合价且氧原子的个数为1,此时"1"要读出来,如CO2,读作“二氧化碳",CO读作“一氧化碳"。
例5 (2018上海黄浦一模)下列物质的化学式书写正确的是( )
A.氯化镁:MgCl B.氧化铝:AlO C.硫酸锌:ZnSO4 D.氢氧化铁:Fe(OH)2
解析 氯化镁(MgC1)的化学式书写错误,因为(+2)+(-1)≠0,不符合“在化合物中,各元素的正负化合价之和为零”的原则,应改为MgCl2;因氧化铝中氧元素的化合价为-2,铝元素的化合价为+3,由化合物中各元素的正负化合价之和为零可知,氧化铝的化学式应为Al2O3;氢氧化铁中,铁元素的化合价是+3,氢氧根的化合价是-1,故氢氧化铁的化学式是Fe(OH)3。
答案 C
例6 A、B、C三种元素的化合骨分剥为+1、+5、- 2.由这三种元素组成的化合物为( )
A2BC4 B.ABC3 C.A2BC3 D.A3BC4
解析 根据在化合场中,各元素的正负化会骨之和为零的原则,计算各个选项中的化合之和是否为零即可,A中,2×(+1)+(+5)- 4×(-2)≠0,错误;B中,(+1)+(+5)+3×(-2)=0,正确;C中,2×(+1)+(+5)+3×(-2)≠0,错误;D中,3×(+1)+(+5)+4×(+1)=0,正确。
答案 BD
知识点四 有关化学式的计算
1.化学式量的计算
化学式量就是某物质化学式中各原子的相对原子质量的总和,对于由分子构成的物质,其化学式量也叫作相对分子质量。
如化学式为AmBn的物质的化学式量=A的相对原子质量×m+8的相时原子质量×n。
2.根据化学式计算其组成元素的质量比
化合物中各元素的质量比是原子个数与相对原子质量的乘积之比,即各元素原子的祖时原子质童总和之比。
如化学式为AmBn的物质中,A、B两元素的质量比=(A的相时原子质量× m): (B的相对原子质量×n)。
【知识规展】(1)在化学式中,原子个数比等于元素的质量除以其相对原子质量的商之比。如AmBn中A、B两元素的质量分别为M、N,则化学式中A、B两元素的原子个数比m:n = 。
(2)当化学式中含有多种元素时,根据化学式可以计算出全部元素的质量比,也可以计算出其中某几种元素的质量比。
例7 某氮的氧化物中,氮氧元素的质量比为7:16,则该此合物的化学式是( )
A.NO B.NO2 C.N2O3 D.N2O4
解析 根据“化合物中各元素的质量比 = 各原子的相对原子质量×原子个数之比”进行分析解答。某氮的氧化物中,氮、氧的质量比为7 : 16,则该氮的氧化物中的氮原子和氧原子的个数比为=1 : 2,故该化合物的化学式NO2或N2O4。
答案 BD
3.计算物质中某元素的质量分数
(1)定义:物质中某元素的质量分数,就是该元素的质量与物质的总质量之比。
计算公式:某元素的质量分数=×100%
如AmBn中A元素的质量分数=×100%
(2)化学式中质量分数的应用
①已知物质的质量求所含某元素的质量
利用公式:元素的质量=物质的质量×该元素的质量分数
②已知所含元素的质量求物质的质量
利用公式:物质的质量=元素的质量÷该元素的质量分数
③根据元素的质量分数确定物质的化学式
例8 (2019甘肃兰州中考改编)苯甲酸钠(C7H5O2Na)是一种食品添加剂,广泛用于食品工业中。请计算:
(1)C7H5O2Na的化学式量是_______________;
(2)C7H5O2Na中碳、氧两种元素的质量比是________________;
(3) 14.4 g苯甲酸钠中含有钠元素多少克? (写出计算过程)
解析 (1)化学式量等于各原子的相对原子质量×原子个数之和C7H5O2Na的化学式量为12×7+1×5+16×2+23=144 ;(2)=中碳、氧元素的质量比为(12×7):(16×2)= 21 : 8;(3)一定质量的物质中某元素的质量等于物质的质量乘以该元素的质量分数,14.4 g苯甲酸钠中钠元素的质量为14.4 g ×( ×100%) = 2.3 g。
答案 (1) 144 (2)21: 8 (3)14.4 g ×( ×100%) = 2.3 g
答:14.4 g苯甲酸钠中含有钠元素的质量是2.3g。
基础闯关全练
知识点一 物质组成的表示
1.(2019上海徐汇一模)化学符号“H2O”表示的意义错误的是( )
A.水这种物质 B.水由氢元素和氧元素组成
C.水分子中含有氢分子 D.一个水分子由两个氢原子和一个氧原子构成
2.铁是我们生活中最常见的物质之一,其化学式为Fe,下列四位同学在讨论Fe的意义,其中错误的是( )
知识点二 化合价
3.次氯酸(HCIO)具有杀菌消毒的作用,HCO中氯元素的化合价表示正确的是( )
A. B. C. D.
4.(2019山东滨州中考)根据你对元素知识的认识,请在横线上依次填写有关铝元素的5个信息:
知识点三 化合价与化学式
5.下列物质的化学式,书写正确的是( )
A.碳酸钠:Na2CO3 B.氢氧化钠:NaOH2 C.氧化铁:FeO D.硫酸:HSO4
6.(2018山东菏泽曹县期末)地壳中含量最多的金属元素与含量最多的非金属元素形成的化合物是( )
A. SiO2 B. Fe2O3 C.CaO D.Al2O3
7.(2019甘肃兰州中考)高铁酸钠是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。其化学式为Na2FeO4,其中Fe元素的化合价是( )
A.+6 B.+4 C.+3 D.+2
知识点四 有关化学式的计算
8.下列计算错误的是( )
A.Mg(OH)2的化学式量:24+(16+1)×2=58
B.SO2中硫元素与氧元素的质量比为1:1
C.NH4NO3中氮元素的质量分数:×100%=17.5%
D.18g水(H2O)中含氢元素的质量:18g×(×100%)=2 g
9.维生素C(C6H8O6)主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。计算:
(1)维生素C的相对分子质量为_______________。
(2)维生素C中碳、氢两种元素的质量比为____________(写最简比)。
(3)维生素C中___________元素的质量分数最大。
能力提升全练
知识点一 物质组成的表示
1.绿茶中的单宁酸具有清热解毒、抗癌等功效,其化学式为C76H52O46下列关于单宁酸的说法不正确的是( )
A.它由C、H、O三种元素组成 B.一个分子中含76个碳原子
C.分子中C、H、O原子个数比为38:26:23 D.一个分子中含23个氧分子
2.口香糖中的木糖醇是一种新型甜味剂,它的结构如图3-3-1。下列关于木糖醇的说法错误的是
( )
A.木糖醇分子中C、H、O原子的个数比为5:12:5
B.一个木糖醇分子中含有22个原子
C.木糖醇属于化合物
D.木糖醇是由多个原子构成的纯净物
知识点二 化合价
3.(2018山东威海经济技术开发区期末)下列化学符号中数字表示的意义正确的是( )
A.2Na:“2”表示两个钠元素
B.S2-:“2-”表示硫元素的化合价为负二价
C. :“+2”表示镁离子带有两个单位的正电荷
D.CO2:“2”表示一个二氧化碳分子中含有两个氧原子
4.录像用的高性能磁粉的主要材料之一是由三种元素组成的、化学式为CoxFe3-xO3+x的化合物。已知氧元素的化合价为-2,钴(Co)和铁元素的化合价可能是+2或+3,且上述化合物中每种元素只有一种化合价,则x值为_________,铁元素的化合价为________,钴元素的化合价为__________。
5.我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律。如图3-3-2列出的是1~18号元素的部分最高正化合价和最低负化合价。请阅读并回答下列问题。
(1)11号元素属于_________(填“金属”或“非金属”)元素,它在化学反应中形成的离子与______(填元素符号)原子具有相同的核外电子排布。
(2)16号元素的原子核外电子数为__________,推测该元素的最低负化合价为________,其最高正化合价与氧元素组成的化合物的化学式为__________。
(3)第二横行中金属元素共有________种(填“1”“2”“3”“4”或“5”)。
知识点三 化合价与化学式
6.现有、、、四种元素,如果用指定化合价将它们按两种或三种元素结合成化合物,则最多可形成化合物的种类是( )
A.4种 B.5种 C.6种 D.7种
7. (2018山东淄博高青期末)X、Y元素为核电荷数小于18的元素,元素X的原子的最外电子层上有1个电子,元素Y的原子的最外电子层上有6个电子,由x,Y两元素形成的化合物的化学式可能是( )
A.XY6 B.X2Y C.XY2 D.X6Y
8. (2017福建厦门中考)含硫元素物质间发生转化SSO2SO3H2SO4
Al2(SO4)3,其中硫元素化合价发生变化的是( )
A.①② B.③④ C.①③ D.②④
9.2015年11月12日,2015年版第五套人民币100元纸币正式发行面世。新版100元人民币采用光变色防伪油墨印刷,防伪油器中含有MgF2", MgF2中F元素的化合价是( )
A.+2 B.+1 C.-2 D.-1
知识点四 有关化学式的计算
10.2015年10月,中国女药学家屠呦呦因创制新型抗疟药——青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖。青蒿素的化学式为C15H22O5。请回答:
(1)青蒿素分子中碳、氧原子的个数比为____________;
(2)青蒿素中含量最高的元素是___________;
(3)564 g青蒿素中含氧元素的质量是_____________。
11. (2017山东滨州邹平实验中学期中)钙是人体中的常量元素,每日必需摄入足够量的钙。目前市场上的补钙药剂很多,图3-3-4是某种品牌的补钙药品的部分说明书。
图3-3-4
请回答下列问题:
(1)碳酸钙共含有__________种元素,其中钙、碳、氧元素的质量比为____________, CaCO3中钙元素的质量分数为_______________。
(2)若每片钙片的质量为1 g,则钙片中钙元素的质量分数为_____________。
(3)如果按用量服用,每天摄入钙元素的质量为__________ g。
直击中考
1.(2018山东淄博高青期末)下列关于化合价的说法,正确的是( )
A.五氧化二磷(P2O5)中磷元素显+2价 B.氧元素的化合价一定是-2
C.非金属元素在化合物中总显负价 D.一种元素在同一种化合物中,可能显示不同的化合价
2.(2018山东青岛黄岛期末)下列化学用语与其所表达的意义一致的是( )
A.Co——1个一氧化碳分子 B.2SO4-2 ——2个硫酸根离子
C.——氧化铜中铜元素的化合价为+2 D.H2——2个氢原子
3.(2017山东烟台招远期末)2014年4月兰州发生了自来水中苯超标事故,引起人们对水安全的关注。已知苯的化学式为C6H6,下列有关说法正确的是( )
A.苯中的C、H元素的质量比为12:1
B.苯分子是由6个碳元素和6个氢元素组成的
C.苯分子中碳原子的结构示意图为
D.苯中碳、氢元素位于元素周期表的同一横行
4.(2019山东济宁中考)下列化学反应中,元素的化合价没有发生变化的是( )
①CO2+H2O H2CO3
②NH4HCO3 H2O+CO2↑+NH3↑
③2H2S+O2 2S↓+2H2O
④2NaOH+CuCl2 Cu(OH)2↓+2NaCl
A.①②③ B.①②④ C.②③④ D.①③④
5.(2018山东聊城中考)很多饮料中都含有柠檬酸(C6H8O7)。下列关于柠檬酸的说法中正确的是( )
A.属于氧化物 B.由6个碳原子、8个氢原子和7个氧原子组成
C.分子中氧元素的质量分数最大 D.分子中碳、氢、氧三种元素的质量比为6:8:7
6.(2019山东淄博中考)如图3-3-5是钠元素和硫元素的原子结构示意图,以及这两种元素摘自元素周期表的图示,下列说法错误的是( )
A.钠元素和硫元素的原子序数分别为11和16
B.钠元素和硫元素的核外电子数分别是1和6
C.钠元素和硫元素的原子核外都有3个电子层
D.钠元素和硫元素形成的常见化合物的化学式为Na2S
7.(2019山东泰安中考改编)在世界范围内,据统计化肥对粮食增产的贡献率已超过40%。图3-3-6是两种氮肥标签的一部分。
请根据图示中的信息回答下列问题:
(1)从标签上看,碳酸氢铵不同于尿素的化学性质是_____________(填字母序号);
A.易溶于水 B.受热易分解 C.有挥发性
(2)碳酸氢铵的化学式量为________________;
(3)纯尿素中氮元素的质量分数为__________,这种尿素肥料的纯度至少为_________。(计算结果精确至0.1%)
参考答案及解析
基础闯关全练
1.C 水分子中含有氢原子和氧原子,不含氢分子。
2.D 铁是由铁原子直接构成的,其元素符号为Fe,可表示铁这种物质、一个铁原子,还可表示铁是由铁元素组成的,不能表示一个铁分子。
3. C HCIO中H的化合价为+1、O的化合价为-2,设氯元素的化合价为x,根据在化合物中各元素正负化合价之和为零,可知(+1)+x+(-2)=0,解得x=+1,所以氯元素的化合价表示为。
4.答案 3 金属 失 +3 A12O3
解析 原子中,质子数=核外电子数,因此铝原子最外层电子数为13-2-8=3;铝含“钅”部首,属于金属元素;铝原子的最外层电子数为3,在化学反应中易失去这3个电子而形成带3个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,则该元素的化合价为+3;氧化铝中铝元素显+3价,氧元素显-2价,其化学式为Al2O3。
5.A 碳酸钠中钠元素的化合价为+1,而碳酸根的化合价为-2,所以碳酸钠的化学式为Na2CO3;氢氧化钠中,钠元素显+1价,氢氧根显-1价,其化学式为NaOH;氧化铁中铁元素的化合价为+3,氧元素的化合价为-2,其化学式为Fe2O3;硫酸中氢元素显+1价,硫酸根显-2价,其化学式为H2SO4。
6.D 地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素。铝的化合价是+3,氧一般显-2价,因此二者形成的化合物的化学式为Al2O3。
7.A 根据在化合物中,各元素的正负化合价之和为零的原则,钠元素显+1价,氧元素显-2价,设铁元素的化合价是x,可知高铁酸钠(Na2FeO4)中(+1)×2+x+(-2)×4=0,则x=+6。
8.C NH4NO3中氮元素的质量分数为×100%=35%。
9.答案 (1)176 (2)9:1 (3)氧
解析 (1)维生素C的相对分子质量为12×6+1×8+16×6=176。
(2)维生素C中碳、氢两种元素的质量比是(12×6):(1×8)=9:1。
(3)维生素C中碳元素的质量为12×6=72,氢元素的质量为1×8=8,氧元素的质量为16×6=96,氧元素的质量最大,则氧元素的质量分数最大。
能力提升全练
1.D 根据单宁酸的化学式C76H52O46可知,单宁酸含有C、H、O三种元素;每一个分子中含有76个碳原子、52个氢原子、46个氧原子,而不是含有23个氧分子。
2.D 分析题图可知,木糖醇的化学式为C5H12O5。木糖醇的一个分子是由5个碳原子、12个氢原子和5个氧原子构成的,因而木糖醇分子中C、H、O的原子个数比为5 : 12:5。木糖醇的一个分子中含有的原子个数为5+12+5 = 22个。木糖醇是由C、H、O三种元素组成的纯净物,是化合物。木糖醇是由木糖醇分子构成的,不是由原子直接构成的物质。
3.D 元素只讲种类,不讲个数,2Na表示2个钠原子,不能表示2个钠元素,A错误;S2- 表示的是硫离子,"2-"表示硫离子带两个单位的负电荷,不表示化合价,B错误;O表示氧化镁中镁元素的化合价为+2,不表示镁离子,C错误。
4.C 答案 1 +3 +2
解析 通过观察分析,若钴和铁元素的化合价相同,根据化合物中各元素的正负化合价之和为零,得x=0或1.5,不符合题意,则该化合物中钻和铁元素的化合价不同,因此钴、铁元素的化合价可能分别为+2,+3或+3,+2,考虑到x≠0,符合要求的应是钻元素的化合价为+2,铁元素的化合价为+3.根据化合物中,各元素的正负化合价之和为零,得到(+2)×x+(+3)×(3-x)+(-2)×(3+x)=0,解得x=1.
5.答案 (1)金属 Ne (2)16 -2 SO3 (3)2
解析 (1)11号元素是钠元素,属于金属元素,失去电子后,形成的钠离子与氛原子具有相同的核外电子排布。
(2) 16号元素的原子核外电子数为16,在化学反应中能得到两个电子,形成硫离子,带两个单位的负电荷,化合价为-2,最外层电子数为6,故其最高正化合价为+6,氧元素的化合价通常为-2,因此二者组成的化合物的化学式为SO3 。
(3)元素周期表的第二横行中金属元索共有钾、铍两种。
6.C 根据各种元素的化合价可以形成的化合物有:氢元素能和氧元素形成水,能和氧元素、硫元素形成硫酸,能和氧元素、钠元素形成氢氧化钠;氧元素能和硫元素形成三氧化硫,能和钠元素形成氧化钠,能和硫元素、钠元素形成硫酸钠,故最多可形成化合物的种类是6种。
7.B 元素X原子的最外层有1个电子,在化学反应中易失去电子,其化合价为+1;元素Y原子的最外层电子数为6,在化学反应中易得到两个电子,其化合价为-2,故X、Y形成的化合物的化学式可能为X2Y。
8.A 根据单质中元素的化合价为零,5属于单质,故硫元素的化合价为0,氧元素显-2价,设一氧化硫中硫元素的化合价是x,根据在化合物中,各元素的正负化合价之和为零,可得x+(-2)×2=0,则x=+4,以此法计算其余各物质中硫元素的化合价,然后进行判定,经计算知,硫元素化合价发生变化的是①、②。
9.D 根据在化合物中,各元素的正负化合价之和为零,设MgF2中F元素的化合价为x,则:(+2)+2x=0,x= -1
10. 答案 (1)3 :1 (2)C (3)160 g
解析 (1)由青蒿素的化学式可知,一个青蒿素分子是由15个碳原子22个氢原子和5个氧原子构成的,则青蒿素分子中C、O原子个数比为15 : 5=3 : 1。
(2)青蒿素分子中C、H、O三种元素的质量比为(12×15):(1×22) :(16×5)=90 : 11 : 40,由此可以判断青蒿素中碳元素的含量最高。
(3)564 g青蒿素中含氧元素的质量为564g×(×100%)= 160 g。
11.答案 (1)三 10:3: 12 40% (2)25% (3)0.5
解析 (1)根据碳酸钙的化学式可确定,碳酸钙是由Ga、C、O三种元素组成的,其中Ca、C、O的质量比为40: 12:(16×3)=10:3:12;其中钙元素的质量分数×100%=40%。
(2)每片钙片的质量为1 g,每片含碳酸钙0.625 g,则每片含钙元素的质量为0.625 g×40%=0.25g,钙片中钙元素的质量分数为×100%=25%。
(3)每片含碳酸钙0.625 g,每次一片,每天2次,则每天补充钙元素的质量为0.625g×2×40%=0.5g。
直击中考
1.D 五氧化二磷中氧元素的化合价为-2,设磷元素的化合价为x,根据在化合物中各元素的正负化合价之和为零,可得2x+5×(-2)=0,解得x=+5,A错误;氧元素在化合物中一般显-2价,但在氧气单质中,氧元素的化合价为0,B错误;非金属元素在与氢或金属元素化合时,一般显负价,但当其与氧元素化合时,则一般显正价,如SO2中,硫元素的化合价为+4,C错误;一种元素在同一种化合物中可以显示不同的化合价,如NH4NO3中氮元素分别显-3价和+5价,D正确。
2.C Co表示1个原子,或表示钴元素,或表示钻这种物质,不能表示一氧化碳分子,1个一氧化碳分子应该是CO,A错误;硫酸根离子的符号应为SO42-,选项中硫酸根离子的符号书写错误,B错误;H2是氢气的化学式,表示氢气(氢气是由氢元素组成的)、表示一个氢分子、表示每个氢分子是由两个氢原子构成的,而2个氢原子应该是在氢元素符号的前面书写2,即2H,D错误。
3.A 苯的化学式是C6H6,其中碳、氢元素的质量比为(12×6):(1×6)=12:1,A正确;苯是由碳元素和氢元素组成的,元素只讲种类,不讲个数,B错误;碳是6号元素,核外电子数与核内质子数相等,其原子结构示意图的最外层电子数是4,C错误;碳原子的核外有两个电子层,位于第二横行,氢原子有一个电子层,在元素周期表的第一横行,D错误.
4.B ①、②、④反应中,各元素的化合价都没有发生变化,③反应中,反应前硫元素的化合价为-2,氧元素的化合价为0,反应后硫元素的化合价为0,氧元素的化合价为-2,氧元素和硫。
5.C 柠檬酸中有C、H、O三种元素,不属于氧化物,故A错误柠檬酸由C、H、O三种元素组成,每个柠檬酸分子由6个碳原子、8个氢原子和7个氧原子构成,故B错误;由柠檬酸分子的构成及各元素原子的相对原子质量可推知,氧元素的质量分数最大,故C正确;柠檬酸中C、HO三种元素的质量比为(12×6):(1×8):(16×7)=9:1:14,故D错误。
6.B 钠元素与硫元素的核外电子数均等于各自的质子数,钠元素的质子数是11,核外电子数是11;硫元素的质子数是16,核外电子数也是16。
7.答案 (1)B (2)79 (3)46.7% 90.6%
解析 (1)二者保存时都要防潮说明二者都易溶于水;碳酸氢铵要避免高温天气施用,说明碳酸氢铵受热易分解,此为碳酸氢铵的化学性质。
(2)碳酸氢铵的化学式量为14+1×4+1+12+16×3=79。
(3)纯尿素中氮元素的质量分数为×100%≈46.7%,题给尿素肥料的纯度至少为=90.6%。
第三节 物质组成的表示
教材知识全解
知识点一 物质组成的表示
1.定义:用元素符号和数字表示物质组成的式子叫作化学式。任何纯净物都有固定的组成,不同的物质组成不同。因此,只有纯净物才有化学式,且一种纯净物只有一种化学式。
2.化学式表示的意义
化学式表示的意义
举例
宏观
意义
①表示一种物质
②表示该物质是由哪些元素组成的
宏
观
意
义
③由分子构成的物质的化学式可以表示该物质的一个分子
④表示该物质的一个分子是由哪些原子构成的
【知识拓展】 化学符号中各数字所代表的意义主要有以下几种:(1)化学符号前面的数字表示粒子(原子、离子或分子)的数目;(2)化学符号右下角的数字表示一个粒子中某原子或原子团的数目,如“2O2”中两个“2”的含义是不同的,前面的“2”表示2个氧气分子,右下角的“2”表示每个氧气分子由2个氧原子构成。
例1 (2018湖南邵阳中考改编)“塑化剂”是一种工业原料,但不法商家把它添加到饮用品当中,对人的身体造成严重危害。已知“塑化剂”的主要成分是邻苯二甲酸二辛酯,化学式为C24H38O4。下列有关邻苯二甲酸二辛酯的说法中错误的是( )
A.它属于纯净物
B.它是由C、H、O三种元素组成的
C.一个邻苯二甲酸二辛酯分子中共有66个原子
D.苯二甲酸二辛酯是由碳原子、氢原子、氧原子构成的
解析 C24H38O4是由C、H、O三种元素组成的化合物,属于纯净物,A、B项正确;一个C24H38O4分子中共有66个原子,C项正确;邻苯二甲酸二辛酯分子是由碳原子、氢原子、氧原子构成的,D项错误。
答案 D
知识点二 化合价
1.化合价的含义
化合价就是元素的一种性质,它用来表示原子之间相互化合的数目。化合价有正、负之分。
2.化合价的确定
(1)靠原子得失电子形成的化合物:在化合物中,元素的化合价是由这种元素的一个原子得到或失去电子的数目决定的。
(2)靠原子提供电子形成共用电子对的化合物:有些情下,化合价的数值就是这种元素的一个原子与其他原子形成共用电子对的数目。
3.原子团
一般来说,由两种元素形成的化合物中没有原子团,由三种或三种以上的元素形成的化合物中一般都有原子团即原子团是由两种或两种以上元素的原子按照一定的个数比组成的原子集团,是化合物组成的一部分,不是独立存在的物质,这样的原子团在很多反应中,作为一个整体参加反应,就好像一个原子一样。原子团常命名为“某某根”。
常见的原子团有硫酸根(SO4)、碳酸根(CO3)、硝酸根(NO3)、氢氧根(OH)、铵根(NH4)
4.化合价的表示方法
在元素符号或原子团的正上方用“+n或“-n”表示(“+n”或“-n”的书写顺序是先写正负,后写数值),如。
【知识拓展】离子符号与化合价之间的区别、相同之处和联系
离子符号
化合价
区别
写法
或标
法不
同
正负号及数值的位置不同
标在元素符号右上角
标在元素符号正上方
正负号与数值的书写顺序不同
数值在前,正负号在后
正负号在前,数值在后
别数值是“1”时
省略不写
不能省略
实例
Na+
SO42-
读法不同
1个钠离子
1个硫酸根离子
钠元素为+1价
硫酸根为-2价
相同处
数值相同,正负号相同
联系
根据元素(或原子团)的化合价能推出离子的符号
例2(2018山东滨州中考)化学用语是学习化学的重要工具。下列对化学用语的叙述或使用中正确的是( )
A.—— NH3中氮元素显-3价 B.4H——4个氢元素
C.镁离子——Mg+2 D.氧化亚铁——Fe3O4
解析 化合价的表示方法为在其化学式中该元素的正上方用正负号和数字表示,正负号在前,数字在后,A正确。4H表示4个原子,元素只讲种类、不讲个数,B项错误。离子的表示方法为在表示该离子的元素符号的右上角,标出该离子所带的正负电荷数,数字在前,正、负号在后。带1个单位电荷时,1要省略。镁离子可表示为Mg2+,C错误。氧化亚铁中铁元素显+2价,氧元素显-2价,其化学式为FeO,D错误。
答案 A
5.化合价规则
(1)化合价有正价和负价之分。
(2)金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价,如MgCl2中Mg为+2价,Cl为-1价;非金属元素和氧元素形成化合物时,非金属元素通常显正价,氧元素通常显 -2价,如SO2中S为+4价,O为 -2价。
(3)一些元素在不同物质中可显示不同的化合价,如KMnO4、K2MnO4中锰元素的化合价分别为+7、+6。
(4)在化合物中,各元素的正负化合价之和为零。
(5)因为化合价是元素的原子在形成化合物时才表现出来的一种性质,所以单质中元素的化合价为零。
(6)原子团不能独立存在,只是化合物的一个组成部分,所以原子团的化合价由其组成元素的化合价的代数和算出,原子团的化合价一定不为零。
例3 下列有关化合价的叙述,正确的是( )
A.化合价是元素与元素间化合时表现出来的性质
B.任何元素都可能显正价和负价
C.一种元素在不同化合物中可能有多种化合价,但在一种物质中只能有一种化合价
D.在原子团中各元素的正负化合价之和为零
解析 化合价是元素在形成化合物时表现出来的一种性质,故A正确。氟无正价,稀有气体元素通常显零价,故B错。有些元素可以在一种物质中显示不同的化合价,如在硝酸铵中铵根中的氮元素显-3价,硝酸根中的氮元素显+5价,故C错。原子团是化合物的一个组成部分,不能独立存在,因此所有的原子团中各元素的正负化合价之和均不为零,故D错。
答案 A
知识点三 化合价与化学式
1.根据化学式求化合价
(1)已知物质的化学式,根据化合物中,各元素的正负化合价之和为零的原则确定元素的化合价。如:
标出已知、未知化合价:;
列出式子求解:(+1)×2+x×1+(-2)×3=0,x=+4
(2)根据化合价原则,判断化学式的正误,如判断化学式KCO3是否正确。
标出元素或原子团的化合价:;
计算正负化合价之和是否为零:(+1)×1+(-2)×1=-1≠0,所以给出的化学式是错误的,正确的为K2CO3。
(3)根据化合价原则,计算原子团中某元素的化合价,如计算中氮元素的化合价和(磷酸二氢根)中磷元素的化合价。
由于带一个单位的正电荷,不是电中性的,因此各元素的化合价之和不为0,而是等于+1。
设氮元素的化合价为x,x+(+1)×4=+1 x=-3
所以在中,氮元素的化合价为-3。同理带一个单位的负电荷,也不是电中性的,因此各元素的正负化合价之和不为零,而是-1。
设磷元素的化合价为y,(+1)×2+y×1+(-2)4=-1 y=+5
所以在中磷元素的化合价为+5。
(4)根据化合价原则,确定物质按化合价排序。如H2S、S、SO2、H2SO4四种物质中均含有硫元素,并且硫元素的化合价在四种物质中分别为-2、0、+4、+6,故这四种物质是按硫元素的化合价由低到高的顺序排列的。
例4 偏钛酸钡(Bax TiO3)因其显著的“压电效应”而广泛地应用于超声波发生装置中。已知偏钛酸钡中钛元素的化合价为+4,则其化学式中x的数值为( )
A.1 B.2 C.3 D.4
解析 钡元素显+2价,钛元素显+4价,氧元素显-2价,根据在化合物中,各元素的正负化合价之和为零,可得:(+2)×x+(+4)+(-2)×3=0,则x=1
答案 A
2.根据化合价写化学式
根据在化合物中,各元素的正负化合价之和等于零的原则,已知元素的化合价可以推出实际存在的物质的化学式以最小公倍数法为例:
各步
简记
步骤
举例
写
写出化合物中各元素的符号,通常把正价元素(或原子团)写在左边,负价元素(或原子团)写在右边
Al O
求
求出两种元素的正负化合价绝对值的最小公倍数,然后求出各元素的原子数
因为=6,所以Al的原子数为6÷3=2,O的原子数为6÷2=3
标
把原子数写在各元素符号的右下角,即得化学式(如果原子数为1,则省略不写)
Al2O3
验
计算正价总数跟负价总数的代数和是否等于零,检查化学式的正确性
(+3)×2+(-2)×3=0,所
以该化学式正确
【知识拓展】 十字交叉法
各步
简记
步骤
例1:硫酸铝
例2:氧化钙
排列
分析名称,确定元素符号(或原子团)的顺序
铝 硫酸根
Al SO4
钙 氧
Ca O
标价
标上化合价
、
、
约简
将化合价的绝对值约成最简整数比
、
、
交叉
将整数交叉写在元素符号(或原子闭)的右下角
检验
根据各元素正负化合价之和是否为零,检验正误
(+3)×2+(-2)×3=0
(+2)+(-2)=0
3.化学式的书写
(1)单质化学式的书写
单质种类
化学式的书写方法
书写示例
解释
稀有气体
用元素符号表示
氦气:He
氖气:Ne
稀有气体都是由原子直接构成的
金属
用元素符号表示
铁:Fe
铜:Cu
金属都是由原子直接构成的
常温下为固态的大多数非金属
用元素符号表示
硫:S
碳:C
固态非金属的结构比较复杂,因此规定直接用元素符号表示它们的化学式
由双原子或多原子分子构成的非金属
先写出组成该非金属的元素符号,再在元素符号的右下角标出原子个数来表示它的化学式
氧气:O2
氢气:H2
臭氧:O3
这样不但能表示该非金属是由什么元素组成的,还能表示它的分子构成
(2)化合物化学式的书写
化学式的写法
化学式的读法
氧化物
氧元素符号在后,另一元素符号在前,如CuO,CO2,等
从后向前读作“氧化某",如CuO读作氧化铜;有时需读出原子个数,如Fe3O4,读作“四氧化三铁”
由金属元素和非金属元素(除氧元素外)组成的化合物
非金属元素符号在后,金属元素符号在前,如 K2S、CaCl2,等
从后向前读作“某化某”,如K2S读作“硫化钾”;有时需读出原子个数,如FeCl3,读作“三氯化铁”
【知识拓展】 在读氧化物时,一般读作“几氧化儿某”,数字为1时一般不读;若元素具有可变化合价且氧原子的个数为1,此时"1"要读出来,如CO2,读作“二氧化碳",CO读作“一氧化碳"。
例5 (2018上海黄浦一模)下列物质的化学式书写正确的是( )
A.氯化镁:MgCl B.氧化铝:AlO C.硫酸锌:ZnSO4 D.氢氧化铁:Fe(OH)2
解析 氯化镁(MgC1)的化学式书写错误,因为(+2)+(-1)≠0,不符合“在化合物中,各元素的正负化合价之和为零”的原则,应改为MgCl2;因氧化铝中氧元素的化合价为-2,铝元素的化合价为+3,由化合物中各元素的正负化合价之和为零可知,氧化铝的化学式应为Al2O3;氢氧化铁中,铁元素的化合价是+3,氢氧根的化合价是-1,故氢氧化铁的化学式是Fe(OH)3。
答案 C
例6 A、B、C三种元素的化合骨分剥为+1、+5、- 2.由这三种元素组成的化合物为( )
A2BC4 B.ABC3 C.A2BC3 D.A3BC4
解析 根据在化合场中,各元素的正负化会骨之和为零的原则,计算各个选项中的化合之和是否为零即可,A中,2×(+1)+(+5)- 4×(-2)≠0,错误;B中,(+1)+(+5)+3×(-2)=0,正确;C中,2×(+1)+(+5)+3×(-2)≠0,错误;D中,3×(+1)+(+5)+4×(+1)=0,正确。
答案 BD
知识点四 有关化学式的计算
1.化学式量的计算
化学式量就是某物质化学式中各原子的相对原子质量的总和,对于由分子构成的物质,其化学式量也叫作相对分子质量。
如化学式为AmBn的物质的化学式量=A的相对原子质量×m+8的相时原子质量×n。
2.根据化学式计算其组成元素的质量比
化合物中各元素的质量比是原子个数与相对原子质量的乘积之比,即各元素原子的祖时原子质童总和之比。
如化学式为AmBn的物质中,A、B两元素的质量比=(A的相时原子质量× m): (B的相对原子质量×n)。
【知识规展】(1)在化学式中,原子个数比等于元素的质量除以其相对原子质量的商之比。如AmBn中A、B两元素的质量分别为M、N,则化学式中A、B两元素的原子个数比m:n = 。
(2)当化学式中含有多种元素时,根据化学式可以计算出全部元素的质量比,也可以计算出其中某几种元素的质量比。
例7 某氮的氧化物中,氮氧元素的质量比为7:16,则该此合物的化学式是( )
A.NO B.NO2 C.N2O3 D.N2O4
解析 根据“化合物中各元素的质量比 = 各原子的相对原子质量×原子个数之比”进行分析解答。某氮的氧化物中,氮、氧的质量比为7 : 16,则该氮的氧化物中的氮原子和氧原子的个数比为=1 : 2,故该化合物的化学式NO2或N2O4。
答案 BD
3.计算物质中某元素的质量分数
(1)定义:物质中某元素的质量分数,就是该元素的质量与物质的总质量之比。
计算公式:某元素的质量分数=×100%
如AmBn中A元素的质量分数=×100%
(2)化学式中质量分数的应用
①已知物质的质量求所含某元素的质量
利用公式:元素的质量=物质的质量×该元素的质量分数
②已知所含元素的质量求物质的质量
利用公式:物质的质量=元素的质量÷该元素的质量分数
③根据元素的质量分数确定物质的化学式
例8 (2019甘肃兰州中考改编)苯甲酸钠(C7H5O2Na)是一种食品添加剂,广泛用于食品工业中。请计算:
(1)C7H5O2Na的化学式量是_______________;
(2)C7H5O2Na中碳、氧两种元素的质量比是________________;
(3) 14.4 g苯甲酸钠中含有钠元素多少克? (写出计算过程)
解析 (1)化学式量等于各原子的相对原子质量×原子个数之和C7H5O2Na的化学式量为12×7+1×5+16×2+23=144 ;(2)=中碳、氧元素的质量比为(12×7):(16×2)= 21 : 8;(3)一定质量的物质中某元素的质量等于物质的质量乘以该元素的质量分数,14.4 g苯甲酸钠中钠元素的质量为14.4 g ×( ×100%) = 2.3 g。
答案 (1) 144 (2)21: 8 (3)14.4 g ×( ×100%) = 2.3 g
答:14.4 g苯甲酸钠中含有钠元素的质量是2.3g。
基础闯关全练
知识点一 物质组成的表示
1.(2019上海徐汇一模)化学符号“H2O”表示的意义错误的是( )
A.水这种物质 B.水由氢元素和氧元素组成
C.水分子中含有氢分子 D.一个水分子由两个氢原子和一个氧原子构成
2.铁是我们生活中最常见的物质之一,其化学式为Fe,下列四位同学在讨论Fe的意义,其中错误的是( )
知识点二 化合价
3.次氯酸(HCIO)具有杀菌消毒的作用,HCO中氯元素的化合价表示正确的是( )
A. B. C. D.
4.(2019山东滨州中考)根据你对元素知识的认识,请在横线上依次填写有关铝元素的5个信息:
知识点三 化合价与化学式
5.下列物质的化学式,书写正确的是( )
A.碳酸钠:Na2CO3 B.氢氧化钠:NaOH2 C.氧化铁:FeO D.硫酸:HSO4
6.(2018山东菏泽曹县期末)地壳中含量最多的金属元素与含量最多的非金属元素形成的化合物是( )
A. SiO2 B. Fe2O3 C.CaO D.Al2O3
7.(2019甘肃兰州中考)高铁酸钠是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。其化学式为Na2FeO4,其中Fe元素的化合价是( )
A.+6 B.+4 C.+3 D.+2
知识点四 有关化学式的计算
8.下列计算错误的是( )
A.Mg(OH)2的化学式量:24+(16+1)×2=58
B.SO2中硫元素与氧元素的质量比为1:1
C.NH4NO3中氮元素的质量分数:×100%=17.5%
D.18g水(H2O)中含氢元素的质量:18g×(×100%)=2 g
9.维生素C(C6H8O6)主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。计算:
(1)维生素C的相对分子质量为_______________。
(2)维生素C中碳、氢两种元素的质量比为____________(写最简比)。
(3)维生素C中___________元素的质量分数最大。
能力提升全练
知识点一 物质组成的表示
1.绿茶中的单宁酸具有清热解毒、抗癌等功效,其化学式为C76H52O46下列关于单宁酸的说法不正确的是( )
A.它由C、H、O三种元素组成 B.一个分子中含76个碳原子
C.分子中C、H、O原子个数比为38:26:23 D.一个分子中含23个氧分子
2.口香糖中的木糖醇是一种新型甜味剂,它的结构如图3-3-1。下列关于木糖醇的说法错误的是
( )
A.木糖醇分子中C、H、O原子的个数比为5:12:5
B.一个木糖醇分子中含有22个原子
C.木糖醇属于化合物
D.木糖醇是由多个原子构成的纯净物
知识点二 化合价
3.(2018山东威海经济技术开发区期末)下列化学符号中数字表示的意义正确的是( )
A.2Na:“2”表示两个钠元素
B.S2-:“2-”表示硫元素的化合价为负二价
C. :“+2”表示镁离子带有两个单位的正电荷
D.CO2:“2”表示一个二氧化碳分子中含有两个氧原子
4.录像用的高性能磁粉的主要材料之一是由三种元素组成的、化学式为CoxFe3-xO3+x的化合物。已知氧元素的化合价为-2,钴(Co)和铁元素的化合价可能是+2或+3,且上述化合物中每种元素只有一种化合价,则x值为_________,铁元素的化合价为________,钴元素的化合价为__________。
5.我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律。如图3-3-2列出的是1~18号元素的部分最高正化合价和最低负化合价。请阅读并回答下列问题。
(1)11号元素属于_________(填“金属”或“非金属”)元素,它在化学反应中形成的离子与______(填元素符号)原子具有相同的核外电子排布。
(2)16号元素的原子核外电子数为__________,推测该元素的最低负化合价为________,其最高正化合价与氧元素组成的化合物的化学式为__________。
(3)第二横行中金属元素共有________种(填“1”“2”“3”“4”或“5”)。
知识点三 化合价与化学式
6.现有、、、四种元素,如果用指定化合价将它们按两种或三种元素结合成化合物,则最多可形成化合物的种类是( )
A.4种 B.5种 C.6种 D.7种
7. (2018山东淄博高青期末)X、Y元素为核电荷数小于18的元素,元素X的原子的最外电子层上有1个电子,元素Y的原子的最外电子层上有6个电子,由x,Y两元素形成的化合物的化学式可能是( )
A.XY6 B.X2Y C.XY2 D.X6Y
8. (2017福建厦门中考)含硫元素物质间发生转化SSO2SO3H2SO4
Al2(SO4)3,其中硫元素化合价发生变化的是( )
A.①② B.③④ C.①③ D.②④
9.2015年11月12日,2015年版第五套人民币100元纸币正式发行面世。新版100元人民币采用光变色防伪油墨印刷,防伪油器中含有MgF2", MgF2中F元素的化合价是( )
A.+2 B.+1 C.-2 D.-1
知识点四 有关化学式的计算
10.2015年10月,中国女药学家屠呦呦因创制新型抗疟药——青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖。青蒿素的化学式为C15H22O5。请回答:
(1)青蒿素分子中碳、氧原子的个数比为____________;
(2)青蒿素中含量最高的元素是___________;
(3)564 g青蒿素中含氧元素的质量是_____________。
11. (2017山东滨州邹平实验中学期中)钙是人体中的常量元素,每日必需摄入足够量的钙。目前市场上的补钙药剂很多,图3-3-4是某种品牌的补钙药品的部分说明书。
图3-3-4
请回答下列问题:
(1)碳酸钙共含有__________种元素,其中钙、碳、氧元素的质量比为____________, CaCO3中钙元素的质量分数为_______________。
(2)若每片钙片的质量为1 g,则钙片中钙元素的质量分数为_____________。
(3)如果按用量服用,每天摄入钙元素的质量为__________ g。
直击中考
1.(2018山东淄博高青期末)下列关于化合价的说法,正确的是( )
A.五氧化二磷(P2O5)中磷元素显+2价 B.氧元素的化合价一定是-2
C.非金属元素在化合物中总显负价 D.一种元素在同一种化合物中,可能显示不同的化合价
2.(2018山东青岛黄岛期末)下列化学用语与其所表达的意义一致的是( )
A.Co——1个一氧化碳分子 B.2SO4-2 ——2个硫酸根离子
C.——氧化铜中铜元素的化合价为+2 D.H2——2个氢原子
3.(2017山东烟台招远期末)2014年4月兰州发生了自来水中苯超标事故,引起人们对水安全的关注。已知苯的化学式为C6H6,下列有关说法正确的是( )
A.苯中的C、H元素的质量比为12:1
B.苯分子是由6个碳元素和6个氢元素组成的
C.苯分子中碳原子的结构示意图为
D.苯中碳、氢元素位于元素周期表的同一横行
4.(2019山东济宁中考)下列化学反应中,元素的化合价没有发生变化的是( )
①CO2+H2O H2CO3
②NH4HCO3 H2O+CO2↑+NH3↑
③2H2S+O2 2S↓+2H2O
④2NaOH+CuCl2 Cu(OH)2↓+2NaCl
A.①②③ B.①②④ C.②③④ D.①③④
5.(2018山东聊城中考)很多饮料中都含有柠檬酸(C6H8O7)。下列关于柠檬酸的说法中正确的是( )
A.属于氧化物 B.由6个碳原子、8个氢原子和7个氧原子组成
C.分子中氧元素的质量分数最大 D.分子中碳、氢、氧三种元素的质量比为6:8:7
6.(2019山东淄博中考)如图3-3-5是钠元素和硫元素的原子结构示意图,以及这两种元素摘自元素周期表的图示,下列说法错误的是( )
A.钠元素和硫元素的原子序数分别为11和16
B.钠元素和硫元素的核外电子数分别是1和6
C.钠元素和硫元素的原子核外都有3个电子层
D.钠元素和硫元素形成的常见化合物的化学式为Na2S
7.(2019山东泰安中考改编)在世界范围内,据统计化肥对粮食增产的贡献率已超过40%。图3-3-6是两种氮肥标签的一部分。
请根据图示中的信息回答下列问题:
(1)从标签上看,碳酸氢铵不同于尿素的化学性质是_____________(填字母序号);
A.易溶于水 B.受热易分解 C.有挥发性
(2)碳酸氢铵的化学式量为________________;
(3)纯尿素中氮元素的质量分数为__________,这种尿素肥料的纯度至少为_________。(计算结果精确至0.1%)
参考答案及解析
基础闯关全练
1.C 水分子中含有氢原子和氧原子,不含氢分子。
2.D 铁是由铁原子直接构成的,其元素符号为Fe,可表示铁这种物质、一个铁原子,还可表示铁是由铁元素组成的,不能表示一个铁分子。
3. C HCIO中H的化合价为+1、O的化合价为-2,设氯元素的化合价为x,根据在化合物中各元素正负化合价之和为零,可知(+1)+x+(-2)=0,解得x=+1,所以氯元素的化合价表示为。
4.答案 3 金属 失 +3 A12O3
解析 原子中,质子数=核外电子数,因此铝原子最外层电子数为13-2-8=3;铝含“钅”部首,属于金属元素;铝原子的最外层电子数为3,在化学反应中易失去这3个电子而形成带3个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,则该元素的化合价为+3;氧化铝中铝元素显+3价,氧元素显-2价,其化学式为Al2O3。
5.A 碳酸钠中钠元素的化合价为+1,而碳酸根的化合价为-2,所以碳酸钠的化学式为Na2CO3;氢氧化钠中,钠元素显+1价,氢氧根显-1价,其化学式为NaOH;氧化铁中铁元素的化合价为+3,氧元素的化合价为-2,其化学式为Fe2O3;硫酸中氢元素显+1价,硫酸根显-2价,其化学式为H2SO4。
6.D 地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素。铝的化合价是+3,氧一般显-2价,因此二者形成的化合物的化学式为Al2O3。
7.A 根据在化合物中,各元素的正负化合价之和为零的原则,钠元素显+1价,氧元素显-2价,设铁元素的化合价是x,可知高铁酸钠(Na2FeO4)中(+1)×2+x+(-2)×4=0,则x=+6。
8.C NH4NO3中氮元素的质量分数为×100%=35%。
9.答案 (1)176 (2)9:1 (3)氧
解析 (1)维生素C的相对分子质量为12×6+1×8+16×6=176。
(2)维生素C中碳、氢两种元素的质量比是(12×6):(1×8)=9:1。
(3)维生素C中碳元素的质量为12×6=72,氢元素的质量为1×8=8,氧元素的质量为16×6=96,氧元素的质量最大,则氧元素的质量分数最大。
能力提升全练
1.D 根据单宁酸的化学式C76H52O46可知,单宁酸含有C、H、O三种元素;每一个分子中含有76个碳原子、52个氢原子、46个氧原子,而不是含有23个氧分子。
2.D 分析题图可知,木糖醇的化学式为C5H12O5。木糖醇的一个分子是由5个碳原子、12个氢原子和5个氧原子构成的,因而木糖醇分子中C、H、O的原子个数比为5 : 12:5。木糖醇的一个分子中含有的原子个数为5+12+5 = 22个。木糖醇是由C、H、O三种元素组成的纯净物,是化合物。木糖醇是由木糖醇分子构成的,不是由原子直接构成的物质。
3.D 元素只讲种类,不讲个数,2Na表示2个钠原子,不能表示2个钠元素,A错误;S2- 表示的是硫离子,"2-"表示硫离子带两个单位的负电荷,不表示化合价,B错误;O表示氧化镁中镁元素的化合价为+2,不表示镁离子,C错误。
4.C 答案 1 +3 +2
解析 通过观察分析,若钴和铁元素的化合价相同,根据化合物中各元素的正负化合价之和为零,得x=0或1.5,不符合题意,则该化合物中钻和铁元素的化合价不同,因此钴、铁元素的化合价可能分别为+2,+3或+3,+2,考虑到x≠0,符合要求的应是钻元素的化合价为+2,铁元素的化合价为+3.根据化合物中,各元素的正负化合价之和为零,得到(+2)×x+(+3)×(3-x)+(-2)×(3+x)=0,解得x=1.
5.答案 (1)金属 Ne (2)16 -2 SO3 (3)2
解析 (1)11号元素是钠元素,属于金属元素,失去电子后,形成的钠离子与氛原子具有相同的核外电子排布。
(2) 16号元素的原子核外电子数为16,在化学反应中能得到两个电子,形成硫离子,带两个单位的负电荷,化合价为-2,最外层电子数为6,故其最高正化合价为+6,氧元素的化合价通常为-2,因此二者组成的化合物的化学式为SO3 。
(3)元素周期表的第二横行中金属元索共有钾、铍两种。
6.C 根据各种元素的化合价可以形成的化合物有:氢元素能和氧元素形成水,能和氧元素、硫元素形成硫酸,能和氧元素、钠元素形成氢氧化钠;氧元素能和硫元素形成三氧化硫,能和钠元素形成氧化钠,能和硫元素、钠元素形成硫酸钠,故最多可形成化合物的种类是6种。
7.B 元素X原子的最外层有1个电子,在化学反应中易失去电子,其化合价为+1;元素Y原子的最外层电子数为6,在化学反应中易得到两个电子,其化合价为-2,故X、Y形成的化合物的化学式可能为X2Y。
8.A 根据单质中元素的化合价为零,5属于单质,故硫元素的化合价为0,氧元素显-2价,设一氧化硫中硫元素的化合价是x,根据在化合物中,各元素的正负化合价之和为零,可得x+(-2)×2=0,则x=+4,以此法计算其余各物质中硫元素的化合价,然后进行判定,经计算知,硫元素化合价发生变化的是①、②。
9.D 根据在化合物中,各元素的正负化合价之和为零,设MgF2中F元素的化合价为x,则:(+2)+2x=0,x= -1
10. 答案 (1)3 :1 (2)C (3)160 g
解析 (1)由青蒿素的化学式可知,一个青蒿素分子是由15个碳原子22个氢原子和5个氧原子构成的,则青蒿素分子中C、O原子个数比为15 : 5=3 : 1。
(2)青蒿素分子中C、H、O三种元素的质量比为(12×15):(1×22) :(16×5)=90 : 11 : 40,由此可以判断青蒿素中碳元素的含量最高。
(3)564 g青蒿素中含氧元素的质量为564g×(×100%)= 160 g。
11.答案 (1)三 10:3: 12 40% (2)25% (3)0.5
解析 (1)根据碳酸钙的化学式可确定,碳酸钙是由Ga、C、O三种元素组成的,其中Ca、C、O的质量比为40: 12:(16×3)=10:3:12;其中钙元素的质量分数×100%=40%。
(2)每片钙片的质量为1 g,每片含碳酸钙0.625 g,则每片含钙元素的质量为0.625 g×40%=0.25g,钙片中钙元素的质量分数为×100%=25%。
(3)每片含碳酸钙0.625 g,每次一片,每天2次,则每天补充钙元素的质量为0.625g×2×40%=0.5g。
直击中考
1.D 五氧化二磷中氧元素的化合价为-2,设磷元素的化合价为x,根据在化合物中各元素的正负化合价之和为零,可得2x+5×(-2)=0,解得x=+5,A错误;氧元素在化合物中一般显-2价,但在氧气单质中,氧元素的化合价为0,B错误;非金属元素在与氢或金属元素化合时,一般显负价,但当其与氧元素化合时,则一般显正价,如SO2中,硫元素的化合价为+4,C错误;一种元素在同一种化合物中可以显示不同的化合价,如NH4NO3中氮元素分别显-3价和+5价,D正确。
2.C Co表示1个原子,或表示钴元素,或表示钻这种物质,不能表示一氧化碳分子,1个一氧化碳分子应该是CO,A错误;硫酸根离子的符号应为SO42-,选项中硫酸根离子的符号书写错误,B错误;H2是氢气的化学式,表示氢气(氢气是由氢元素组成的)、表示一个氢分子、表示每个氢分子是由两个氢原子构成的,而2个氢原子应该是在氢元素符号的前面书写2,即2H,D错误。
3.A 苯的化学式是C6H6,其中碳、氢元素的质量比为(12×6):(1×6)=12:1,A正确;苯是由碳元素和氢元素组成的,元素只讲种类,不讲个数,B错误;碳是6号元素,核外电子数与核内质子数相等,其原子结构示意图的最外层电子数是4,C错误;碳原子的核外有两个电子层,位于第二横行,氢原子有一个电子层,在元素周期表的第一横行,D错误.
4.B ①、②、④反应中,各元素的化合价都没有发生变化,③反应中,反应前硫元素的化合价为-2,氧元素的化合价为0,反应后硫元素的化合价为0,氧元素的化合价为-2,氧元素和硫。
5.C 柠檬酸中有C、H、O三种元素,不属于氧化物,故A错误柠檬酸由C、H、O三种元素组成,每个柠檬酸分子由6个碳原子、8个氢原子和7个氧原子构成,故B错误;由柠檬酸分子的构成及各元素原子的相对原子质量可推知,氧元素的质量分数最大,故C正确;柠檬酸中C、HO三种元素的质量比为(12×6):(1×8):(16×7)=9:1:14,故D错误。
6.B 钠元素与硫元素的核外电子数均等于各自的质子数,钠元素的质子数是11,核外电子数是11;硫元素的质子数是16,核外电子数也是16。
7.答案 (1)B (2)79 (3)46.7% 90.6%
解析 (1)二者保存时都要防潮说明二者都易溶于水;碳酸氢铵要避免高温天气施用,说明碳酸氢铵受热易分解,此为碳酸氢铵的化学性质。
(2)碳酸氢铵的化学式量为14+1×4+1+12+16×3=79。
(3)纯尿素中氮元素的质量分数为×100%≈46.7%,题给尿素肥料的纯度至少为=90.6%。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
