粤教版九上化学 3.4 物质构成的表示式 课件 (20张PPT)
文档属性
| 名称 | 粤教版九上化学 3.4 物质构成的表示式 课件 (20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 404.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-08-18 00:00:00 | ||
图片预览








文档简介
课件20张PPT。3.4 物质组成的表示式
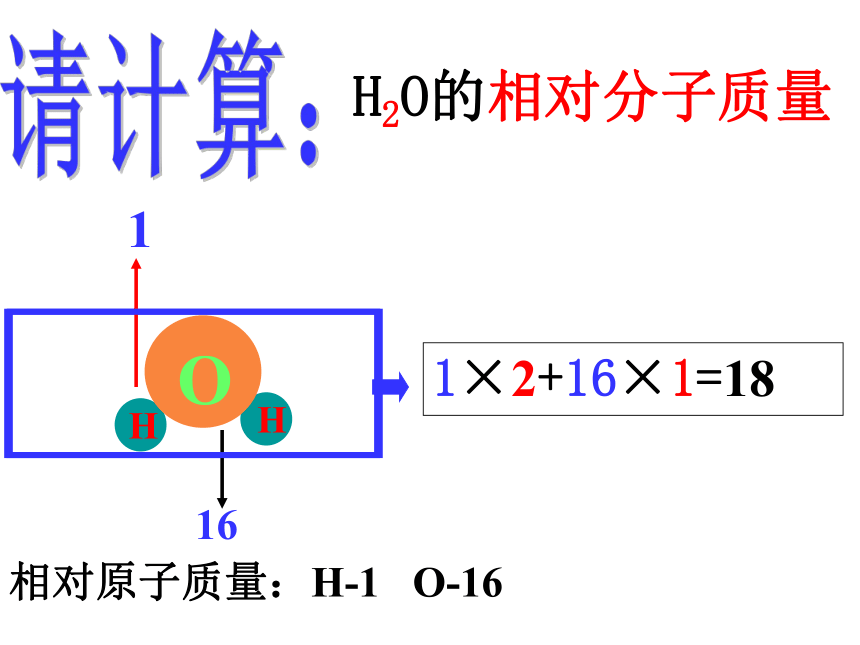
----怎样根据化学式进行计算H2O所表示的意义宏观1.表示水这种物质2.表示水由氢元素和氧元素组成微观1.表示一个水分子2.表示一个分子由两个氢原子和一个氧原子构成4.表示水由水分子构成3.表示水分子由氢原子和氧原子构成原子的质量很小,故我们采用相对原子质量,那么由原子构成的分子,分子质量仍然很小,又如何表示呢?思考0.166 ×10-26kg 2.657 ×10-26kg1×2+16×1=18请计算: 1 16
H2O的相对分子质量相对原子质量:H-1 O-16概念:化学式中各原子的相对原子质量的总和,就是相对分子质量。1.相对分子质量 概念:(相对原子质量:Ca-40 H-1 O-16)例2.计算氢氧化钙Ca(OH)2的相对分子质量
解:Ca(OH)2的相对分子质量为:
40+(16+1)×2=74
答:Ca(OH)2的相对分子质量为74巩固与提高
计算下列物质的相对分子质量。
( 相对原子质量:H—1 K—39 O—16 Mn—55
Mg —24 Cl—35.5 Cu—64 S — 32)
(1)氯酸钾[KClO3 ] (2)高锰酸钾[KMnO4]
(3)硫酸铜[CuSO4·5H2O](4)氢氧化镁[ Mg(OH) 2]
快乐尝试:学法指导:
当化学式中含括号时,可先将括号内的相对原子质量和计算出来,再乘以括号外的数字。2、计算分子中各原子个数比及原子数总和。 例、一个H2O分子中共______个原子。水分子中氢原子与氧原子个数比= _____
练习、一个H2SO4分子中共含 ______ 个原子。
H2SO4分子中氢原子与氧原子的个数比 ______活动与探究32:171 :2H2O
活动与探究=(1×2):(16×1)=1:83、计算化合物中各元素的质量之比
计算硝酸铵(NH4NO3)中氮元素、氢元素和氧元素的质量比。 (相对原子质量:H-1 N-14 O-16) 解: 硝酸铵(NH4NO3)中氮元素、氢元素和氧元素
的质量比为:
(14×2):(1×4):(16×3)=28 : 4 : 48=7 : 1 : 12学法指导: 在计算物质中各元素的质量比时应注意:同种元素的原子要合并计算。快乐尝试: 练一练:
1.氧化铁(Fe2O3)中铁元素和氧元素的质量比。
2.氢氧化镁Mg(OH)2中各元素的质量比。
3.硝酸铵(NH4NO3)中各元素的质量比。
(相对原子质量:H-1 O-16) 水(H2O)中氢元素的质量分数。4.计算化合物中某元素的质量分数交流与讨论= ×100% ≈ 11% 1. 碳酸氢酸铵是一种常用的化肥,化学式是NH4HCO3,计算碳酸氢铵中氮元素的质量分数≈17.7%解: NH4HCO3中氮元素的质量分数为:快乐尝试:2.计算硝酸铵(NH4NO3)中氮元素的质量分数。
(相对原子质量:H-1 N-14 O-16)思考:经测定某硝酸铵(NH4NO3)样品的含氮量
为30%,请判断它是纯净物还是混合物。相对分子质量的运用 1、一定量的某物质中含有某元素的质量
元素的质量=某物质的质量×某元素的质量分数
例、求32g氧化铁(Fe2O3)中铁元素的质量?解:Fe2O3的相对分子质量=56 ×2+16 ×3=160Fe2O3中铁元素的质量分数=Fe的相对原子质量×2Fe2O3的相对分子质量×100%=56 ×2160×100%=70%32gFe2O3中铁元素的质量=32g ×70%=22.4g答:32gFe2O3中铁元素的质量为=22.4g。2、某农田里的作物需施含氮 56kg的氮肥,如果施用的氮肥是尿素[ CO(NH2)2 ],则需要多少kg 尿素才含有56kg的氮元素?解:尿素的相对分子质量=12+16+(14+1×2) ×2=60尿素中氮元素的质量分数=N的相对原子质量×2尿素的相对分子质量×100%=14×260×100%=46.7%要含56kg的氮元素需尿素质量=56kg÷46.7%=120kg答:需要尿素的质量为120kg。实战训练营
1.Mg(OH)2相对分子质量的计算式为 ( )
A.24+16+1×2 B. 24×(16+1)×2
C. 24×16+1×2 D. 24+(16+1)×2
2.2 H2O的计算式为 ( )
A. 2+1×2+16 B. 2×1×2×16
C. 2 ×(1×2+16) D. 2×1×2+16
学以致用DC2.N(NO2)3是科学空2011年发现的一种新型火箭燃料。试计算: (1)N(NO2)3的相对分子质量; (2)N(NO2)3中氮元素和氧元素的质量比; (3)N(NO2)3中氮元素的质量分数 通过本节课的学习,你有哪些收获?课堂小结:
----怎样根据化学式进行计算H2O所表示的意义宏观1.表示水这种物质2.表示水由氢元素和氧元素组成微观1.表示一个水分子2.表示一个分子由两个氢原子和一个氧原子构成4.表示水由水分子构成3.表示水分子由氢原子和氧原子构成原子的质量很小,故我们采用相对原子质量,那么由原子构成的分子,分子质量仍然很小,又如何表示呢?思考0.166 ×10-26kg 2.657 ×10-26kg1×2+16×1=18请计算: 1 16
H2O的相对分子质量相对原子质量:H-1 O-16概念:化学式中各原子的相对原子质量的总和,就是相对分子质量。1.相对分子质量 概念:(相对原子质量:Ca-40 H-1 O-16)例2.计算氢氧化钙Ca(OH)2的相对分子质量
解:Ca(OH)2的相对分子质量为:
40+(16+1)×2=74
答:Ca(OH)2的相对分子质量为74巩固与提高
计算下列物质的相对分子质量。
( 相对原子质量:H—1 K—39 O—16 Mn—55
Mg —24 Cl—35.5 Cu—64 S — 32)
(1)氯酸钾[KClO3 ] (2)高锰酸钾[KMnO4]
(3)硫酸铜[CuSO4·5H2O](4)氢氧化镁[ Mg(OH) 2]
快乐尝试:学法指导:
当化学式中含括号时,可先将括号内的相对原子质量和计算出来,再乘以括号外的数字。2、计算分子中各原子个数比及原子数总和。 例、一个H2O分子中共______个原子。水分子中氢原子与氧原子个数比= _____
练习、一个H2SO4分子中共含 ______ 个原子。
H2SO4分子中氢原子与氧原子的个数比 ______活动与探究32:171 :2H2O
活动与探究=(1×2):(16×1)=1:83、计算化合物中各元素的质量之比
计算硝酸铵(NH4NO3)中氮元素、氢元素和氧元素的质量比。 (相对原子质量:H-1 N-14 O-16) 解: 硝酸铵(NH4NO3)中氮元素、氢元素和氧元素
的质量比为:
(14×2):(1×4):(16×3)=28 : 4 : 48=7 : 1 : 12学法指导: 在计算物质中各元素的质量比时应注意:同种元素的原子要合并计算。快乐尝试: 练一练:
1.氧化铁(Fe2O3)中铁元素和氧元素的质量比。
2.氢氧化镁Mg(OH)2中各元素的质量比。
3.硝酸铵(NH4NO3)中各元素的质量比。
(相对原子质量:H-1 O-16) 水(H2O)中氢元素的质量分数。4.计算化合物中某元素的质量分数交流与讨论= ×100% ≈ 11% 1. 碳酸氢酸铵是一种常用的化肥,化学式是NH4HCO3,计算碳酸氢铵中氮元素的质量分数≈17.7%解: NH4HCO3中氮元素的质量分数为:快乐尝试:2.计算硝酸铵(NH4NO3)中氮元素的质量分数。
(相对原子质量:H-1 N-14 O-16)思考:经测定某硝酸铵(NH4NO3)样品的含氮量
为30%,请判断它是纯净物还是混合物。相对分子质量的运用 1、一定量的某物质中含有某元素的质量
元素的质量=某物质的质量×某元素的质量分数
例、求32g氧化铁(Fe2O3)中铁元素的质量?解:Fe2O3的相对分子质量=56 ×2+16 ×3=160Fe2O3中铁元素的质量分数=Fe的相对原子质量×2Fe2O3的相对分子质量×100%=56 ×2160×100%=70%32gFe2O3中铁元素的质量=32g ×70%=22.4g答:32gFe2O3中铁元素的质量为=22.4g。2、某农田里的作物需施含氮 56kg的氮肥,如果施用的氮肥是尿素[ CO(NH2)2 ],则需要多少kg 尿素才含有56kg的氮元素?解:尿素的相对分子质量=12+16+(14+1×2) ×2=60尿素中氮元素的质量分数=N的相对原子质量×2尿素的相对分子质量×100%=14×260×100%=46.7%要含56kg的氮元素需尿素质量=56kg÷46.7%=120kg答:需要尿素的质量为120kg。实战训练营
1.Mg(OH)2相对分子质量的计算式为 ( )
A.24+16+1×2 B. 24×(16+1)×2
C. 24×16+1×2 D. 24+(16+1)×2
2.2 H2O的计算式为 ( )
A. 2+1×2+16 B. 2×1×2×16
C. 2 ×(1×2+16) D. 2×1×2+16
学以致用DC2.N(NO2)3是科学空2011年发现的一种新型火箭燃料。试计算: (1)N(NO2)3的相对分子质量; (2)N(NO2)3中氮元素和氧元素的质量比; (3)N(NO2)3中氮元素的质量分数 通过本节课的学习,你有哪些收获?课堂小结:
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
