京改版九年级上册化学 7.1 质量守恒定律 课件(47张PPT)
文档属性
| 名称 | 京改版九年级上册化学 7.1 质量守恒定律 课件(47张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-08-20 00:00:00 | ||
图片预览










文档简介
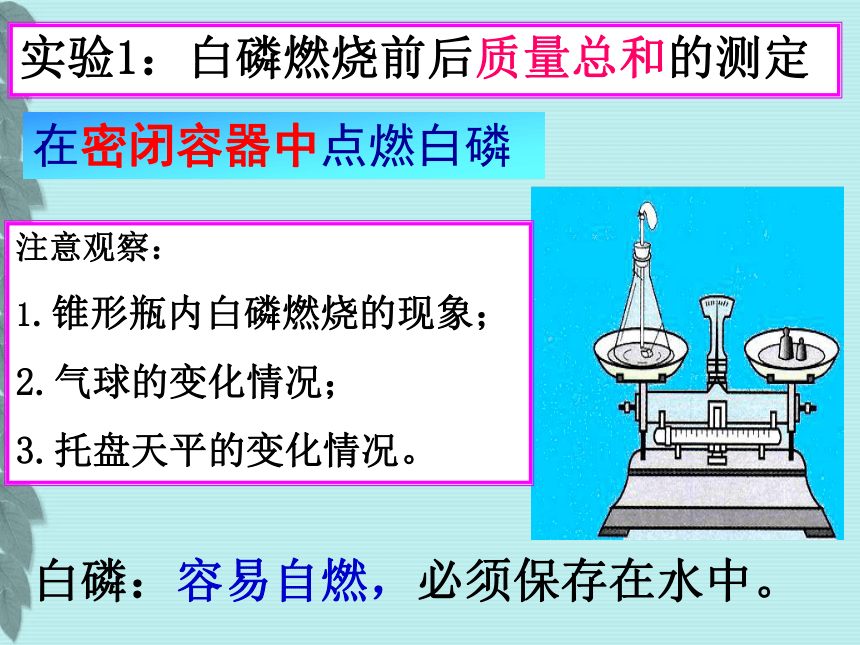
课件47张PPT。课题1 质量守恒定律想一想 物质在发生化学变化时,反应物的质量总和与生成物的质量总和之间存在什么关系呢?我们的猜想:可能。。。= 或 > 或 <有以下2个实验,请注意观察实验现象,讨论实验结果:1、白磷在空气中燃烧2、铁钉与硫酸铜溶液反应在密闭容器中点燃白磷白磷:容易自燃,必须保存在水中。实验1:白磷燃烧前后质量总和的测定注意观察:
1.锥形瓶内白磷燃烧的现象;
2.气球的变化情况;
3.托盘天平的变化情况。 白磷燃烧产生大量白烟,放出热量,
气球先变大后变小,结论:
反应物质量总和 生成物质量总和
现象:天平仍保持平衡。=总质量总质量=对比思考:反应前物质(或物体)反应后物质(或物体)锥形瓶细砂橡皮塞玻璃管、气球(空气)氧气氮气白磷锥形瓶细砂橡皮塞玻璃管、气球五氧化二磷(剩余气体)氮气结论:白磷质量+氧气质量=五氧化二磷质量稀有气体等稀有气体等白磷五氧化二磷氧气气球的作用:防止由于气体膨胀而冲开瓶塞。实验前实验中实验后铁钉跟硫酸铜溶液反应
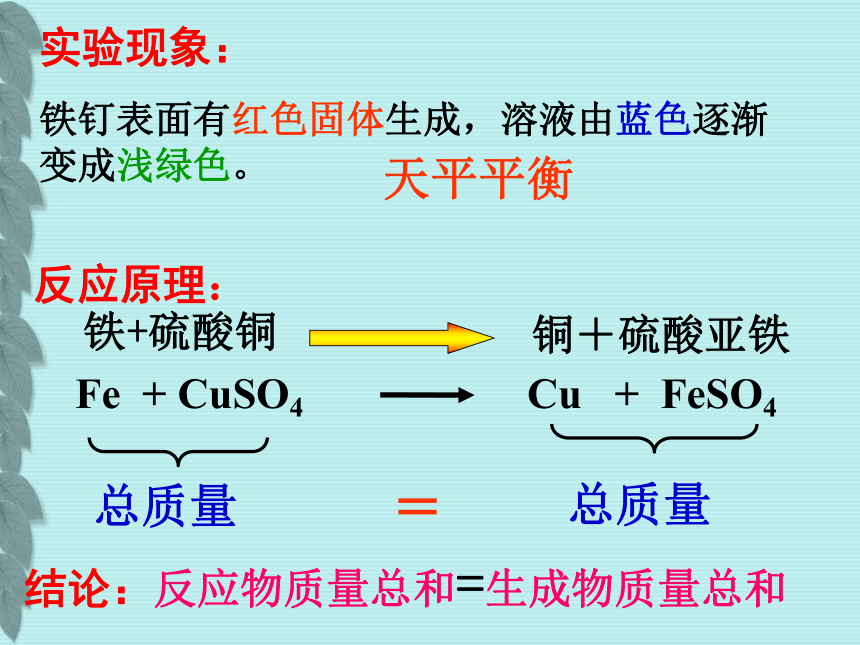
前后质量总和的测定实验中实验现象:反应原理:结论:反应物质量总和=生成物质量总和
铁钉表面有红色固体生成,溶液由蓝色逐渐变成浅绿色。天平平衡总质量总质量=质量守恒定律参加反应的
各物质的质
量总 和生成的各物质的质量
总和参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。实验现象:固体粉末溶解,有大量的气泡产生;反应原理:天平指针向右倾斜(变轻)天平平衡情况:(如何改进实验装置?)怎么反应后天平不平衡了呢?
那么,这个反应遵守质量守恒定律吗?反应后称量到的A装置B装置碳酸钠粉末稀盐酸改进后的实验装置思考:1、该实验的现象是什么?发出耀眼的白光,放出热量,生成白色固体思考:2、该反应的原理是什么?天平?同时还有白烟产生思考:1、该实验的现象是什么?发出耀眼的白光,放出热量,生成白色固体思考:2、该反应的原理是什么?天平?同时还有白烟产生小结:
在有气体参加或生成的化学变化
中,验证质量守恒定律时候,必
须在密闭容器中进行把握质量守恒定律应注意几点1、只适用于化学变化,不包括物理变化
2、是指质量守恒, 而不是体积、分子个数守恒 。
3、“总质量”,不能忽略气体、沉淀。
4、守恒的范围是“参加反应的物质”,没有参加反应的物质不能算在内。 质量守恒定律:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。 为什么化学反应前后的物质的质量总和相等?试用分子、原子的观点解释质量守恒的原因。想一想:思考:原子的种类 ,原子的数目 。原子的质量 。不变不变不变水电解微观示意图氧原子氢原子质量守恒的原因质量守恒的原因在一切化学反应中,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。质量守恒定律的实质 P93思考:化学反应前后,分子变化了吗?元素变化了吗?分子的种类 ,元素的种类 。物质的种类 。改变不变改变水电解微观示意图氧原子氢原子化学反应前后动动脑一定不变:原子的种类原子的数目原子的质量微观元素的种类元素的质量宏观结果:物质总质量不变(六不变)化学反应前后动动脑一定改变:(宏观)物质的种类(微观)分子的种类可能改变:分子的个数本节课你有哪些收获?质量守恒定律内容:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和原因:反应前后原子的种类、数目、质量都没有改变感受成功小结参加化学反应的各物质 生成的各物质的质量总和的质量总和等于反应后 原子数目没有增减原子种类没有改变原子质量没有变化进行有关的计算解释一些实验事实内容原因应用质量守恒定律“水变成含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”广而告之同学们,假如你是老板,你是否会加盟呢?请谈一谈你的想法?化学反应前后,元素种类不变思考:如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么结果?没有参加反应的物质包括:1、这种物质未参与反应。
例如红磷在装有空气的密闭的容器中燃烧,容器内的氮气的质量。
2、剩余的反应物。
例如,高锰酸钾分解制取氧气,未反应完的高锰酸钾质量。小结: 1、质量守恒定律:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。2、质量守恒的原因:在化学变化中
都没改变原子的种类原子的数目原子的质量3、在有气体参加或生成的化学变化中,验证质量守恒定律时候,必须在密闭容器中进行质量守恒定律的应用: 1 、解释反应前后物质的质量变化及用质量差确定某反应物或生成物的质量。
(1)在A+B=2C 的反应中,足量B与W克A完全反应后,生成12克C,则参加反应的B的质量是____________ 克(12-W)(2)反应A+B=C+D中,已知2克A和5克B参加了反应,生成了4克C,则有____克D生成。3A + B = C + D2 g 5g 4g2、推断反应物或生成物的组成元素 酒精在空气中燃烧生成二氧化碳和水,能否根据这一事实,推断出酒精中肯定会有什么元素?可能会有什么元素? 一定有的元素:
可能有的元素:C,HO
有人说他能点石(主要成分CaCO3)成金(Au),他的说法是否有科学道理?
1、定义:用化学式来表示化学反应的式子。二.化学方程式2、表明反应条件4、表示各物质之间粒子个数比1、表明反应物3、表明生成物讨论:2、化学方程式提供的信息:3、化学方程式的意义(读法)(1) 表示反应物,生成物和反应条件(宏观意义)
表示碳和氧气在点燃条件下反应,生成二氧化碳
(2)表示反应物和生成物之间各物质的质量比(宏观意义)
表示每12份质量的碳与32份质量的氧气完全反应,生成44份质量的二氧化碳。
(3)表示反应物和生成物的各粒子个数比(微观意义)
(粒子个数比即化学式前面的化学计量数之比)
表示每1个碳原子与1个氧分子反应,生成1个二氧化碳分子
化学方程式的意义 4P + 5O2 2P2O5
4×31 5×32 2×142 点燃1、表示磷和氧气在点燃条件下反应,生成五氧化二磷。3、表示每4个磷原子和5个氧分子反应,生成2个五氧化二磷分子。2、表示每124份质量的磷与160份质量的氧气完全反应, 生成284份质量的五氧化二磷。你能说!考考你 化学方程式2H2+O2 2H2O表示
A 氢气加氧气等于水
B 氢气跟氧气混合可生成水
C 在点燃条件下,每4份质量的氢气与32份质量的氧气反应生成36份的水
D 2分子氢气与1分子氧气反应,生成2分子水
C点燃 4Al+3O2 2Al2O3反应中铝,氧气,三氧化二铝的质量比是
A 27:32:102
B 27:16:43
C 4:3:2
D 9:8:17
D点燃化学方程式:遵循原则: 1、以客观事实为依据 2、遵守质量守恒定律(反应前后原子数目相等) 试一试:
看看谁最先写出氢气在氧气中燃烧生成水
化学方程式?
1、根据实验事实写出反应物和生成物的化学式P + O2 —— P2O54P + 5O2 —— 2P2O54P + 5O2 ==== 2P2O5点燃 2、配平化学方程式(使反应前后各原子数目相 等) 3、注明:反应条件(点燃、加热“△”、高温、通 电、催化剂)、生成物状态(气体↑或沉淀↓)化学方程式书写步骤(以磷在氧气中燃烧为例) 4. 改横线为等号加热:对物质的升温,常用 符号代替点燃:达到可燃物的着火点高温:达到一定的温度(>600℃)只有在反应物中没有气体参加生成物中的气体才能用气体符号在溶液中只有在反应物中没有固体参加生成物中的固体才能用沉淀符号催化剂(具体名称)最小公倍数法首先找出其中出现次数较多,且原子个数相差较多的原子作为配平起点,求出其最小公倍数,再由最小公倍数确定相关化学式的化学计量数,配平化学方程式
Fe + O2 —— Fe3O4
Mg + O2 —— MgO
H2O —— H2 + O2你能配平吗?练习:配平下列化学方程式并注明反应发生的条件:
1.锥形瓶内白磷燃烧的现象;
2.气球的变化情况;
3.托盘天平的变化情况。 白磷燃烧产生大量白烟,放出热量,
气球先变大后变小,结论:
反应物质量总和 生成物质量总和
现象:天平仍保持平衡。=总质量总质量=对比思考:反应前物质(或物体)反应后物质(或物体)锥形瓶细砂橡皮塞玻璃管、气球(空气)氧气氮气白磷锥形瓶细砂橡皮塞玻璃管、气球五氧化二磷(剩余气体)氮气结论:白磷质量+氧气质量=五氧化二磷质量稀有气体等稀有气体等白磷五氧化二磷氧气气球的作用:防止由于气体膨胀而冲开瓶塞。实验前实验中实验后铁钉跟硫酸铜溶液反应
前后质量总和的测定实验中实验现象:反应原理:结论:反应物质量总和=生成物质量总和
铁钉表面有红色固体生成,溶液由蓝色逐渐变成浅绿色。天平平衡总质量总质量=质量守恒定律参加反应的
各物质的质
量总 和生成的各物质的质量
总和参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。实验现象:固体粉末溶解,有大量的气泡产生;反应原理:天平指针向右倾斜(变轻)天平平衡情况:(如何改进实验装置?)怎么反应后天平不平衡了呢?
那么,这个反应遵守质量守恒定律吗?反应后称量到的A装置B装置碳酸钠粉末稀盐酸改进后的实验装置思考:1、该实验的现象是什么?发出耀眼的白光,放出热量,生成白色固体思考:2、该反应的原理是什么?天平?同时还有白烟产生思考:1、该实验的现象是什么?发出耀眼的白光,放出热量,生成白色固体思考:2、该反应的原理是什么?天平?同时还有白烟产生小结:
在有气体参加或生成的化学变化
中,验证质量守恒定律时候,必
须在密闭容器中进行把握质量守恒定律应注意几点1、只适用于化学变化,不包括物理变化
2、是指质量守恒, 而不是体积、分子个数守恒 。
3、“总质量”,不能忽略气体、沉淀。
4、守恒的范围是“参加反应的物质”,没有参加反应的物质不能算在内。 质量守恒定律:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。 为什么化学反应前后的物质的质量总和相等?试用分子、原子的观点解释质量守恒的原因。想一想:思考:原子的种类 ,原子的数目 。原子的质量 。不变不变不变水电解微观示意图氧原子氢原子质量守恒的原因质量守恒的原因在一切化学反应中,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。质量守恒定律的实质 P93思考:化学反应前后,分子变化了吗?元素变化了吗?分子的种类 ,元素的种类 。物质的种类 。改变不变改变水电解微观示意图氧原子氢原子化学反应前后动动脑一定不变:原子的种类原子的数目原子的质量微观元素的种类元素的质量宏观结果:物质总质量不变(六不变)化学反应前后动动脑一定改变:(宏观)物质的种类(微观)分子的种类可能改变:分子的个数本节课你有哪些收获?质量守恒定律内容:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和原因:反应前后原子的种类、数目、质量都没有改变感受成功小结参加化学反应的各物质 生成的各物质的质量总和的质量总和等于反应后 原子数目没有增减原子种类没有改变原子质量没有变化进行有关的计算解释一些实验事实内容原因应用质量守恒定律“水变成含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”广而告之同学们,假如你是老板,你是否会加盟呢?请谈一谈你的想法?化学反应前后,元素种类不变思考:如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么结果?没有参加反应的物质包括:1、这种物质未参与反应。
例如红磷在装有空气的密闭的容器中燃烧,容器内的氮气的质量。
2、剩余的反应物。
例如,高锰酸钾分解制取氧气,未反应完的高锰酸钾质量。小结: 1、质量守恒定律:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。2、质量守恒的原因:在化学变化中
都没改变原子的种类原子的数目原子的质量3、在有气体参加或生成的化学变化中,验证质量守恒定律时候,必须在密闭容器中进行质量守恒定律的应用: 1 、解释反应前后物质的质量变化及用质量差确定某反应物或生成物的质量。
(1)在A+B=2C 的反应中,足量B与W克A完全反应后,生成12克C,则参加反应的B的质量是____________ 克(12-W)(2)反应A+B=C+D中,已知2克A和5克B参加了反应,生成了4克C,则有____克D生成。3A + B = C + D2 g 5g 4g2、推断反应物或生成物的组成元素 酒精在空气中燃烧生成二氧化碳和水,能否根据这一事实,推断出酒精中肯定会有什么元素?可能会有什么元素? 一定有的元素:
可能有的元素:C,HO
有人说他能点石(主要成分CaCO3)成金(Au),他的说法是否有科学道理?
1、定义:用化学式来表示化学反应的式子。二.化学方程式2、表明反应条件4、表示各物质之间粒子个数比1、表明反应物3、表明生成物讨论:2、化学方程式提供的信息:3、化学方程式的意义(读法)(1) 表示反应物,生成物和反应条件(宏观意义)
表示碳和氧气在点燃条件下反应,生成二氧化碳
(2)表示反应物和生成物之间各物质的质量比(宏观意义)
表示每12份质量的碳与32份质量的氧气完全反应,生成44份质量的二氧化碳。
(3)表示反应物和生成物的各粒子个数比(微观意义)
(粒子个数比即化学式前面的化学计量数之比)
表示每1个碳原子与1个氧分子反应,生成1个二氧化碳分子
化学方程式的意义 4P + 5O2 2P2O5
4×31 5×32 2×142 点燃1、表示磷和氧气在点燃条件下反应,生成五氧化二磷。3、表示每4个磷原子和5个氧分子反应,生成2个五氧化二磷分子。2、表示每124份质量的磷与160份质量的氧气完全反应, 生成284份质量的五氧化二磷。你能说!考考你 化学方程式2H2+O2 2H2O表示
A 氢气加氧气等于水
B 氢气跟氧气混合可生成水
C 在点燃条件下,每4份质量的氢气与32份质量的氧气反应生成36份的水
D 2分子氢气与1分子氧气反应,生成2分子水
C点燃 4Al+3O2 2Al2O3反应中铝,氧气,三氧化二铝的质量比是
A 27:32:102
B 27:16:43
C 4:3:2
D 9:8:17
D点燃化学方程式:遵循原则: 1、以客观事实为依据 2、遵守质量守恒定律(反应前后原子数目相等) 试一试:
看看谁最先写出氢气在氧气中燃烧生成水
化学方程式?
1、根据实验事实写出反应物和生成物的化学式P + O2 —— P2O54P + 5O2 —— 2P2O54P + 5O2 ==== 2P2O5点燃 2、配平化学方程式(使反应前后各原子数目相 等) 3、注明:反应条件(点燃、加热“△”、高温、通 电、催化剂)、生成物状态(气体↑或沉淀↓)化学方程式书写步骤(以磷在氧气中燃烧为例) 4. 改横线为等号加热:对物质的升温,常用 符号代替点燃:达到可燃物的着火点高温:达到一定的温度(>600℃)只有在反应物中没有气体参加生成物中的气体才能用气体符号在溶液中只有在反应物中没有固体参加生成物中的固体才能用沉淀符号催化剂(具体名称)最小公倍数法首先找出其中出现次数较多,且原子个数相差较多的原子作为配平起点,求出其最小公倍数,再由最小公倍数确定相关化学式的化学计量数,配平化学方程式
Fe + O2 —— Fe3O4
Mg + O2 —— MgO
H2O —— H2 + O2你能配平吗?练习:配平下列化学方程式并注明反应发生的条件:
同课章节目录
- 第1章 走进化学
- 第一节 化学让世界更美好
- 第二节 实验是化学的基础
- 第2章 空气之谜
- 第一节 空气
- 第二节 氧气的制法
- 第三节 氧气的性质
- 第3章 构成物质的微粒
- 第一节 原子
- 第二节 原子核外电子的排布 离子
- 第三节 分子
- 第4章 最常见的液体——水
- 第一节 水的净化
- 第二节 水的变化
- 第三节 水资源的开发、利用和保护
- 第5章 化学元素与物质组成的表示
- 第一节 初步认识化学元素
- 第二节 物质组成的表示——化学式
- 第三节 化合价
- 第6章 燃烧的学问
- 第一节 探索燃烧与灭火
- 第二节 化学反应中的能量变化
- 第三节 化石燃料
- 第7章 化学反应的定量研究
- 第一节 质量守恒定律
- 第二节 化学方程式
- 第三节 依据化学方程式的简单计算
- 第8章 碳的世界
- 第一节 碳的单质
- 第二节 二氧化碳的性质和用途
- 第三节 二氧化碳的实验室制法
