粤教版九上化学 3.3 燃烧条件与灭火原理 课件(21张PPT)
文档属性
| 名称 | 粤教版九上化学 3.3 燃烧条件与灭火原理 课件(21张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 7.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-08-27 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
燃烧条件与灭火原理
刘 翠
随着社会的进步,火的使用越来越重要,但是,火可以造福人类,有时也会带来灾难,所以,我们就很有必要掌握燃烧条件和灭火原理。
刘 翠
燃烧需要哪些条件?
有哪些灭火的原理和方法?
这节课我们学习燃烧和灭火来解决上述问题。
下一页
上一页
刘 翠
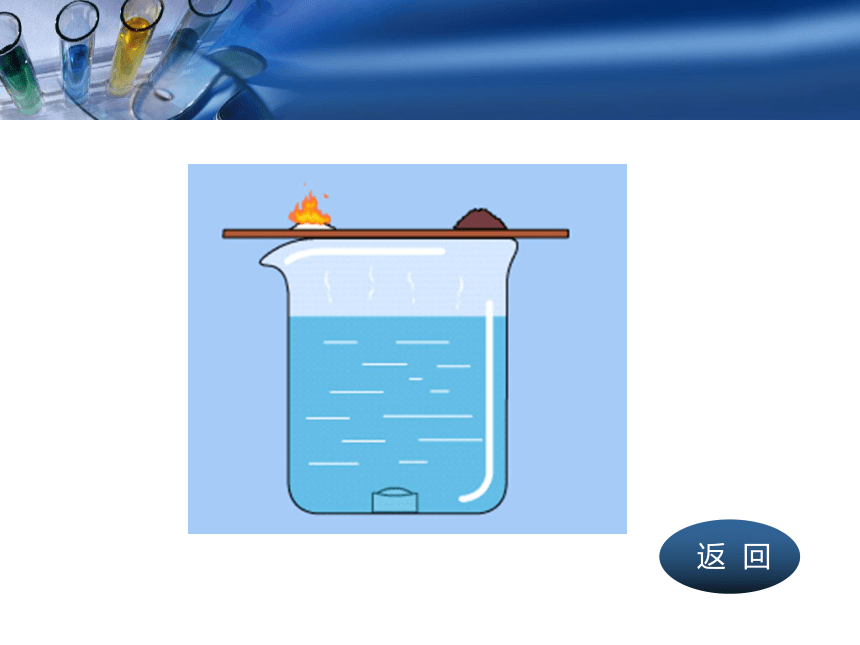
一、可燃物燃烧条件的探究:
在500ml的烧杯中注入400ml热水,热水中放入一小块白磷,烧杯上放一片薄铜片,薄铜片一端放一小堆红磷,另一端放一小块吸干水的白磷,进行实验。
上一页
下一页
刘 翠
返 回
刘 翠
1、由上述实验中铜片上的红磷不燃烧而白磷燃烧的事实,说明燃烧需要什么条件?
分析:热水的最高温度是 100 oC,加热白磷 达到白磷的着火点40 oC,加热红磷 达到红磷的着火点240 oC 。说明燃烧需要
下一页
能
不能
达到着火点
上一页
刘 翠
2、由铜片上的白磷燃烧,但水中的白磷不燃烧的事实,说明燃烧还需要什么条件
分析:铜片上的白磷和 接触,热水中的白磷 没有和 接触。说明燃烧还需要
下一页
空气
空气
空气或氧气
上一页
刘 翠
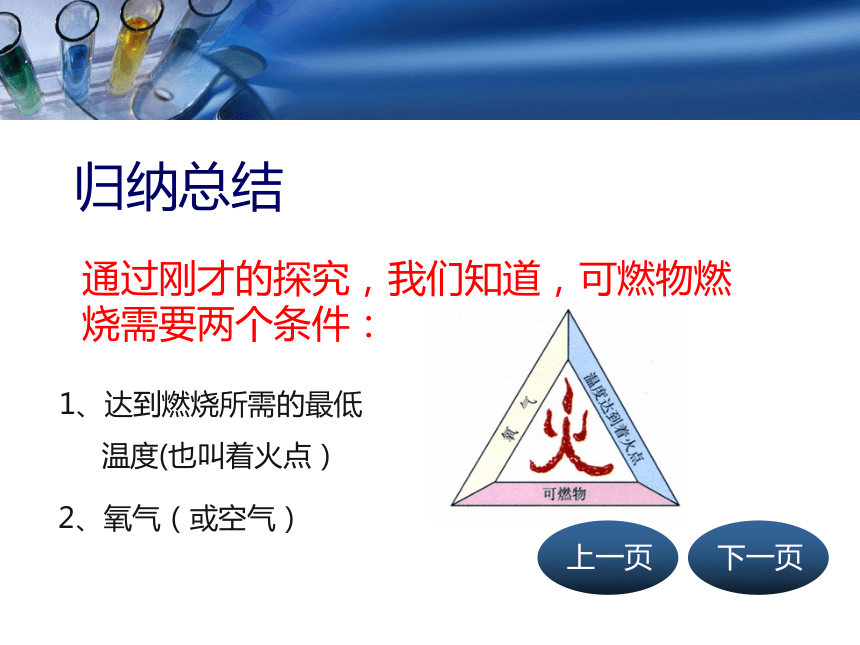
归纳总结
1、达到燃烧所需的最低
温度(也叫着火点)
下一页
通过刚才的探究,我们知道,可燃物燃烧需要两个条件:
2、氧气(或空气)
上一页
刘 翠
什么是燃烧?
通常情况下,燃烧是可燃物与氧气发生的一种发光、放热的剧烈的氧化反应。
下一页
上一页
缓慢氧化(如:动植物的呼吸作用、金属锈蚀、食物腐败、酒和醋的酿造、农家肥腐熟等)
缓慢氧化也放热,可以引起自燃
燃烧和缓慢氧化的相同点:
1、都有氧气参加
2、都放热
区别:燃烧发光,缓慢氧化不发光
上一
刘 翠
二、灭火的原理和方法
下一页
实验1
实验2
原理:破坏燃烧条件中的一个或两个条件即可灭火
上一页
刘 翠
讨论:根据燃烧的条件推论灭火的原理
1.破坏可燃物灭火原理是:
下一页
隔绝氧气或空气。
使温度降到着火点以下。
清除可燃物或使可燃物与其他物品隔离。
2.破坏氧气或空气灭火原理是:
3.破坏达到着火点灭火原理是:
上一页
刘 翠
返 回
请问以下灭火方式与破坏哪一个燃烧条件有关?
刘 翠
返 回
刘 翠
返 回
刘 翠
练习:用扇子扇煤炉火,为什么越扇越旺?而用
扇子扇蜡烛火焰,为什么一扇就灭?
分析:空气流动带走热量都会降温,煤炉火没有熄灭是因为:
下一页
补充了空气。
蜡烛火热量少,温度降到蜡烛的着火点以下。
煤炉火热量多,温度没有降到煤的着火点以下。
蜡烛火焰熄灭的是因为:
煤炉火燃烧更旺是因为:
上一页
刘 翠
课堂小结
下一页
燃烧需要三个条件:
1。物质是可燃物 2 .可燃物与氧气或空气接触
3.达到可燃物的着火点(燃烧所需要的最低温度)
灭火的原理:
1.清除可燃物或使可燃物与其他物品隔绝。
2.隔绝氧气或空气。
3.使温度降到着火点以下。(注意:着火点一般是不变的,所以不能降低着火点)
上一页
生活中的化学
这些标志你都认识吗:
逃生小知识
生活中的化学
燃烧条件与灭火原理
刘 翠
随着社会的进步,火的使用越来越重要,但是,火可以造福人类,有时也会带来灾难,所以,我们就很有必要掌握燃烧条件和灭火原理。
刘 翠
燃烧需要哪些条件?
有哪些灭火的原理和方法?
这节课我们学习燃烧和灭火来解决上述问题。
下一页
上一页
刘 翠
一、可燃物燃烧条件的探究:
在500ml的烧杯中注入400ml热水,热水中放入一小块白磷,烧杯上放一片薄铜片,薄铜片一端放一小堆红磷,另一端放一小块吸干水的白磷,进行实验。
上一页
下一页
刘 翠
返 回
刘 翠
1、由上述实验中铜片上的红磷不燃烧而白磷燃烧的事实,说明燃烧需要什么条件?
分析:热水的最高温度是 100 oC,加热白磷 达到白磷的着火点40 oC,加热红磷 达到红磷的着火点240 oC 。说明燃烧需要
下一页
能
不能
达到着火点
上一页
刘 翠
2、由铜片上的白磷燃烧,但水中的白磷不燃烧的事实,说明燃烧还需要什么条件
分析:铜片上的白磷和 接触,热水中的白磷 没有和 接触。说明燃烧还需要
下一页
空气
空气
空气或氧气
上一页
刘 翠
归纳总结
1、达到燃烧所需的最低
温度(也叫着火点)
下一页
通过刚才的探究,我们知道,可燃物燃烧需要两个条件:
2、氧气(或空气)
上一页
刘 翠
什么是燃烧?
通常情况下,燃烧是可燃物与氧气发生的一种发光、放热的剧烈的氧化反应。
下一页
上一页
缓慢氧化(如:动植物的呼吸作用、金属锈蚀、食物腐败、酒和醋的酿造、农家肥腐熟等)
缓慢氧化也放热,可以引起自燃
燃烧和缓慢氧化的相同点:
1、都有氧气参加
2、都放热
区别:燃烧发光,缓慢氧化不发光
上一
刘 翠
二、灭火的原理和方法
下一页
实验1
实验2
原理:破坏燃烧条件中的一个或两个条件即可灭火
上一页
刘 翠
讨论:根据燃烧的条件推论灭火的原理
1.破坏可燃物灭火原理是:
下一页
隔绝氧气或空气。
使温度降到着火点以下。
清除可燃物或使可燃物与其他物品隔离。
2.破坏氧气或空气灭火原理是:
3.破坏达到着火点灭火原理是:
上一页
刘 翠
返 回
请问以下灭火方式与破坏哪一个燃烧条件有关?
刘 翠
返 回
刘 翠
返 回
刘 翠
练习:用扇子扇煤炉火,为什么越扇越旺?而用
扇子扇蜡烛火焰,为什么一扇就灭?
分析:空气流动带走热量都会降温,煤炉火没有熄灭是因为:
下一页
补充了空气。
蜡烛火热量少,温度降到蜡烛的着火点以下。
煤炉火热量多,温度没有降到煤的着火点以下。
蜡烛火焰熄灭的是因为:
煤炉火燃烧更旺是因为:
上一页
刘 翠
课堂小结
下一页
燃烧需要三个条件:
1。物质是可燃物 2 .可燃物与氧气或空气接触
3.达到可燃物的着火点(燃烧所需要的最低温度)
灭火的原理:
1.清除可燃物或使可燃物与其他物品隔绝。
2.隔绝氧气或空气。
3.使温度降到着火点以下。(注意:着火点一般是不变的,所以不能降低着火点)
上一页
生活中的化学
这些标志你都认识吗:
逃生小知识
生活中的化学
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
