粤教版九上化学 3.4 物质构成的表示式 课件(25张PPT)
文档属性
| 名称 | 粤教版九上化学 3.4 物质构成的表示式 课件(25张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 91.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-08-27 00:00:00 | ||
图片预览





文档简介
课件25张PPT。1、元素符号复习巩固表示某元素表示一个某原子H(氢元素)如:三个氢原子______表示多个某原子:在元素符号前加阿拉伯数字3H(一个氢原子)元素符号==原子符号HH3、4 表示物质组成的化学式一、什么是化学式
用元素符号表示物质组成的式子叫化学式。
表示每种纯净物的组成的化学式只有一个。如:
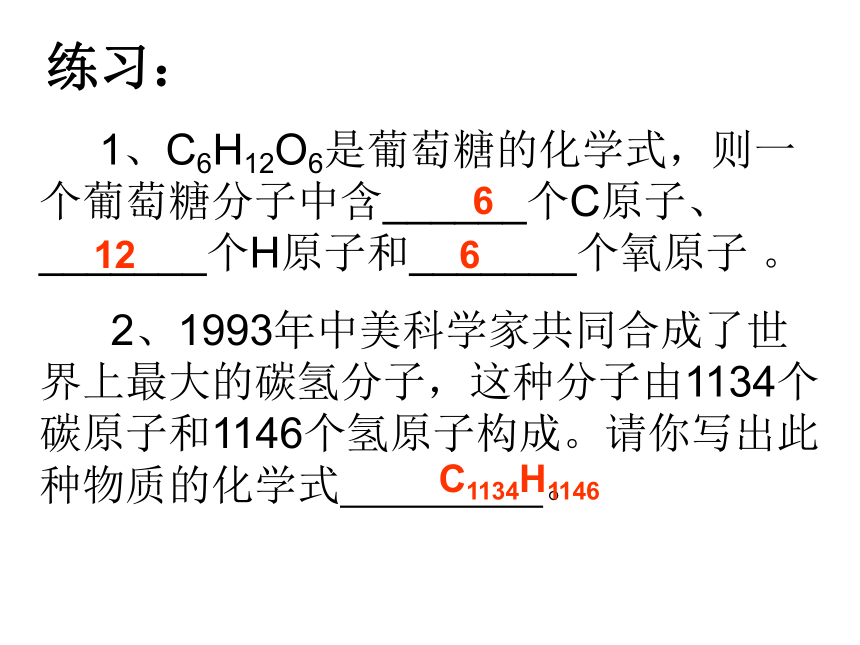
镁 Mg 铜 Cu 碳 C 磷 P 氧气 O2 氮气N2 水 H2O 五氧化二磷 P2O5 氯酸钾KClO3 1、C6H12O6是葡萄糖的化学式,则一个葡萄糖分子中含______个C原子、_______个H原子和_______个氧原子 。
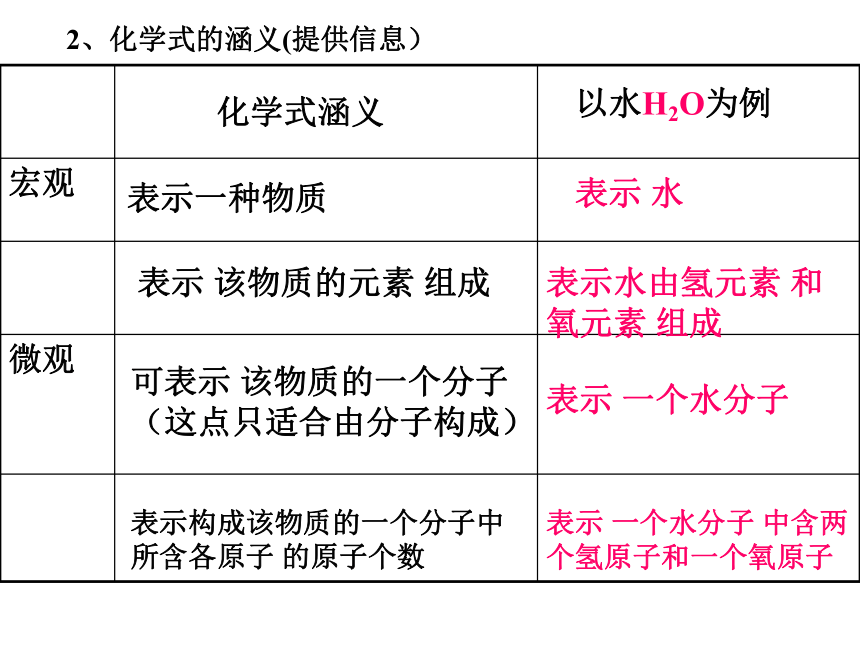
2、1993年中美科学家共同合成了世界上最大的碳氢分子,这种分子由1134个碳原子和1146个氢原子构成。请你写出此种物质的化学式 。练习:6126C1134H11462、化学式的涵义(提供信息)练一练:表示__________________表示________________________表示__________________表示________________________
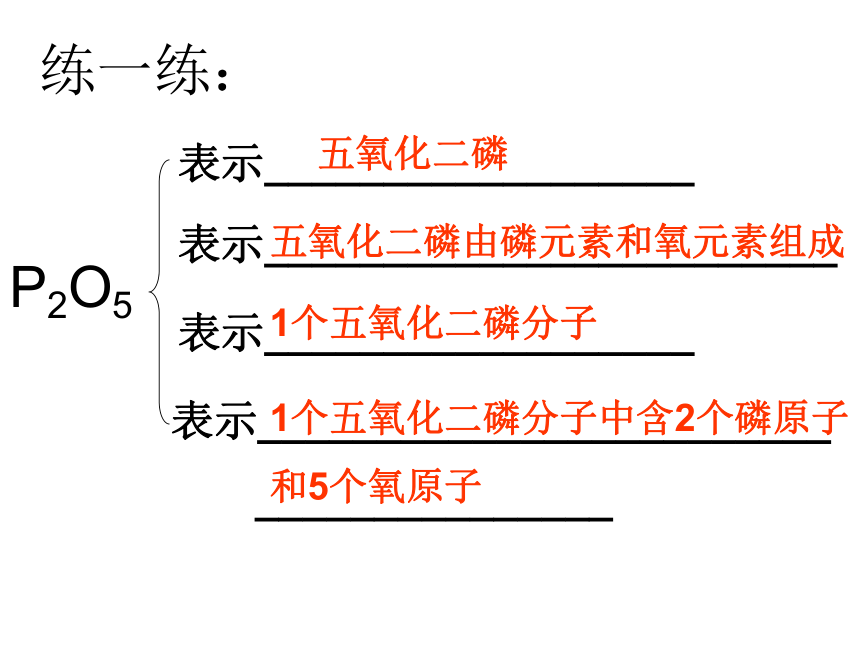
_______________P2O5五氧化二磷五氧化二磷由磷元素和氧元素组成1个五氧化二磷分子1个五氧化二磷分子中含2个磷原子
和5个氧原子3、表示多个分子的方法:
在化学式前面加上阿拉伯数字。
如:5个二氧化碳分子_______,3个氢分子______。
同样在化学式前加了阿拉伯数字就只表示多个分子,不再表示物质。
如:2O2表示2个氧分子,4H2O表示4个水分子5CO23H2化学式==分子符号CO2CO2三、单质化学式的写法由分子构成的单质(常见气体单质)
如:氧气O2、氮气N2、氢气H2、
氯气Cl2 、臭氧O3等金属单质、固态非金属单质和稀有气体:由原子直接构成,直接用元素符号表示。如:铁Fe、铜Cu、,碳C、磷P,氦气He、氩气Ar等四、化合物的化学式的写法1、化学式的书写规律; (1)知道这种物质由那些元素组成 (2)知道元素的化合价
(3)化学式中元素排列顺序的规定 “正价左,负价右”。2、元素的化合价:①化合价顺口溜: +1钾钠银与氢 (K)
+2钙镁钡铜锌(Ca) +3元素金属铝 (Al) +2、+3铁, (Fe Fe)
+2、+4碳 (C C) -2、+4、+6硫真特别
氯结金属显-1 (Cl)
通常氧是-2价(O)+1+2+3+4+2-1-2②原子团(根)的化合价铵根 NH4
硝酸根NO3
氢氧根OH
硫酸根SO4
碳酸根CO3 化合价标在元素符号的正上方。+1-1-1-2-2+2+3①化合价有正价和负价
②金属元素显正价,非金属元素一般显负价.
“金+, 非-”
③一些元素 在不同的物质里有不同的化合价注意 3、化合价的有关规律④在任何化合物里,正负化合价的代数和为零。
⑤单质里元素的化合价为零。4、化合物的化学式的写法正左负右,交叉约简氧化铝_______二氧化碳_______P O+5 -2Al Cl+3 -1S O+6-2Ca S+2 -2CaS更正下列化学式中的错误Fe3O2Mn2O4
Cl2Ca
Ca NO32+4 -2+3 -2-1 +2+2 -1MnO2
Fe2O3CaCl2
Ca(NO3)2我们不能用化合价推求实际上不存在的物质的化学式。五、已知化学式求出化合价:
P117 例2练习:求出下列物质中硫元素的化合价:
SO2 SO3 H2SO4五、化学式的读法: 一般从右向左读作“某化某”、“某酸某”。
(1) 氧化物:如CuO . MgO .CO2 ,读作“氧化某”,如CuO读作氧化铜;有时还要读出化学式中各种元素的原子个数,读作“几氧化几某”,如Fe3O4读作四氧化三铁 。 (2) 金属元素与非金属元素两种组成 的化合物:如NaCl . KCl . ZnS.读作“某化某” 如NaCl读作氯化钠、ZnS读作硫化锌。(3)含有原子团的化合物,要读出原子团的名称:读作“某酸某”。如CaCO3(碳酸钙)AgNO3(硝酸银) CuSO4(硫酸铜)思考:原子的质量很小,故我们采用相对原子质量,那么由原子构成的分子,质量仍然很小,又如何表示呢?1、根据化学式计算相对分子质量
化学式中各原子的相对原子质量的总和,就是相对分子质量。
例1、计算:O2、SO2、NaOH、NH4NO3的相对分子质量。解:O2 的相对分子质量=16×2=32
SO2 的相对分子质量=32+ 16×2=64
NaOH的相对分子质量=23+16 + 1=40
NH4NO3的相对分子质量 =14+1×4+14+16×3=80练习1、求H2O2、 Fe3O4、H2SO4的相对分子质量?六、有关化学式的计算(二)、根据物质的化学式计算:2、计算物质组成元素的质量比:思考与计算:
①计算2个氢原子与1个氧原子的质量比是_______________。
②计算1个水分子( )中 氢原子与氧原子的质量比是___________________。
③计算2个水分子( 、 )中 氢原子与氧原子的质量比是___________________________。
④计算n个水分子( …… )中 氢原子与氧原子的质量比是_________________________________。
1×2∶16=1∶81×2∶16=1∶8(1×2)×2∶16×2=1∶8(1×2)×n∶16×n=1∶8结论:不论有多少个水分子,它们中的氢原子与氧原子的质量比是1∶8 。水(H2O)中氢元素与氧元素的质量比为:____。1∶8各元素之间的质量比=各原子的相对原子质量与原子个数的乘积之比解:水中氢元素与氧元素的质量比=(1×2)∶16 = 1∶8 各元素之间的质量比=各原子的相对原子质量与原子个数的乘积之比
例2、MnO2中锰元素和氧元素的质量比等于___________________________。
1、 H2O2中各元素的质量比?
2、NH4NO3中各元素的质量比?
55∶16×2 = 55 ∶32解: H2O2中氢元素与氧元素的质量比为:1×2 ∶16×2 = 2 ∶ 32 = 1 ∶16解: NH4NO3中氮元素、氢元素与氧元素的质量比为=14×2 ∶ 1×4 ∶ 16×3
= 28 ∶4 ∶ 48 = 7 ∶ 1 ∶122、计算物质组成各元素的质量 比:
CO2 P2O53.求物质中某元素的质量分数例3、CO2中碳元素的质量分数?
=27.3%练习3、计算下列物质中氮元素的质量分数?
①NO2、② NH4NO3 、③ (NH4)2SO4=30.4%练习:计算下列物质中氮元素的质量分数:
NH4NO3 (NH4)2SO4 解: 4、一定质量的化合物中含有某元素质量计算:
计算式:某元素的质量=化合物的质量×该元素的质量分数
例4、求18gH2O中氢元素的质量?
练习4、某农田里的作物需施含35kg N的氮肥,如果施用的氮肥是尿素( CO(NH2)2 ),则需要尿素多少kg?课堂练习:根据化学式计算:
1、已知硫酸的化学式为H2SO4,则:
① H2SO4中硫元素的化合价为_________,
② H2SO4的相对分子质量为___________,
③ H2SO4中H、S与O的质量比为_______________,
④ H2SO4中硫元素的质量分数为________。
2、2001年诺贝尔奖授予美国化学家诺尔斯博士,他应用不对称合成技术合成了一种重要物质—丙烯醇,该物质用于生产一种治疗心脏病的药物,丙烯醇的化学式为:C3H6O2。则
① C3H6O2由_____种元素组成,
②每个C3H6O2分子中共含_____个原子, ③碳、氢、氧的原子个数比为___________。+6981∶16 ∶3232.7%3113∶6 ∶2
用元素符号表示物质组成的式子叫化学式。
表示每种纯净物的组成的化学式只有一个。如:
镁 Mg 铜 Cu 碳 C 磷 P 氧气 O2 氮气N2 水 H2O 五氧化二磷 P2O5 氯酸钾KClO3 1、C6H12O6是葡萄糖的化学式,则一个葡萄糖分子中含______个C原子、_______个H原子和_______个氧原子 。
2、1993年中美科学家共同合成了世界上最大的碳氢分子,这种分子由1134个碳原子和1146个氢原子构成。请你写出此种物质的化学式 。练习:6126C1134H11462、化学式的涵义(提供信息)练一练:表示__________________表示________________________表示__________________表示________________________
_______________P2O5五氧化二磷五氧化二磷由磷元素和氧元素组成1个五氧化二磷分子1个五氧化二磷分子中含2个磷原子
和5个氧原子3、表示多个分子的方法:
在化学式前面加上阿拉伯数字。
如:5个二氧化碳分子_______,3个氢分子______。
同样在化学式前加了阿拉伯数字就只表示多个分子,不再表示物质。
如:2O2表示2个氧分子,4H2O表示4个水分子5CO23H2化学式==分子符号CO2CO2三、单质化学式的写法由分子构成的单质(常见气体单质)
如:氧气O2、氮气N2、氢气H2、
氯气Cl2 、臭氧O3等金属单质、固态非金属单质和稀有气体:由原子直接构成,直接用元素符号表示。如:铁Fe、铜Cu、,碳C、磷P,氦气He、氩气Ar等四、化合物的化学式的写法1、化学式的书写规律; (1)知道这种物质由那些元素组成 (2)知道元素的化合价
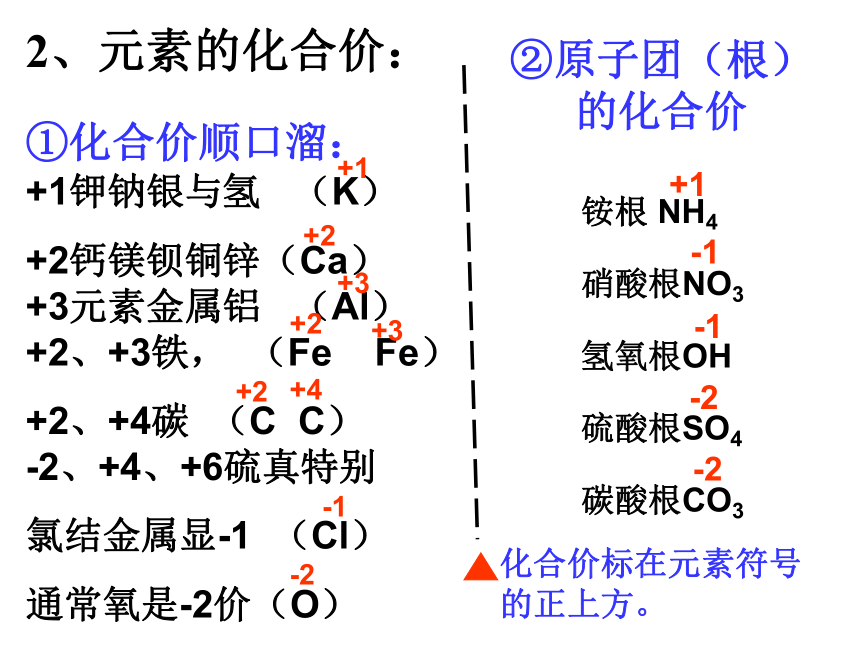
(3)化学式中元素排列顺序的规定 “正价左,负价右”。2、元素的化合价:①化合价顺口溜: +1钾钠银与氢 (K)
+2钙镁钡铜锌(Ca) +3元素金属铝 (Al) +2、+3铁, (Fe Fe)
+2、+4碳 (C C) -2、+4、+6硫真特别
氯结金属显-1 (Cl)
通常氧是-2价(O)+1+2+3+4+2-1-2②原子团(根)的化合价铵根 NH4
硝酸根NO3
氢氧根OH
硫酸根SO4
碳酸根CO3 化合价标在元素符号的正上方。+1-1-1-2-2+2+3①化合价有正价和负价
②金属元素显正价,非金属元素一般显负价.
“金+, 非-”
③一些元素 在不同的物质里有不同的化合价注意 3、化合价的有关规律④在任何化合物里,正负化合价的代数和为零。
⑤单质里元素的化合价为零。4、化合物的化学式的写法正左负右,交叉约简氧化铝_______二氧化碳_______P O+5 -2Al Cl+3 -1S O+6-2Ca S+2 -2CaS更正下列化学式中的错误Fe3O2Mn2O4
Cl2Ca
Ca NO32+4 -2+3 -2-1 +2+2 -1MnO2
Fe2O3CaCl2
Ca(NO3)2我们不能用化合价推求实际上不存在的物质的化学式。五、已知化学式求出化合价:
P117 例2练习:求出下列物质中硫元素的化合价:
SO2 SO3 H2SO4五、化学式的读法: 一般从右向左读作“某化某”、“某酸某”。
(1) 氧化物:如CuO . MgO .CO2 ,读作“氧化某”,如CuO读作氧化铜;有时还要读出化学式中各种元素的原子个数,读作“几氧化几某”,如Fe3O4读作四氧化三铁 。 (2) 金属元素与非金属元素两种组成 的化合物:如NaCl . KCl . ZnS.读作“某化某” 如NaCl读作氯化钠、ZnS读作硫化锌。(3)含有原子团的化合物,要读出原子团的名称:读作“某酸某”。如CaCO3(碳酸钙)AgNO3(硝酸银) CuSO4(硫酸铜)思考:原子的质量很小,故我们采用相对原子质量,那么由原子构成的分子,质量仍然很小,又如何表示呢?1、根据化学式计算相对分子质量
化学式中各原子的相对原子质量的总和,就是相对分子质量。
例1、计算:O2、SO2、NaOH、NH4NO3的相对分子质量。解:O2 的相对分子质量=16×2=32
SO2 的相对分子质量=32+ 16×2=64
NaOH的相对分子质量=23+16 + 1=40
NH4NO3的相对分子质量 =14+1×4+14+16×3=80练习1、求H2O2、 Fe3O4、H2SO4的相对分子质量?六、有关化学式的计算(二)、根据物质的化学式计算:2、计算物质组成元素的质量比:思考与计算:
①计算2个氢原子与1个氧原子的质量比是_______________。
②计算1个水分子( )中 氢原子与氧原子的质量比是___________________。
③计算2个水分子( 、 )中 氢原子与氧原子的质量比是___________________________。
④计算n个水分子( …… )中 氢原子与氧原子的质量比是_________________________________。
1×2∶16=1∶81×2∶16=1∶8(1×2)×2∶16×2=1∶8(1×2)×n∶16×n=1∶8结论:不论有多少个水分子,它们中的氢原子与氧原子的质量比是1∶8 。水(H2O)中氢元素与氧元素的质量比为:____。1∶8各元素之间的质量比=各原子的相对原子质量与原子个数的乘积之比解:水中氢元素与氧元素的质量比=(1×2)∶16 = 1∶8 各元素之间的质量比=各原子的相对原子质量与原子个数的乘积之比
例2、MnO2中锰元素和氧元素的质量比等于___________________________。
1、 H2O2中各元素的质量比?
2、NH4NO3中各元素的质量比?
55∶16×2 = 55 ∶32解: H2O2中氢元素与氧元素的质量比为:1×2 ∶16×2 = 2 ∶ 32 = 1 ∶16解: NH4NO3中氮元素、氢元素与氧元素的质量比为=14×2 ∶ 1×4 ∶ 16×3
= 28 ∶4 ∶ 48 = 7 ∶ 1 ∶122、计算物质组成各元素的质量 比:
CO2 P2O53.求物质中某元素的质量分数例3、CO2中碳元素的质量分数?
=27.3%练习3、计算下列物质中氮元素的质量分数?
①NO2、② NH4NO3 、③ (NH4)2SO4=30.4%练习:计算下列物质中氮元素的质量分数:
NH4NO3 (NH4)2SO4 解: 4、一定质量的化合物中含有某元素质量计算:
计算式:某元素的质量=化合物的质量×该元素的质量分数
例4、求18gH2O中氢元素的质量?
练习4、某农田里的作物需施含35kg N的氮肥,如果施用的氮肥是尿素( CO(NH2)2 ),则需要尿素多少kg?课堂练习:根据化学式计算:
1、已知硫酸的化学式为H2SO4,则:
① H2SO4中硫元素的化合价为_________,
② H2SO4的相对分子质量为___________,
③ H2SO4中H、S与O的质量比为_______________,
④ H2SO4中硫元素的质量分数为________。
2、2001年诺贝尔奖授予美国化学家诺尔斯博士,他应用不对称合成技术合成了一种重要物质—丙烯醇,该物质用于生产一种治疗心脏病的药物,丙烯醇的化学式为:C3H6O2。则
① C3H6O2由_____种元素组成,
②每个C3H6O2分子中共含_____个原子, ③碳、氢、氧的原子个数比为___________。+6981∶16 ∶3232.7%3113∶6 ∶2
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
