第3章 微项目 论证重污染天气 “汽车限行”的合理性 课件(共41张PPT)
文档属性
| 名称 | 第3章 微项目 论证重污染天气 “汽车限行”的合理性 课件(共41张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-09-04 15:48:47 | ||
图片预览










文档简介
课件41张PPT。※微项目※
论证重污染天气“汽车限行”的合理性
——探讨社会性科学议题知识铺垫新知预习人类社会进入二十世纪八十年代以来,人们越来越关心环境问题。我们在享受科学技术迅速发展带来物质文明的同时,也因一次次以牺牲环境为代价,而受到大自然的一次次报复,如雾霾天气等,北京、广州等多个城市采取了“汽车限行”。人们逐渐意识到:保护环境,就是保护人类赖以生存的空间。
控制“雾霾”的根本措施是减少烟尘和NOx的人为排放量。面对社会性科学议题,首先需要明确议题中的科学知识和科学问题,正确认识议题;然后从环境、经济、社会等视角寻找议题涉及的利与弊,论证这些利与弊是否成立,最后结合实际情况综合考虑,权衡利弊、作出决策。知识铺垫新知预习1.氮及其化合物的转化关系 知识铺垫新知预习2.氮氧化物催化转化法
在汽车排气管上安装催化转化器,使汽车尾气中的NOx(NO或NO2)与CO反应转化成无毒的物质,反应原理为知识铺垫新知预习【微思考】如何治理汽车尾气?
提示:NOx尾气处理方法
①碱液吸收法:
2NO2+2NaOH === NaNO3+NaNO2+H2O
NO2+NO+2NaOH === 2NaNO2+H2O
NO2、NO的混合气体能被足量烧碱溶液完全吸收的条件是n(NO2)≥n(NO)。一般适合工业尾气中NOx的处理。
②催化转化法:
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体N2;NOx与CO在一定温度下催化转化为无毒气体N2和CO2(一般适用于汽车尾气的处理)。探究1探究2探究3素养脉络随堂检测科学认识社会性科学议题,寻找利与弊
问题探究
汽车尾气有什么危害?
提示:汽车尾气中的NOx在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生了一种有毒的烟雾——光化学烟雾,光化学烟雾中含甲醛、乙醛等刺激性有毒物质,会刺激人的呼吸道。探究1探究2探究3素养脉络随堂检测知识归纳
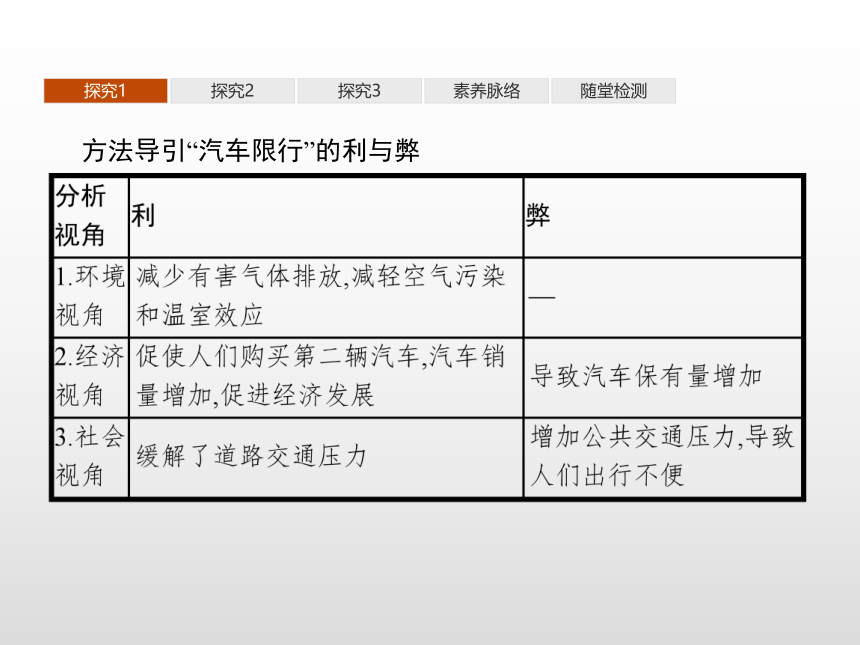
车辆限行,顾名思义,就是为了缓解交通压力或防治大气污染,而采取限制某些车辆通行的措施。车辆限行有很多种,有的是某个路段限行,有的是某个时段限行,有的是某种车型限行,还有最常见的是尾号限行。其中,尾号限行制度是为了缓解城市交通压力而催生的一种交通制度。如2008年的北京奥运测试赛期间,北京开始单双号限行。单号日子时候,只能车号的末尾数字是单号的私家车可以上路,双号日子的时候,只能车号末尾数字是双号的私家车可以上路。探究1探究2探究3素养脉络随堂检测方法导引“汽车限行”的利与弊 探究1探究2探究3素养脉络随堂检测典例剖析
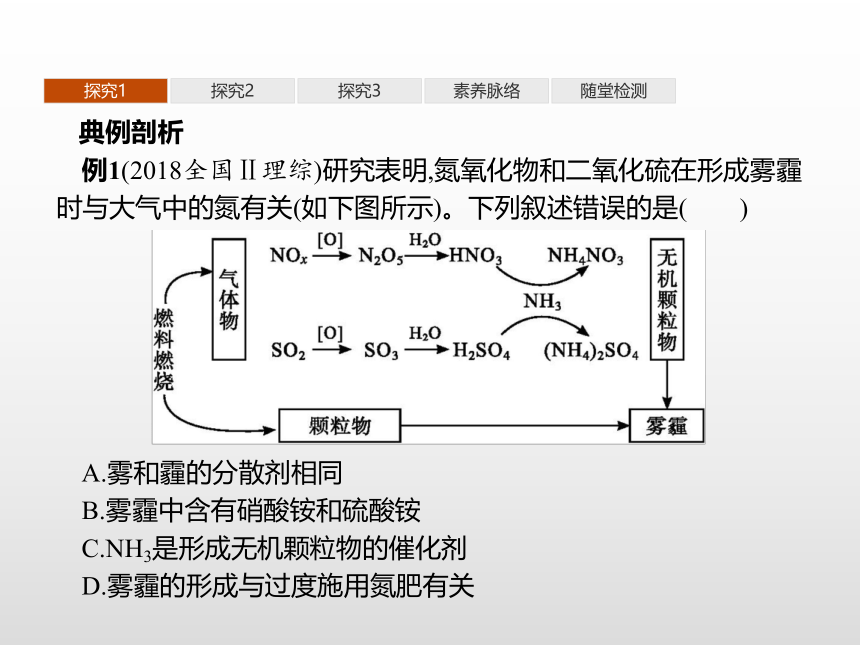
例1(2018全国Ⅱ理综)研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氮有关(如下图所示)。下列叙述错误的是( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH3是形成无机颗粒物的催化剂
D.雾霾的形成与过度施用氮肥有关探究1探究2探究3素养脉络随堂检测答案:C
解析:雾和霾的分散剂均为空气,A项正确;根据题目信息,硝酸铵和硫酸铵均为无机颗粒物,是形成雾霾的因素之一,B项正确;氨气分别和硝酸、硫酸生成硝酸铵和硫酸铵,是形成无机颗粒物的反应物,C项错误;过度施用化肥会导致空气中氨气含量增加,促进了无机颗粒物中硝酸铵、硫酸铵含量的增加,D项正确。探究1探究2探究3素养脉络随堂检测对点训练1汽车尾气主要含有CO2、CO、SO2、NOx等物质,这种尾气逐渐成为城市空气污染的主要来源之一。
(1)汽车尾气中的CO来自于 ,NO来自于 。汽车尾气对环境的危害主要有 (至少填两种)。?
(2)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:? 。?
(3)汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:? ? 。?探究1探究2探究3素养脉络随堂检测答案:(1)汽油的不完全燃烧 N2与O2在汽车汽缸内的高温环境下的反应 形成硝酸型酸雨、导致光化学烟雾、产生温室效应(任填两种即可)
解析:(1)汽车汽缸内不断进行着汽油的燃烧反应,当空气不足时,汽油不完全燃烧会产生CO;当空气过量时,N2和O2在放电或高温条件下反应生成NO。汽车尾气对环境的危害很大,可以形成硝酸型酸雨、导致光化学烟雾、产生温室效应等。(3)CO、NOx反应后生成的无毒气体为CO2和N2。探究1探究2探究3素养脉络随堂检测学习科学论证,论证利与弊
问题探究
汽车尾号限行对治理空气污染有用吗?
提示:通过一定的实际测定和对比,得出结论:汽车尾号限行的举措对于减轻空气污染是有一定效果的。
知识归纳
机动车尾气排放成为一个备受指责的因素,特别是柴油车和某些重型小轿车。这些汽车尾气中的化学元凶包括悬浮微粒(PM)和氮氧化物(NOx)。悬浮微粒是一种烟尘,能够侵入肺部并引起心血管疾病,氮氧化物则会加剧呼吸困难。探究1探究2探究3素养脉络随堂检测方法导引科学论证的水平 探究1探究2探究3素养脉络随堂检测探究1探究2探究3素养脉络随堂检测探究1探究2探究3素养脉络随堂检测典例剖析
例2汽车排放的尾气中含有NO2,NO2是城市大气污染的主要污染物之一。在日光照射下,NO2发生一系列光化学烟雾的循环反应,从而不断产生O3,加重空气污染。反应过程为①2NO2→2NO+2O,②2NO+O2→2NO2,③O+O2→O3。下列对该反应过程及生成物叙述正确的是( )
A.NO2只起催化剂作用 B.NO起催化剂作用
C.NO2只起氧化剂作用 D.O3与O2为同素异形体
答案:D
解析:反应过程①+②得O2→2O,③O+O2→O3,NO2起催化剂作用,反应过程中NO2还做氧化剂,A、B、C项错误;O3与O2属于同素异形体,D项正确。探究1探究2探究3素养脉络随堂检测对点训练2下列现象的产生,与氮循环无关的是 ( )
A.光化学烟雾 B.白色污染
C.水体富营养化 D.酸雨
答案:B
解析:光化学污染是氮的氧化物和有机烃类在光作用下的一系列复杂变化,与氮循环有关;白色污染是指难降解的塑料垃圾(多指塑料袋)对环境的污染;水体富营养化是指水中的氮、磷等元素浓度过大造成的水污染,会导致藻类疯长,从而引起水中缺氧,导致水生生物大量死亡,与氮循环有关;酸雨是二氧化硫和氮氧化物与雨水作用的结果,与氮循环有关。探究1探究2探究3素养脉络随堂检测权衡利弊,作出决策
问题探究
根据汽车限行的利弊,如何作出决策?
提示:经过充分的论证分析后,分清主次,权衡利弊,作出决策。
知识归纳探究1探究2探究3素养脉络随堂检测方法导引评价要素及评价等级 探究1探究2探究3素养脉络随堂检测探究1探究2探究3素养脉络随堂检测典例剖析
例3“保护环境就是保护人类自己。”下列环境问题与产生的主要原因不相符的是( )
①“光化学烟雾”主要是由汽车排放的氮氧化物所引起的;②“酸雨”主要是由空气中CO2的浓度增大引起的;③“温室效应”主要是由空气中CO2浓度增大引起的;④“赤潮”主要是由于水体中N、P等元素含量过高而引起的
A.①② B.②③ C.①②③④ D.②
答案:D
解析:“酸雨”主要是空气中的SO2或NOx的浓度增大引起的。探究1探究2探究3素养脉络随堂检测对点训练3回答下列有关环境的问题:
(1)造成水体富营养化的元素是 和 ,水体富营养化的后果是导致水生藻类“疯长”,并迅速覆盖在水面上,在海水中形成 现象,而这种现象在淡水中称为 。?
(2)大气中的下列氧化物的存在既不能形成酸雨,也不能形成光化学污染的是 。?
A.二氧化硫 B.二氧化碳 C.二氧化氮 D.一氧化氮
(3)目前,大城市内的光化学污染是大气主要污染形式之一,该污染的现象是形成烟雾,故又叫光化学烟雾,形成光化学烟雾的过程属于 (填“化学变化”或“物理变化”)。?
(4)汽车尾气中氮的氧化物来源除因为燃油中含有氮元素(燃烧时,氮转化为氮的氧化物)外,还有一个原因。请你用化学方程式表示这个原因: 。?探究1探究2探究3素养脉络随堂检测答案:(1)氮 磷 赤潮 水华
(2)B (3)化学变化
解析:(1)水体中过量的氮、磷造成了水体的富营养化,温度适宜则会导致近海水域的赤潮现象,在江河湖泊等淡水中爆发性生长藻类则叫水华。
(2)酸雨是指pH小于5.6的雨、雪、霜或其他形式的大气降水。二氧化碳溶解于水,尽管也可以使水显酸性,但大气中的二氧化碳在水中溶解后pH不可能小于5.6,故二氧化碳不是酸雨形成的原因。
(3)光化学烟雾的形成是一个复杂的氧化还原反应过程。
(4)机动车在工作时,其汽缸内的温度和压力非常高,故吸入其中的空气(氮气与氧气)会相互反应,生成氮的氧化物。探究1探究2探究3素养脉络随堂检测1.世界大学生夏季运动会是规模仅次于夏季奥运会的世界级综合性运动会。2021年第31届世界大学生运动会将在成都举办。“绿色”是成都的城市发展理念,也是这次运动会的组织理念。下面有关说法不正确的是( )
A.成都市目前推广使用的清洁燃料压缩天然气(CNG)和液化石油气(LPG)的主要成分均是烃类
B.兴建运动会场馆所用到的金属材料中可能含有非金属元素
C.“绿色化学”的核心是应用化学原理对环境污染进行治理
D.新能源汽车的使用有助于减少氮氧化物的排放
答案:C探究1探究2探究3素养脉络随堂检测解析:A项,压缩天然气(CNG)类的主要成分是甲烷,液化石油气(LPG)类的成分是丙烷、丁烷等,所以这两类燃料的主要成分都是烃类,故A正确;B项,合金可能含有非金属元素,故B正确;C项,“绿色化学”的核心是从源头上控制污染,而不是治理污染,故C错误;D项,新能源汽车的使用可减少化石燃料的使用,可减少常规汽车的使用,能减少氮氧化物的排放,故D正确。探究1探究2探究3素养脉络随堂检测2.当前,汽车尾气已成为许多城市空气的主要污染源。研究表明,含TiO2的混凝土或沥青可以部分消除汽车尾气中的氮氧化物,其原理如下:
下列关于该“消除”过程的叙述不正确的是( )
A.部分光能转变为化学能
B.消除总变化为NOx+O2+H2O→HNO3
C.消除反应能全天候发生
D.使用纳米TiO2的消除效率更高探究1探究2探究3素养脉络随堂检测答案:C
解析:在TiO2的催化作用下紫外线提供能量,部分光能转变为化学能,故A项正确,不符合题意;题中示意图表明,在TiO2的催化作用下紫外线提供能量,发生反应:NOx+O2+H2O→HNO3,故B项正确,不符合题意;没有紫外线时上述反应不能发生,故C项错误,符合题意;纳米与紫外线接触面积更大,将产生更多的光生电子和光生空穴,从而消除更多的NOx,故D项正确,不符合题意。探究1探究2探究3素养脉络随堂检测3.对含有氮氧化物的废气进行处理。
(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH === 2NaNO2+H2O①
2NO2+2NaOH === NaNO2+NaNO3+H2O②
在反应①中,氧化剂是 ,还原剂是 。在反应②中,氧化剂和还原剂的物质的量之比为 。?
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应生成N2和CO2,该反应的化学方程式为 。?
(3)在一定条件下,氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气与二氧化氮在一定条件下反应的化学方程式: 。?探究1探究2探究3素养脉络随堂检测解析:(1)反应①中NO2中氮元素化合价降低做氧化剂,NO中氮元素化合价升高做还原剂;反应②中氧化剂和还原剂都是NO2,它们的物质的量之比为1∶1。
(2)根据质量守恒定律,结合题目信息可知,一氧化氮与一氧化碳反应后生成对大气无污染的物质应为氮气和二氧化碳:2CO+2NO探究1探究2探究3素养脉络随堂检测4.氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此要对含有氮氧化物的废气进行处理。
用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH === 2NaNO2+H2O①
2NO2+2NaOH === NaNO2+NaNO3+H2O②
(1)由反应②判断二氧化氮是否为酸性氧化物 (填“是”或“不是”),原因是 。?探究1探究2探究3素养脉络随堂检测(2)目前有一种治理方法是在一定条件下,用氨气将氮氧化物转化为无污染的物质,请写出该反应的化学方程式: ,该反应中,氧化剂是 ,氧化产物是 ,当生成1.4 mol氮气时,转移电子的物质的量为 。?
(3)为了保护环境,工业上常通入NH3与氮的氧化物反应转化为无毒的N2。现有NO2和NO的混合气体3 L,通入3 L(同温同压下)NH3,恰好使其完全转化为N2,则原混合气体中NO2和NO的物质的量之比为 。?探究1探究2探究3素养脉络随堂检测答案:(1)不是 因为二氧化氮与碱反应生成两种盐,且氮元素化合价发生变化
(3)1∶1探究1探究2探究3素养脉络随堂检测解析:(1)二氧化氮与碱反应生成两种盐,且氮元素化合价发生变化,二氧化氮不是酸性氧化物。
(2)根据原子守恒定律结合题目信息可知,氨气和二氧化氮反应后生成的无污染的物质为氮气和水。NO2中+4价的N被NH3中-3价的N还原为N2中0价的N,剩下的氢、氧元素结合成水,因而氧化剂是NO2,氧化产物、还原产物均为N2。生成7 mol N2时,转移电子24 mol,则生成1.4 mol N2时,转移电子4.8 mol。探究1探究2探究3素养脉络随堂检测5.SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:
①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式为 。
②反应器中NH3还原NO2的化学方程式为 。?
③当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成: 。?探究1探究2探究3素养脉络随堂检测④尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60 g·mol-1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的V1 mL c1 mol·L-1 H2SO4溶液吸收完全,剩余H2SO4用V2 mL c2 mol·L-1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是 。?探究1探究2探究3素养脉络随堂检测(2)NSR(NOx储存还原)工作原理:
NOx的储存和还原在不同时段交替进行,如图a所示。探究1探究2探究3素养脉络随堂检测①通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是 。?
②用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是 。?探究1探究2探究3素养脉络随堂检测探究1探究2探究3素养脉络随堂检测(2)①由图示可知BaO和NOx作用生成Ba(NO3)2,Ba(NO3)2再还原为N2,则储存NOx的物质是BaO;②由图示可知,第一步反应为H2与Ba(NO3)2反应生成NH3,1 mol Ba(NO3)2作用生成NH3共转移16 mol电子,根据电子守恒,参加反应的氢气的物质的量为16 mol÷2=8 mol,则消耗的H2与Ba(NO3)2的物质的量之比是8∶1。
控制“雾霾”的根本措施是减少烟尘和NOx的人为排放量。面对社会性科学议题,首先需要明确议题中的科学知识和科学问题,正确认识议题;然后从环境、经济、社会等视角寻找议题涉及的利与弊,论证这些利与弊是否成立,最后结合实际情况综合考虑,权衡利弊、作出决策。知识铺垫新知预习1.氮及其化合物的转化关系 知识铺垫新知预习2.氮氧化物催化转化法
在汽车排气管上安装催化转化器,使汽车尾气中的NOx(NO或NO2)与CO反应转化成无毒的物质,反应原理为知识铺垫新知预习【微思考】如何治理汽车尾气?
提示:NOx尾气处理方法
①碱液吸收法:
2NO2+2NaOH === NaNO3+NaNO2+H2O
NO2+NO+2NaOH === 2NaNO2+H2O
NO2、NO的混合气体能被足量烧碱溶液完全吸收的条件是n(NO2)≥n(NO)。一般适合工业尾气中NOx的处理。
②催化转化法:
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体N2;NOx与CO在一定温度下催化转化为无毒气体N2和CO2(一般适用于汽车尾气的处理)。探究1探究2探究3素养脉络随堂检测科学认识社会性科学议题,寻找利与弊
问题探究
汽车尾气有什么危害?
提示:汽车尾气中的NOx在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生了一种有毒的烟雾——光化学烟雾,光化学烟雾中含甲醛、乙醛等刺激性有毒物质,会刺激人的呼吸道。探究1探究2探究3素养脉络随堂检测知识归纳
车辆限行,顾名思义,就是为了缓解交通压力或防治大气污染,而采取限制某些车辆通行的措施。车辆限行有很多种,有的是某个路段限行,有的是某个时段限行,有的是某种车型限行,还有最常见的是尾号限行。其中,尾号限行制度是为了缓解城市交通压力而催生的一种交通制度。如2008年的北京奥运测试赛期间,北京开始单双号限行。单号日子时候,只能车号的末尾数字是单号的私家车可以上路,双号日子的时候,只能车号末尾数字是双号的私家车可以上路。探究1探究2探究3素养脉络随堂检测方法导引“汽车限行”的利与弊 探究1探究2探究3素养脉络随堂检测典例剖析
例1(2018全国Ⅱ理综)研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氮有关(如下图所示)。下列叙述错误的是( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH3是形成无机颗粒物的催化剂
D.雾霾的形成与过度施用氮肥有关探究1探究2探究3素养脉络随堂检测答案:C
解析:雾和霾的分散剂均为空气,A项正确;根据题目信息,硝酸铵和硫酸铵均为无机颗粒物,是形成雾霾的因素之一,B项正确;氨气分别和硝酸、硫酸生成硝酸铵和硫酸铵,是形成无机颗粒物的反应物,C项错误;过度施用化肥会导致空气中氨气含量增加,促进了无机颗粒物中硝酸铵、硫酸铵含量的增加,D项正确。探究1探究2探究3素养脉络随堂检测对点训练1汽车尾气主要含有CO2、CO、SO2、NOx等物质,这种尾气逐渐成为城市空气污染的主要来源之一。
(1)汽车尾气中的CO来自于 ,NO来自于 。汽车尾气对环境的危害主要有 (至少填两种)。?
(2)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:? 。?
(3)汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:? ? 。?探究1探究2探究3素养脉络随堂检测答案:(1)汽油的不完全燃烧 N2与O2在汽车汽缸内的高温环境下的反应 形成硝酸型酸雨、导致光化学烟雾、产生温室效应(任填两种即可)
解析:(1)汽车汽缸内不断进行着汽油的燃烧反应,当空气不足时,汽油不完全燃烧会产生CO;当空气过量时,N2和O2在放电或高温条件下反应生成NO。汽车尾气对环境的危害很大,可以形成硝酸型酸雨、导致光化学烟雾、产生温室效应等。(3)CO、NOx反应后生成的无毒气体为CO2和N2。探究1探究2探究3素养脉络随堂检测学习科学论证,论证利与弊
问题探究
汽车尾号限行对治理空气污染有用吗?
提示:通过一定的实际测定和对比,得出结论:汽车尾号限行的举措对于减轻空气污染是有一定效果的。
知识归纳
机动车尾气排放成为一个备受指责的因素,特别是柴油车和某些重型小轿车。这些汽车尾气中的化学元凶包括悬浮微粒(PM)和氮氧化物(NOx)。悬浮微粒是一种烟尘,能够侵入肺部并引起心血管疾病,氮氧化物则会加剧呼吸困难。探究1探究2探究3素养脉络随堂检测方法导引科学论证的水平 探究1探究2探究3素养脉络随堂检测探究1探究2探究3素养脉络随堂检测探究1探究2探究3素养脉络随堂检测典例剖析
例2汽车排放的尾气中含有NO2,NO2是城市大气污染的主要污染物之一。在日光照射下,NO2发生一系列光化学烟雾的循环反应,从而不断产生O3,加重空气污染。反应过程为①2NO2→2NO+2O,②2NO+O2→2NO2,③O+O2→O3。下列对该反应过程及生成物叙述正确的是( )
A.NO2只起催化剂作用 B.NO起催化剂作用
C.NO2只起氧化剂作用 D.O3与O2为同素异形体
答案:D
解析:反应过程①+②得O2→2O,③O+O2→O3,NO2起催化剂作用,反应过程中NO2还做氧化剂,A、B、C项错误;O3与O2属于同素异形体,D项正确。探究1探究2探究3素养脉络随堂检测对点训练2下列现象的产生,与氮循环无关的是 ( )
A.光化学烟雾 B.白色污染
C.水体富营养化 D.酸雨
答案:B
解析:光化学污染是氮的氧化物和有机烃类在光作用下的一系列复杂变化,与氮循环有关;白色污染是指难降解的塑料垃圾(多指塑料袋)对环境的污染;水体富营养化是指水中的氮、磷等元素浓度过大造成的水污染,会导致藻类疯长,从而引起水中缺氧,导致水生生物大量死亡,与氮循环有关;酸雨是二氧化硫和氮氧化物与雨水作用的结果,与氮循环有关。探究1探究2探究3素养脉络随堂检测权衡利弊,作出决策
问题探究
根据汽车限行的利弊,如何作出决策?
提示:经过充分的论证分析后,分清主次,权衡利弊,作出决策。
知识归纳探究1探究2探究3素养脉络随堂检测方法导引评价要素及评价等级 探究1探究2探究3素养脉络随堂检测探究1探究2探究3素养脉络随堂检测典例剖析
例3“保护环境就是保护人类自己。”下列环境问题与产生的主要原因不相符的是( )
①“光化学烟雾”主要是由汽车排放的氮氧化物所引起的;②“酸雨”主要是由空气中CO2的浓度增大引起的;③“温室效应”主要是由空气中CO2浓度增大引起的;④“赤潮”主要是由于水体中N、P等元素含量过高而引起的
A.①② B.②③ C.①②③④ D.②
答案:D
解析:“酸雨”主要是空气中的SO2或NOx的浓度增大引起的。探究1探究2探究3素养脉络随堂检测对点训练3回答下列有关环境的问题:
(1)造成水体富营养化的元素是 和 ,水体富营养化的后果是导致水生藻类“疯长”,并迅速覆盖在水面上,在海水中形成 现象,而这种现象在淡水中称为 。?
(2)大气中的下列氧化物的存在既不能形成酸雨,也不能形成光化学污染的是 。?
A.二氧化硫 B.二氧化碳 C.二氧化氮 D.一氧化氮
(3)目前,大城市内的光化学污染是大气主要污染形式之一,该污染的现象是形成烟雾,故又叫光化学烟雾,形成光化学烟雾的过程属于 (填“化学变化”或“物理变化”)。?
(4)汽车尾气中氮的氧化物来源除因为燃油中含有氮元素(燃烧时,氮转化为氮的氧化物)外,还有一个原因。请你用化学方程式表示这个原因: 。?探究1探究2探究3素养脉络随堂检测答案:(1)氮 磷 赤潮 水华
(2)B (3)化学变化
解析:(1)水体中过量的氮、磷造成了水体的富营养化,温度适宜则会导致近海水域的赤潮现象,在江河湖泊等淡水中爆发性生长藻类则叫水华。
(2)酸雨是指pH小于5.6的雨、雪、霜或其他形式的大气降水。二氧化碳溶解于水,尽管也可以使水显酸性,但大气中的二氧化碳在水中溶解后pH不可能小于5.6,故二氧化碳不是酸雨形成的原因。
(3)光化学烟雾的形成是一个复杂的氧化还原反应过程。
(4)机动车在工作时,其汽缸内的温度和压力非常高,故吸入其中的空气(氮气与氧气)会相互反应,生成氮的氧化物。探究1探究2探究3素养脉络随堂检测1.世界大学生夏季运动会是规模仅次于夏季奥运会的世界级综合性运动会。2021年第31届世界大学生运动会将在成都举办。“绿色”是成都的城市发展理念,也是这次运动会的组织理念。下面有关说法不正确的是( )
A.成都市目前推广使用的清洁燃料压缩天然气(CNG)和液化石油气(LPG)的主要成分均是烃类
B.兴建运动会场馆所用到的金属材料中可能含有非金属元素
C.“绿色化学”的核心是应用化学原理对环境污染进行治理
D.新能源汽车的使用有助于减少氮氧化物的排放
答案:C探究1探究2探究3素养脉络随堂检测解析:A项,压缩天然气(CNG)类的主要成分是甲烷,液化石油气(LPG)类的成分是丙烷、丁烷等,所以这两类燃料的主要成分都是烃类,故A正确;B项,合金可能含有非金属元素,故B正确;C项,“绿色化学”的核心是从源头上控制污染,而不是治理污染,故C错误;D项,新能源汽车的使用可减少化石燃料的使用,可减少常规汽车的使用,能减少氮氧化物的排放,故D正确。探究1探究2探究3素养脉络随堂检测2.当前,汽车尾气已成为许多城市空气的主要污染源。研究表明,含TiO2的混凝土或沥青可以部分消除汽车尾气中的氮氧化物,其原理如下:
下列关于该“消除”过程的叙述不正确的是( )
A.部分光能转变为化学能
B.消除总变化为NOx+O2+H2O→HNO3
C.消除反应能全天候发生
D.使用纳米TiO2的消除效率更高探究1探究2探究3素养脉络随堂检测答案:C
解析:在TiO2的催化作用下紫外线提供能量,部分光能转变为化学能,故A项正确,不符合题意;题中示意图表明,在TiO2的催化作用下紫外线提供能量,发生反应:NOx+O2+H2O→HNO3,故B项正确,不符合题意;没有紫外线时上述反应不能发生,故C项错误,符合题意;纳米与紫外线接触面积更大,将产生更多的光生电子和光生空穴,从而消除更多的NOx,故D项正确,不符合题意。探究1探究2探究3素养脉络随堂检测3.对含有氮氧化物的废气进行处理。
(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH === 2NaNO2+H2O①
2NO2+2NaOH === NaNO2+NaNO3+H2O②
在反应①中,氧化剂是 ,还原剂是 。在反应②中,氧化剂和还原剂的物质的量之比为 。?
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应生成N2和CO2,该反应的化学方程式为 。?
(3)在一定条件下,氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气与二氧化氮在一定条件下反应的化学方程式: 。?探究1探究2探究3素养脉络随堂检测解析:(1)反应①中NO2中氮元素化合价降低做氧化剂,NO中氮元素化合价升高做还原剂;反应②中氧化剂和还原剂都是NO2,它们的物质的量之比为1∶1。
(2)根据质量守恒定律,结合题目信息可知,一氧化氮与一氧化碳反应后生成对大气无污染的物质应为氮气和二氧化碳:2CO+2NO探究1探究2探究3素养脉络随堂检测4.氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此要对含有氮氧化物的废气进行处理。
用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH === 2NaNO2+H2O①
2NO2+2NaOH === NaNO2+NaNO3+H2O②
(1)由反应②判断二氧化氮是否为酸性氧化物 (填“是”或“不是”),原因是 。?探究1探究2探究3素养脉络随堂检测(2)目前有一种治理方法是在一定条件下,用氨气将氮氧化物转化为无污染的物质,请写出该反应的化学方程式: ,该反应中,氧化剂是 ,氧化产物是 ,当生成1.4 mol氮气时,转移电子的物质的量为 。?
(3)为了保护环境,工业上常通入NH3与氮的氧化物反应转化为无毒的N2。现有NO2和NO的混合气体3 L,通入3 L(同温同压下)NH3,恰好使其完全转化为N2,则原混合气体中NO2和NO的物质的量之比为 。?探究1探究2探究3素养脉络随堂检测答案:(1)不是 因为二氧化氮与碱反应生成两种盐,且氮元素化合价发生变化
(3)1∶1探究1探究2探究3素养脉络随堂检测解析:(1)二氧化氮与碱反应生成两种盐,且氮元素化合价发生变化,二氧化氮不是酸性氧化物。
(2)根据原子守恒定律结合题目信息可知,氨气和二氧化氮反应后生成的无污染的物质为氮气和水。NO2中+4价的N被NH3中-3价的N还原为N2中0价的N,剩下的氢、氧元素结合成水,因而氧化剂是NO2,氧化产物、还原产物均为N2。生成7 mol N2时,转移电子24 mol,则生成1.4 mol N2时,转移电子4.8 mol。探究1探究2探究3素养脉络随堂检测5.SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:
①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式为 。
②反应器中NH3还原NO2的化学方程式为 。?
③当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成: 。?探究1探究2探究3素养脉络随堂检测④尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60 g·mol-1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的V1 mL c1 mol·L-1 H2SO4溶液吸收完全,剩余H2SO4用V2 mL c2 mol·L-1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是 。?探究1探究2探究3素养脉络随堂检测(2)NSR(NOx储存还原)工作原理:
NOx的储存和还原在不同时段交替进行,如图a所示。探究1探究2探究3素养脉络随堂检测①通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是 。?
②用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是 。?探究1探究2探究3素养脉络随堂检测探究1探究2探究3素养脉络随堂检测(2)①由图示可知BaO和NOx作用生成Ba(NO3)2,Ba(NO3)2再还原为N2,则储存NOx的物质是BaO;②由图示可知,第一步反应为H2与Ba(NO3)2反应生成NH3,1 mol Ba(NO3)2作用生成NH3共转移16 mol电子,根据电子守恒,参加反应的氢气的物质的量为16 mol÷2=8 mol,则消耗的H2与Ba(NO3)2的物质的量之比是8∶1。
