1.3物质的量(第二课时)课件
图片预览



文档简介
(共23张PPT)
第 1 章 认识化学科学
第 3 节 化学中常用的物理量——物质的量
第 2 课时 气体摩尔体积
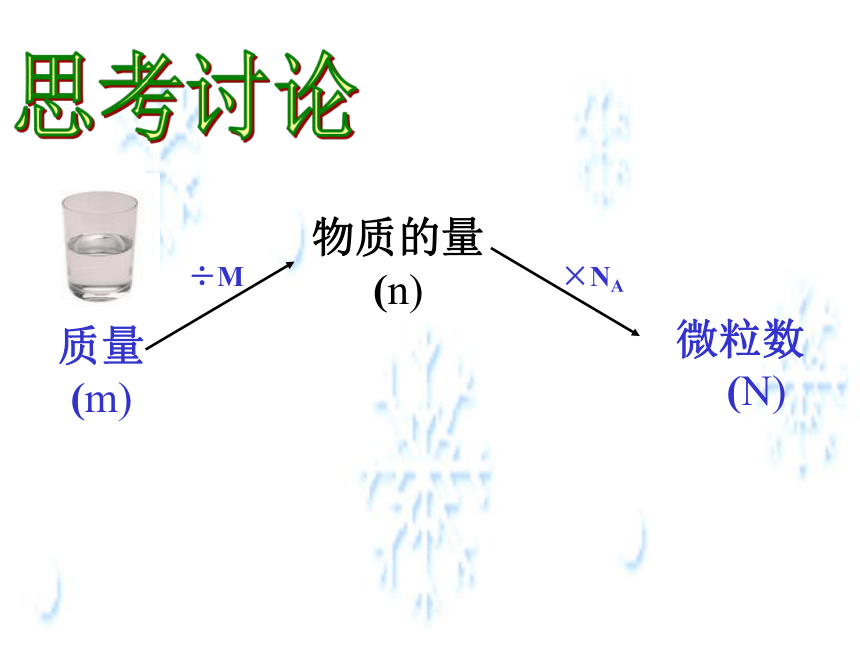
微粒数
(N)
×NA
物质的量 (n)
质量 (m)
÷M
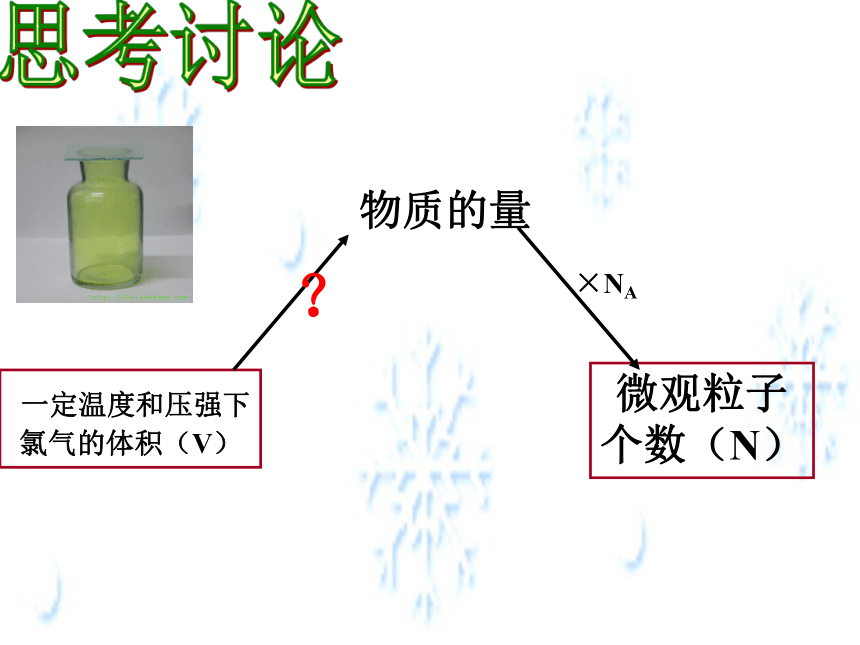
一定温度和压强下氯气的体积(V)
微观粒子
个数(N)
物质的量
×NA
?
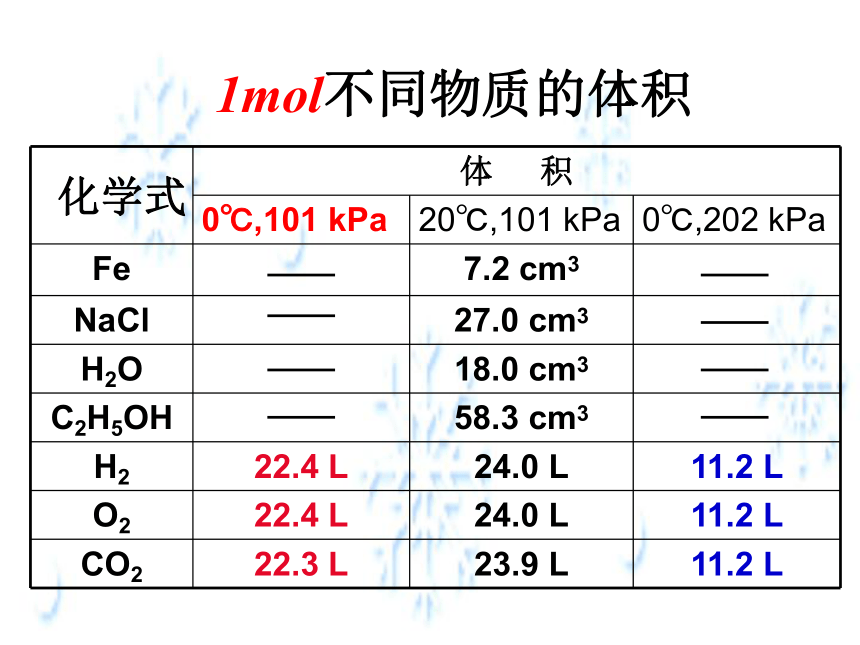
化学式
1mol不同物质的体积
体 积
0℃,101 kPa 20℃,101 kPa 0℃,202 kPa
Fe 7.2 cm3
NaCl 27.0 cm3
H2O 18.0 cm3
C2H5OH 58.3 cm3
H2 22.4 L 24.0 L 11.2 L
O2 22.4 L 24.0 L 11.2 L
CO2 22.3 L 23.9 L 11.2 L
思考:
1.在相同条件下,为什么1mol固体或液体所占
的体积不同呢?
2. 在相同条件下,为什么1mol任何气体的体
积都近似相同呢?
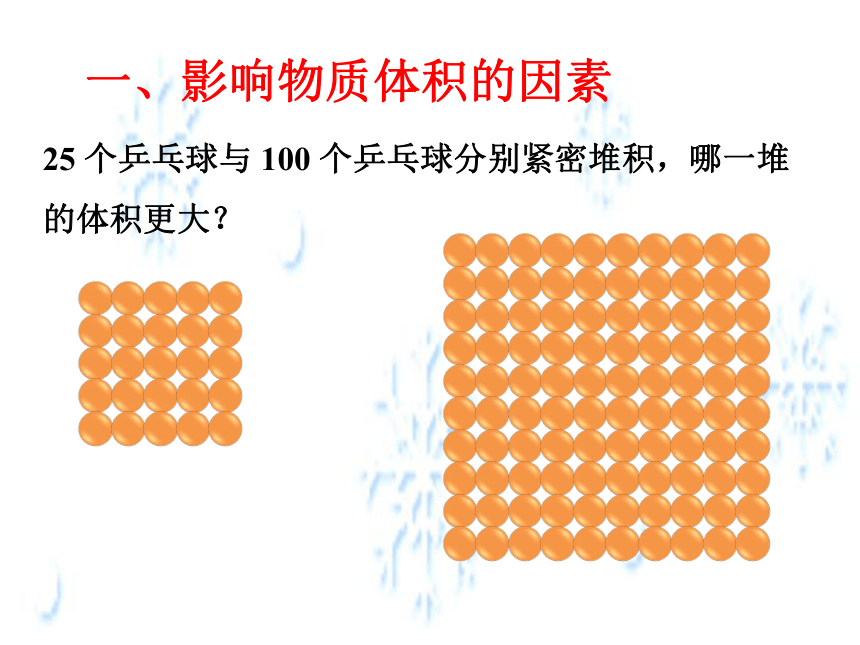
一、影响物质体积的因素
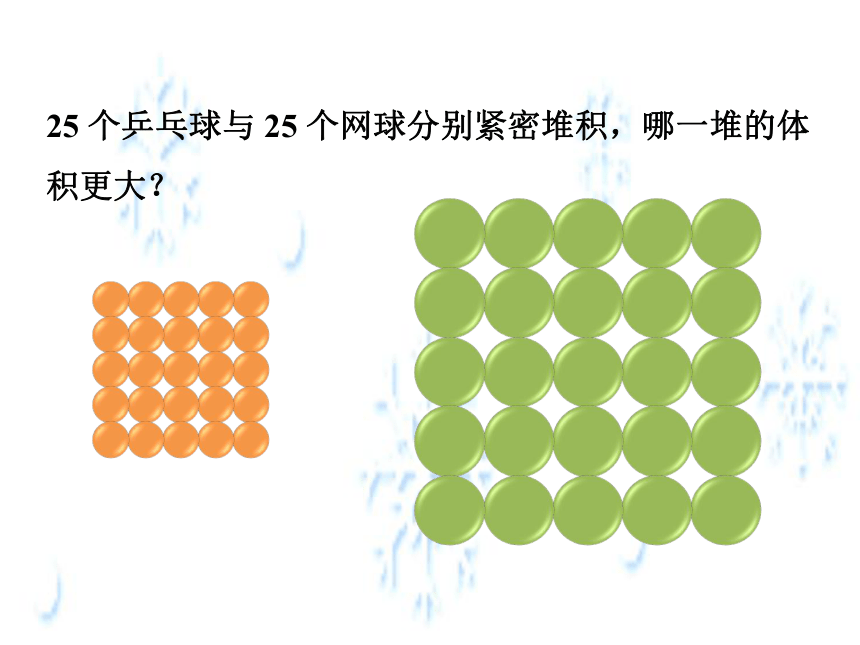
25 个乒乓球与 25 个网球分别紧密堆积,哪一堆的体积更大?
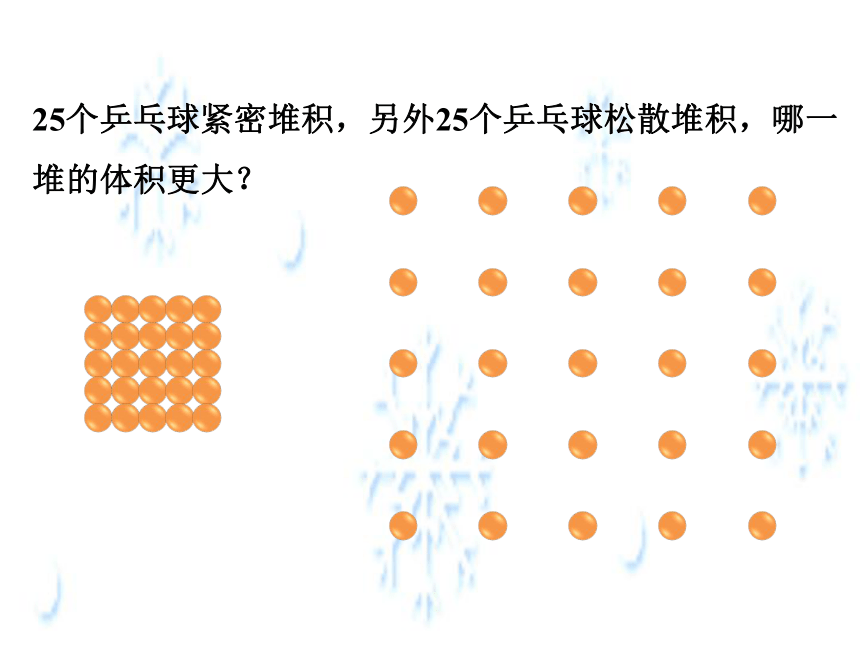
25个乒乓球紧密堆积,另外25个乒乓球松散堆积,哪一堆的体积更大?
物质体积大小的决定因素:
粒子之间的距离
粒子数目
粒子的大小
间隔
物质体积大小的决定因素:
粒子之间的距离
粒子数目
粒子的大小
气体分子间距(d)受哪些因素影响?
温度
压强
三、气体摩尔体积
1、定义:在一定的温度和压强下,单位
物质的量的气体所占的体积。
2、符号:Vm
4、单位:L·mol-1 或 (m3·mol-1)
2、标准状况(0 ℃,101 kPa)下, 气体摩尔体积约为 22.4 L · mol-1 。
1、一定 T、p下,Vm 的数值是固定不变的。
3、在标准状况下(0 ℃ 101 kPa) 1 mol 任何气体所占的体积都约是 22.4 L。
注意:
1.下列说法是否正确?为什么?
(1)?1mol任何气体的体积都约为22.4L。
(2)?1mol任何物质在标况下所占体积都约为22.4L。
(3)标准状况下,0.4molN2和0.6molO2的混合气体
的体积约为22.4 L。
(4)?标准状况下,任何气体的体积都约为22.4L。
(5)标准状况下,任何气体的气体摩尔体积都约为22.4L
×
√
×
×
×
同温同压,相同分子数的气体,体积 。
同温同压,体积相同的气体,分子数 。
同温同压,气体体积大小与分子数目成 比。
相同
相同
正
我们记作“三同定一同” 。
三、阿伏加德罗定律
①同温同压下: = = 。
②同温同压下: = = D (相对密度)
③同温同体积下: = = 。
阿伏加德罗定律推论
当堂检测
1.下列有关气体摩尔体积的描述中正确的是 ( )
A.单位物质的量的气体所占的体积就是气体摩尔体积
B.非标准状况下,1 mol O2 的体积必定不是 22.4 L
C.某物质含有阿伏加德罗常数个微粒,该物质在标准状
况下的体积为 22.4 L
D.标准状况下,1 mol H2和O2的混合气体的体积不一定
为 22.4 L
A
2.下列说法正确的是 ( )
A.32 g O2占有的体积约为 22.4 L
B.22.4 L N2含有阿伏加德罗常数个氮气分子
C.在标准状况下,22.4 L水的质量约为 18 g
D.22 g 二氧化碳与标准状况下 11.2 L HCl含有
相同的分子数
D
3. 已知在标准状况下的四种气体
① 6.72 L CH4 ② 3.01×1023 个 HCl 分子
③13.6 g H2S ④ 0.2 mol NH3
用相应的序号填写下列空白:
(1) 体积最大的是___________;
(2) 密度最大的是___________;
(3) 质量最小的是___________;
(4) 含氢原子数最少的是_______。
②
②
②
④
m (g)
n (mol)
N (个)
V (L)
课堂小结
固态和液态物质结构微粒间的距离很小
气态物质
气态物质结构微粒间的距离很大
返回
第 1 章 认识化学科学
第 3 节 化学中常用的物理量——物质的量
第 2 课时 气体摩尔体积
微粒数
(N)
×NA
物质的量 (n)
质量 (m)
÷M
一定温度和压强下氯气的体积(V)
微观粒子
个数(N)
物质的量
×NA
?
化学式
1mol不同物质的体积
体 积
0℃,101 kPa 20℃,101 kPa 0℃,202 kPa
Fe 7.2 cm3
NaCl 27.0 cm3
H2O 18.0 cm3
C2H5OH 58.3 cm3
H2 22.4 L 24.0 L 11.2 L
O2 22.4 L 24.0 L 11.2 L
CO2 22.3 L 23.9 L 11.2 L
思考:
1.在相同条件下,为什么1mol固体或液体所占
的体积不同呢?
2. 在相同条件下,为什么1mol任何气体的体
积都近似相同呢?
一、影响物质体积的因素
25 个乒乓球与 25 个网球分别紧密堆积,哪一堆的体积更大?
25个乒乓球紧密堆积,另外25个乒乓球松散堆积,哪一堆的体积更大?
物质体积大小的决定因素:
粒子之间的距离
粒子数目
粒子的大小
间隔
物质体积大小的决定因素:
粒子之间的距离
粒子数目
粒子的大小
气体分子间距(d)受哪些因素影响?
温度
压强
三、气体摩尔体积
1、定义:在一定的温度和压强下,单位
物质的量的气体所占的体积。
2、符号:Vm
4、单位:L·mol-1 或 (m3·mol-1)
2、标准状况(0 ℃,101 kPa)下, 气体摩尔体积约为 22.4 L · mol-1 。
1、一定 T、p下,Vm 的数值是固定不变的。
3、在标准状况下(0 ℃ 101 kPa) 1 mol 任何气体所占的体积都约是 22.4 L。
注意:
1.下列说法是否正确?为什么?
(1)?1mol任何气体的体积都约为22.4L。
(2)?1mol任何物质在标况下所占体积都约为22.4L。
(3)标准状况下,0.4molN2和0.6molO2的混合气体
的体积约为22.4 L。
(4)?标准状况下,任何气体的体积都约为22.4L。
(5)标准状况下,任何气体的气体摩尔体积都约为22.4L
×
√
×
×
×
同温同压,相同分子数的气体,体积 。
同温同压,体积相同的气体,分子数 。
同温同压,气体体积大小与分子数目成 比。
相同
相同
正
我们记作“三同定一同” 。
三、阿伏加德罗定律
①同温同压下: = = 。
②同温同压下: = = D (相对密度)
③同温同体积下: = = 。
阿伏加德罗定律推论
当堂检测
1.下列有关气体摩尔体积的描述中正确的是 ( )
A.单位物质的量的气体所占的体积就是气体摩尔体积
B.非标准状况下,1 mol O2 的体积必定不是 22.4 L
C.某物质含有阿伏加德罗常数个微粒,该物质在标准状
况下的体积为 22.4 L
D.标准状况下,1 mol H2和O2的混合气体的体积不一定
为 22.4 L
A
2.下列说法正确的是 ( )
A.32 g O2占有的体积约为 22.4 L
B.22.4 L N2含有阿伏加德罗常数个氮气分子
C.在标准状况下,22.4 L水的质量约为 18 g
D.22 g 二氧化碳与标准状况下 11.2 L HCl含有
相同的分子数
D
3. 已知在标准状况下的四种气体
① 6.72 L CH4 ② 3.01×1023 个 HCl 分子
③13.6 g H2S ④ 0.2 mol NH3
用相应的序号填写下列空白:
(1) 体积最大的是___________;
(2) 密度最大的是___________;
(3) 质量最小的是___________;
(4) 含氢原子数最少的是_______。
②
②
②
④
m (g)
n (mol)
N (个)
V (L)
课堂小结
固态和液态物质结构微粒间的距离很小
气态物质
气态物质结构微粒间的距离很大
返回
