人教版九年级化学上册 第三单元 课题3 元素 教学课件(共37张PPT)
文档属性
| 名称 | 人教版九年级化学上册 第三单元 课题3 元素 教学课件(共37张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-09-16 00:00:00 | ||
图片预览









文档简介
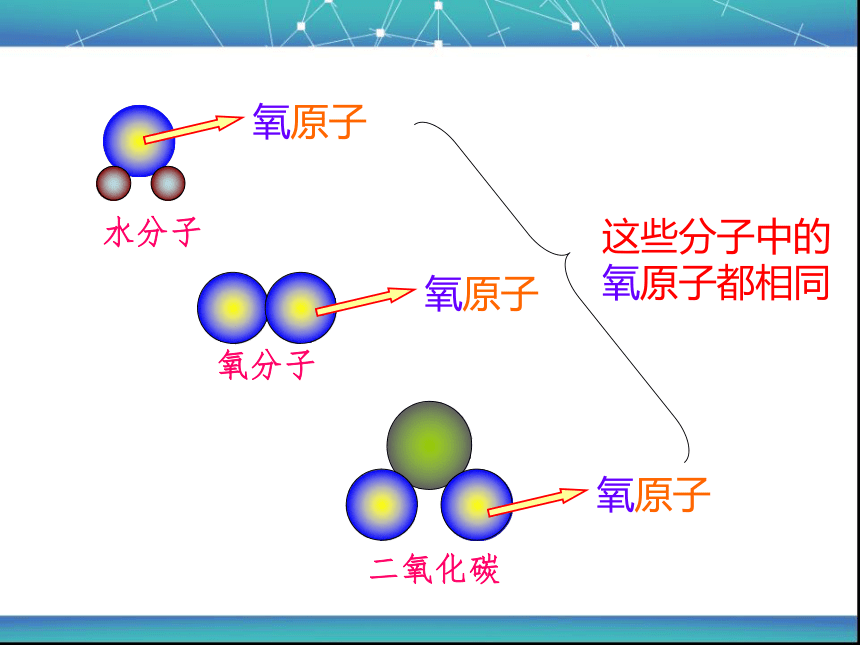
课件37张PPT。高纯氢气氢气球氢气气艇——氢气是由氢元素组成。课题3 元素氧气——氧气是由氧元素组成。——水是由氢、氧两种元素组成。水氧原子氧原子氧原子这些分子中的
氧原子都相同知识与技能 1.了解元素的概念,统一对物质的宏观组成与微观结构的认识;
2.了解元素符号所表示的意义,学会元素符号的正确写法,逐步记住一些常见的元素符号;
3.初步认识元素周期表,知道它是学习和研究化学的工具,能根据原子序数,在元素周期表中找到指定元素和有关该元素的一些其他信息。教学目标 1.通过微观想像、分析、讨论、对比,认识到化学反应中分子可以发生变化而元素不发生变化;
2.通过联想记忆、卡片问答等趣味活动,帮助学生认识元素符号;
3.通过同学之间相互合作、查阅资料,了解地壳、生物的细胞和一些食品中元素的含量。过程与方法 1.进一步建立科学的物质观,增进对物质的宏观组成与微观结构的认识;
2.发展善于合作、勤于思考、勇于实践的科学精神。情感态度与价值观 重点 难点1.元素的概念;
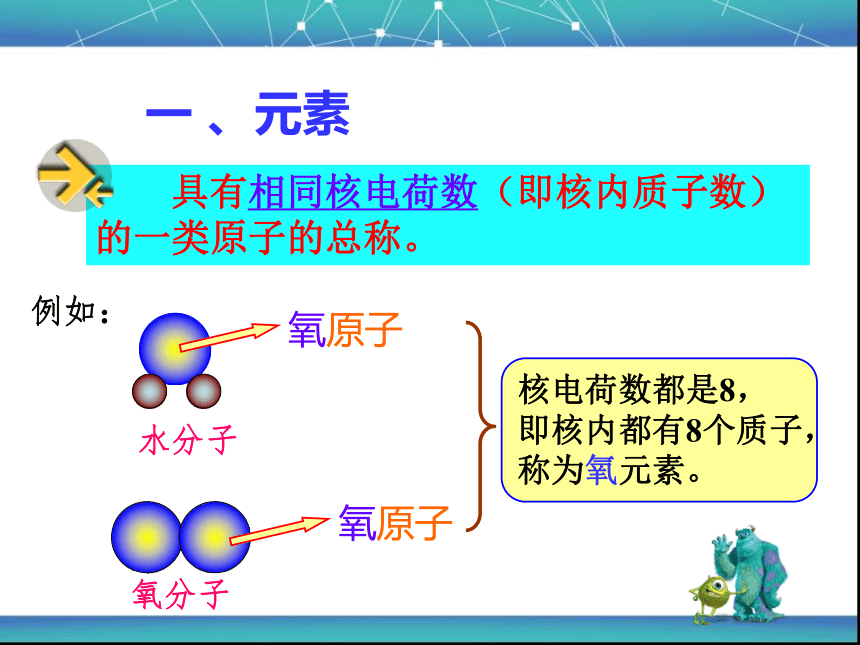
2.元素符号的读法及意义。元素符号的读法及意义。一 、元素 具有相同核电荷数(即核内质子数)的一类原子的总称。氧原子氧原子例如:物质的种类:2 000 多万种
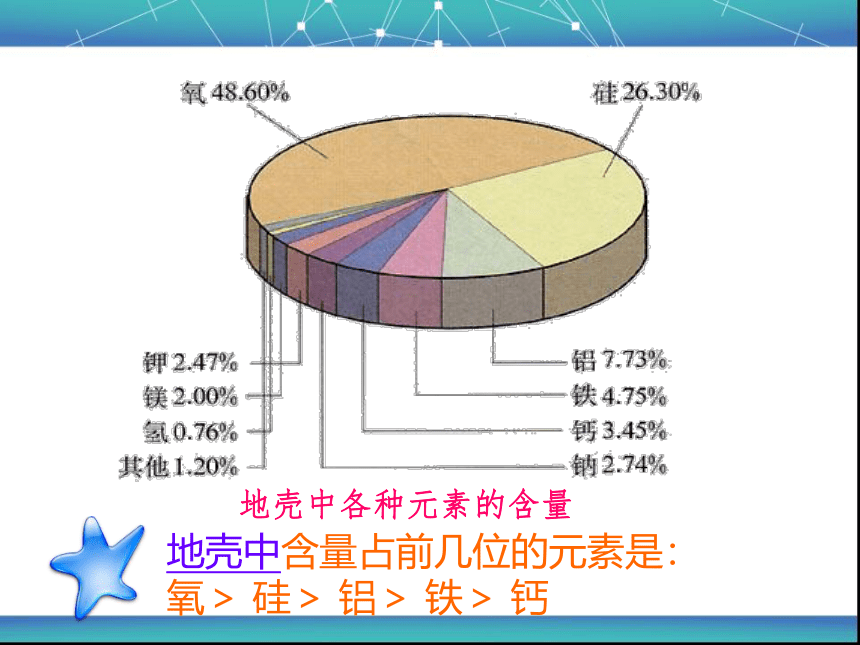
元素的种类:100 余种 劳伦斯伯克利国家实验室2002年公开承认1999年发现的118和116号元素的实验数据是捏造的。 “对一个实验室来讲,没有比科学诚实更重要的东西了”。地壳中各种元素的含量地壳中含量占前几位的元素是:
氧> 硅> 铝> 铁> 钙生物细胞中各元素的含量:
氧>碳> 氢>氮 人体缺少或存在过多的常量元素或某些微量元素,都会发生病变。有些元素如砷、铅、镉、汞进入人体会引起中毒,这些元素称为有毒元素。所以,我们必须通过保护环境,控制污染,减少与有毒元素的接触,防止有毒元素进入人体而导致中毒。人体中各元素的含量 人需要合理膳食来补充人体所缺的微量元素奶类豆类钙片——补钙动物肝脏黑木耳蛋类——补铁牡蛎鱼类瘦肉——补锌 金属元素 —— 钠(Na)、镁(Mg)、
铝(Al)、铁(Fe)、
汞(Hg)、金(Au )……
非金属元素—— 碳(C)、氮(N)、
氧(O)、硫(S)、
氯( Cl )……
稀有气体元素——氦(He)、氖(Ne)、
氩(Ar)……1.元素的分类:2.分子、原子、元素的区别:真实的粒子宏观称谓真实的粒子有个数、有种类分子由原子构成水分子(H2O) 有个数、有种类无个数、有种类由质子、中子、电子构成是一类原子的总称氢原子(H)
氧原子(O) 氢元素 、氧元素 历史上,道尔顿曾用图形加字母的方式作为元素符号 二 、元素符号1.元素符号的发展:常见元素中英文名称对照表2.元素符号的意义: (1)表示一种元素
(2)表示该元素的一个原子HFe例如:氢元素一个氢原子铁元素一个铁原子铁2H3Fe两个氢原子三个铁原子3.元素符号的书写: (1)由一个字母表示的元素符号要大写如氢H、氧O、氮N。
(2)由两个字母表示的元素符号第一个字母要大写,第二个字母要小写如氦He、铁Fe、锌Zn 、钙Ca、氯Cl、氦He、镁Mg。 记住并会正确书写下列元素符号:
氢 氦 碳 氮 氧 氟 氖
H He C N O F Ne
钠 镁 铝 硅 磷 硫 氯
Na Mg Al Si P S Cl
氩 钾 钙 锰 铁 铜 锌
Ar K Ca Mn Fe Cu Zn
银 钡 汞 金
Ag Ba Hg Au三、元素周期表简介 1869年2月,俄国化学家门捷列夫发现了他的第一张元素周期表,表中除收入了当时已知的63种元素外,还给尚未发现的元素留下了27个空位,并大胆地预言了11种未知的新元素和它们在元素周期表的位置,同时根据它们的性质取了名字,如类铝、类硼、类硅等,后来都得到了验证。门捷列夫7个横行18个纵列(周期)(族)原子序数= 核电荷数金属元素区非金属元素区元素周期表的意义: (1)为寻找新元素提供了理论依据。
(2)由于元素周期表中位置越接近的元素化学性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、催化剂、农药)。半导体材料铜基催化剂农药 元素就是具有相同核电荷数(即核内质子数)的一类原子的总称。
元素符号的意义:
(1)表示一种元素。
(2)表示该元素的一个原子。课堂小结 1. 一种元素与另一种元素最本质的区别在于( )
A.质子数
B.中子数
C.电子数
D.相对原子质量D课堂练习 2.大气中的臭氧层可吸收太阳的紫外线,对地球起保护作用。有关臭氧O3的说法不正确的是( )
A.臭氧是一种单质。
B.每个臭氧分子由三个氧原子构成。
C.臭氧中含有氧气。
D.臭氧和氧气组成的气体是混合物。C 3.实验室测得某物质只含有一种元素,则该物质( )
A.一定是单质
B.一定是纯净物
C.一定是混合物
D.一定不是化合物D
氧原子都相同知识与技能 1.了解元素的概念,统一对物质的宏观组成与微观结构的认识;
2.了解元素符号所表示的意义,学会元素符号的正确写法,逐步记住一些常见的元素符号;
3.初步认识元素周期表,知道它是学习和研究化学的工具,能根据原子序数,在元素周期表中找到指定元素和有关该元素的一些其他信息。教学目标 1.通过微观想像、分析、讨论、对比,认识到化学反应中分子可以发生变化而元素不发生变化;
2.通过联想记忆、卡片问答等趣味活动,帮助学生认识元素符号;
3.通过同学之间相互合作、查阅资料,了解地壳、生物的细胞和一些食品中元素的含量。过程与方法 1.进一步建立科学的物质观,增进对物质的宏观组成与微观结构的认识;
2.发展善于合作、勤于思考、勇于实践的科学精神。情感态度与价值观 重点 难点1.元素的概念;
2.元素符号的读法及意义。元素符号的读法及意义。一 、元素 具有相同核电荷数(即核内质子数)的一类原子的总称。氧原子氧原子例如:物质的种类:2 000 多万种
元素的种类:100 余种 劳伦斯伯克利国家实验室2002年公开承认1999年发现的118和116号元素的实验数据是捏造的。 “对一个实验室来讲,没有比科学诚实更重要的东西了”。地壳中各种元素的含量地壳中含量占前几位的元素是:
氧> 硅> 铝> 铁> 钙生物细胞中各元素的含量:
氧>碳> 氢>氮 人体缺少或存在过多的常量元素或某些微量元素,都会发生病变。有些元素如砷、铅、镉、汞进入人体会引起中毒,这些元素称为有毒元素。所以,我们必须通过保护环境,控制污染,减少与有毒元素的接触,防止有毒元素进入人体而导致中毒。人体中各元素的含量 人需要合理膳食来补充人体所缺的微量元素奶类豆类钙片——补钙动物肝脏黑木耳蛋类——补铁牡蛎鱼类瘦肉——补锌 金属元素 —— 钠(Na)、镁(Mg)、
铝(Al)、铁(Fe)、
汞(Hg)、金(Au )……
非金属元素—— 碳(C)、氮(N)、
氧(O)、硫(S)、
氯( Cl )……
稀有气体元素——氦(He)、氖(Ne)、
氩(Ar)……1.元素的分类:2.分子、原子、元素的区别:真实的粒子宏观称谓真实的粒子有个数、有种类分子由原子构成水分子(H2O) 有个数、有种类无个数、有种类由质子、中子、电子构成是一类原子的总称氢原子(H)
氧原子(O) 氢元素 、氧元素 历史上,道尔顿曾用图形加字母的方式作为元素符号 二 、元素符号1.元素符号的发展:常见元素中英文名称对照表2.元素符号的意义: (1)表示一种元素
(2)表示该元素的一个原子HFe例如:氢元素一个氢原子铁元素一个铁原子铁2H3Fe两个氢原子三个铁原子3.元素符号的书写: (1)由一个字母表示的元素符号要大写如氢H、氧O、氮N。
(2)由两个字母表示的元素符号第一个字母要大写,第二个字母要小写如氦He、铁Fe、锌Zn 、钙Ca、氯Cl、氦He、镁Mg。 记住并会正确书写下列元素符号:
氢 氦 碳 氮 氧 氟 氖
H He C N O F Ne
钠 镁 铝 硅 磷 硫 氯
Na Mg Al Si P S Cl
氩 钾 钙 锰 铁 铜 锌
Ar K Ca Mn Fe Cu Zn
银 钡 汞 金
Ag Ba Hg Au三、元素周期表简介 1869年2月,俄国化学家门捷列夫发现了他的第一张元素周期表,表中除收入了当时已知的63种元素外,还给尚未发现的元素留下了27个空位,并大胆地预言了11种未知的新元素和它们在元素周期表的位置,同时根据它们的性质取了名字,如类铝、类硼、类硅等,后来都得到了验证。门捷列夫7个横行18个纵列(周期)(族)原子序数= 核电荷数金属元素区非金属元素区元素周期表的意义: (1)为寻找新元素提供了理论依据。
(2)由于元素周期表中位置越接近的元素化学性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、催化剂、农药)。半导体材料铜基催化剂农药 元素就是具有相同核电荷数(即核内质子数)的一类原子的总称。
元素符号的意义:
(1)表示一种元素。
(2)表示该元素的一个原子。课堂小结 1. 一种元素与另一种元素最本质的区别在于( )
A.质子数
B.中子数
C.电子数
D.相对原子质量D课堂练习 2.大气中的臭氧层可吸收太阳的紫外线,对地球起保护作用。有关臭氧O3的说法不正确的是( )
A.臭氧是一种单质。
B.每个臭氧分子由三个氧原子构成。
C.臭氧中含有氧气。
D.臭氧和氧气组成的气体是混合物。C 3.实验室测得某物质只含有一种元素,则该物质( )
A.一定是单质
B.一定是纯净物
C.一定是混合物
D.一定不是化合物D
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
