人教版九年级化学课件:6.2二氧化碳制取的研究 (共24张PPT)
文档属性
| 名称 | 人教版九年级化学课件:6.2二氧化碳制取的研究 (共24张PPT) |
|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-09-17 00:00:00 | ||
图片预览




文档简介
(共24张PPT)
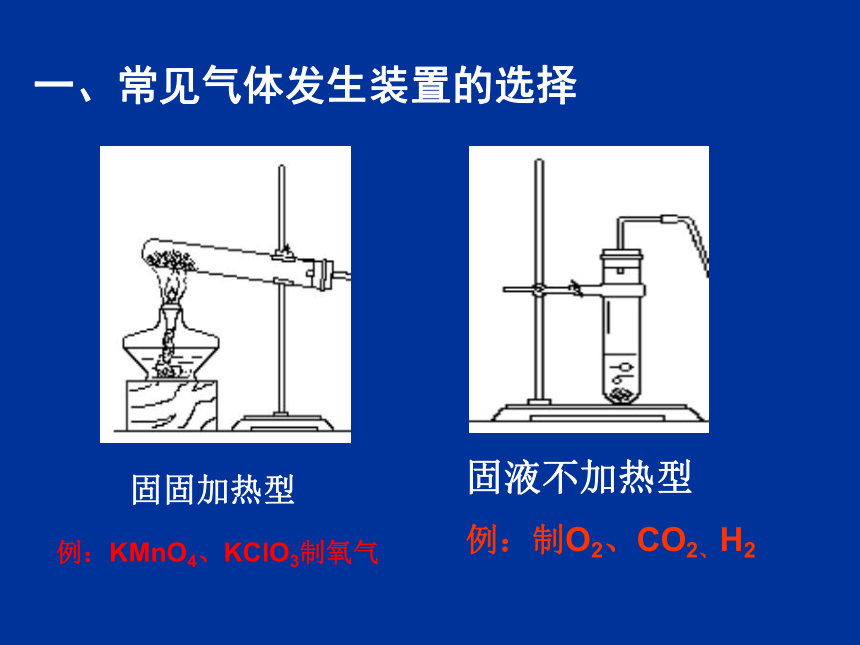
气体的制、净、集、处理和测量专题
发生装置的
选择依据
反应物状态
反应条件
固体+固体
固体+液体
加热型
不加热型
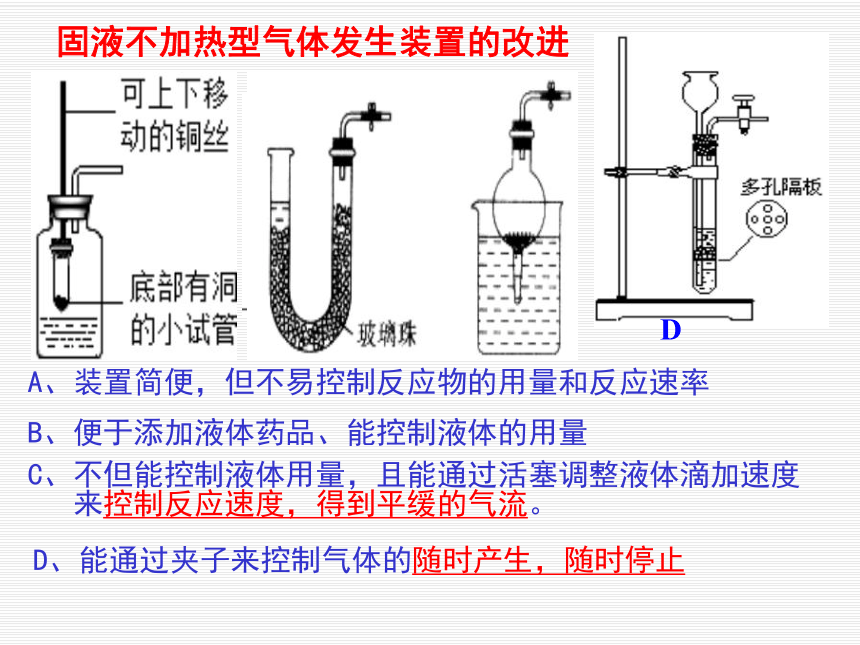
一、常见气体发生装置的选择
一、常见气体发生装置的选择
固固加热型
固液不加热型
例:KMnO4、KClO3制氧气
例:制O2、CO2、H2
A
A、装置简便,但不易控制反应物的用量和反应速率
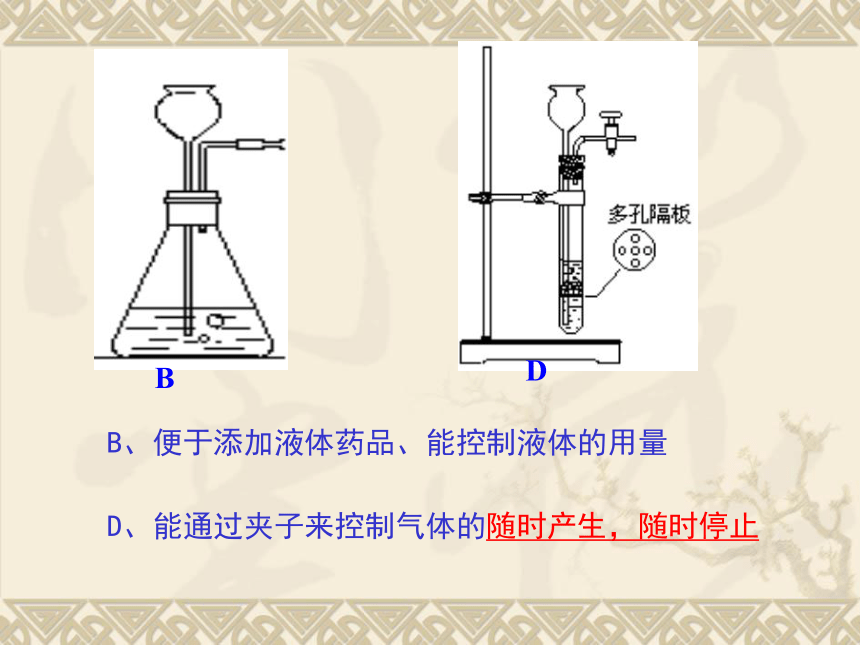
B、便于添加液体药品、能控制液体的用量
C、不但能控制液体用量,且能通过活塞调整液体滴加速度
来控制反应速度,得到平缓的气流。
D、能通过夹子来控制气体的随时产生,随时停止
固液不加热型气体发生装置的改进
D、能通过夹子来控制气体的随时产生,随时停止
B、便于添加液体药品、能控制液体的用量
二、气体的净化
2、净化原则
将不纯净的气体中的杂质气体除去得到较纯净的气体的过程。
1、选择的试剂要能吸收杂质气体
2、被净化的气体不能与除杂试剂反应
1、杂质的来源
反应物的挥发(如盐酸挥发出的HCl、H2O)
副反应的发生(如碳不完全燃烧产生CO)
同一反应同时产生几种气体(如电解水)
3、不能引入新杂质
H2中混有HCl
CO中混有CO2
将混合气体通过碱液(NaOH)
CO2中混有CO、H2
(将混合气体通过灼热的CuO)
CO2中混有O2
(将混合气体通过饱和NaHCO3溶液)
例:
3、常见气体的净化
4、气体的干燥(除水蒸气)
常见的干燥剂
生石灰、固体NaOH(不能干燥CO2、HCl等
酸性气体)
浓硫酸(不能干燥NH3等碱性气体)
CO2中混有HCl
(将混合气体通过灼热的Cu网)
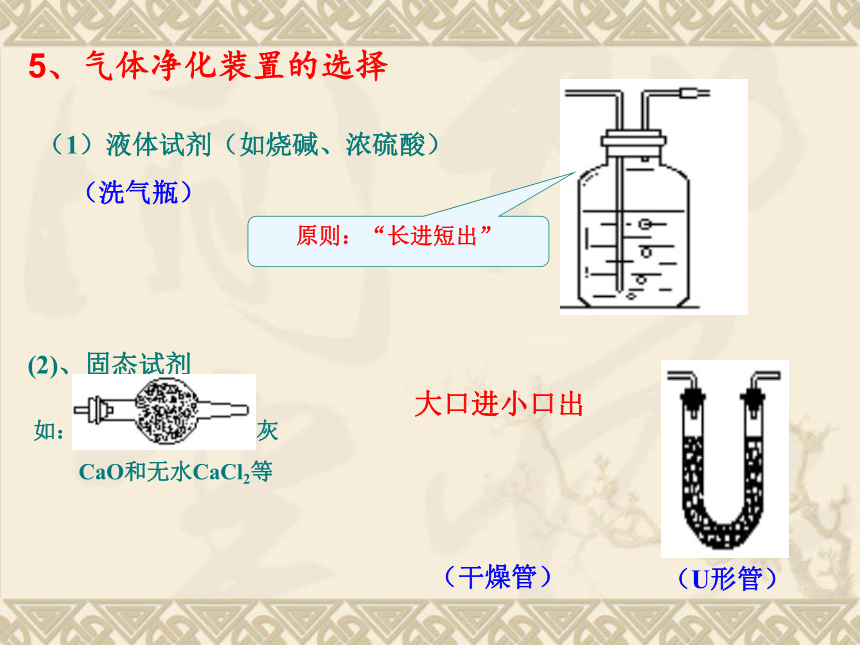
(1)液体试剂(如烧碱、浓硫酸)
(洗气瓶)
原则:“长进短出”
(2)、固态试剂
如:固体NaOH、生石灰
CaO和无水CaCl2等
大口进小口出
5、气体净化装置的选择
(干燥管)
(U形管)
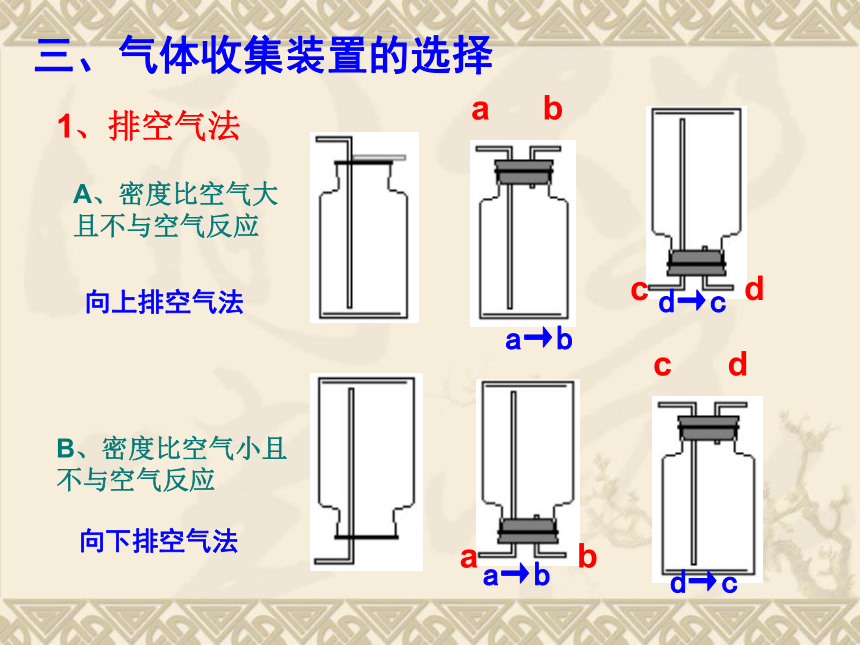
1、排空气法
A、密度比空气大且不与空气反应
B、密度比空气小且不与空气反应
向上排空气法
向下排空气法
三、气体收集装置的选择
a→b
d→c
a→b
d→c
2、排水法
气体不易溶于水且
不与水反应
a→b
c→d
四、尾气的处理(防污染)
⑵ 倒置漏斗、干燥管吸收法
1、通常有毒和有污染的尾气必须适当处理。
常用方法有:
? ⑴ 直接吸收法
用NaOH吸收CO2 、SO2
(气体溶解或反应速度不很
快,不易引起倒吸);
吸收极易溶且溶解很快的气体。
如HCl、NH3等, 增大气体与吸收
液的接触面积,防止吸收液的倒吸。
? ⑷ 燃烧法
(有毒且可燃的气体,如CO等)?
⑶ 收集法
(用球胆收集,如多余的CO的处理)
五、气体体积的测量
上下移动使两边液面相平
排水法(量筒中先装满水)
间接测量法
排出液体的体积等于所集气体体积
------
油层防气体溶解
发 生
装 置
净 化
装 置
干 燥
装 置
收 集
装 置
吸 收
装 置
气体的制取与净化
小结
1、下列制取二氧化碳的装置中,不能做到“随时控制反应的发生与停止”的是( )
A
A
B
C
D
2、在H2、O2、CH4、CO2、CO气体中,
①能用装置A收集的有_____________________
②能用装置C收集的有_____________________
③若用装置B收集气体应从___端进入
④若用装置D收集H2气体应从____端进入。
O2、CO2
H2、O2、CH4、CO
d
b
a
b
d
c
3、一氧化氮气体难溶于水,密度比空气略大,常温下还能与空气中的氧气发生反应生成二氧化氮,则收集一氧化氮气体的方法可用( )
A、向上排空气法 B、向下排空气法
C、排水法 D、A和C都行
C
4、 已知氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。在实验室中通常用加热固体氯化铵和熟石灰的混合物来制取氨气。试回答下列问题:
(1)实验室制取氨气的装置可以和制取 装置相同。
(2)氨气可以用 法收集,收集氨气的集气瓶必须十分干燥,这是因为 。
(3)现欲制取一瓶氨气,除已有试管、带导管的橡皮塞、铁架台(带铁夹)外,要完成该实验,还必须用到的仪器有 。
O2
向下排空气
酒精灯
集气瓶
氨气极易溶于水
5. 某实验小组同学对双氧水制氧气的若干问
题进行探究。
(1)利用图甲中A、B仪器可以组装一套测量氧
气体积的装置,该装置导管的连接顺序
是 接C(填接口编号)
(2)A瓶中原有的空气对氧气体积测定
(填”有或没有”)影响?
(3)右图乙装置也可以用来测量反应中生成
的氧气体积。为了较准确的测量氧气体积,
在读取量气管中液面读数时,应注意哪些
问题? , 。(答两点)
如管中出现左低右高,应将水准管 (填“上
移”,“下移”“不动”)
b
水位不变时
没有
两边水位相同
下移
6.同学们利用装修后剩下的大理石碎片进行相关实验.
(1)用装置A制取CO2,该装置能通过上下移动粗铜丝来控制
反应的发生或停止,大理石应放在 中,A中反应的方程式为 .
A中的粗铜丝能否用铁丝代替 ,原因是 .
(2)如用装置B中浓H2SO4干燥CO2,则CO2应从 (填字母)端口通入.
(3)如用装置C收集CO2,则CO2应从 (填字母)端口通入.
(4)装置D用于测量CO2的体积,植物油的作用是 .
有孔塑料瓶
铁会与盐酸反应
影响CO2反应速率的因素探究
1、反应物:
大理石、稀盐酸
盐酸体积
CaCO3+2HCl=CaCl2+H2O+CO2↑
3、猜想:
盐酸浓度
2、反应原理:
大理石质量
反应温度
颗粒大小
CaCO3含量
4、实验操作及现象:
3、实验结论:
例:在一次实验课上,各小组同学在不同地点找来的小石块与稀盐酸反应制取二氧化碳。此反应的化学方程式为??????????? 。
小明发现,相邻小组气体产生的速率比自己小组的快。小明将这一情况报告老师,老师鼓励他们对此问题共同探究。
【提出问题】影响二氧化碳气体产生速率的因素是什么?
【作出猜想】①不同地点石块中碳酸钙含量不同;
????????? ??②所用盐酸的溶质质量分数不同;
?????? ???? ?③还可能是????????????????????????????????? 。
大理石颗粒大小、温度、质量
【设计实验】(1)验证猜想①是否成立,要设计的实验:
分别取大小相同、质量相同、?????? ???? 的石块,加入质量相同、???????? ????????????? 的稀盐酸进行实验。
(2)验证猜想②是否成立,对盐酸的要求
是???????????????????????????????????????????????? 。?
【交流讨论】实验中可以通过观察气泡产生的剧烈程度,粗略地比较反应速率。若要做到精确比较,应该测量的实验数据
是???????????????????????????????????????????????????????????? 。
①不同地点石块中碳酸钙含量不同;
不同地点的碳酸钙
浓度相同
②所用盐酸的溶质质量分数不同;
质量相同、浓度不同
相同时间收集气体的体积或收集相同体积气体所需时间
【拓展延伸】上述实验中,小明采用了控制变量的研究方法。用此方法探究“催化剂对用过氧化氢溶液制取氧气的反应速率的影响”,需要控制不变的因素有(答出两点即可)??????????? ???????????????? 等。
过氧化氢的浓度、质量、反应温度等
气体的制、净、集、处理和测量专题
发生装置的
选择依据
反应物状态
反应条件
固体+固体
固体+液体
加热型
不加热型
一、常见气体发生装置的选择
一、常见气体发生装置的选择
固固加热型
固液不加热型
例:KMnO4、KClO3制氧气
例:制O2、CO2、H2
A
A、装置简便,但不易控制反应物的用量和反应速率
B、便于添加液体药品、能控制液体的用量
C、不但能控制液体用量,且能通过活塞调整液体滴加速度
来控制反应速度,得到平缓的气流。
D、能通过夹子来控制气体的随时产生,随时停止
固液不加热型气体发生装置的改进
D、能通过夹子来控制气体的随时产生,随时停止
B、便于添加液体药品、能控制液体的用量
二、气体的净化
2、净化原则
将不纯净的气体中的杂质气体除去得到较纯净的气体的过程。
1、选择的试剂要能吸收杂质气体
2、被净化的气体不能与除杂试剂反应
1、杂质的来源
反应物的挥发(如盐酸挥发出的HCl、H2O)
副反应的发生(如碳不完全燃烧产生CO)
同一反应同时产生几种气体(如电解水)
3、不能引入新杂质
H2中混有HCl
CO中混有CO2
将混合气体通过碱液(NaOH)
CO2中混有CO、H2
(将混合气体通过灼热的CuO)
CO2中混有O2
(将混合气体通过饱和NaHCO3溶液)
例:
3、常见气体的净化
4、气体的干燥(除水蒸气)
常见的干燥剂
生石灰、固体NaOH(不能干燥CO2、HCl等
酸性气体)
浓硫酸(不能干燥NH3等碱性气体)
CO2中混有HCl
(将混合气体通过灼热的Cu网)
(1)液体试剂(如烧碱、浓硫酸)
(洗气瓶)
原则:“长进短出”
(2)、固态试剂
如:固体NaOH、生石灰
CaO和无水CaCl2等
大口进小口出
5、气体净化装置的选择
(干燥管)
(U形管)
1、排空气法
A、密度比空气大且不与空气反应
B、密度比空气小且不与空气反应
向上排空气法
向下排空气法
三、气体收集装置的选择
a→b
d→c
a→b
d→c
2、排水法
气体不易溶于水且
不与水反应
a→b
c→d
四、尾气的处理(防污染)
⑵ 倒置漏斗、干燥管吸收法
1、通常有毒和有污染的尾气必须适当处理。
常用方法有:
? ⑴ 直接吸收法
用NaOH吸收CO2 、SO2
(气体溶解或反应速度不很
快,不易引起倒吸);
吸收极易溶且溶解很快的气体。
如HCl、NH3等, 增大气体与吸收
液的接触面积,防止吸收液的倒吸。
? ⑷ 燃烧法
(有毒且可燃的气体,如CO等)?
⑶ 收集法
(用球胆收集,如多余的CO的处理)
五、气体体积的测量
上下移动使两边液面相平
排水法(量筒中先装满水)
间接测量法
排出液体的体积等于所集气体体积
------
油层防气体溶解
发 生
装 置
净 化
装 置
干 燥
装 置
收 集
装 置
吸 收
装 置
气体的制取与净化
小结
1、下列制取二氧化碳的装置中,不能做到“随时控制反应的发生与停止”的是( )
A
A
B
C
D
2、在H2、O2、CH4、CO2、CO气体中,
①能用装置A收集的有_____________________
②能用装置C收集的有_____________________
③若用装置B收集气体应从___端进入
④若用装置D收集H2气体应从____端进入。
O2、CO2
H2、O2、CH4、CO
d
b
a
b
d
c
3、一氧化氮气体难溶于水,密度比空气略大,常温下还能与空气中的氧气发生反应生成二氧化氮,则收集一氧化氮气体的方法可用( )
A、向上排空气法 B、向下排空气法
C、排水法 D、A和C都行
C
4、 已知氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。在实验室中通常用加热固体氯化铵和熟石灰的混合物来制取氨气。试回答下列问题:
(1)实验室制取氨气的装置可以和制取 装置相同。
(2)氨气可以用 法收集,收集氨气的集气瓶必须十分干燥,这是因为 。
(3)现欲制取一瓶氨气,除已有试管、带导管的橡皮塞、铁架台(带铁夹)外,要完成该实验,还必须用到的仪器有 。
O2
向下排空气
酒精灯
集气瓶
氨气极易溶于水
5. 某实验小组同学对双氧水制氧气的若干问
题进行探究。
(1)利用图甲中A、B仪器可以组装一套测量氧
气体积的装置,该装置导管的连接顺序
是 接C(填接口编号)
(2)A瓶中原有的空气对氧气体积测定
(填”有或没有”)影响?
(3)右图乙装置也可以用来测量反应中生成
的氧气体积。为了较准确的测量氧气体积,
在读取量气管中液面读数时,应注意哪些
问题? , 。(答两点)
如管中出现左低右高,应将水准管 (填“上
移”,“下移”“不动”)
b
水位不变时
没有
两边水位相同
下移
6.同学们利用装修后剩下的大理石碎片进行相关实验.
(1)用装置A制取CO2,该装置能通过上下移动粗铜丝来控制
反应的发生或停止,大理石应放在 中,A中反应的方程式为 .
A中的粗铜丝能否用铁丝代替 ,原因是 .
(2)如用装置B中浓H2SO4干燥CO2,则CO2应从 (填字母)端口通入.
(3)如用装置C收集CO2,则CO2应从 (填字母)端口通入.
(4)装置D用于测量CO2的体积,植物油的作用是 .
有孔塑料瓶
铁会与盐酸反应
影响CO2反应速率的因素探究
1、反应物:
大理石、稀盐酸
盐酸体积
CaCO3+2HCl=CaCl2+H2O+CO2↑
3、猜想:
盐酸浓度
2、反应原理:
大理石质量
反应温度
颗粒大小
CaCO3含量
4、实验操作及现象:
3、实验结论:
例:在一次实验课上,各小组同学在不同地点找来的小石块与稀盐酸反应制取二氧化碳。此反应的化学方程式为??????????? 。
小明发现,相邻小组气体产生的速率比自己小组的快。小明将这一情况报告老师,老师鼓励他们对此问题共同探究。
【提出问题】影响二氧化碳气体产生速率的因素是什么?
【作出猜想】①不同地点石块中碳酸钙含量不同;
????????? ??②所用盐酸的溶质质量分数不同;
?????? ???? ?③还可能是????????????????????????????????? 。
大理石颗粒大小、温度、质量
【设计实验】(1)验证猜想①是否成立,要设计的实验:
分别取大小相同、质量相同、?????? ???? 的石块,加入质量相同、???????? ????????????? 的稀盐酸进行实验。
(2)验证猜想②是否成立,对盐酸的要求
是???????????????????????????????????????????????? 。?
【交流讨论】实验中可以通过观察气泡产生的剧烈程度,粗略地比较反应速率。若要做到精确比较,应该测量的实验数据
是???????????????????????????????????????????????????????????? 。
①不同地点石块中碳酸钙含量不同;
不同地点的碳酸钙
浓度相同
②所用盐酸的溶质质量分数不同;
质量相同、浓度不同
相同时间收集气体的体积或收集相同体积气体所需时间
【拓展延伸】上述实验中,小明采用了控制变量的研究方法。用此方法探究“催化剂对用过氧化氢溶液制取氧气的反应速率的影响”,需要控制不变的因素有(答出两点即可)??????????? ???????????????? 等。
过氧化氢的浓度、质量、反应温度等
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
