1.3物质的量——物质的量浓度(第三课时)课件
文档属性
| 名称 | 1.3物质的量——物质的量浓度(第三课时)课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-09-19 00:00:00 | ||
图片预览





文档简介
(共23张PPT)
第1章 认识化学科学
第3节 化学中常用的物理量——物质的量
第3课时 物质的量浓度溶液的配制
1、都是高锰酸钾溶液,为什么颜色不同呢?
讨论:
2、怎样表示溶液的浓度?
3、如何配制含0。04molNaCI,体积为0.1L的溶液?
配制0.1L NaCl溶液,其中溶质的物质的量为 0.04 mol.
目的
操作
步骤
合适的仪器
活动˙探究
方法导引
怎样取 0.04 mol NaCl?
怎样实现最后溶液为 0.1 L?
1、特点:容量瓶上标有温度、容积、刻度线。
2、常用规格:100mL、250 mL、500mL、1000mL。
认识容量瓶
1、使用前先检查是否漏液。
2、用蒸馏水清洗,不干燥不影响实验。
3、仅作配制一定体积、浓度准确的溶液,不能用于量取、贮存、溶解、反应。
容量瓶的使用
配制100mL含NaCl 0.04 mol的溶液。
计算
m(NaCl) =0.04mol×58.5g/mol=2.34g
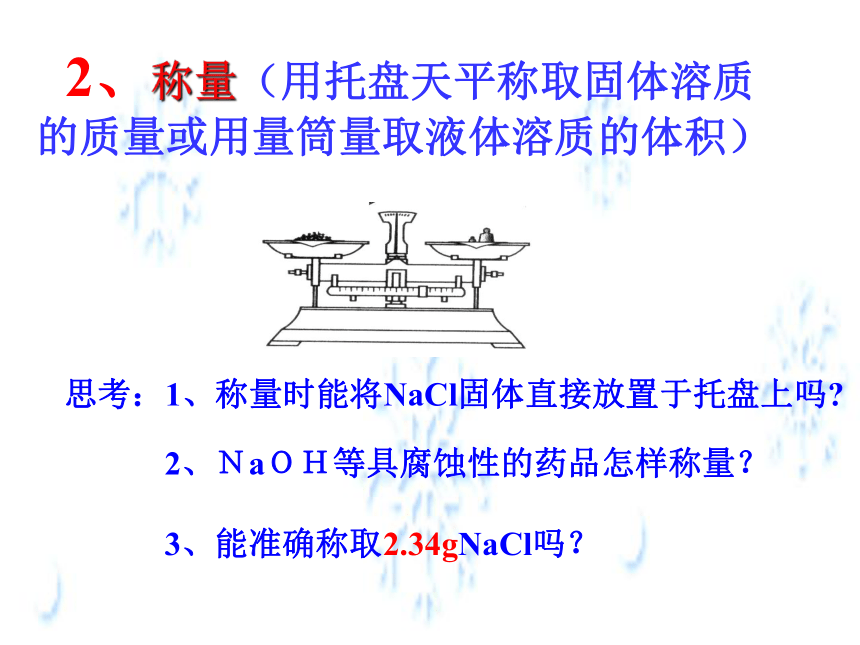
2、称量(用托盘天平称取固体溶质的质量或用量筒量取液体溶质的体积)
思考:1、称量时能将NaCl固体直接放置于托盘上吗?
2、NaOH等具腐蚀性的药品怎样称量?
3、能准确称取2.34gNaCl吗?
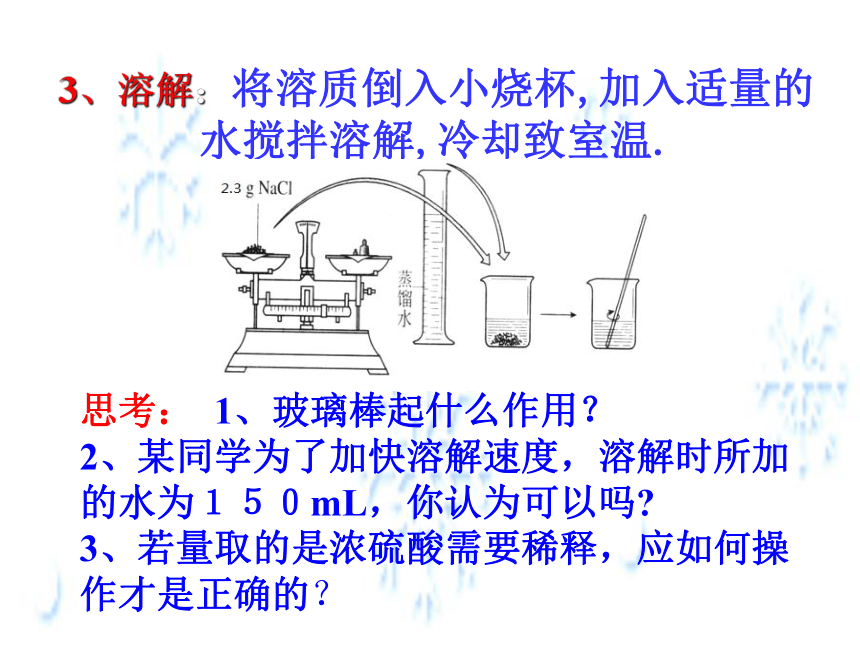
3、溶解:将溶质倒入小烧杯,加入适量的水搅拌溶解,冷却致室温.
思考: 1、玻璃棒起什么作用?
2、某同学为了加快溶解速度,溶解时所加的水为150mL,你认为可以吗?
3、若量取的是浓硫酸需要稀释,应如何操
作才是正确的?
4. 转移
思考:1、为避免液体洒在外面,应怎样操作?。
2、将烧杯中的氯化钠溶液转移到容量瓶中,此时溶质是否完全被转移到容量瓶中?应如何处理?
5.定容
向容量瓶中加入蒸馏水,在距离刻度1~2cm时,
改用胶头滴管滴加蒸馏水至刻度线。
思考:
若定容时不小心液面超过了刻度线,怎么办?
注意:液体凹液面最低处与刻度线相切
加水加少了
加水加多了
6. 摇匀
将容量瓶盖好塞子,如图所示,把容量瓶倒转和摇动多
次,使得溶液混合均匀。
思考:摇匀后发现液面低于刻线,能否补充水?
7. 装瓶
标签的书写
如何书写
1、定义:
若1L溶液里含溶质B的物质的量为n mol,则溶质B的物质的量浓度为n mol·L-1。
符号:CB 单位:mol·L-1
物质的量浓度
注意:体积是溶液的,溶质用物质的量。
2、数学表达式:
1、用5mol NaOH配成500mL溶液,其物质的量浓度为
_____mol·L-1,取5mL该溶液,其物质的量浓度为___
mol·L-1。
10
10
2、2 L 1 mol·L-1 的H2SO4溶液,含溶质的物质的量
为 ,含H+ 个。
2 mol
4×6.02×1023
含H+的物质的量为 ,
含H+的物质的量浓度为 。
4mol
2 mol·L-1
3、下列说法正确的是( )
A、将1 mol NaCl溶于1 L水中,所得溶液的物质的量
浓度为1 mol·L-1 B、将2 mol KCl溶于适量水中,配成1L溶液, 所得溶液的物质的量浓度为2 mol·L-1 C、在500 mL 5 mol·L-1 Na2CO3溶液中,Na+的物质
的量浓度为5mol·L-1
D、1 mol·L-1 NaOH溶液中,Na+的物质的量浓度为
1 mol·L-1
BD
4、下列说法正确的是:( )
A、将1molNaCl溶于1L水中,所得溶液的物质的量浓度为1 mol·L-1。 B、将2 molKCl溶于适量水中,配成1L溶液,所得溶液的物质的量浓度为2 mol·L-1。 C、在500mL 5mol·L-1 Na2CO3溶液中取出100 mL,则取出溶液的浓度为1 mol·L-1。 D、将2 mol CuSO4·5H2O溶于适量水中配成2L溶液,所得溶液的物质的量浓度为1 mol·L-1
BD
A
D
5、在相同体积、相同物质的量浓度的溶液中,必然相等
的是( )
A、溶质的物质的量
B、溶质离子的物质的量浓度
C、溶质的质量分数
D、溶质的质量
6、配制500 mL 0.1 mol·L-1硫酸铜溶液,需胆矾( )
A、8.00 g????B、16.0 g????C、25.0 g???D、12.5 g
7、某同学配制NaOH溶液,下列操作对所配溶液浓度有何影响?
偏小
无影响
偏大
偏小
偏小
偏大
偏小
操作实情 物质的量浓度的变化
称量前天平未调零点,指针偏左
物体砝码放颠倒
容量瓶洗涤后未干燥
定容时眼睛俯视的刻度线
液体未冷却到室温就加水定容
烧杯和玻璃棒未洗涤
摇匀后发现凹液面的最低点
低于刻度线,再加水至刻度线
课堂总结
×V液(L)
÷V液(L)
÷22.4L/mol
×22.4L/mol
物质的质量m (g)
物质的量
n (mol)
微粒数N(个)
÷M(g/mol)
×M(g/mol)
×NA
÷NA
标况下气体体积V (L)
溶液的物质的量浓度CB(mol/L)
溶解、冷却
转移
定容
颠倒、摇匀
洗涤、转移
计算、称量
第1章 认识化学科学
第3节 化学中常用的物理量——物质的量
第3课时 物质的量浓度溶液的配制
1、都是高锰酸钾溶液,为什么颜色不同呢?
讨论:
2、怎样表示溶液的浓度?
3、如何配制含0。04molNaCI,体积为0.1L的溶液?
配制0.1L NaCl溶液,其中溶质的物质的量为 0.04 mol.
目的
操作
步骤
合适的仪器
活动˙探究
方法导引
怎样取 0.04 mol NaCl?
怎样实现最后溶液为 0.1 L?
1、特点:容量瓶上标有温度、容积、刻度线。
2、常用规格:100mL、250 mL、500mL、1000mL。
认识容量瓶
1、使用前先检查是否漏液。
2、用蒸馏水清洗,不干燥不影响实验。
3、仅作配制一定体积、浓度准确的溶液,不能用于量取、贮存、溶解、反应。
容量瓶的使用
配制100mL含NaCl 0.04 mol的溶液。
计算
m(NaCl) =0.04mol×58.5g/mol=2.34g
2、称量(用托盘天平称取固体溶质的质量或用量筒量取液体溶质的体积)
思考:1、称量时能将NaCl固体直接放置于托盘上吗?
2、NaOH等具腐蚀性的药品怎样称量?
3、能准确称取2.34gNaCl吗?
3、溶解:将溶质倒入小烧杯,加入适量的水搅拌溶解,冷却致室温.
思考: 1、玻璃棒起什么作用?
2、某同学为了加快溶解速度,溶解时所加的水为150mL,你认为可以吗?
3、若量取的是浓硫酸需要稀释,应如何操
作才是正确的?
4. 转移
思考:1、为避免液体洒在外面,应怎样操作?。
2、将烧杯中的氯化钠溶液转移到容量瓶中,此时溶质是否完全被转移到容量瓶中?应如何处理?
5.定容
向容量瓶中加入蒸馏水,在距离刻度1~2cm时,
改用胶头滴管滴加蒸馏水至刻度线。
思考:
若定容时不小心液面超过了刻度线,怎么办?
注意:液体凹液面最低处与刻度线相切
加水加少了
加水加多了
6. 摇匀
将容量瓶盖好塞子,如图所示,把容量瓶倒转和摇动多
次,使得溶液混合均匀。
思考:摇匀后发现液面低于刻线,能否补充水?
7. 装瓶
标签的书写
如何书写
1、定义:
若1L溶液里含溶质B的物质的量为n mol,则溶质B的物质的量浓度为n mol·L-1。
符号:CB 单位:mol·L-1
物质的量浓度
注意:体积是溶液的,溶质用物质的量。
2、数学表达式:
1、用5mol NaOH配成500mL溶液,其物质的量浓度为
_____mol·L-1,取5mL该溶液,其物质的量浓度为___
mol·L-1。
10
10
2、2 L 1 mol·L-1 的H2SO4溶液,含溶质的物质的量
为 ,含H+ 个。
2 mol
4×6.02×1023
含H+的物质的量为 ,
含H+的物质的量浓度为 。
4mol
2 mol·L-1
3、下列说法正确的是( )
A、将1 mol NaCl溶于1 L水中,所得溶液的物质的量
浓度为1 mol·L-1 B、将2 mol KCl溶于适量水中,配成1L溶液, 所得溶液的物质的量浓度为2 mol·L-1 C、在500 mL 5 mol·L-1 Na2CO3溶液中,Na+的物质
的量浓度为5mol·L-1
D、1 mol·L-1 NaOH溶液中,Na+的物质的量浓度为
1 mol·L-1
BD
4、下列说法正确的是:( )
A、将1molNaCl溶于1L水中,所得溶液的物质的量浓度为1 mol·L-1。 B、将2 molKCl溶于适量水中,配成1L溶液,所得溶液的物质的量浓度为2 mol·L-1。 C、在500mL 5mol·L-1 Na2CO3溶液中取出100 mL,则取出溶液的浓度为1 mol·L-1。 D、将2 mol CuSO4·5H2O溶于适量水中配成2L溶液,所得溶液的物质的量浓度为1 mol·L-1
BD
A
D
5、在相同体积、相同物质的量浓度的溶液中,必然相等
的是( )
A、溶质的物质的量
B、溶质离子的物质的量浓度
C、溶质的质量分数
D、溶质的质量
6、配制500 mL 0.1 mol·L-1硫酸铜溶液,需胆矾( )
A、8.00 g????B、16.0 g????C、25.0 g???D、12.5 g
7、某同学配制NaOH溶液,下列操作对所配溶液浓度有何影响?
偏小
无影响
偏大
偏小
偏小
偏大
偏小
操作实情 物质的量浓度的变化
称量前天平未调零点,指针偏左
物体砝码放颠倒
容量瓶洗涤后未干燥
定容时眼睛俯视的刻度线
液体未冷却到室温就加水定容
烧杯和玻璃棒未洗涤
摇匀后发现凹液面的最低点
低于刻度线,再加水至刻度线
课堂总结
×V液(L)
÷V液(L)
÷22.4L/mol
×22.4L/mol
物质的质量m (g)
物质的量
n (mol)
微粒数N(个)
÷M(g/mol)
×M(g/mol)
×NA
÷NA
标况下气体体积V (L)
溶液的物质的量浓度CB(mol/L)
溶解、冷却
转移
定容
颠倒、摇匀
洗涤、转移
计算、称量
