第2章 物质转化与材料利用 检测题(课件25张ppt)
文档属性
| 名称 | 第2章 物质转化与材料利用 检测题(课件25张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-09-22 00:00:00 | ||
图片预览






文档简介
课件25张PPT。第2章检测题(上册) 一、选择题(15×3分=45分)
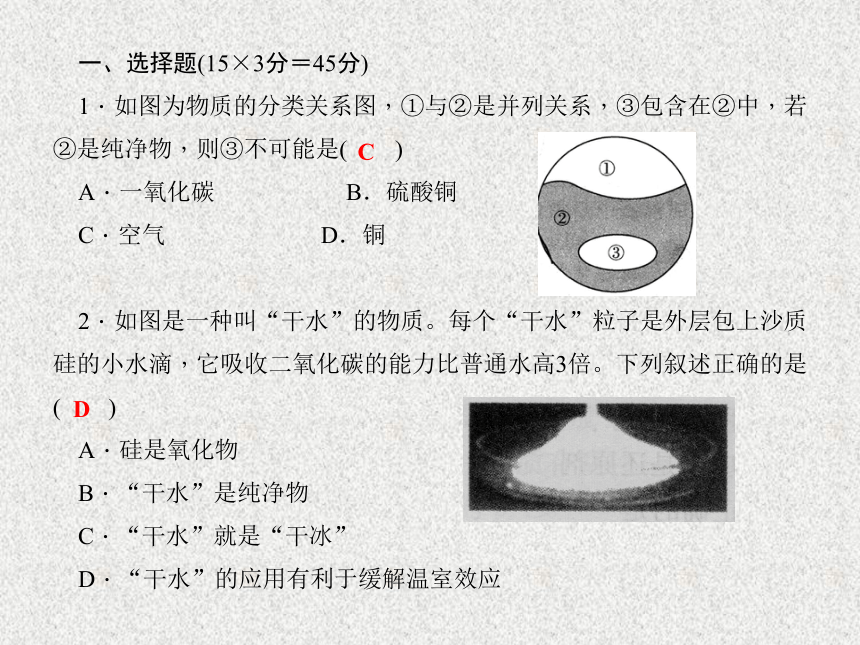
1.如图为物质的分类关系图,①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )
A.一氧化碳 B.硫酸铜
C.空气 D.铜
2.如图是一种叫“干水”的物质。每个“干水”粒子是外层包上沙质硅的小水滴,它吸收二氧化碳的能力比普通水高3倍。下列叙述正确的是( )
A.硅是氧化物
B.“干水”是纯净物
C.“干水”就是“干冰”
D.“干水”的应用有利于缓解温室效应CD3.材料与人类的生活密切相关,下列物品中是由有机合成材料制成的是( )
4.鉴别下列各组物质,所用试剂或方法不正确的是( )
A.待鉴定的物质:稀盐酸和稀硫酸 鉴定试剂:BaCl2溶液
B.待鉴定的物质:硝酸铵固体和氢氧化钠固体 鉴定试剂:水
C.待鉴定的物质:氯化钠溶液和碳酸钠溶液 鉴定试剂:酚酞试液
D.待鉴定的物质:氧气、二氧化碳、氮气 鉴定方法:燃着的木条BD5.下列各组物质能按箭头方向能一步实现转化的是( )
A.NaOH―→NaNO3―→Na2SO4 B.CaO―→CaCl2―→CaCO3
C.CO―→Na2CO3―→CaCO3―→CO2 D.Fe―→Fe2O3―→FeSO4―→FeBC7.下列说法不正确的是( )
A.铁有良好的导热性,常用来制作炊具 B.对废旧电池中汞的回收可减少对环境的污染
C.铜的化学性质不活泼,在潮湿的空气中不会生锈 D.铝表面易形成致密的氧化膜,可阻止铝进一步被氧化
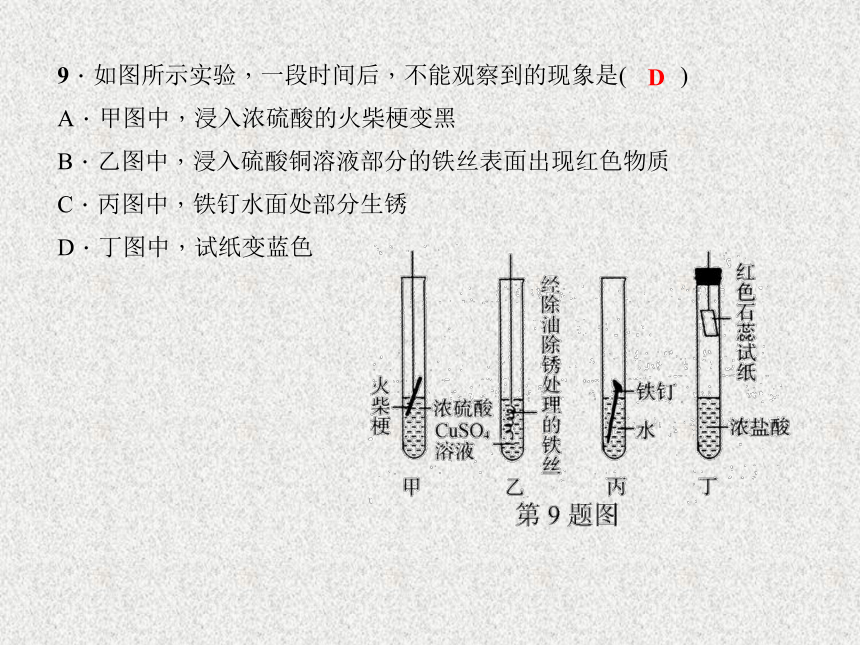
8.区分下列各组物质的两种方法均正确的是( )CD9.如图所示实验,一段时间后,不能观察到的现象是( )
A.甲图中,浸入浓硫酸的火柴梗变黑
B.乙图中,浸入硫酸铜溶液部分的铁丝表面出现红色物质
C.丙图中,铁钉水面处部分生锈
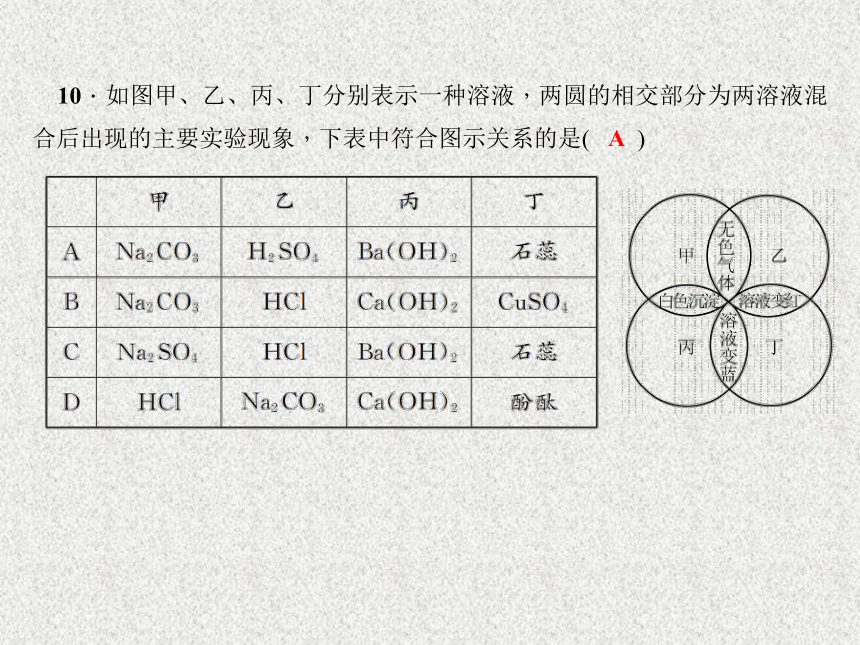
D.丁图中,试纸变蓝色D10.如图甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,下表中符合图示关系的是( )AC12.有等质量的镁和铁,前者放入质量分数为10%的稀硫酸中,后者放入质量分数为10%的稀盐酸中,产生氢气的质量随时间变化曲线如图所示。下列说法错误的是( )
A.镁和铁中至少有一种剩余 B.消耗的稀硫酸和盐酸质量相等
C.消耗铁的质量一定大于消耗镁的质量 D.产生氢气的质量相等B13.为提纯下列物质,所选用的除杂试剂和分离方法都正确的是( )A14.向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液。反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法不正确的是( )
A.图中Oa段表示生成气体的过程 B.b点溶液中溶质有两种
C.c点溶液的pH>7 D.x值为106.0B15.图中“——”表示相应的物质间能发生反应,“―→”表示这种物质可转化为另一种物质,则下列各物质符合对应转化关系的是( )A二、填空题(每空2分,共48分)
16.化学就在我们身边。
(1)婴儿配方奶粉中含有蛋白质、糖类、钙、铁、硒等营养成分,这里的钙、铁、硒是指_ _(填“元素”“单质”或“化合物”)。
(2)用下列材料的对应字母填空。
A.金属材料 B.天然有机高分子材料 C.合成材料
①棉花、羊毛属于_ _。
②可用于制造人造骨、航天飞机等的钛合金属于_ _。元素BA17.金属在生产、生活中应用广泛。
(1)最初输水管材用铸铁,目前多用塑料管和塑料金属复合管,输送热水一般用铜管。下列管材中,属于金属材料的是_ _。(填字母,可多选)
(2)铁生锈的条件是_ _。
(3)金属的回收和利用是保护金属资源的一条有效途径。A、B②将铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后,对剩余固体成分的判断正确的是_ _。(可多选)
A.肯定有银 B.肯定有铜 C.可能有铁 D.可能是铁和银有水和氧气A、C18.某兴趣小组用NaCl溶液、NaOH溶液和稀H2SO4三种试剂,将含有Cu2+、Ba2+、Ag+和NO3-混合液中的三种阳离子逐一除去。步骤如下(所加试剂均过量):
步骤一:混合液中加入试剂A,过滤得到沉淀1和滤液1;
步骤二:滤液1中加入试剂B,过滤得到沉淀2和滤液2;
步骤三:滤液2中加入试剂C,过滤得到沉淀3和滤液3。
(1)同学们确认试剂A是NaCl溶液,写出步骤一中反应的化学方程式:__________________________________。
(2)三种沉淀中,能溶于稀盐酸的是________。
(3)滤液3中,除NaNO3外还含有的盐是_ _。NaCl+AgNO3===AgCl↓+NaNO3Cu(OH)2NaCl、Na2SO419.工业上以大理石和赤铁矿为主要原料制取B和G,其转化关系如图所示,已知D、G为单质。回答下列问题。
(1)写出以上工业制取两种物质的化学式:
B_ _,G_ _。CaOFe(1)用滴入浓硫酸方法制取CO,应选_ _(填序号)装置;如果要除去CO中混有的少量甲酸气体,最好选择上图中的_ _(填序号)进行洗气。
(2)用上述方法制取的CO还原氧化铁,并检验气体产生,则各仪器的接口按气流方向的连接顺序为:_ _。
(3)在对氧化铁粉末加热前,为安全起见,应进行的一项重要操作是_________________________________________。
(4)上述实验后的尾气不能直接排放到空气中,请你说出一种处理尾气的方法:_____________________________。②③B接D、C接G(或H)、H(或G)接F加热前先通CO排出装置中的空气将尾气点燃(或用集气瓶收集)21.氢气还原氧化铜生成红色固体,这些红色固体是什么物质,某科学兴趣小组查阅资料得知,反应温度不同,氢气还原氧化铜的产物可能是Cu或Cu2O,Cu和Cu2O均为不溶于水的红色固体,但Cu2O能与稀硫酸反应,化学方程式为:Cu2O+H2SO4===CuSO4+Cu+H2O。
为探究反应后的红色固体中含有什么物质,他们提出了以下假设:
假设一:红色固体只有Cu 假设二:红色固体只有Cu2O 假设三:红色固体只有Cu和Cu2O
请回答有关问题。
(1)取少量红色固体,加入足量的稀硫酸。若无明显现象,则假设_ _成立;若看到溶液变成蓝色且仍有红色固体,则能否支持假设三?_ _(填“能”或“不能”)。
(2)现将3克红色固体加入足量的稀硫酸中,再将反应后的溶液过滤,称得烘干后的滤渣质量为1.4克。则原红色固体中含有什么物质?_ _。一不能Cu和Cu2O22.氯化钠是日常生活的必需品,也是重要的化工原料。粗盐中除含NaCl外,还含少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。
提供的试剂:Na2CO3溶液、K2CO3、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
(1)欲除去溶液Ⅰ中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按正确滴加顺序依次为:过量的NaOH溶液、_ _、______________________。
(2)在滤液中加盐酸的作用是_ _。过量BaCl2溶液过量Na2CO3溶液(不能对调)除去过量的NaOH和Na2CO3三、实验探究题(12分+15分=27分)
23.工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中常含有杂质碳酸钠,某科学学习小组同学围绕工业烧碱样品纯度测定问题,展开了讨论与探究。
利用Na2CO3与稀H2SO4反应产生CO2通过CO2质量的测定,确定样品中碳酸钠的质量,从而计算样品的纯度。
(1)小科同学根据以上思路,设计了如图甲的实验方案(固定装置省略),图中仪器A的名称是_________。锥形瓶(2)小明认为图甲实验方案的设计有缺陷,若按该方案进行测定会导致难以避免的误差,如装置内空气中的CO2没有排出,反应产生的CO2未被完全吸收等。为减小误差,使CO2质量的测定更准确,该小组同学根据以上讨论,对图甲方案进行改进,设计了如图乙的实验方案(固定装置省略)。图乙B装置中样品在与稀硫酸反应前和停止反应后,都通过过量的空气,反应前通空气时a、b、c三个弹簧夹开闭情况是________________。关闭c、打开a、b(3)若撤去图乙中的C装置,则测得工业烧碱的纯度将_ _(填“偏高”“偏低”或“无影响”)。
(4)已知:碳酸钠溶液与稀硫酸反应先生成碳酸氢钠,当碳酸钠全部转变为碳酸氢钠后,生成的碳酸氢钠能继续与稀硫酸反应生成二氧化碳。现向纯碱样品中加一定量的稀硫酸,反应后产生无色气体并得到X溶液。请分析推断反应后所得X溶液的溶质,其所有的可能组成为______________________________________________。偏低Na2SO4和H2SO4;Na2SO4;Na2SO4和NaHCO324.用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计了以下实验装置,准确称取15克干燥样品进行实验。
(1)在实验中,乙装置的作用是_____________________________。检验氢气中的水分是否全部被吸收(2)准确称取完全反应前后装置丙和丁的质量如上表:
小明根据装置丙减少的质量就是氧元素质量,求得氧化铜质量为11.5克,纯度为76.7%。小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度(写出计算过程)。
(3)比较两种计算结果,请分析导致这一结果的原因可能是__。
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.空气中的二氧化碳被丁处浓硫酸吸收80%B
1.如图为物质的分类关系图,①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )
A.一氧化碳 B.硫酸铜
C.空气 D.铜
2.如图是一种叫“干水”的物质。每个“干水”粒子是外层包上沙质硅的小水滴,它吸收二氧化碳的能力比普通水高3倍。下列叙述正确的是( )
A.硅是氧化物
B.“干水”是纯净物
C.“干水”就是“干冰”
D.“干水”的应用有利于缓解温室效应CD3.材料与人类的生活密切相关,下列物品中是由有机合成材料制成的是( )
4.鉴别下列各组物质,所用试剂或方法不正确的是( )
A.待鉴定的物质:稀盐酸和稀硫酸 鉴定试剂:BaCl2溶液
B.待鉴定的物质:硝酸铵固体和氢氧化钠固体 鉴定试剂:水
C.待鉴定的物质:氯化钠溶液和碳酸钠溶液 鉴定试剂:酚酞试液
D.待鉴定的物质:氧气、二氧化碳、氮气 鉴定方法:燃着的木条BD5.下列各组物质能按箭头方向能一步实现转化的是( )
A.NaOH―→NaNO3―→Na2SO4 B.CaO―→CaCl2―→CaCO3
C.CO―→Na2CO3―→CaCO3―→CO2 D.Fe―→Fe2O3―→FeSO4―→FeBC7.下列说法不正确的是( )
A.铁有良好的导热性,常用来制作炊具 B.对废旧电池中汞的回收可减少对环境的污染
C.铜的化学性质不活泼,在潮湿的空气中不会生锈 D.铝表面易形成致密的氧化膜,可阻止铝进一步被氧化
8.区分下列各组物质的两种方法均正确的是( )CD9.如图所示实验,一段时间后,不能观察到的现象是( )
A.甲图中,浸入浓硫酸的火柴梗变黑
B.乙图中,浸入硫酸铜溶液部分的铁丝表面出现红色物质
C.丙图中,铁钉水面处部分生锈
D.丁图中,试纸变蓝色D10.如图甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,下表中符合图示关系的是( )AC12.有等质量的镁和铁,前者放入质量分数为10%的稀硫酸中,后者放入质量分数为10%的稀盐酸中,产生氢气的质量随时间变化曲线如图所示。下列说法错误的是( )
A.镁和铁中至少有一种剩余 B.消耗的稀硫酸和盐酸质量相等
C.消耗铁的质量一定大于消耗镁的质量 D.产生氢气的质量相等B13.为提纯下列物质,所选用的除杂试剂和分离方法都正确的是( )A14.向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.0%的Na2CO3溶液。反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法不正确的是( )
A.图中Oa段表示生成气体的过程 B.b点溶液中溶质有两种
C.c点溶液的pH>7 D.x值为106.0B15.图中“——”表示相应的物质间能发生反应,“―→”表示这种物质可转化为另一种物质,则下列各物质符合对应转化关系的是( )A二、填空题(每空2分,共48分)
16.化学就在我们身边。
(1)婴儿配方奶粉中含有蛋白质、糖类、钙、铁、硒等营养成分,这里的钙、铁、硒是指_ _(填“元素”“单质”或“化合物”)。
(2)用下列材料的对应字母填空。
A.金属材料 B.天然有机高分子材料 C.合成材料
①棉花、羊毛属于_ _。
②可用于制造人造骨、航天飞机等的钛合金属于_ _。元素BA17.金属在生产、生活中应用广泛。
(1)最初输水管材用铸铁,目前多用塑料管和塑料金属复合管,输送热水一般用铜管。下列管材中,属于金属材料的是_ _。(填字母,可多选)
(2)铁生锈的条件是_ _。
(3)金属的回收和利用是保护金属资源的一条有效途径。A、B②将铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后,对剩余固体成分的判断正确的是_ _。(可多选)
A.肯定有银 B.肯定有铜 C.可能有铁 D.可能是铁和银有水和氧气A、C18.某兴趣小组用NaCl溶液、NaOH溶液和稀H2SO4三种试剂,将含有Cu2+、Ba2+、Ag+和NO3-混合液中的三种阳离子逐一除去。步骤如下(所加试剂均过量):
步骤一:混合液中加入试剂A,过滤得到沉淀1和滤液1;
步骤二:滤液1中加入试剂B,过滤得到沉淀2和滤液2;
步骤三:滤液2中加入试剂C,过滤得到沉淀3和滤液3。
(1)同学们确认试剂A是NaCl溶液,写出步骤一中反应的化学方程式:__________________________________。
(2)三种沉淀中,能溶于稀盐酸的是________。
(3)滤液3中,除NaNO3外还含有的盐是_ _。NaCl+AgNO3===AgCl↓+NaNO3Cu(OH)2NaCl、Na2SO419.工业上以大理石和赤铁矿为主要原料制取B和G,其转化关系如图所示,已知D、G为单质。回答下列问题。
(1)写出以上工业制取两种物质的化学式:
B_ _,G_ _。CaOFe(1)用滴入浓硫酸方法制取CO,应选_ _(填序号)装置;如果要除去CO中混有的少量甲酸气体,最好选择上图中的_ _(填序号)进行洗气。
(2)用上述方法制取的CO还原氧化铁,并检验气体产生,则各仪器的接口按气流方向的连接顺序为:_ _。
(3)在对氧化铁粉末加热前,为安全起见,应进行的一项重要操作是_________________________________________。
(4)上述实验后的尾气不能直接排放到空气中,请你说出一种处理尾气的方法:_____________________________。②③B接D、C接G(或H)、H(或G)接F加热前先通CO排出装置中的空气将尾气点燃(或用集气瓶收集)21.氢气还原氧化铜生成红色固体,这些红色固体是什么物质,某科学兴趣小组查阅资料得知,反应温度不同,氢气还原氧化铜的产物可能是Cu或Cu2O,Cu和Cu2O均为不溶于水的红色固体,但Cu2O能与稀硫酸反应,化学方程式为:Cu2O+H2SO4===CuSO4+Cu+H2O。
为探究反应后的红色固体中含有什么物质,他们提出了以下假设:
假设一:红色固体只有Cu 假设二:红色固体只有Cu2O 假设三:红色固体只有Cu和Cu2O
请回答有关问题。
(1)取少量红色固体,加入足量的稀硫酸。若无明显现象,则假设_ _成立;若看到溶液变成蓝色且仍有红色固体,则能否支持假设三?_ _(填“能”或“不能”)。
(2)现将3克红色固体加入足量的稀硫酸中,再将反应后的溶液过滤,称得烘干后的滤渣质量为1.4克。则原红色固体中含有什么物质?_ _。一不能Cu和Cu2O22.氯化钠是日常生活的必需品,也是重要的化工原料。粗盐中除含NaCl外,还含少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。
提供的试剂:Na2CO3溶液、K2CO3、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
(1)欲除去溶液Ⅰ中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按正确滴加顺序依次为:过量的NaOH溶液、_ _、______________________。
(2)在滤液中加盐酸的作用是_ _。过量BaCl2溶液过量Na2CO3溶液(不能对调)除去过量的NaOH和Na2CO3三、实验探究题(12分+15分=27分)
23.工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中常含有杂质碳酸钠,某科学学习小组同学围绕工业烧碱样品纯度测定问题,展开了讨论与探究。
利用Na2CO3与稀H2SO4反应产生CO2通过CO2质量的测定,确定样品中碳酸钠的质量,从而计算样品的纯度。
(1)小科同学根据以上思路,设计了如图甲的实验方案(固定装置省略),图中仪器A的名称是_________。锥形瓶(2)小明认为图甲实验方案的设计有缺陷,若按该方案进行测定会导致难以避免的误差,如装置内空气中的CO2没有排出,反应产生的CO2未被完全吸收等。为减小误差,使CO2质量的测定更准确,该小组同学根据以上讨论,对图甲方案进行改进,设计了如图乙的实验方案(固定装置省略)。图乙B装置中样品在与稀硫酸反应前和停止反应后,都通过过量的空气,反应前通空气时a、b、c三个弹簧夹开闭情况是________________。关闭c、打开a、b(3)若撤去图乙中的C装置,则测得工业烧碱的纯度将_ _(填“偏高”“偏低”或“无影响”)。
(4)已知:碳酸钠溶液与稀硫酸反应先生成碳酸氢钠,当碳酸钠全部转变为碳酸氢钠后,生成的碳酸氢钠能继续与稀硫酸反应生成二氧化碳。现向纯碱样品中加一定量的稀硫酸,反应后产生无色气体并得到X溶液。请分析推断反应后所得X溶液的溶质,其所有的可能组成为______________________________________________。偏低Na2SO4和H2SO4;Na2SO4;Na2SO4和NaHCO324.用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计了以下实验装置,准确称取15克干燥样品进行实验。
(1)在实验中,乙装置的作用是_____________________________。检验氢气中的水分是否全部被吸收(2)准确称取完全反应前后装置丙和丁的质量如上表:
小明根据装置丙减少的质量就是氧元素质量,求得氧化铜质量为11.5克,纯度为76.7%。小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度(写出计算过程)。
(3)比较两种计算结果,请分析导致这一结果的原因可能是__。
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.空气中的二氧化碳被丁处浓硫酸吸收80%B
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
