人教版高中化学必修一第三章第二节几种重要的金属化合物 课件(共27张PPT)
文档属性
| 名称 | 人教版高中化学必修一第三章第二节几种重要的金属化合物 课件(共27张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 575.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-10-02 00:00:00 | ||
图片预览







文档简介
课件27张PPT。第二节几种重要的金属化合物
镁、铝及其化合物一、镁、铝的性质1、铝的化
学性质与非金属单质的反应:O2、Cl2、S与酸反应:铝热反应:与碱反应:非氧化性酸:氧化性酸:冷浓H2SO4、
浓HNO3钝化思考:镁的化学性质与铝有何异同?焊接铁轨冶炼难熔金属与酸反应:非氧化性酸:氧化性酸:浓H2SO4、
HNO3 不产生氢气 2、镁的化
学性质与非金属单质的反应在:O2、Cl2、N2与盐反应:CuSO4溶液、浓NH4Cl溶液 与CO2反应:DA2、将某份铁铝合金样品均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,同温同压下产生的气体体积比为3∶2,则样品中铁、铝物质的量之比为( )
A. 3∶2 B. 2∶1 C. 3∶4 D. 4∶3C3.将铝粉与Fe3O4粉末配制成铝热剂,分成三等份。
①一份直接放入足量的烧碱溶液中,充分反应后放
出气体在标准状况下的体积为V1;②一份在高温下
恰好反应完全,反应后的混合物与足量的盐酸反应后,
放出的气体在标准状况下的体积为V2;③一份直接放
入足量的盐酸中,充分反应后放出气体在标准状况下的
体积为V3。下列说法正确的是( )
A.V1=V3>V2 B.V2>V1=V3
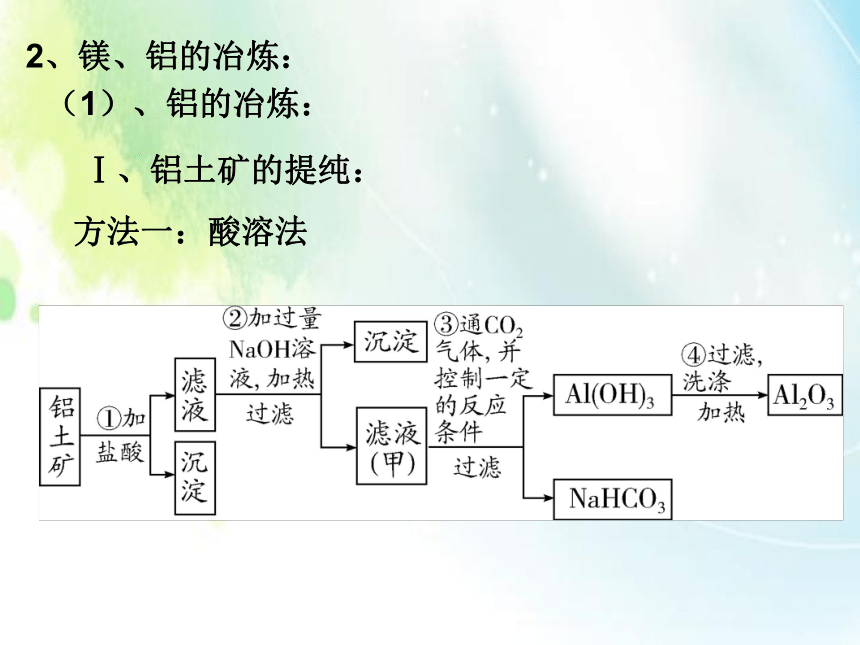
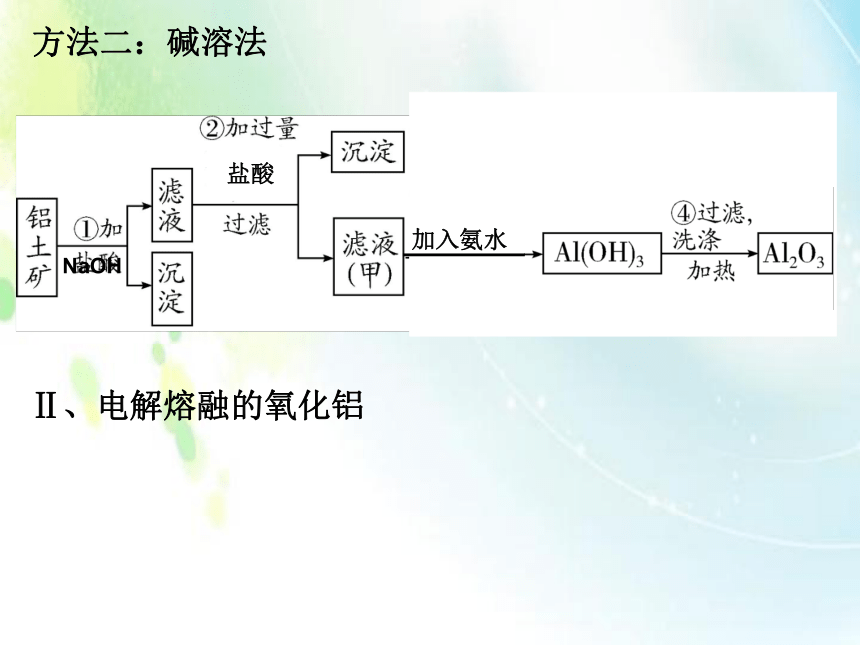
C.V1=V2>V3 D.V1>V3>V2A2、镁、铝的冶炼:Ⅰ、铝土矿的提纯:方法一:酸溶法(1)、铝的冶炼:方法二:碱溶法Ⅱ、电解熔融的氧化铝煅
烧水过
滤盐酸蒸发
结晶干
燥电解(2)、镁的冶炼:Ⅰ 、海水中提取氯化镁Ⅱ 、电解熔融的氯化镁3、既能与酸反应又能与碱反应的物质(1)、Al、Al2O3、Al(OH)3(2)、弱酸酸式盐(3)、弱酸铵盐A(4)、氨基酸、蛋白质例:下列除去杂质的方法不正确的是( )
A、镁粉中混有少量铝粉:加入过量烧碱溶液充分
反应后,过滤、洗涤、干燥
B、用过量氨水除去Fe3+溶液中的少量Al3+
C、用新制的生石灰,通过加热蒸馏,以除去乙醇
中的少量水
D、 Al(OH)3中混有少量Mg(OH)2:加入足量烧碱
溶液,充分反应,过滤,向滤液中通入过量
CO2后过滤B二、铝及其化合物的转化及相关计算1、铝三角之间的转化2、应用(1)Al(OH)3的制备①铝盐溶液与氨水反应②偏铝盐溶液通CO2③偏铝盐溶液与铝盐溶液(2)鉴别(利用滴加顺序不同,现象不同):① AlCl3溶液中滴加NaOH溶液:现象:先产生白色沉淀,后沉淀逐渐溶解;②NaOH溶液中滴加AlCl3溶液:现象:开始无明显现象,后产生白色沉淀,沉淀不
溶解。(1)AlCl3溶液和NaOH溶液,
(2)NaAlO2溶液和盐酸溶液,
(3)Na2CO3溶液和盐酸,
(4)AgNO3溶液和氨水。例1、下列各组物质,前者逐滴滴加到后者中直至过量,
先出现白色沉淀,后来沉淀又消失的是( )
A. H2SO4滴入NaAlO2溶液中
B. Ba(OH)2溶液滴入Al2(SO4)3溶液中
C. Al2(SO4)3溶液滴入NaOH溶液中
D. 氨水滴入Al2(SO4)3溶液中A(3)、有关Al(OH)3沉淀的计算n【Al(OH)3】=1/3 n(OH-)无白色沉淀n【Al(OH)3】=4 n(Al3+) -n(OH-)CBB三、有关铝及其化合物的反应图像立即产生白色沉淀→
渐多→最多→渐少→
消失立即产生白色沉淀→
渐多→最多→渐少→
消失NaOH溶液中逐滴加入可溶性铝盐溶液至过量盐酸中逐滴加偏铝
酸盐溶液至过量无沉淀出现沉淀 逐渐增多最多沉淀量不变无沉淀出现沉淀 逐渐增多最多沉淀量不变思考:1、向AlCl3、 MgCl2、溶液中逐滴加入NaOH溶液至过量?
写出该过程的化学反应方程式,并画出生成的沉淀随
加入的NaOH的物质的量的图像。2、向HCl、 AlCl3、 MgCl2、溶液中逐滴加入NaOH溶液
至过量?写出该过程的化学反应方程式,并画出生成
的沉淀随加入的NaOH的物质的量的图像。 例 1.在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢
氧化钠溶液至过量,表示氢氧化钠加入量(x)与溶液中
沉淀物的量(y)的关系示意图正确的是 ( ) 例2 .将物质X逐渐加入(或通入)Y溶液中,生成沉淀的量
与加入X的物质的量关系如图所示,符合图示情况的是 例3、某一固体物质可能由NaOH、AlCl3、MgCl2中的几
种组成,将其一定量溶于水,有沉淀产生,在所得
悬浊液中逐滴加入5mol/L的盐酸,下图表示盐酸加
入量与沉淀量的变化关系,图中M点表示已加入的
盐酸体积,则M点的体积是( )
A. 70mL B. 100mL
C. 120mL D. 130mL例4.将一定质量的镁、铜合金加入到稀硝酸中,两者恰好
完全反应,假设反应过程中还原产物全是NO,向所得溶
液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,
测得生成沉淀的质量比原合金的质量增加5.1g,则下列有
关叙述中正确的是( )
A.加入合金的质量不可能为6.4g
B.参加反应的硝酸的物质的量为0.1mol
C.沉淀完全时消耗NaOH溶液的体积为150mL
D.溶解合金时收集到NO气体的体积为2.24LD例5、在标准状况下,进行甲、乙、丙三组实验:三组各
取60mL同浓度盐酸溶液,加入同一种镁铝合金粉末,
产生气体,有关数据列表如下:
则下列说法正确的是( )
A. 甲组和乙组的实验中,盐酸均是过量的
B. 盐酸的物质的量浓度为0.8mol·L-1
C. 合金中镁、铝的物质的量之比为1∶1
D. 丙组中铝的物质的量为0.009molC例6、 下列各组物质,不能按 (“→”表示反应一步完成)关系转化的是 ( )C一、镁、铝的性质1、镁、铝的化学性质2、铝的冶炼:3、既能与酸反应又能与碱反应的物质二、铝及其化合物的转化及相关计算1、铝三角之间的转化2、应用(3)、有关Al(OH)3沉淀的计算三、有关铝及其化合物的反应图像小结
镁、铝及其化合物一、镁、铝的性质1、铝的化
学性质与非金属单质的反应:O2、Cl2、S与酸反应:铝热反应:与碱反应:非氧化性酸:氧化性酸:冷浓H2SO4、
浓HNO3钝化思考:镁的化学性质与铝有何异同?焊接铁轨冶炼难熔金属与酸反应:非氧化性酸:氧化性酸:浓H2SO4、
HNO3 不产生氢气 2、镁的化
学性质与非金属单质的反应在:O2、Cl2、N2与盐反应:CuSO4溶液、浓NH4Cl溶液 与CO2反应:DA2、将某份铁铝合金样品均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,同温同压下产生的气体体积比为3∶2,则样品中铁、铝物质的量之比为( )
A. 3∶2 B. 2∶1 C. 3∶4 D. 4∶3C3.将铝粉与Fe3O4粉末配制成铝热剂,分成三等份。
①一份直接放入足量的烧碱溶液中,充分反应后放
出气体在标准状况下的体积为V1;②一份在高温下
恰好反应完全,反应后的混合物与足量的盐酸反应后,
放出的气体在标准状况下的体积为V2;③一份直接放
入足量的盐酸中,充分反应后放出气体在标准状况下的
体积为V3。下列说法正确的是( )
A.V1=V3>V2 B.V2>V1=V3
C.V1=V2>V3 D.V1>V3>V2A2、镁、铝的冶炼:Ⅰ、铝土矿的提纯:方法一:酸溶法(1)、铝的冶炼:方法二:碱溶法Ⅱ、电解熔融的氧化铝煅
烧水过
滤盐酸蒸发
结晶干
燥电解(2)、镁的冶炼:Ⅰ 、海水中提取氯化镁Ⅱ 、电解熔融的氯化镁3、既能与酸反应又能与碱反应的物质(1)、Al、Al2O3、Al(OH)3(2)、弱酸酸式盐(3)、弱酸铵盐A(4)、氨基酸、蛋白质例:下列除去杂质的方法不正确的是( )
A、镁粉中混有少量铝粉:加入过量烧碱溶液充分
反应后,过滤、洗涤、干燥
B、用过量氨水除去Fe3+溶液中的少量Al3+
C、用新制的生石灰,通过加热蒸馏,以除去乙醇
中的少量水
D、 Al(OH)3中混有少量Mg(OH)2:加入足量烧碱
溶液,充分反应,过滤,向滤液中通入过量
CO2后过滤B二、铝及其化合物的转化及相关计算1、铝三角之间的转化2、应用(1)Al(OH)3的制备①铝盐溶液与氨水反应②偏铝盐溶液通CO2③偏铝盐溶液与铝盐溶液(2)鉴别(利用滴加顺序不同,现象不同):① AlCl3溶液中滴加NaOH溶液:现象:先产生白色沉淀,后沉淀逐渐溶解;②NaOH溶液中滴加AlCl3溶液:现象:开始无明显现象,后产生白色沉淀,沉淀不
溶解。(1)AlCl3溶液和NaOH溶液,
(2)NaAlO2溶液和盐酸溶液,
(3)Na2CO3溶液和盐酸,
(4)AgNO3溶液和氨水。例1、下列各组物质,前者逐滴滴加到后者中直至过量,
先出现白色沉淀,后来沉淀又消失的是( )
A. H2SO4滴入NaAlO2溶液中
B. Ba(OH)2溶液滴入Al2(SO4)3溶液中
C. Al2(SO4)3溶液滴入NaOH溶液中
D. 氨水滴入Al2(SO4)3溶液中A(3)、有关Al(OH)3沉淀的计算n【Al(OH)3】=1/3 n(OH-)无白色沉淀n【Al(OH)3】=4 n(Al3+) -n(OH-)CBB三、有关铝及其化合物的反应图像立即产生白色沉淀→
渐多→最多→渐少→
消失立即产生白色沉淀→
渐多→最多→渐少→
消失NaOH溶液中逐滴加入可溶性铝盐溶液至过量盐酸中逐滴加偏铝
酸盐溶液至过量无沉淀出现沉淀 逐渐增多最多沉淀量不变无沉淀出现沉淀 逐渐增多最多沉淀量不变思考:1、向AlCl3、 MgCl2、溶液中逐滴加入NaOH溶液至过量?
写出该过程的化学反应方程式,并画出生成的沉淀随
加入的NaOH的物质的量的图像。2、向HCl、 AlCl3、 MgCl2、溶液中逐滴加入NaOH溶液
至过量?写出该过程的化学反应方程式,并画出生成
的沉淀随加入的NaOH的物质的量的图像。 例 1.在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢
氧化钠溶液至过量,表示氢氧化钠加入量(x)与溶液中
沉淀物的量(y)的关系示意图正确的是 ( ) 例2 .将物质X逐渐加入(或通入)Y溶液中,生成沉淀的量
与加入X的物质的量关系如图所示,符合图示情况的是 例3、某一固体物质可能由NaOH、AlCl3、MgCl2中的几
种组成,将其一定量溶于水,有沉淀产生,在所得
悬浊液中逐滴加入5mol/L的盐酸,下图表示盐酸加
入量与沉淀量的变化关系,图中M点表示已加入的
盐酸体积,则M点的体积是( )
A. 70mL B. 100mL
C. 120mL D. 130mL例4.将一定质量的镁、铜合金加入到稀硝酸中,两者恰好
完全反应,假设反应过程中还原产物全是NO,向所得溶
液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,
测得生成沉淀的质量比原合金的质量增加5.1g,则下列有
关叙述中正确的是( )
A.加入合金的质量不可能为6.4g
B.参加反应的硝酸的物质的量为0.1mol
C.沉淀完全时消耗NaOH溶液的体积为150mL
D.溶解合金时收集到NO气体的体积为2.24LD例5、在标准状况下,进行甲、乙、丙三组实验:三组各
取60mL同浓度盐酸溶液,加入同一种镁铝合金粉末,
产生气体,有关数据列表如下:
则下列说法正确的是( )
A. 甲组和乙组的实验中,盐酸均是过量的
B. 盐酸的物质的量浓度为0.8mol·L-1
C. 合金中镁、铝的物质的量之比为1∶1
D. 丙组中铝的物质的量为0.009molC例6、 下列各组物质,不能按 (“→”表示反应一步完成)关系转化的是 ( )C一、镁、铝的性质1、镁、铝的化学性质2、铝的冶炼:3、既能与酸反应又能与碱反应的物质二、铝及其化合物的转化及相关计算1、铝三角之间的转化2、应用(3)、有关Al(OH)3沉淀的计算三、有关铝及其化合物的反应图像小结
