鲁教版九年级上册化学 5.3 化学反应中的有关计算 课件(20张PPT)
文档属性
| 名称 | 鲁教版九年级上册化学 5.3 化学反应中的有关计算 课件(20张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-10-05 00:00:00 | ||
图片预览








文档简介
课件20张PPT。 化学反应中的有关计算学习目标:
1、进一步认识化学反应中各物质之间的质量关系,初步学会根据化学方程式进行简单的计算。
2、初步认识定量研究化学反应对于生产和生活的重要意义。
学习重、难点:根据化学方程式进行计算的解题思路和一般步骤。原料产品?反应物生成物 36 4 3218g( ) ( )2g16gxy各物质间恒定的质量比:温故知新(相对原子质量:H-1 O-16)72g64g物质的实际质量比等于相对质量比 氢气是未来汽车的理想燃料。假如1kg氢气能供一辆功率为50kw的汽车跑上100km,那么一桶18kg的水完全分解产生多少kg氢气?可供汽车跑多远?(相对原子质量:H-1 O-16)
宝马H2R
氢动力汽车 (1)由反应物: 的质量求生成物: 的质量,
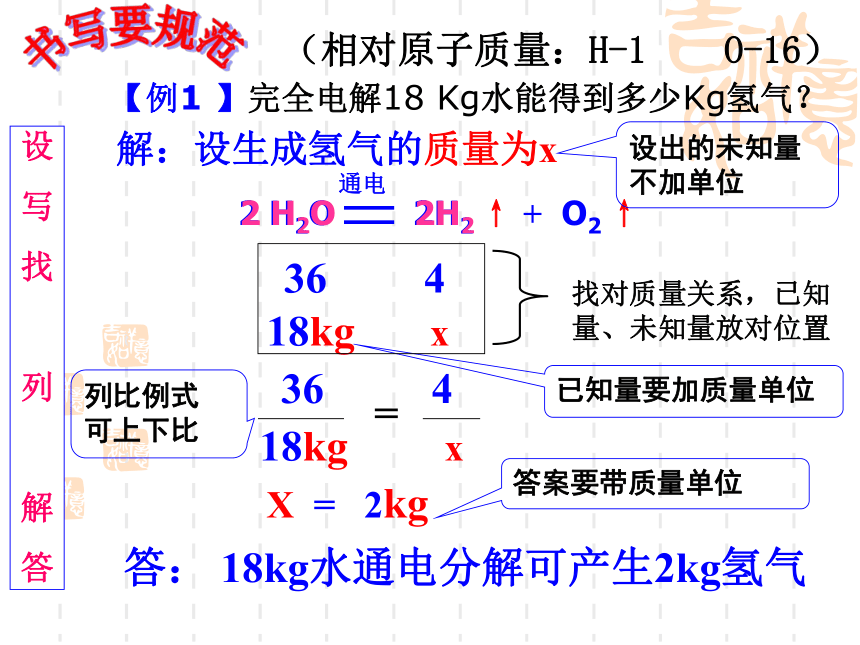
(2)利用反应中纯净物 和 的恒定质量比【例1 】完全电解18 Kg水能得到多少Kg氢气?学会审题水氢气 36 4化学反应中各物质质量比:(系数×相对分子质量)相对原子质量:H-1 O-16【例1 】完全电解18 Kg水能得到多少Kg氢气?解:设生成氢气的质量为x18kg x 36 4X = 2kg答: 18kg水通电分解可产生2kg氢气已知量要加质量单位
设出的未知量不加单位
答案要带质量单位
设
写
找
列
解
答书写要规范(相对原子质量:H-1 O-16)列比例式
可上下比
2 H2O 2H2【例1 】完全电解18 Kg水能得到多少Kg氢气?解:设生成氢气的质量为x18kg x 36 4X = 2kg答: 18kg水通电分解可产生2kg氢气设
写
找
列
解
答书写要规范(相对原子质量:H-1 O-16)2 H2O 2H2(1)确定未知量;(格式:“ 解:设……的质量为x )
(2)再正确写出有关反应的化学方程式(要配平)
(3)计算出相关物质的质量比值
(相对分子质量×化学式前系数),写在化学式正下方;
(4)再把已知量和未知量分别放到对应的化学式下面(已知量要带质量单位,未知量不带单位);
(5)列出比例式;
(6)解出答案要带单位,按要求保留有效数字;
(除不尽通常保留到0.1g)
(7)要写答。步骤细节你能行【例2 】工业上电解氧化铝制取金属铝,反应的化学方程式为:
2Al2O3 4Al+3O2
如果加工一个铝锅需要1.08kg铝,至少需要电解多少kg的氧化铝(Al2O3 )才能制成这个铝锅?通电↑(相对原子质量:Al-27 O-16) 【例2 】课本P111 (Al—27 O—16)解:设需要氧化铝的质量为x x 1.08kg204 108X = 2.04kg答:需要氧化铝的质量为2.04kg设:
写:
找:
列:
解:
答:2 Al2O3 4Al小诊所下面是某同学做的根据化学方程式的计算题,请你会会诊,指出他的错误。题目:计算48g镁带在氧气中完全燃烧,能生成多少克氧化镁?解:设生成氧化镁的质量为xg
Mg+O2 MgO
24 40
48 xg
24 40
48 xg
48×40
X= =80
24
答:生成氧化镁80g。点燃=解:设生成氧化镁的质量为x
2Mg+O2 2MgO
48 80
48 g x
48 80
48g x
48g×80
X= =80 g
48
答:生成氧化镁80g。相对原子质量:Mg-24 O-161、用电解水的方法制取8g氧气,需要消耗水多少克?同时可得到氢气多少克? 解:设需要消耗水的质量为x,生成氢气的质量为y多个未知量 36 4 32 8gxy化学方程式我的果子①方程式要正确:化学式 、配平
②计算要准确:相对分子质量要乘以化学计量数
③除不尽时:按要求保留有效数字
④求多个物质质量时,可在一个方程式中设多个未知数(x、y、z…)
细节决定成功2、 要使8.58 g镁在氧气中完全燃烧,至少需要氧气的
质量为多少?体积为多少升?
(氧气的密度为1.43g/L )
挑战自我实验室需要22.4L氧气做实验,需要多少克过氧化氢完全反应?
(氧气的密度为1.43g/L)小心陷阱解:设需要过氧化氢的质量为X68 32 X22.4L22.4L×1.43g/L3、某学生用36.5g稀盐酸与一定量的水垢(主要成分是碳酸钙)恰好反应,产生了4.4g的CO2气体。求:
⑴ 可生成氯化钙的质量是多少?
⑵这种稀盐酸的溶质质量分数是多少?慧眼识珠CaCO3+2HCl=CaCl2+H2O+CO2↑ 73 44 36.5g 4.4g111√×x y化学方程式的计算表示的是纯物质之间的质量关系,所以代入化学方程式的数据必须是参加反应或生成的纯物质的质量!②遇混合物和溶液,找纯净物的质量
作为计算其他物质的依据。时刻记住祝大家再攀高峰
1、进一步认识化学反应中各物质之间的质量关系,初步学会根据化学方程式进行简单的计算。
2、初步认识定量研究化学反应对于生产和生活的重要意义。
学习重、难点:根据化学方程式进行计算的解题思路和一般步骤。原料产品?反应物生成物 36 4 3218g( ) ( )2g16gxy各物质间恒定的质量比:温故知新(相对原子质量:H-1 O-16)72g64g物质的实际质量比等于相对质量比 氢气是未来汽车的理想燃料。假如1kg氢气能供一辆功率为50kw的汽车跑上100km,那么一桶18kg的水完全分解产生多少kg氢气?可供汽车跑多远?(相对原子质量:H-1 O-16)
宝马H2R
氢动力汽车 (1)由反应物: 的质量求生成物: 的质量,
(2)利用反应中纯净物 和 的恒定质量比【例1 】完全电解18 Kg水能得到多少Kg氢气?学会审题水氢气 36 4化学反应中各物质质量比:(系数×相对分子质量)相对原子质量:H-1 O-16【例1 】完全电解18 Kg水能得到多少Kg氢气?解:设生成氢气的质量为x18kg x 36 4X = 2kg答: 18kg水通电分解可产生2kg氢气已知量要加质量单位
设出的未知量不加单位
答案要带质量单位
设
写
找
列
解
答书写要规范(相对原子质量:H-1 O-16)列比例式
可上下比
2 H2O 2H2【例1 】完全电解18 Kg水能得到多少Kg氢气?解:设生成氢气的质量为x18kg x 36 4X = 2kg答: 18kg水通电分解可产生2kg氢气设
写
找
列
解
答书写要规范(相对原子质量:H-1 O-16)2 H2O 2H2(1)确定未知量;(格式:“ 解:设……的质量为x )
(2)再正确写出有关反应的化学方程式(要配平)
(3)计算出相关物质的质量比值
(相对分子质量×化学式前系数),写在化学式正下方;
(4)再把已知量和未知量分别放到对应的化学式下面(已知量要带质量单位,未知量不带单位);
(5)列出比例式;
(6)解出答案要带单位,按要求保留有效数字;
(除不尽通常保留到0.1g)
(7)要写答。步骤细节你能行【例2 】工业上电解氧化铝制取金属铝,反应的化学方程式为:
2Al2O3 4Al+3O2
如果加工一个铝锅需要1.08kg铝,至少需要电解多少kg的氧化铝(Al2O3 )才能制成这个铝锅?通电↑(相对原子质量:Al-27 O-16) 【例2 】课本P111 (Al—27 O—16)解:设需要氧化铝的质量为x x 1.08kg204 108X = 2.04kg答:需要氧化铝的质量为2.04kg设:
写:
找:
列:
解:
答:2 Al2O3 4Al小诊所下面是某同学做的根据化学方程式的计算题,请你会会诊,指出他的错误。题目:计算48g镁带在氧气中完全燃烧,能生成多少克氧化镁?解:设生成氧化镁的质量为xg
Mg+O2 MgO
24 40
48 xg
24 40
48 xg
48×40
X= =80
24
答:生成氧化镁80g。点燃=解:设生成氧化镁的质量为x
2Mg+O2 2MgO
48 80
48 g x
48 80
48g x
48g×80
X= =80 g
48
答:生成氧化镁80g。相对原子质量:Mg-24 O-161、用电解水的方法制取8g氧气,需要消耗水多少克?同时可得到氢气多少克? 解:设需要消耗水的质量为x,生成氢气的质量为y多个未知量 36 4 32 8gxy化学方程式我的果子①方程式要正确:化学式 、配平
②计算要准确:相对分子质量要乘以化学计量数
③除不尽时:按要求保留有效数字
④求多个物质质量时,可在一个方程式中设多个未知数(x、y、z…)
细节决定成功2、 要使8.58 g镁在氧气中完全燃烧,至少需要氧气的
质量为多少?体积为多少升?
(氧气的密度为1.43g/L )
挑战自我实验室需要22.4L氧气做实验,需要多少克过氧化氢完全反应?
(氧气的密度为1.43g/L)小心陷阱解:设需要过氧化氢的质量为X68 32 X22.4L22.4L×1.43g/L3、某学生用36.5g稀盐酸与一定量的水垢(主要成分是碳酸钙)恰好反应,产生了4.4g的CO2气体。求:
⑴ 可生成氯化钙的质量是多少?
⑵这种稀盐酸的溶质质量分数是多少?慧眼识珠CaCO3+2HCl=CaCl2+H2O+CO2↑ 73 44 36.5g 4.4g111√×x y化学方程式的计算表示的是纯物质之间的质量关系,所以代入化学方程式的数据必须是参加反应或生成的纯物质的质量!②遇混合物和溶液,找纯净物的质量
作为计算其他物质的依据。时刻记住祝大家再攀高峰
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
