第6节 物质的分离 重难点突破(课件 34张ppt)
文档属性
| 名称 | 第6节 物质的分离 重难点突破(课件 34张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 628.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2019-10-11 20:49:14 | ||
图片预览








文档简介
课件34张PPT。第 6 节 物质的分离常 考 透 视第 1 章 水和水的溶液挑 战 自 我常考透视常考1 能区别晶体与非晶体;了解晶体形成的几种方法及原理。第 6 节 物质的分离【考试热度】 ★★★ 例1 下列说法不正确的是( )
A.从溶液中析出晶体的过程叫作结晶
B.溶解和结晶是两个相反的过程
C.蒸发食盐水可获得氯化钠的晶体
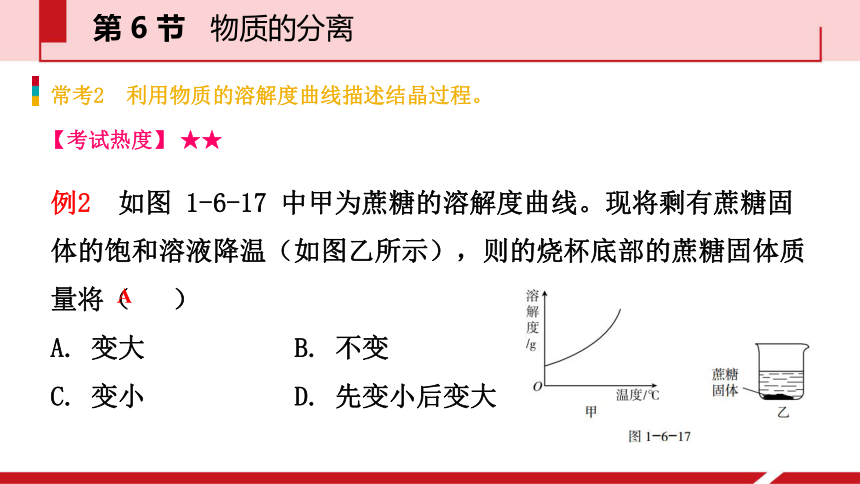
D.冷却热饱和溶液结晶适用于溶解度受温度影响小的物质D解析 结晶是溶液中无法再溶解的固体物质从溶液中析出的过程,溶解和结晶是两个相反的过程,冷却热饱和溶液结晶适用于溶解度受温度影响大的固体物质。第 6 节 物质的分离方法透视 结晶的方法有蒸发溶剂法和冷却热饱和溶液法。 蒸发溶剂法适用于溶解度受温度影响比较小的固体物质, 冷却热饱和溶液法适用于溶解度受温度影响比较大的固体物质。【试题链接】 小试身手 5,创新培优 8第 6 节 物质的分离常考2 利用物质的溶解度曲线描述结晶过程。【考试热度】 ★★例2 如图 1-6-17 中甲为蔗糖的溶解度曲线。现将剩有蔗糖固体的饱和溶液降温(如图乙所示),则的烧杯底部的蔗糖固体质量将( )
A. 变大 B. 不变
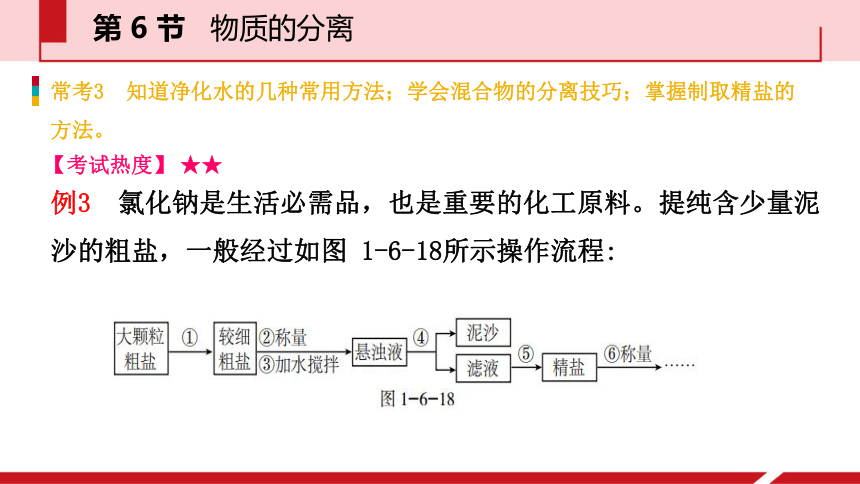
C. 变小 D. 先变小后变大A第 6 节 物质的分离解析 从图甲蔗糖的溶解度曲线可以看出,蔗糖的溶解度随着温度的降低而减小,所以降温后蔗糖饱和溶液有晶体析出,烧杯底部的蔗糖固体质量将变大。第 6 节 物质的分离方法透视 某物质的溶解度曲线可以清楚地表示这种物质的溶解度随温度变化的情况。当温度降低时,若溶质的溶解度变小,则溶液中有固体物质析出。当溶质的溶解度随温度变化比较明显时,适合降温结晶,如硝酸钾;当溶质的溶解度随温度变化不明显时,适合蒸发结晶,如氯化钠。【试题链接】 小试身手 5,创新培优 8第 6 节 物质的分离常考3 知道净化水的几种常用方法;学会混合物的分离技巧;掌握制取精盐的方法。【考试热度】 ★★例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:第 6 节 物质的分离例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:
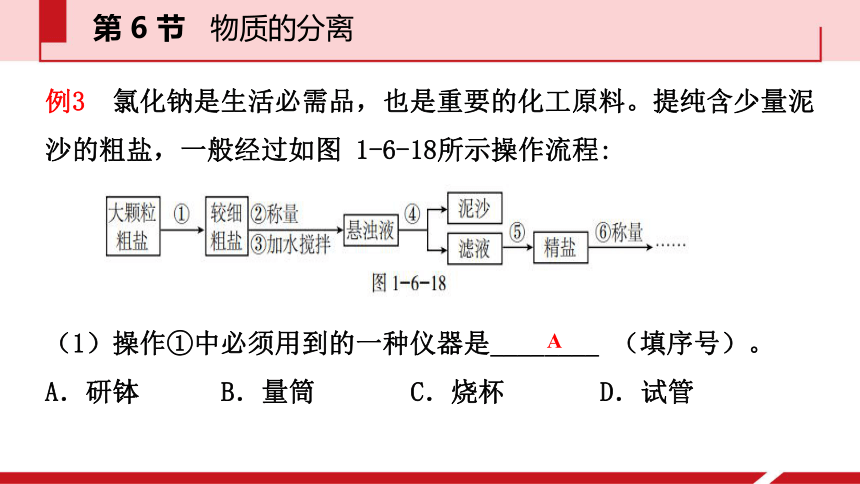
(1)操作①中必须用到的一种仪器是________ (填序号)。
A.研钵 B.量筒 C.烧杯 D.试管A第 6 节 物质的分离解析 量筒用来量取液体的体积,烧杯用来作大量液体的反应容器,试管用作少量试剂的反应容器,也可以加热少量液体,研钵用于研磨硬度不太大的固体物质。第 6 节 物质的分离例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:
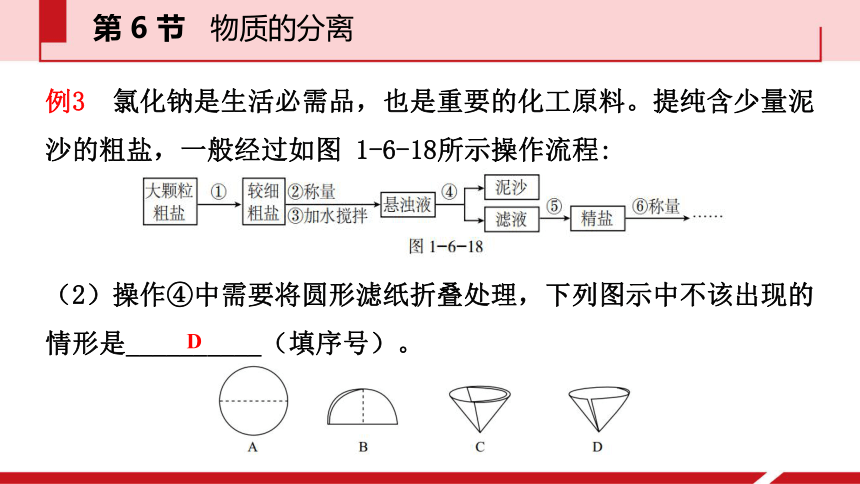
(2)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是__________(填序号)。D第 6 节 物质的分离解析 A、 B、 C 是滤纸正确的折叠方法, D 中的滤纸,接口处有缝隙,若用于过滤,液体会直接进入下面的烧杯,起不到过滤作用。第 6 节 物质的分离例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:
(3)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到__________ 等仪器。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,还可采取_______________ 等措施。蒸发皿 来回移动酒精灯第 6 节 物质的分离解析 进行蒸发操作时,除了所给的仪器,还需要盛放液体的加热装置,即蒸发皿。为了使液体受热更均匀可来回移动酒精灯。第 6 节 物质的分离例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:
(4)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到 等仪器。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,还可采取___________ 等措施。ABD第 6 节 物质的分离解析 精盐的产率低,说明在提纯时,损失了精盐。粗盐没有完全溶解就过滤,会导致最终得到的精盐的质量减少;食盐飞溅导致精盐的质量减少;精盐很潮湿会使所称量的精盐的质量偏大,使制得率偏高;蒸发皿中的精盐没有全部转移到称量纸上,会使精盐的质量减少。第 6 节 物质的分离方法透视 粗盐提纯的步骤: 溶解、 过滤、 蒸发。注意在粗盐的提纯过程中玻璃棒的作用,另外要明确过滤操作的要点: 一贴、 二低、 三靠。【试题链接】 小试身手 2、3、4、6,创新培优 7、9第 6 节 物质的分离挑战自我小试身手1. 如 图 1-6-19 所 示 是a、 b、 c 三种固体物质的溶解度随温度变化的曲线。下列说法中正确的是( )
A. a 的溶解度大于 c的溶解度
B. 在 t1℃时, a、 c 两种物质的饱和溶液
中溶质的质量分数相同
C. c 的不饱和溶液由 t2℃降温至 t1℃时,变成饱和溶液
D. 要从 b 溶液中得到 b,通常可采用冷却热饱和溶液的方法 B第 6 节 物质的分离解析 比较溶解度的大小,需要明确在什么温度下;在t1℃时,a、c两种物质的溶解度相等,所以此温度下两种物质的饱和溶液中溶质的质量分数也相等;c的不饱和溶液由t2℃降温至t1℃时,溶解度增大,所以不可能变成饱和溶液;由于b的溶解度受温度影响不大,所以结晶时最好用蒸发溶剂的方法。第 6 节 物质的分离2. 在进行过滤操作时,除了使用铁架台、烧杯、玻璃棒外,还需要使用的仪器是( )
A. 酒精灯 B. 托盘天平
C. 蒸发皿 D. 漏斗D第 6 节 物质的分离3. 在粗盐提纯的实验中,下列操作正确的是( )B第 6 节 物质的分离解析 托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了;粗盐溶解时,为加快溶解速率,可用玻璃棒搅拌;过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流;蒸发时,应用玻璃棒不断搅拌,以防液体因受热不均匀而飞溅。第 6 节 物质的分离4. [台州中考]科学家用石墨烯膜制成“筛子”,可以筛掉盐类物质。当海水流过该膜时,钠离子和氯离子被水分子包裹而不能通过,独立的水分子却能通过(如图 1-6-20)。下列关于石墨烯膜“筛掉”氯化钠的说法错误的是( )
A.该过程属于物理变化
B.该过程可应用于海水淡化
C.“筛掉”氯化钠的过程类似于过滤操作
D. “筛掉”氯化钠后的海水溶质质量分数增大D第 6 节 物质的分离5.从硝酸钾和氯化钠的饱和溶液中分离出硝酸钾,主要采用的方法是( )
A.溶解过滤 B.过滤
C.蒸发结晶 D.降温结晶D第 6 节 物质的分离6. 从自然界中获得的粗盐,含有较多的杂质,需要精制。为了除去粗盐中泥沙等不溶性杂质设计了如图 1-6-21 的 A、 B、 C 三个步骤。
(1) B 步骤称为____________ 。过滤 第 6 节 物质的分离解析 B步骤为过滤,是将不溶于水的泥沙与食盐水分离的操作。6. 从自然界中获得的粗盐,含有较多的杂质,需要精制。为了除去粗盐中泥沙等不溶性杂质设计了如图 1-6-21 的 A、 B、 C 三个步骤。
(2) C 步骤中,当蒸发皿内出现较多固体时,应该__________ (填字母)。
A.移去酒精灯,停止搅拌
B.移去酒精灯,用玻璃棒继续搅拌
C.继续加热蒸干水分,再移去酒精灯B第 6 节 物质的分离解析 在蒸发操作中,当蒸发皿内出现较多固体时,应移去酒精灯停止加热,用玻璃棒继续搅拌,利用余热把剩余滤液蒸干。第 6 节 物质的分离创新培优7.下列是关于“粗盐提纯”实验的几种说法,其中正确的是( )
A. 为加快过滤速率,应用玻璃棒不断搅拌过滤器内的液体
B. 如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因
C. 蒸发滤液时要用玻璃棒不断搅拌,用酒精灯持续加热直到蒸干为止
D. 为使食盐快速溶解,应用较多的水溶解食盐B 第 6 节 物质的分离解析 过滤时,若搅拌易造成滤纸破损;蒸发时,当有较多量食盐析出时停止加热;溶解时,水量过多会造成过滤和蒸发时间过长。8.小明同学绘制了如图 1-6-22 所示的 A、 B两种固体物质的溶解度随温度变化的曲线。
(1)当温度为_________ ℃时, A 物质与 B 物质的溶解度相等。
(2)若将 B 物质从溶液中结晶析出,宜
采用的方法是______________________ 。
40
蒸发结晶第 6 节 物质的分离8.小明同学绘制了如图 1-6-22 所示的 A、 B两种固体物质的溶解度随温度变化的曲线。
(3)我国有许多盐碱湖,湖中溶有大量的氯化钠和碳酸钠,那里的人们“冬天捞碱,夏天晒盐”。据此你认为
________________(填“A”或“B”)物质的溶
解度曲线与纯碱的相似。A第 6 节 物质的分离解析 B物质的溶解度受温度变化的影响较小,可采用蒸发溶剂的方法获得晶体;“冬天捞碱”说明碳酸钠的溶解度受温度变化的影响较大,图中A物质的溶解度曲线与碳酸钠的溶解度曲线相似。第 6 节 物质的分离9.25 ℃时,将 10 g 某盐加入一定量的水中,完 全 溶 解 后, 得 到 不 饱 和 溶 液, 若 蒸 发12.5 g 水后得到溶质质量分数为 20 % 的饱和溶液。
请计算:
(1)25 ℃时,该盐的溶解度。
(2)原不饱和溶液的溶质质量分数。
(3)25 ℃时,若要使 5 g 该盐从饱和溶液中析出来,需蒸发多少克水?
第 6 节 物质的分离第 6 节 物质的分离
A.从溶液中析出晶体的过程叫作结晶
B.溶解和结晶是两个相反的过程
C.蒸发食盐水可获得氯化钠的晶体
D.冷却热饱和溶液结晶适用于溶解度受温度影响小的物质D解析 结晶是溶液中无法再溶解的固体物质从溶液中析出的过程,溶解和结晶是两个相反的过程,冷却热饱和溶液结晶适用于溶解度受温度影响大的固体物质。第 6 节 物质的分离方法透视 结晶的方法有蒸发溶剂法和冷却热饱和溶液法。 蒸发溶剂法适用于溶解度受温度影响比较小的固体物质, 冷却热饱和溶液法适用于溶解度受温度影响比较大的固体物质。【试题链接】 小试身手 5,创新培优 8第 6 节 物质的分离常考2 利用物质的溶解度曲线描述结晶过程。【考试热度】 ★★例2 如图 1-6-17 中甲为蔗糖的溶解度曲线。现将剩有蔗糖固体的饱和溶液降温(如图乙所示),则的烧杯底部的蔗糖固体质量将( )
A. 变大 B. 不变
C. 变小 D. 先变小后变大A第 6 节 物质的分离解析 从图甲蔗糖的溶解度曲线可以看出,蔗糖的溶解度随着温度的降低而减小,所以降温后蔗糖饱和溶液有晶体析出,烧杯底部的蔗糖固体质量将变大。第 6 节 物质的分离方法透视 某物质的溶解度曲线可以清楚地表示这种物质的溶解度随温度变化的情况。当温度降低时,若溶质的溶解度变小,则溶液中有固体物质析出。当溶质的溶解度随温度变化比较明显时,适合降温结晶,如硝酸钾;当溶质的溶解度随温度变化不明显时,适合蒸发结晶,如氯化钠。【试题链接】 小试身手 5,创新培优 8第 6 节 物质的分离常考3 知道净化水的几种常用方法;学会混合物的分离技巧;掌握制取精盐的方法。【考试热度】 ★★例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:第 6 节 物质的分离例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:
(1)操作①中必须用到的一种仪器是________ (填序号)。
A.研钵 B.量筒 C.烧杯 D.试管A第 6 节 物质的分离解析 量筒用来量取液体的体积,烧杯用来作大量液体的反应容器,试管用作少量试剂的反应容器,也可以加热少量液体,研钵用于研磨硬度不太大的固体物质。第 6 节 物质的分离例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:
(2)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是__________(填序号)。D第 6 节 物质的分离解析 A、 B、 C 是滤纸正确的折叠方法, D 中的滤纸,接口处有缝隙,若用于过滤,液体会直接进入下面的烧杯,起不到过滤作用。第 6 节 物质的分离例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:
(3)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到__________ 等仪器。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,还可采取_______________ 等措施。蒸发皿 来回移动酒精灯第 6 节 物质的分离解析 进行蒸发操作时,除了所给的仪器,还需要盛放液体的加热装置,即蒸发皿。为了使液体受热更均匀可来回移动酒精灯。第 6 节 物质的分离例3 氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图 1-6-18所示操作流程:
(4)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到 等仪器。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,还可采取___________ 等措施。ABD第 6 节 物质的分离解析 精盐的产率低,说明在提纯时,损失了精盐。粗盐没有完全溶解就过滤,会导致最终得到的精盐的质量减少;食盐飞溅导致精盐的质量减少;精盐很潮湿会使所称量的精盐的质量偏大,使制得率偏高;蒸发皿中的精盐没有全部转移到称量纸上,会使精盐的质量减少。第 6 节 物质的分离方法透视 粗盐提纯的步骤: 溶解、 过滤、 蒸发。注意在粗盐的提纯过程中玻璃棒的作用,另外要明确过滤操作的要点: 一贴、 二低、 三靠。【试题链接】 小试身手 2、3、4、6,创新培优 7、9第 6 节 物质的分离挑战自我小试身手1. 如 图 1-6-19 所 示 是a、 b、 c 三种固体物质的溶解度随温度变化的曲线。下列说法中正确的是( )
A. a 的溶解度大于 c的溶解度
B. 在 t1℃时, a、 c 两种物质的饱和溶液
中溶质的质量分数相同
C. c 的不饱和溶液由 t2℃降温至 t1℃时,变成饱和溶液
D. 要从 b 溶液中得到 b,通常可采用冷却热饱和溶液的方法 B第 6 节 物质的分离解析 比较溶解度的大小,需要明确在什么温度下;在t1℃时,a、c两种物质的溶解度相等,所以此温度下两种物质的饱和溶液中溶质的质量分数也相等;c的不饱和溶液由t2℃降温至t1℃时,溶解度增大,所以不可能变成饱和溶液;由于b的溶解度受温度影响不大,所以结晶时最好用蒸发溶剂的方法。第 6 节 物质的分离2. 在进行过滤操作时,除了使用铁架台、烧杯、玻璃棒外,还需要使用的仪器是( )
A. 酒精灯 B. 托盘天平
C. 蒸发皿 D. 漏斗D第 6 节 物质的分离3. 在粗盐提纯的实验中,下列操作正确的是( )B第 6 节 物质的分离解析 托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了;粗盐溶解时,为加快溶解速率,可用玻璃棒搅拌;过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流;蒸发时,应用玻璃棒不断搅拌,以防液体因受热不均匀而飞溅。第 6 节 物质的分离4. [台州中考]科学家用石墨烯膜制成“筛子”,可以筛掉盐类物质。当海水流过该膜时,钠离子和氯离子被水分子包裹而不能通过,独立的水分子却能通过(如图 1-6-20)。下列关于石墨烯膜“筛掉”氯化钠的说法错误的是( )
A.该过程属于物理变化
B.该过程可应用于海水淡化
C.“筛掉”氯化钠的过程类似于过滤操作
D. “筛掉”氯化钠后的海水溶质质量分数增大D第 6 节 物质的分离5.从硝酸钾和氯化钠的饱和溶液中分离出硝酸钾,主要采用的方法是( )
A.溶解过滤 B.过滤
C.蒸发结晶 D.降温结晶D第 6 节 物质的分离6. 从自然界中获得的粗盐,含有较多的杂质,需要精制。为了除去粗盐中泥沙等不溶性杂质设计了如图 1-6-21 的 A、 B、 C 三个步骤。
(1) B 步骤称为____________ 。过滤 第 6 节 物质的分离解析 B步骤为过滤,是将不溶于水的泥沙与食盐水分离的操作。6. 从自然界中获得的粗盐,含有较多的杂质,需要精制。为了除去粗盐中泥沙等不溶性杂质设计了如图 1-6-21 的 A、 B、 C 三个步骤。
(2) C 步骤中,当蒸发皿内出现较多固体时,应该__________ (填字母)。
A.移去酒精灯,停止搅拌
B.移去酒精灯,用玻璃棒继续搅拌
C.继续加热蒸干水分,再移去酒精灯B第 6 节 物质的分离解析 在蒸发操作中,当蒸发皿内出现较多固体时,应移去酒精灯停止加热,用玻璃棒继续搅拌,利用余热把剩余滤液蒸干。第 6 节 物质的分离创新培优7.下列是关于“粗盐提纯”实验的几种说法,其中正确的是( )
A. 为加快过滤速率,应用玻璃棒不断搅拌过滤器内的液体
B. 如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因
C. 蒸发滤液时要用玻璃棒不断搅拌,用酒精灯持续加热直到蒸干为止
D. 为使食盐快速溶解,应用较多的水溶解食盐B 第 6 节 物质的分离解析 过滤时,若搅拌易造成滤纸破损;蒸发时,当有较多量食盐析出时停止加热;溶解时,水量过多会造成过滤和蒸发时间过长。8.小明同学绘制了如图 1-6-22 所示的 A、 B两种固体物质的溶解度随温度变化的曲线。
(1)当温度为_________ ℃时, A 物质与 B 物质的溶解度相等。
(2)若将 B 物质从溶液中结晶析出,宜
采用的方法是______________________ 。
40
蒸发结晶第 6 节 物质的分离8.小明同学绘制了如图 1-6-22 所示的 A、 B两种固体物质的溶解度随温度变化的曲线。
(3)我国有许多盐碱湖,湖中溶有大量的氯化钠和碳酸钠,那里的人们“冬天捞碱,夏天晒盐”。据此你认为
________________(填“A”或“B”)物质的溶
解度曲线与纯碱的相似。A第 6 节 物质的分离解析 B物质的溶解度受温度变化的影响较小,可采用蒸发溶剂的方法获得晶体;“冬天捞碱”说明碳酸钠的溶解度受温度变化的影响较大,图中A物质的溶解度曲线与碳酸钠的溶解度曲线相似。第 6 节 物质的分离9.25 ℃时,将 10 g 某盐加入一定量的水中,完 全 溶 解 后, 得 到 不 饱 和 溶 液, 若 蒸 发12.5 g 水后得到溶质质量分数为 20 % 的饱和溶液。
请计算:
(1)25 ℃时,该盐的溶解度。
(2)原不饱和溶液的溶质质量分数。
(3)25 ℃时,若要使 5 g 该盐从饱和溶液中析出来,需蒸发多少克水?
第 6 节 物质的分离第 6 节 物质的分离
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
