2.5 物质的转化 提高练习
图片预览
文档简介
中小学教育资源及组卷应用平台
2.5 物质的转化提高练习
一、选择题(共15题;共30分)
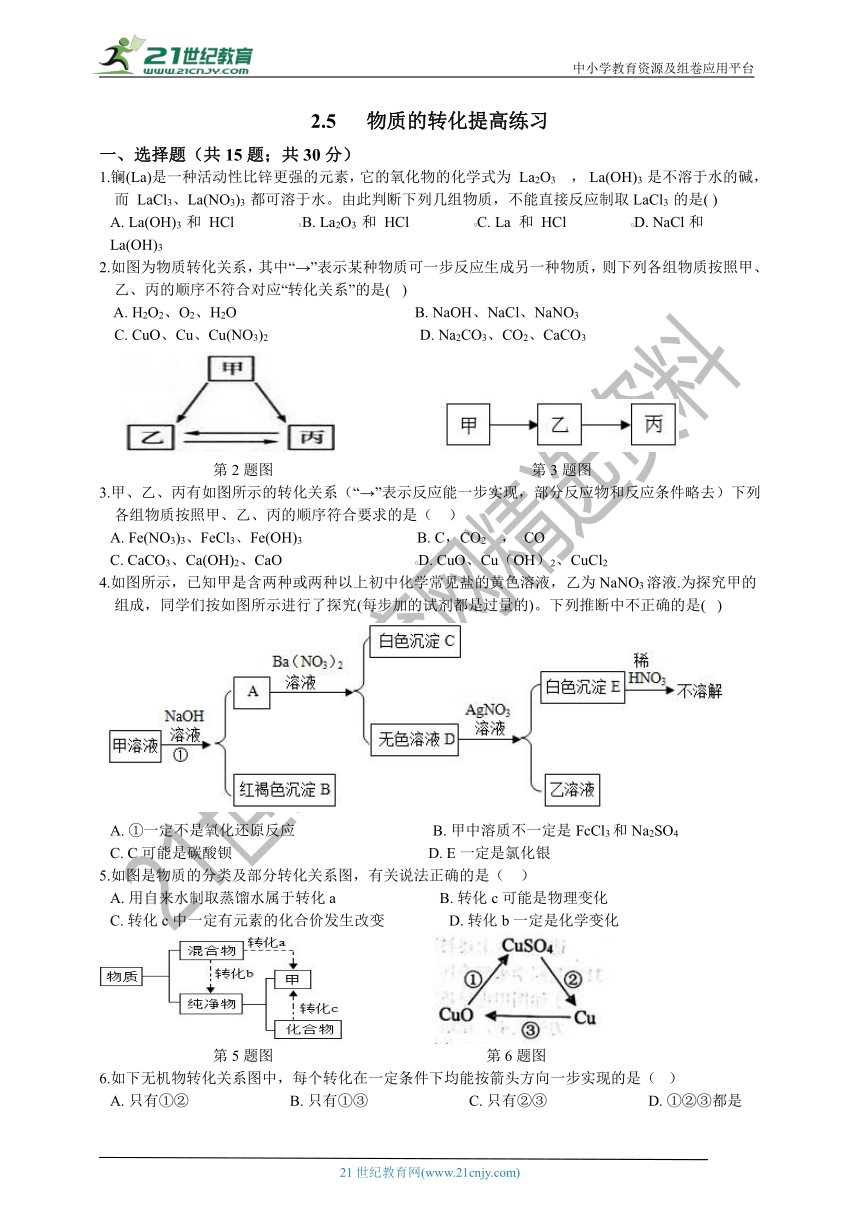
1.镧(La)是一种活动性比锌更强的元素,它的氧化物的化学式为 La2O3 , La(OH)3 是不溶于水的碱,而 LaCl3、La(NO3)3 都可溶于水。由此判断下列几组物质,不能直接反应制取LaCl3 的是( )
A.?La(OH)3 和 HCl?????????????????B.?La2O3 和 HCl?????????????????C.?La 和 HCl?????????????????D.?NaCl和 La(OH)3
2.如图为物质转化关系,其中“→”表示某种物质可一步反应生成另一种物质,则下列各组物质按照甲、乙、丙的顺序不符合对应“转化关系”的是(? )
A.?H2O2、O2、H2O???????????????????????????????????????????????B.?NaOH、NaCl、NaNO3
C.?CuO、Cu、Cu(NO3)2????????????????????????????????????????D.?Na2CO3、CO2、CaCO3
第2题图 第3题图
3.甲、乙、丙有如图所示的转化关系(“→”表示反应能一步实现,部分反应物和反应条件略去)下列各组物质按照甲、乙、丙的顺序符合要求的是(?? )
A.?Fe(NO3)3、FeCl3、Fe(OH)3??????????????????????????????B.?C,CO2 , CO
C.?CaCO3、Ca(OH)2、CaO???????????????????????????????????D.?CuO、Cu(OH)2、CuCl2
4.如图所示,已知甲是含两种或两种以上初中化学常见盐的黄色溶液,乙为NaNO3溶液.为探究甲的组成,同学们按如图所示进行了探究(每步加的试剂都是过量的)。下列推断中不正确的是(? )
A.?①一定不是氧化还原反应????????????????????????????????????B.?甲中溶质不一定是FcCl3和Na2SO4
C.?C可能是碳酸钡???????????????????????????????????????????????????D.?E一定是氯化银
5.如图是物质的分类及部分转化关系图,有关说法正确的是( ??)
A.?用自来水制取蒸馏水属于转化a???????????????????????????B.?转化c可能是物理变化
C.?转化c中一定有元素的化合价发生改变?????????????????D.?转化b一定是化学变化
第5题图 第6题图
6.如下无机物转化关系图中,每个转化在一定条件下均能按箭头方向一步实现的是(? )
A.?只有①②??????????????????????????B.?只有①③??????????????????????????C.?只有②③??????????????????????????D.?①②③都是
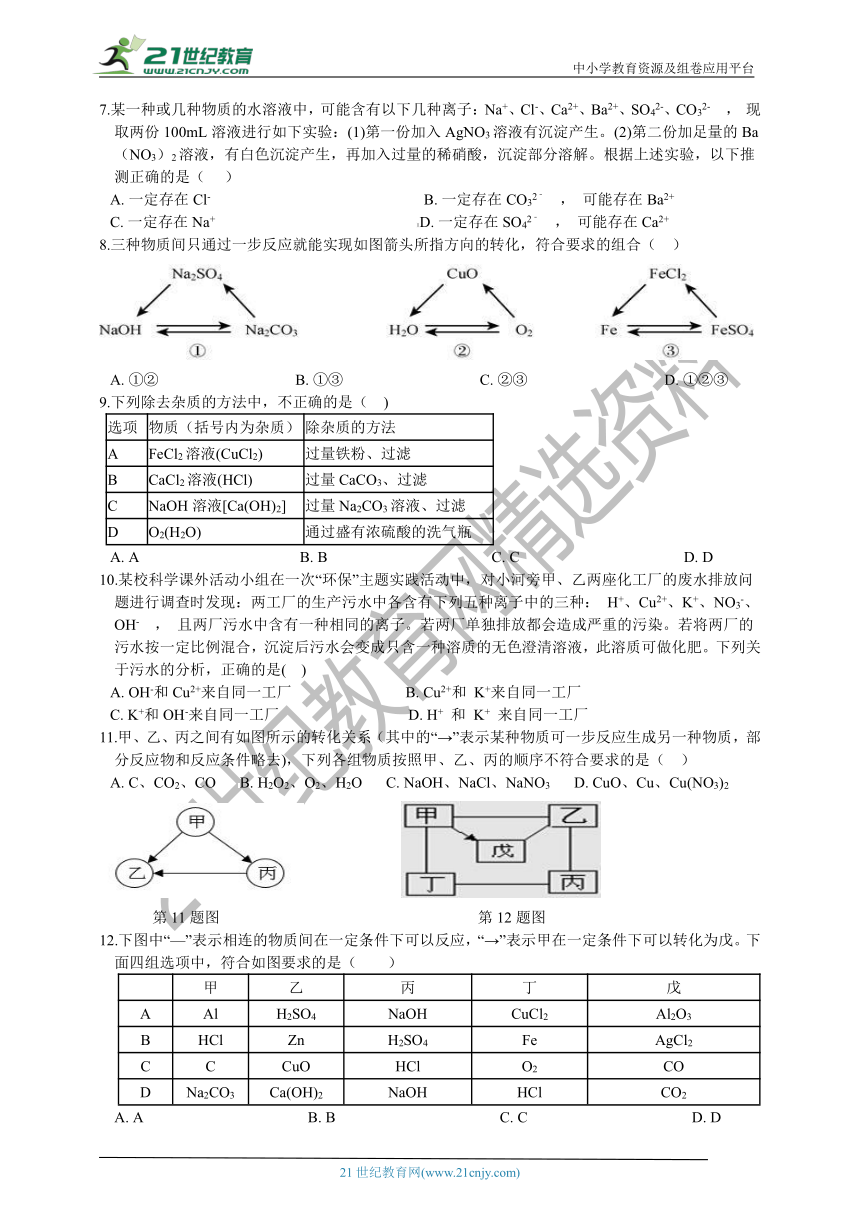
7.某一种或几种物质的水溶液中,可能含有以下几种离子:Na+、Cl-、Ca2+、Ba2+、SO42-、CO32- , 现取两份100mL溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生。(2)第二份加足量的Ba(NO3)2溶液,有白色沉淀产生,再加入过量的稀硝酸,沉淀部分溶解。根据上述实验,以下推测正确的是(??? )????????????????????????????????????????
A.?一定存在Cl-????????????????????????????????????????????????????????B.?一定存在CO32﹣ , 可能存在Ba2+
C.?一定存在Na+?????????????????????????????????????????????????????D.?一定存在SO42﹣ , 可能存在Ca2+
8.三种物质间只通过一步反应就能实现如图箭头所指方向的转化,符合要求的组合( ??)
A.?①②????????????????????????????????????B.?①③????????????????????????????????????C.?②③????????????????????????????????????D.?①②③
9.下列除去杂质的方法中,不正确的是( ??)
选项 物质(括号内为杂质) 除杂质的方法
A FeCl2溶液(CuCl2) 过量铁粉、过滤
B CaCl2溶液(HCl) 过量CaCO3、过滤
C NaOH溶液[Ca(OH)2] 过量Na2CO3溶液、过滤
D O2(H2O) 通过盛有浓硫酸的洗气瓶
A.?A??????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D?
10.某校科学课外活动小组在一次“环保”主题实践活动中,对小河旁甲、乙两座化工厂的废水排放问题进行调查时发现:两工厂的生产污水中各含有下列五种离子中的三种: H+、Cu2+、K+、NO3-、OH- , 且两厂污水中含有一种相同的离子。若两厂单独排放都会造成严重的污染。若将两厂的污水按一定比例混合,沉淀后污水会变成只含一种溶质的无色澄清溶液,此溶质可做化肥。下列关于污水的分析,正确的是(? ?)
A.?OH?和Cu2+来自同一工厂 B.?Cu2+和 K+来自同一工厂
C.?K+和OH?来自同一工厂 D.?H+ 和 K+ 来自同一工厂
11.甲、乙、丙之间有如图所示的转化关系(其中的“→”表示某种物质可一步反应生成另一种物质,部分反应物和反应条件略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是( ??)
A.?C、CO2、CO??????B.?H2O2、O2、H2O??????C.?NaOH、NaCl、NaNO3??????D.?CuO、Cu、Cu(NO3)2
第11题图 第12题图
12.下图中“—”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以转化为戊。下面四组选项中,符合如图要求的是(?????? )
甲 乙 丙 丁 戊
A Al H2SO4 NaOH CuCl2 Al2O3
B HCl Zn H2SO4 Fe AgCl2
C C CuO HCl O2 CO
D Na2CO3 Ca(OH)2 NaOH HCl CO2
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
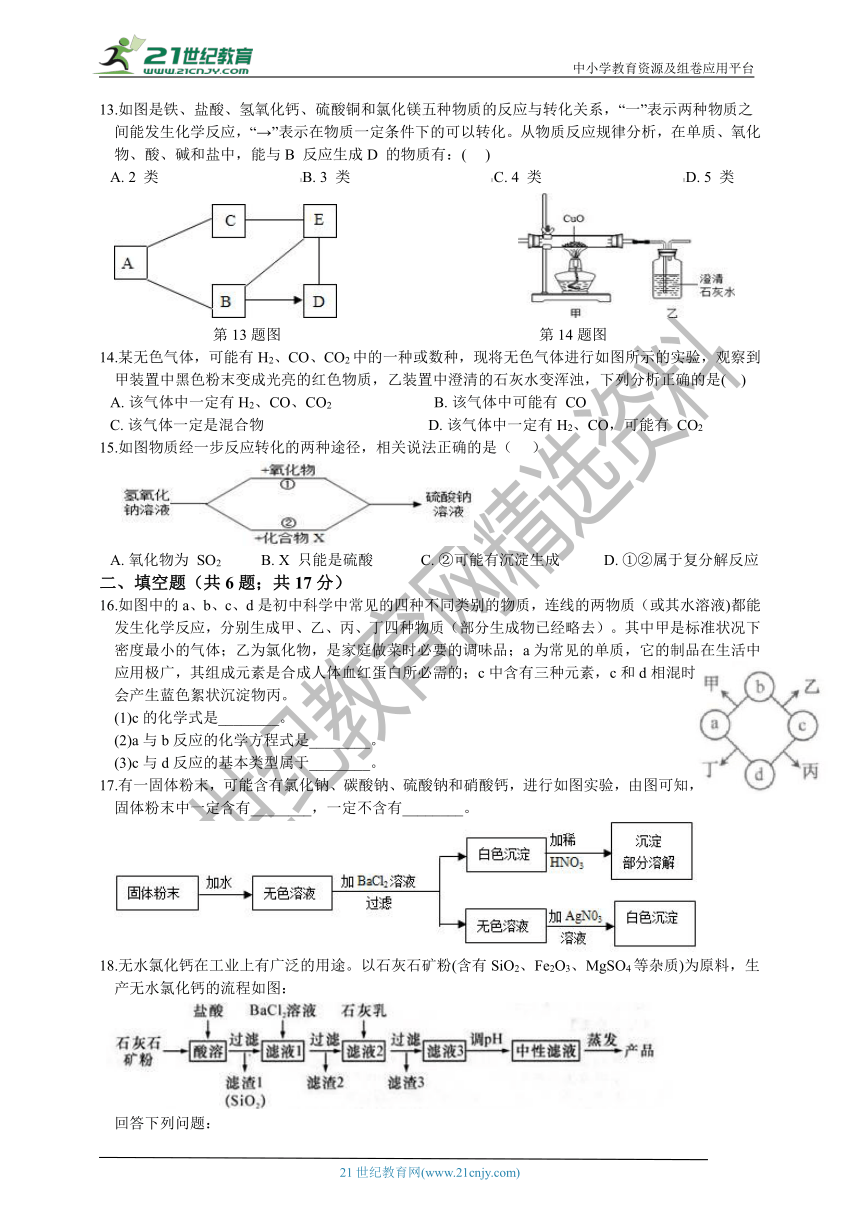
13.如图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“一”表示两种物质之间能发生化学反应,“→”表示在物质一定条件下的可以转化。从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B 反应生成D 的物质有:(??? )
A.?2 类?????????????????????????????????????B.?3 类?????????????????????????????????????C.?4 类?????????????????????????????????????D.?5 类
第13题图 第14题图
14.某无色气体,可能有H2、CO、CO2中的一种或数种,现将无色气体进行如图所示的实验,观察到甲装置中黑色粉末变成光亮的红色物质,乙装置中澄清的石灰水变浑浊,下列分析正确的是(?? )
A.?该气体中一定有H2、CO、CO2???????????????????????????B.?该气体中可能有 CO
C.?该气体一定是混合物???????????????????????????????????????????D.?该气体中一定有H2、CO,可能有 CO2
15.如图物质经一步反应转化的两种途径,相关说法正确的是( ???)
A.?氧化物为 SO2???? ????B.?X 只能是硫酸????????????C.?②可能有沉淀生成???????????D.?①②属于复分解反应
二、填空题(共6题;共17分)
16.如图中的a、b、c、d是初中科学中常见的四种不同类别的物质,连线的两物质(或其水溶液)都能发生化学反应,分别生成甲、乙、丙、丁四种物质(部分生成物已经略去)。其中甲是标准状况下密度最小的气体;乙为氯化物,是家庭做菜时必要的调味品;a为常见的单质,它的制品在生活中应用极广,其组成元素是合成人体血红蛋白所必需的;c中含有三种元素,c和d相混时会产生蓝色絮状沉淀物丙。
(1)c的化学式是________。
(2)a与b反应的化学方程式是________。
(3)c与d反应的基本类型属于________。
17.有一固体粉末,可能含有氯化钠、碳酸钠、硫酸钠和硝酸钙,进行如图实验,由图可知,固体粉末中一定含有________,一定不含有________。
18.无水氯化钙在工业上有广泛的用途。以石灰石矿粉(含有SiO2、Fe2O3、MgSO4等杂质)为原料,生产无水氯化钙的流程如图:
回答下列问题:
(1)从流程图中推知:SiO2具有的化学性质是________。
(2)加入BaCl2溶液的主要作用是 ________。
(3)滤渣3中除有Ca(OH)2外,还有________(填化学式)。
(4)产品中的杂质除极少量H2O外,最有可能含的是________(填化学式)。
19.化合物甲、乙、丙和单质A、B、C均由氢、氯、铜、铁元素的一种或几种组成,它们之间的转化关系如图所示。其中B是密度最小的气体。
(1)A与甲反应的基本类型为________。
(2)A与乙反应的化学方程式为________。
(3)从物质反应的规律分析,在单质、氧化物、酸、碱和盐中,能与甲反一0-g应生成丙的物质有________。(填序号)
①2类????????? ②3类????????? ③4类????????? ④5类
第19题图 第20题图
20.有一包白色固体,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡中的一种或几种物质组成。为探究该白色固体的组成,某小组取适量样品按下列流程进行实验。请回答下列问题:
(1)白色沉淀Ⅱ的化学式________。
(2)原白色固体中含有的物质有________。
21.在Cu(NO3)2和AgNO3的混合溶液中,加入一定量的锌粉,使之充分反应后有下列情况:
(1)若反应后锌有剩余,则溶液中所含溶质为________。
(2)若反应后,将溶液过滤,所得固体物质加盐酸没有气体产生,则固体物质中一定有________。
(3)若反应后,将析出的金属过滤,向滤液中滴加NaCl溶液,有不溶于稀HNO3的白色沉淀生成,则滤液中含有的溶质为________。
三、实验探究题(共3题;每空3分;共30分)
22.有一包白色粉末,可能含有硫酸铜、氯化钠、氯化银、硫酸钠、碳酸钠中的一或几种,现进行下列实验操作:
⑴将白色粉末放入足量水中,得无色澄清溶液。
⑵向无色澄清溶液中加入氯化钡溶液,有白色沉淀生成。
⑶向白色沉淀中加入足量的稀硝酸,有部分沉淀溶解,并生成能使澄清石灰水变浑浊的气体。根据以上实验事实推断,该白色粉末中一定有________,可能有________,一定没有 ________
23.课外探究小组对实验教师提供的一包白色固体(可能是NaCl、Na2SO4、Na2CO3和NaNO3的一种或几种)进行了下面的实验,且每步实验中均加入足量的试剂,至充分反应。实验过程、现象见下图:
?
请分析实验过程并完成以下问题:
(1)实验中不能用稀盐酸代替稀硝酸的原因是 ________;
(2)滴加Ba(NO3)2的目的是________;
(3)通过计算推断:原白色固体的成分为________。
24.某化学兴趣小组利用如图所示装置进行实验,探究工业炼铁的化学原理,试按要求填空:
(1)硬质玻璃管中观察到的现象是________,写出一氧化碳和氧化铁反应的化学方程式________。
(2)实验中先通入一氧化碳的目的是________。
(3)装置中导管末端加一点燃的酒精灯的目的是________。
四、解答题(共2题;25小题9分;26小题14分;共23分)
25.采用“双碱法”使烟气(含SO2)脱硫是我国目前环保领域的的经济、实用、高效的一种方法。其脱硫(除去烟气中的二氧化硫)的工业流程如下,试回答:
(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水。NaOH溶液喷洒成雾状来吸收SO2的好处是________。
(2)写出沉淀室中发生的反应化学方程式________。
(3)“双碱法”中实际使用的碱原料只有________(填名称或化学式)。
26.在一烧杯中盛有CaCl2和HCl的混合溶液100g,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入的Na2CO3溶液的质量关系图像如图所示。
(1)在实验过程中,其中出现冒气泡的是________(填“PA”或“AB”)段。
(2)逐渐滴入碳酸钠溶液的过程中,杯中溶液的PH如何变化?
(3)原溶液中HCl的质量是多少g?
(4)当滴入Na2CO3溶液至图中B点时,通过计算求烧杯中(不饱和溶液)溶质的质量分数为多少?(计算结果精确到0.1%)
答案解析部分
一、选择题
1. D 2. B 3. B 4. C 5. C 6. D 7. C 8. D 9. C 10. C 11. C 12. A 13. C 14. B 15. C
二、填空题
16. (1)NaOH(2)Fe+2HCl=FeCl2+H2↑(3)复分解反应
17. Na2CO3、Na2SO4;Ca(NO3)2
18. (1)不能与盐酸反应(2)除掉滤液中的硫酸根离子(3)Mg(OH)2、Fe(OH)3(4)BaCl2
19. (1)置换反应(2)Fe+CuCl2=FeCl2+Cu(3)③
20. (1)BaCO3(2)CaCO3、NaOH、BaCl2
21. (1)Zn(NO3)2(2)Ag(3)AgNO3、Cu(NO3)2、Zn(NO3)2
三、实验探究题
22. 硫酸钠、碳酸钠;氯化钠;硫酸铜、氯化银
23. (1)稀盐酸中会有 Cl- ,对判断是否有 NaCl 会造成干扰(2)检验是否有Na2SO4(3)NaCl、NaNO3
24. (1)红色固体变为黑色;3CO+Fe2O3 2Fe+3CO2
(2)赶尽玻璃管内的空气,防止加热时爆炸(3)除去多余的CO,防止污染空气
四、解答题
25.(1)增大与二氧化硫的接触面积,从而充分吸收二氧化碳(2)Ca(OH)2+Na2SO3=CaSO3↓+2NaOH
(3)氢氧化钙或Ca(OH)2
26.(1)PA(2)解:先变大至7,然后保持7不变,最后再变大
(3)解:与稀盐酸反应时、与氯化钙反应时,消耗碳酸钠均为106g×10%=10.6g
2HCl + Na2CO3 = 2NaCl + H2O + CO2↑
73 106 117 44
X 10.6g a b
????? X=7.3g????????
a=11.7g????? b=4.4g
(4)解:
CaCl2 + Na2CO3 = 2NaCl + CaCO3↓
106 117 100
10.6g c d
C=11.7g??? d=10g
NaCl%=(11.7+11.7)/(100+212-4.4-10)=23.4/297.6=7.9%
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
