人教版九年级化学上册课件:第四单元 课题4 化学式与化合价(共47张PPT)
文档属性
| 名称 | 人教版九年级化学上册课件:第四单元 课题4 化学式与化合价(共47张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-10-14 00:00:00 | ||
图片预览











文档简介
(共47张PPT)
课题4 化学式与化合价
第1课时 化学式
1.化学式的概念
概 念:用_________和_______的组合表示物质组成的式子。
2.化学式的意义(以H2O为例)
宏 观:(1)表示____________;(2)表示水由________元素组成。
微 观:(1)表示____________;(2)表示1个水分子由____________和_______
_____________构成。
注 意:在化学式前面加数字,那么该化学符号就只能表示微观意义。如:2H2O表示两个水分子。
元素符号
数字
水这种物质
氢、氧
一个水分子
2个氢原子
1个氧原子
3.化学式的书写
单 质:(1)稀有气体:用元素符号表示,如氦写为____,氖写为____;(2)金属和某些固态非金属:习惯上用元素符号表示,如铁写为____,碳写为____;(3)气态非金属:在元素符号右下角写上表示分子中所含原子个数的数字,如氧气写为____。
化 合 物:(1)氧化物:一般把氧的元素符号写在____,另一种元素的符号写在____;
(2)由金属元素与非金属元素组成的化合物:一般把金属的元素符号写在____,非金属的元素符号写在____。
He
Ne
Fe
C
O2
右方
左方
左方
右方
读 法:(1)气体单质一般读作“某气”,如O2读作______,He读作______,固体单质直接读元素的名称,如铁的化学式为Fe,读作铁等。
(2)由两种元素组成的化合物的名称,一般读作“某化某”,如NaCl读作
___________;有时需读出化学式中原子的个数,如P2O5读作____________。
注 意:各种物质的化学式都是通过实验方法测定物质的组成后得出来的,所以化学式中元素符号右下角的数字不能改动。
氧气
氦气
氯化钠
五氧化二磷
考点1 化学式的概念和意义
1.2H2表示( )
A.4个氢原子 B.2个氢分子
C.4个氢分子 D.2个氢原子
2.(兰州中考)化学式H2O2能表示多种意义,下列说法错误的是( )
A.表示过氧化氢这种物质
B.表示过氧化氢由氢元素和氧元素组成
C.表示1个过氧化氢分子
D.表示过氧化氢由2个H原子和2个O原子构成
B
D
3.用元素符号或化学式填空。
(1)碳元素_______;
(2)5个磷原子______;
(3)氮气_______;
(4)3个氮分子________;
(5)钠离子________;
(6)6个二氧化硫分子________;
(7)m个水分子__________。
C
5P
N2
3N2
Na+
6SO2
mH2O
4.化学用语中的数字在不同的位置上意义不同。“2CO2”中数字“2”的意义分别是第一个“2”表示:_______________________,第二个“2”表示:
__________________________________。Mg2+中“2”表示的意义是
______________________________。2N中“2”表示的意义是_______________。
两个二氧化碳分子
每个二氧化碳分子中有两个氧原子
一个镁离子带两个单位的正电荷
两个氮原子
考点2 化学式的读法和写法
5.写出下列物质的化学式。
(1)单质:
①铁____、汞____;
②红磷____、碳____;
③氖气____、氩气____;
④氢气____、氧气____。
(2)氧化物:
二氧化硫____; 五氧化二磷_______;
四氧化三铁________; 二氧化锰_______。
(3)化合物:氯化钠________。
Fe
Hg
P
C
Ne
Ar
H2
O2
SO2
P2O5
Fe3O4
MnO2
NaCl
6.写出下列物质对应的名称。
①Cu_______; ②S_______;
③He_______; ④CO2__________;
⑤H2O______; ⑥KCl________。
铜
硫
氦气
二氧化碳
水
氯化钾
7.(北京中考)下列符号能表示两个氢分子的是( )
A.2H B.2H2 C.H2 D.2H2O2
8.(衡阳中考)下列符号中既能表示一种元素,又能表示这种元素的一个原子,还能表示一种单质的是( )
A.S B.C60 C.H D.Fe2O3
B
A
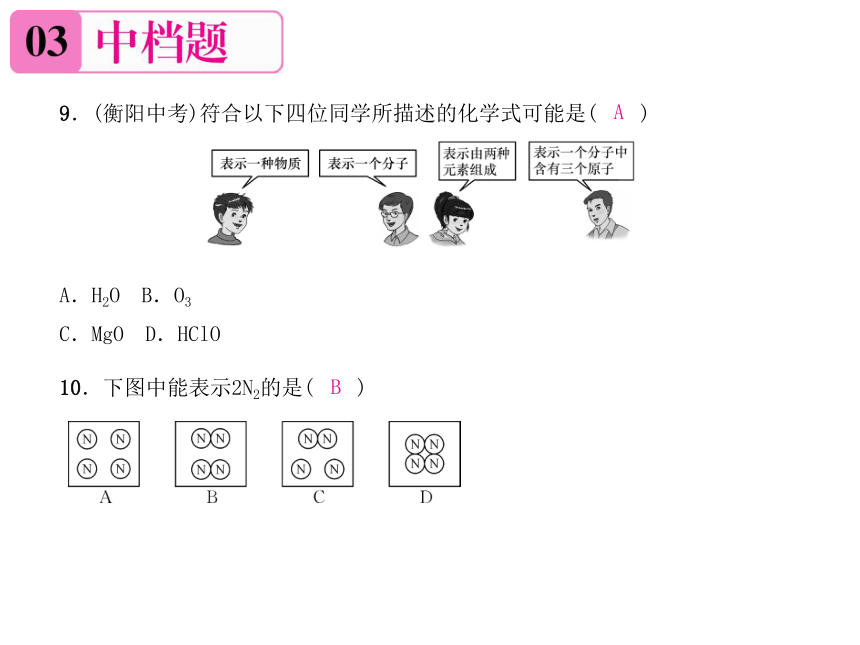
9.(衡阳中考)符合以下四位同学所描述的化学式可能是( )
A.H2O B.O3
C.MgO D.HClO
10.下图中能表示2N2的是( )
A
B
11.(德州中考)下列化学用语书写正确的是( )
A.银元素—AG B.3个氧原子—O3
C.4个水分子—4H2O D.镁离子—Mg+2
12.(内江中考)葡萄糖的分子式为C6H12O6,则下列有关葡萄糖的说法正确的是
( )
A.葡萄糖由碳、氢气和氧气组成
B.葡萄糖由三种元素组成
C.葡萄糖由24个原子构成
D.葡萄糖分子由碳原子和水分子构成
C
B
13.某物质的分子模型如下图所示,下列说法错误的是 ( )
A.该物质属于化合物
B.该物质的化学式为CH4
C.该物质的1个分子中含2个氢分子
D.该物质的1个分子中碳、氢原子的个数比为1∶4
C
14.葡萄糖在人体组织中缓慢氧化放出热量,这是人类生命活动所需能量的重要来源之一。葡萄糖的化学式为C6H12O6,从葡萄糖的化学式你能总结出哪些信息?(请写出两条)
(1)___________________________________________。
(2)___________________________________________________________。
15.(襄阳中考)生活中处处有化学。请你根据所学的知识,用相应的化学式填空。
(1)按体积计算,空气中含量最多的气体是_______。
(2)实验室制取氧气的药品是___________________________(任意写出一种)。
葡萄糖是由碳、氢、氧三种元素组成的
1个葡萄糖分子中含有6个碳原子、12个氢原子和6个氧原子
N2
KClO3(或KMnO4、H2O2)
(1)若用 表示氢原子, 表示氧原子。下列方框中,符合“2H2O”所表示意义的是____(填序号)。
16.形象的微观示意图有助于我们认识化学物质和理解化学反应。
(2)ClO2是一种新一代饮用水的消毒剂,我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示。
上述四种物质中,属于氧化物的是________,一个二氧化氯分子是由
________________________构成的。
C
ClO2
1个氯原子和2个氧原子
请写出下列物质的化学式:
氦气:__________,氖气:____________,氧气:__________,
四氧化三铁:________,二氧化碳:____________,铁:___________,
铜:_____________, 汞:___________, 二氧化硫:________,
五氧化二磷:__________,碳:____________, 氮气:____________,
红磷________, 过氧化氢:__________, 高锰酸钾:____________。
第2课时 化合价
1.化合价的规律
规 律:(1)化合价有______价和______价。①化合物中氧元素通常显______价,氢元素通常显____价。②金属元素与非金属元素化合时,金属元素显____,非金属元素显____。
(2)在化合物里元素正负化合价的代数和为____。
(3)在单质里,元素的化合价为____。
正
负
-2
+1
正价
负价
0
0
2.常见原子团的化合价
注 意:化合价标在元素(原子团)的正上方,符号在前,数字在后,1不能省略;离子符号标在元素(原子团)的右上角,数字在前,符号在后,1省略不写。
口 诀:钾钠氢银正一价,钙镁钡锌正二价;二三铁、二四碳、二四六硫都齐全;铜汞二价最常见;单质为零要记清。负一氢氧硝酸根;负二碳酸硫酸根;正一价的是铵根。
3.化合价的应用:依据化合物里元素正负化合价的代数和为____写化学式。
零
+1
-1
-1
-2
-2
原子团 铵根 氢氧根 硝酸根 硫酸根 碳酸根
离子符号 OH-
化合价 _______
价 _______
价 ________
价 ________
价 ________
价
考点1 化合价及其表示方法
1.下列关于化合价的规律叙述正确的是( )
A.金属元素只能显正价
B.非金属元素只能显负价
C.在化合物中元素正负化合价的代数和为零
D.一种元素只有一种化合价
C
2.写出下列物质的化学式并标出元素的化合价。
(1)标出水中氢元素的化合价:____。
(2)标出二氧化碳中氧元素的化合价:____。
(3)标出氯化钠中氯元素的化合价:_______。
(4)标出氮气中氮元素的化合价:______。
考点2 根据化学式求化合价
3.(山西中考)化学家戴维最早制得了曾用作麻醉剂的笑气(化学式为N2O),其中氮元素的化合价是( )
A.-1 B.-2 C.+1 D.+5
4.(南宁中考)科学家用Xe(氙气)首次合成了XePtF6,在XePtF6中Xe、F元素的化合价分别显+1、-1价,则XePtF6中Pt元素的化合价是( )
A.+2 B.+4 C.+5 D.+7
C
C
5.在下列物质中标出硫元素的化合价。
(1)硫(S)
(2)二氧化硫(SO2)
(3)硫酸(H2SO4)
(4)硫化氢(H2S)
-2
+4
0
+6
考点3 根据化合价书写化学式
6.(邵阳中考)某物质的化学式为CaWOx,其中钙元素为+2价,钨(W)元素为+6价,氧元素为-2价,则x的值是( )
A.2 B.3
C.4 D.5
7.根据化合价写出下列元素或原子团组成的物质的化学式。
C
Na2O
NaCl
NaNO3
CaO
CaCl2
Ca(NO3)2
FeO
FeCl2
Fe(NO3)2
Fe2O3
FeCl3
Fe(NO3)3
? Na+ Ca2+ Fe2+ Fe3+
8.写出下列物质的化学式。
(1)酸:硫酸_______、盐酸________、硝酸________。
(2)碱:氢氧化钠________、氢氧化钙_______、氢氧化铜_______、氢氧化钡_______。
(3)盐:①硫酸钠________、硫酸钡________、硫酸铜________。
②碳酸钠_________、碳酸钙_________、碳酸钡_________。
③硫酸铵_________、氯化铵_________。
(4)其他:氯酸钾________、高锰酸钾________、锰酸钾________、过氧化氢________。
H2SO4
HCl
HNO3
NaOH
Ca(OH)2
Cu(OH)2
Ba(OH)2
Na2SO4
BaSO4
CuSO4
Na2CO3
CaCO3
BaCO3
(HN4)2SO4
NH4Cl
KClO3
KMnO4
K2MnO4
H2O2
9.下列有关化合价的叙述正确的是 ( )
A.化合价与原子最外层电子数无关
B.氨气(NH3)中氮元素的化合价为+3
C.氧气中氧元素的化合价为-2
D.有些元素在不同条件下可表现出不同的化合价
10.(福建中考)下列是《本草纲目》记载的四种无机药物,其成分中Hg的化合价为+1的是( )
A.水银(Hg) B.升丹(HgO)
C.朱砂(HgS) D.轻粉(Hg2Cl2)
D
D
11.(黔东南中考)硝酸铵(NH4NO3)是一种肥效较高、使用广泛的氮肥,但近年来不法分子用它来生产炸药,给社会的安全和稳定带来了很大的压力。为此,国家相关部门加强了对硝酸铵生产和使用的监管,减少了它在农业生产中的使用。科学研究发现,硝酸铵爆炸时,氮元素的化合价会发生变化。下列关于硝酸铵中氮元素化合价的判断,正确的是( )
A.-4 +6 B.+1 +1
C.-3 +5 D.无法确定
12.(重庆中考B卷)某工厂制取漂白液的化学原理为Cl2+2NaOH===NaCl+NaClO+H2O,在该反应中,氯元素没有呈现出的化合价是( )
A.+2 B.+1
C.0 D.-1
C
A
13.元素R在化合物中只有一种化合价,其氧化物的化学式为R2O3,则下列化学式中正确的是( )
A.R(OH)2 B.R2(SO4)3
C.RNO3 D.RCO3
14.用化学用语填空。
(1)镁:_______。
(2)2个氮气分子:________。
(3)5个硫酸根离子:_______。
(4)五氧化二磷:________。
(5)+6价的硫元素:________。
(6)由Fe3+和OH-构成的氢氧化铁:________。
B
Mg
2N2
P2O5
Fe(OH)3
15.通过对已学知识的对比和归纳,我们往往可以得出一些十分有趣的规律,这些规律可以帮助我们掌握学习化学的方法。请你仔细阅读下表中的内容,并回答相应的问题:
(1)由前两行内容对照可得出的规律是元素或原子团的化合价数值往往与相应离子所带的_______数相等。
(2)由后两行内容对照可得出的规律是通过元素或原子团的_______可以确定相应化合物的化学式。
(3)利用表格中所给内容,请你再写出一种化合物的化学式:_____________。
(4)根据硫酸亚铁的化学式FeSO4,可推出该物质所含阳离子的符号为_______。
电荷
化合价
MgSO4(或NaCl等)
Fe2+
常见的几种离子
对应元素及原子团在化合物中的化合价
所能形成化合物的化学式 HCl、H2SO4、NaOH、
Mg(OH)2、MgCl2、Na2SO4
16.(柳州中考)如图是铁元素和氧元素常见化合价的坐标图,试判断a点上形成化合物的化学式为( )
A.Fe B.FeO
C.Fe2O3 D.Fe3O4
B
第3课时 化学式的有关计算
1.相对分子质量:化学式中各原子的______________的总和。符号为Mr。
2.根据化学式的计算
(1)计算相对分子质量
相对分子质量=化学式中各原子的_____________×相应____________的总和。
(2)计算物质组成元素的质量比
化合物中各元素的质量比=化学式中各_____________×相应___________之比。
(3)计算物质中某元素的质量分数
化合物中某元素的质量分数=
__________________________________________________________________。
相对原子质量
相对原子质量
原子个数
相对原子质量
原子个数
(化学式中该元素相对原子质量×原子个数)/化合物的相对分子质量×100%
3.其他类型的计算
(1)求一定量化合物中某一元素的质量某元素质量=化合物质量×化合物中该元素的_______________。
(2)求一定元素所在的某化合物的质量化合物质量=某元素的质量÷化合物中该元素的质量分数。
点 拨:根据化学式的计算常用方法
质量分数
考点1 相对分子质量的相关计算
1.计算出下列物质的相对分子质量。
(1)CO2的相对分子质量为_______。
(2)KClO3的相对分子质量为______。
(3)Al(OH)3的相对分子质量为______。
(4)C2H5OH的相对分子质量为______。
44
122.5
78
46
考点2 物质中各元素质量比
2.计算出下列物质中元素的质量比(填最简整数比)。
(1)P2O5中磷元素和氧元素的质量比=___________。
(2)C6H12O6中碳元素、氢元素和氧元素的质量比=___________。
(3)Fe2(SO4)3中铁元素、硫元素和氧元素的质量比=____________。
31∶40
6∶1∶8
7∶6∶12
考点3 某元素的质量分数的相关计算
3.计算出下列物质中元素的质量分数(结果精确到0.1%)。
(1)H2O中氢元素的质量分数__________。
(2)Mg(OH)2中镁元素的质量分数_________。
(3)CaCO3中钙元素的质量分数__________。
(4)NH4NO3中氮元素的质量分数__________。
11.1%
41.4%
40.0%
35.0%
考点4 化合物中某元素质量的计算
4.根据物质的质量求出下列物质中某元素的质量。
(1)8 g CH4中含有的碳元素的质量是多少?
?
?
(2)80 g NH4NO3中含有的氮元素的质量是多少?
5.根据某元素的质量求出物质的质量。
(1)已知CO中碳元素的质量为12 g,求CO的质量为多少?
?
?
(2)NH4HCO3中氮元素的质量为7 g,求NH4HCO3的质量为多少?
6.(温州中考)茶叶中含有茶氨酸(C7H14O3N2),茶氨酸中各元素质量分数如图所示。其中①表示的元素是( )
A.碳 B.氢 C.氧 D.氮
7.某物质的化学式为ROH,相对分子质量为51,则R的相对原子质量为( )
A.34 B.34 g C.40 D.40 g
A
A
8.(衡阳中考)硫酸新霉素——是“瘦肉精”中添加的“人用西药”,其化学式为C23H18N6O17S,下列关于硫酸新霉素的说法正确的是( )
A.硫酸新霉素中含65个原子
B.硫酸新霉素中氢、硫元素的质量比为18∶1
C.硫酸新霉素中氢元素的质量分数最小
D.硫酸新霉素的相对分子质量为682 g
C
9.(金华中考)如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是
( )
A.苯分子由碳、氢两种元素组成
B.苯中氢元素的质量分数小于10%
C.六氯苯中碳氯两种元素的质量比为1∶1
D.六氯苯由6个碳原子和6个氯原子构成
B
10.已知铁的氧化物中,铁元素与氧元素的质量比为7∶3,则该铁的氧化物的化学式是( )
A.Fe2O3 B.Fe3O4 C.FeO D.Fe2O
11.(内江中考)一种新型环保材料被塑胶跑道工程广泛应用,合成这种新材料的原料是二甲苯烷二异氰酸酯(分子式为C15H10N2O2)。请回答下列有关问题。
(1)二甲苯烷二异氰酸酯中氢、氧元素的质量比为________(填最简整数比)。
(2)二甲苯烷二异氰酸酯的相对分子质量为_______。
(3)500 g二甲苯烷二异氰酸酯中含氮元素的质量为_______g。
A
5∶16
250
56
12.(兰州中考)化学家TimRichard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26)。请计算。
(1)“小狗烯”的相对分子质量是_______。
(2)“小狗烯”中碳元素和氢元素的质量比为_______(填最简整数比)。
(3)16.9 g“小狗烯”中含碳元素多少克?(写出计算过程,结果精确到0.1 g)
338
12∶1
13.(泰安中考)儿童缺锌会引起食欲不振、发育不良等症状。如图为某补锌口服液说明书的部分信息,图中葡萄糖酸锌化学式已不完整,请根据相关信息回答下列问题。
×××牌补锌口服液
主要成分:葡萄糖酸锌
化 学 式:C12HxO14Zn
含 锌:5.0 mg/支
质 量:10.0 g/支
(1)葡萄糖酸锌的相对分子质量是455,则葡萄糖酸锌化学式中氢原子右下角的数字为____。
(2)若儿童1 kg体重每日需要0.5 mg锌,每天从食物中只能摄入所需锌的一半。体重为20 kg的儿童,理论上一天还需服用该口服液____支。
22
1
14.55 g二氧化碳中所含氧元素的质量和多少克水中所含氧元素的质量相等( )
A.18 g B.20 g
C.45 g D.36 g
15.经分析知,某硝酸铵(NH4NO3)样品中氮元素的质量分数为38%,则这种氮肥中可能混入的杂质是( )
A.NH4HCO3 B.NH4Cl
C.CO(NH2)2 D.(NH4)2SO4
C
C
请写出下列离子的符号
氢离子:__________,钾离子:__________,钠离子:__________,
氯离子:__________,氢氧根离子:__________,钙离子:__________,镁离子:__________,钡离子:__________,铝离子:__________,
碳酸根离子:_________,铁离子:_________,亚铁离子:________,
铜离子:_________,锌离子:_________,硫酸根离子:_________。
课题4 化学式与化合价
第1课时 化学式
1.化学式的概念
概 念:用_________和_______的组合表示物质组成的式子。
2.化学式的意义(以H2O为例)
宏 观:(1)表示____________;(2)表示水由________元素组成。
微 观:(1)表示____________;(2)表示1个水分子由____________和_______
_____________构成。
注 意:在化学式前面加数字,那么该化学符号就只能表示微观意义。如:2H2O表示两个水分子。
元素符号
数字
水这种物质
氢、氧
一个水分子
2个氢原子
1个氧原子
3.化学式的书写
单 质:(1)稀有气体:用元素符号表示,如氦写为____,氖写为____;(2)金属和某些固态非金属:习惯上用元素符号表示,如铁写为____,碳写为____;(3)气态非金属:在元素符号右下角写上表示分子中所含原子个数的数字,如氧气写为____。
化 合 物:(1)氧化物:一般把氧的元素符号写在____,另一种元素的符号写在____;
(2)由金属元素与非金属元素组成的化合物:一般把金属的元素符号写在____,非金属的元素符号写在____。
He
Ne
Fe
C
O2
右方
左方
左方
右方
读 法:(1)气体单质一般读作“某气”,如O2读作______,He读作______,固体单质直接读元素的名称,如铁的化学式为Fe,读作铁等。
(2)由两种元素组成的化合物的名称,一般读作“某化某”,如NaCl读作
___________;有时需读出化学式中原子的个数,如P2O5读作____________。
注 意:各种物质的化学式都是通过实验方法测定物质的组成后得出来的,所以化学式中元素符号右下角的数字不能改动。
氧气
氦气
氯化钠
五氧化二磷
考点1 化学式的概念和意义
1.2H2表示( )
A.4个氢原子 B.2个氢分子
C.4个氢分子 D.2个氢原子
2.(兰州中考)化学式H2O2能表示多种意义,下列说法错误的是( )
A.表示过氧化氢这种物质
B.表示过氧化氢由氢元素和氧元素组成
C.表示1个过氧化氢分子
D.表示过氧化氢由2个H原子和2个O原子构成
B
D
3.用元素符号或化学式填空。
(1)碳元素_______;
(2)5个磷原子______;
(3)氮气_______;
(4)3个氮分子________;
(5)钠离子________;
(6)6个二氧化硫分子________;
(7)m个水分子__________。
C
5P
N2
3N2
Na+
6SO2
mH2O
4.化学用语中的数字在不同的位置上意义不同。“2CO2”中数字“2”的意义分别是第一个“2”表示:_______________________,第二个“2”表示:
__________________________________。Mg2+中“2”表示的意义是
______________________________。2N中“2”表示的意义是_______________。
两个二氧化碳分子
每个二氧化碳分子中有两个氧原子
一个镁离子带两个单位的正电荷
两个氮原子
考点2 化学式的读法和写法
5.写出下列物质的化学式。
(1)单质:
①铁____、汞____;
②红磷____、碳____;
③氖气____、氩气____;
④氢气____、氧气____。
(2)氧化物:
二氧化硫____; 五氧化二磷_______;
四氧化三铁________; 二氧化锰_______。
(3)化合物:氯化钠________。
Fe
Hg
P
C
Ne
Ar
H2
O2
SO2
P2O5
Fe3O4
MnO2
NaCl
6.写出下列物质对应的名称。
①Cu_______; ②S_______;
③He_______; ④CO2__________;
⑤H2O______; ⑥KCl________。
铜
硫
氦气
二氧化碳
水
氯化钾
7.(北京中考)下列符号能表示两个氢分子的是( )
A.2H B.2H2 C.H2 D.2H2O2
8.(衡阳中考)下列符号中既能表示一种元素,又能表示这种元素的一个原子,还能表示一种单质的是( )
A.S B.C60 C.H D.Fe2O3
B
A
9.(衡阳中考)符合以下四位同学所描述的化学式可能是( )
A.H2O B.O3
C.MgO D.HClO
10.下图中能表示2N2的是( )
A
B
11.(德州中考)下列化学用语书写正确的是( )
A.银元素—AG B.3个氧原子—O3
C.4个水分子—4H2O D.镁离子—Mg+2
12.(内江中考)葡萄糖的分子式为C6H12O6,则下列有关葡萄糖的说法正确的是
( )
A.葡萄糖由碳、氢气和氧气组成
B.葡萄糖由三种元素组成
C.葡萄糖由24个原子构成
D.葡萄糖分子由碳原子和水分子构成
C
B
13.某物质的分子模型如下图所示,下列说法错误的是 ( )
A.该物质属于化合物
B.该物质的化学式为CH4
C.该物质的1个分子中含2个氢分子
D.该物质的1个分子中碳、氢原子的个数比为1∶4
C
14.葡萄糖在人体组织中缓慢氧化放出热量,这是人类生命活动所需能量的重要来源之一。葡萄糖的化学式为C6H12O6,从葡萄糖的化学式你能总结出哪些信息?(请写出两条)
(1)___________________________________________。
(2)___________________________________________________________。
15.(襄阳中考)生活中处处有化学。请你根据所学的知识,用相应的化学式填空。
(1)按体积计算,空气中含量最多的气体是_______。
(2)实验室制取氧气的药品是___________________________(任意写出一种)。
葡萄糖是由碳、氢、氧三种元素组成的
1个葡萄糖分子中含有6个碳原子、12个氢原子和6个氧原子
N2
KClO3(或KMnO4、H2O2)
(1)若用 表示氢原子, 表示氧原子。下列方框中,符合“2H2O”所表示意义的是____(填序号)。
16.形象的微观示意图有助于我们认识化学物质和理解化学反应。
(2)ClO2是一种新一代饮用水的消毒剂,我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示。
上述四种物质中,属于氧化物的是________,一个二氧化氯分子是由
________________________构成的。
C
ClO2
1个氯原子和2个氧原子
请写出下列物质的化学式:
氦气:__________,氖气:____________,氧气:__________,
四氧化三铁:________,二氧化碳:____________,铁:___________,
铜:_____________, 汞:___________, 二氧化硫:________,
五氧化二磷:__________,碳:____________, 氮气:____________,
红磷________, 过氧化氢:__________, 高锰酸钾:____________。
第2课时 化合价
1.化合价的规律
规 律:(1)化合价有______价和______价。①化合物中氧元素通常显______价,氢元素通常显____价。②金属元素与非金属元素化合时,金属元素显____,非金属元素显____。
(2)在化合物里元素正负化合价的代数和为____。
(3)在单质里,元素的化合价为____。
正
负
-2
+1
正价
负价
0
0
2.常见原子团的化合价
注 意:化合价标在元素(原子团)的正上方,符号在前,数字在后,1不能省略;离子符号标在元素(原子团)的右上角,数字在前,符号在后,1省略不写。
口 诀:钾钠氢银正一价,钙镁钡锌正二价;二三铁、二四碳、二四六硫都齐全;铜汞二价最常见;单质为零要记清。负一氢氧硝酸根;负二碳酸硫酸根;正一价的是铵根。
3.化合价的应用:依据化合物里元素正负化合价的代数和为____写化学式。
零
+1
-1
-1
-2
-2
原子团 铵根 氢氧根 硝酸根 硫酸根 碳酸根
离子符号 OH-
化合价 _______
价 _______
价 ________
价 ________
价 ________
价
考点1 化合价及其表示方法
1.下列关于化合价的规律叙述正确的是( )
A.金属元素只能显正价
B.非金属元素只能显负价
C.在化合物中元素正负化合价的代数和为零
D.一种元素只有一种化合价
C
2.写出下列物质的化学式并标出元素的化合价。
(1)标出水中氢元素的化合价:____。
(2)标出二氧化碳中氧元素的化合价:____。
(3)标出氯化钠中氯元素的化合价:_______。
(4)标出氮气中氮元素的化合价:______。
考点2 根据化学式求化合价
3.(山西中考)化学家戴维最早制得了曾用作麻醉剂的笑气(化学式为N2O),其中氮元素的化合价是( )
A.-1 B.-2 C.+1 D.+5
4.(南宁中考)科学家用Xe(氙气)首次合成了XePtF6,在XePtF6中Xe、F元素的化合价分别显+1、-1价,则XePtF6中Pt元素的化合价是( )
A.+2 B.+4 C.+5 D.+7
C
C
5.在下列物质中标出硫元素的化合价。
(1)硫(S)
(2)二氧化硫(SO2)
(3)硫酸(H2SO4)
(4)硫化氢(H2S)
-2
+4
0
+6
考点3 根据化合价书写化学式
6.(邵阳中考)某物质的化学式为CaWOx,其中钙元素为+2价,钨(W)元素为+6价,氧元素为-2价,则x的值是( )
A.2 B.3
C.4 D.5
7.根据化合价写出下列元素或原子团组成的物质的化学式。
C
Na2O
NaCl
NaNO3
CaO
CaCl2
Ca(NO3)2
FeO
FeCl2
Fe(NO3)2
Fe2O3
FeCl3
Fe(NO3)3
? Na+ Ca2+ Fe2+ Fe3+
8.写出下列物质的化学式。
(1)酸:硫酸_______、盐酸________、硝酸________。
(2)碱:氢氧化钠________、氢氧化钙_______、氢氧化铜_______、氢氧化钡_______。
(3)盐:①硫酸钠________、硫酸钡________、硫酸铜________。
②碳酸钠_________、碳酸钙_________、碳酸钡_________。
③硫酸铵_________、氯化铵_________。
(4)其他:氯酸钾________、高锰酸钾________、锰酸钾________、过氧化氢________。
H2SO4
HCl
HNO3
NaOH
Ca(OH)2
Cu(OH)2
Ba(OH)2
Na2SO4
BaSO4
CuSO4
Na2CO3
CaCO3
BaCO3
(HN4)2SO4
NH4Cl
KClO3
KMnO4
K2MnO4
H2O2
9.下列有关化合价的叙述正确的是 ( )
A.化合价与原子最外层电子数无关
B.氨气(NH3)中氮元素的化合价为+3
C.氧气中氧元素的化合价为-2
D.有些元素在不同条件下可表现出不同的化合价
10.(福建中考)下列是《本草纲目》记载的四种无机药物,其成分中Hg的化合价为+1的是( )
A.水银(Hg) B.升丹(HgO)
C.朱砂(HgS) D.轻粉(Hg2Cl2)
D
D
11.(黔东南中考)硝酸铵(NH4NO3)是一种肥效较高、使用广泛的氮肥,但近年来不法分子用它来生产炸药,给社会的安全和稳定带来了很大的压力。为此,国家相关部门加强了对硝酸铵生产和使用的监管,减少了它在农业生产中的使用。科学研究发现,硝酸铵爆炸时,氮元素的化合价会发生变化。下列关于硝酸铵中氮元素化合价的判断,正确的是( )
A.-4 +6 B.+1 +1
C.-3 +5 D.无法确定
12.(重庆中考B卷)某工厂制取漂白液的化学原理为Cl2+2NaOH===NaCl+NaClO+H2O,在该反应中,氯元素没有呈现出的化合价是( )
A.+2 B.+1
C.0 D.-1
C
A
13.元素R在化合物中只有一种化合价,其氧化物的化学式为R2O3,则下列化学式中正确的是( )
A.R(OH)2 B.R2(SO4)3
C.RNO3 D.RCO3
14.用化学用语填空。
(1)镁:_______。
(2)2个氮气分子:________。
(3)5个硫酸根离子:_______。
(4)五氧化二磷:________。
(5)+6价的硫元素:________。
(6)由Fe3+和OH-构成的氢氧化铁:________。
B
Mg
2N2
P2O5
Fe(OH)3
15.通过对已学知识的对比和归纳,我们往往可以得出一些十分有趣的规律,这些规律可以帮助我们掌握学习化学的方法。请你仔细阅读下表中的内容,并回答相应的问题:
(1)由前两行内容对照可得出的规律是元素或原子团的化合价数值往往与相应离子所带的_______数相等。
(2)由后两行内容对照可得出的规律是通过元素或原子团的_______可以确定相应化合物的化学式。
(3)利用表格中所给内容,请你再写出一种化合物的化学式:_____________。
(4)根据硫酸亚铁的化学式FeSO4,可推出该物质所含阳离子的符号为_______。
电荷
化合价
MgSO4(或NaCl等)
Fe2+
常见的几种离子
对应元素及原子团在化合物中的化合价
所能形成化合物的化学式 HCl、H2SO4、NaOH、
Mg(OH)2、MgCl2、Na2SO4
16.(柳州中考)如图是铁元素和氧元素常见化合价的坐标图,试判断a点上形成化合物的化学式为( )
A.Fe B.FeO
C.Fe2O3 D.Fe3O4
B
第3课时 化学式的有关计算
1.相对分子质量:化学式中各原子的______________的总和。符号为Mr。
2.根据化学式的计算
(1)计算相对分子质量
相对分子质量=化学式中各原子的_____________×相应____________的总和。
(2)计算物质组成元素的质量比
化合物中各元素的质量比=化学式中各_____________×相应___________之比。
(3)计算物质中某元素的质量分数
化合物中某元素的质量分数=
__________________________________________________________________。
相对原子质量
相对原子质量
原子个数
相对原子质量
原子个数
(化学式中该元素相对原子质量×原子个数)/化合物的相对分子质量×100%
3.其他类型的计算
(1)求一定量化合物中某一元素的质量某元素质量=化合物质量×化合物中该元素的_______________。
(2)求一定元素所在的某化合物的质量化合物质量=某元素的质量÷化合物中该元素的质量分数。
点 拨:根据化学式的计算常用方法
质量分数
考点1 相对分子质量的相关计算
1.计算出下列物质的相对分子质量。
(1)CO2的相对分子质量为_______。
(2)KClO3的相对分子质量为______。
(3)Al(OH)3的相对分子质量为______。
(4)C2H5OH的相对分子质量为______。
44
122.5
78
46
考点2 物质中各元素质量比
2.计算出下列物质中元素的质量比(填最简整数比)。
(1)P2O5中磷元素和氧元素的质量比=___________。
(2)C6H12O6中碳元素、氢元素和氧元素的质量比=___________。
(3)Fe2(SO4)3中铁元素、硫元素和氧元素的质量比=____________。
31∶40
6∶1∶8
7∶6∶12
考点3 某元素的质量分数的相关计算
3.计算出下列物质中元素的质量分数(结果精确到0.1%)。
(1)H2O中氢元素的质量分数__________。
(2)Mg(OH)2中镁元素的质量分数_________。
(3)CaCO3中钙元素的质量分数__________。
(4)NH4NO3中氮元素的质量分数__________。
11.1%
41.4%
40.0%
35.0%
考点4 化合物中某元素质量的计算
4.根据物质的质量求出下列物质中某元素的质量。
(1)8 g CH4中含有的碳元素的质量是多少?
?
?
(2)80 g NH4NO3中含有的氮元素的质量是多少?
5.根据某元素的质量求出物质的质量。
(1)已知CO中碳元素的质量为12 g,求CO的质量为多少?
?
?
(2)NH4HCO3中氮元素的质量为7 g,求NH4HCO3的质量为多少?
6.(温州中考)茶叶中含有茶氨酸(C7H14O3N2),茶氨酸中各元素质量分数如图所示。其中①表示的元素是( )
A.碳 B.氢 C.氧 D.氮
7.某物质的化学式为ROH,相对分子质量为51,则R的相对原子质量为( )
A.34 B.34 g C.40 D.40 g
A
A
8.(衡阳中考)硫酸新霉素——是“瘦肉精”中添加的“人用西药”,其化学式为C23H18N6O17S,下列关于硫酸新霉素的说法正确的是( )
A.硫酸新霉素中含65个原子
B.硫酸新霉素中氢、硫元素的质量比为18∶1
C.硫酸新霉素中氢元素的质量分数最小
D.硫酸新霉素的相对分子质量为682 g
C
9.(金华中考)如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是
( )
A.苯分子由碳、氢两种元素组成
B.苯中氢元素的质量分数小于10%
C.六氯苯中碳氯两种元素的质量比为1∶1
D.六氯苯由6个碳原子和6个氯原子构成
B
10.已知铁的氧化物中,铁元素与氧元素的质量比为7∶3,则该铁的氧化物的化学式是( )
A.Fe2O3 B.Fe3O4 C.FeO D.Fe2O
11.(内江中考)一种新型环保材料被塑胶跑道工程广泛应用,合成这种新材料的原料是二甲苯烷二异氰酸酯(分子式为C15H10N2O2)。请回答下列有关问题。
(1)二甲苯烷二异氰酸酯中氢、氧元素的质量比为________(填最简整数比)。
(2)二甲苯烷二异氰酸酯的相对分子质量为_______。
(3)500 g二甲苯烷二异氰酸酯中含氮元素的质量为_______g。
A
5∶16
250
56
12.(兰州中考)化学家TimRichard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26)。请计算。
(1)“小狗烯”的相对分子质量是_______。
(2)“小狗烯”中碳元素和氢元素的质量比为_______(填最简整数比)。
(3)16.9 g“小狗烯”中含碳元素多少克?(写出计算过程,结果精确到0.1 g)
338
12∶1
13.(泰安中考)儿童缺锌会引起食欲不振、发育不良等症状。如图为某补锌口服液说明书的部分信息,图中葡萄糖酸锌化学式已不完整,请根据相关信息回答下列问题。
×××牌补锌口服液
主要成分:葡萄糖酸锌
化 学 式:C12HxO14Zn
含 锌:5.0 mg/支
质 量:10.0 g/支
(1)葡萄糖酸锌的相对分子质量是455,则葡萄糖酸锌化学式中氢原子右下角的数字为____。
(2)若儿童1 kg体重每日需要0.5 mg锌,每天从食物中只能摄入所需锌的一半。体重为20 kg的儿童,理论上一天还需服用该口服液____支。
22
1
14.55 g二氧化碳中所含氧元素的质量和多少克水中所含氧元素的质量相等( )
A.18 g B.20 g
C.45 g D.36 g
15.经分析知,某硝酸铵(NH4NO3)样品中氮元素的质量分数为38%,则这种氮肥中可能混入的杂质是( )
A.NH4HCO3 B.NH4Cl
C.CO(NH2)2 D.(NH4)2SO4
C
C
请写出下列离子的符号
氢离子:__________,钾离子:__________,钠离子:__________,
氯离子:__________,氢氧根离子:__________,钙离子:__________,镁离子:__________,钡离子:__________,铝离子:__________,
碳酸根离子:_________,铁离子:_________,亚铁离子:________,
铜离子:_________,锌离子:_________,硫酸根离子:_________。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
