沪教版九年级化学上册第五章第2节 金属矿物 铁的冶炼基础巩固练习附答案
文档属性
| 名称 | 沪教版九年级化学上册第五章第2节 金属矿物 铁的冶炼基础巩固练习附答案 |

|
|
| 格式 | zip | ||
| 文件大小 | 168.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-10-21 00:00:00 | ||
图片预览


文档简介
第2节 金属矿物 铁的冶炼
一、选择题(共10小题)
1.下列矿石中,其主要成分不属于氧化物的是( )
A.赤铁矿 B.磁铁矿 C.菱铁矿 D.铝土矿
2.菱铁矿的主要成分是FeCO3,下列有关说法正确的是( )
A.菱铁矿是铁的合金
B.菱铁矿中铁元素的质量分数为48.3%
C.FeCO3中铁的化合价为+3
D.FeCO3是含有氧元素的化合物
3.下列说法中,正确的是( )
A.地壳中含量最多的金属元素是铁
B.赤铁矿、磁铁矿是重要的金属资源
C.铝比铁活泼,所以铁比铝耐腐蚀
D.纯铜的熔点小于铜锌合金
4.把铁矿石、焦炭和石灰石一起加入到高炉中进行冶炼,得到的产物是( )
A.钢 B.生铁 C.纯铁 D.锰钢
5.下列关于工业炼铁的叙述中错误的是( )
A.主要原理为:利用焦炭的还原性置换出铁矿石中的铁
B.主要原料为铁矿石、焦炭和石灰石等
C.主要设备为高炉
D.主要产物为生铁
6.炼铁高炉中发生了下列反应:①高温下一氧化碳将铁矿石还原为铁 ②高温煅烧石灰石 ③灼热的焦炭和二氧化碳反应 ④焦炭充分燃烧
其中属于化合反应的是( )
A.①和④ B.②和③ C.③和④ D.只有④
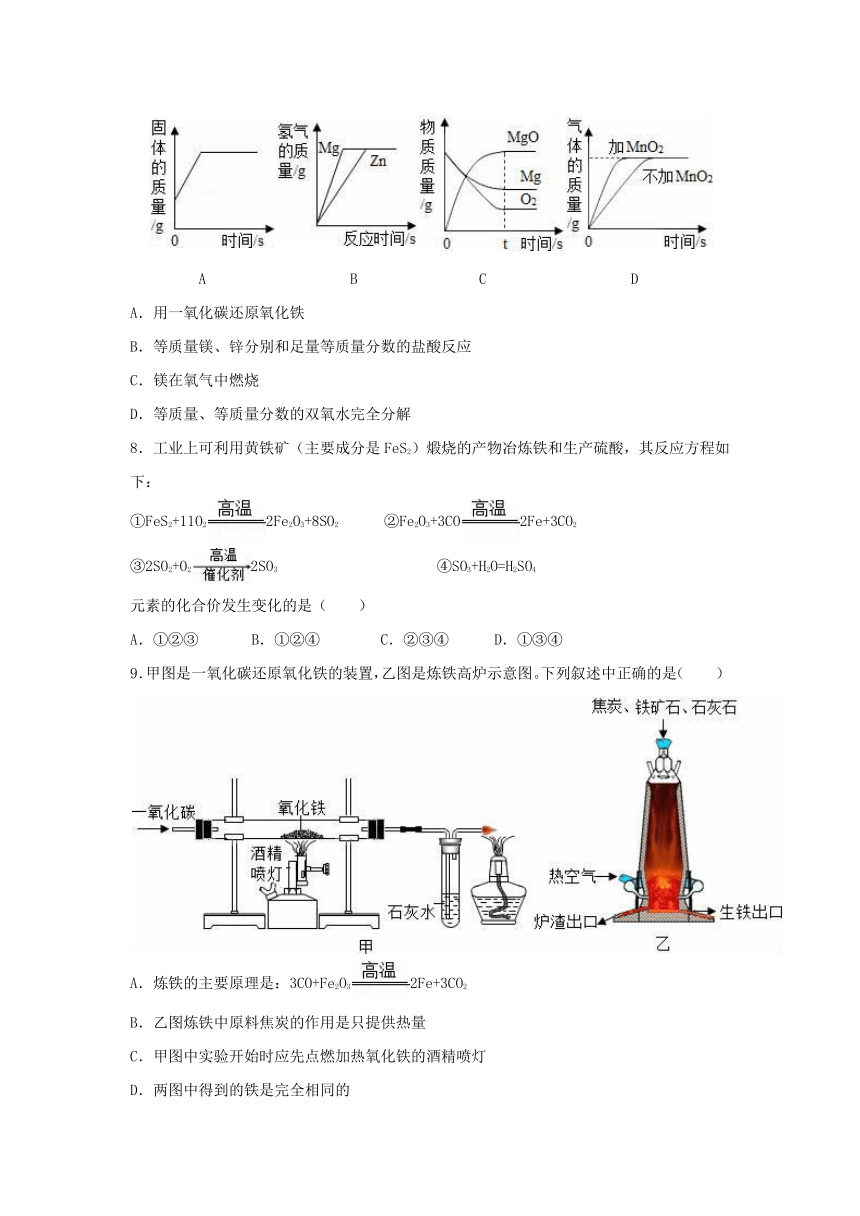
7.能反映相关实验过程中量的变化的图象是( )
////
A B C D
A.用一氧化碳还原氧化铁
B.等质量镁、锌分别和足量等质量分数的盐酸反应
C.镁在氧气中燃烧
D.等质量、等质量分数的双氧水完全分解
8.工业上可利用黄铁矿(主要成分是FeS2)煅烧的产物冶炼铁和生产硫酸,其反应方程如下:
①FeS2+11O2/2Fe2O3+8SO2 ②Fe2O3+3CO/2Fe+3CO2
③2SO2+O2/2SO3 ④SO3+H2O=H2SO4
元素的化合价发生变化的是( )
A.①②③ B.①②④ C.②③④ D.①③④
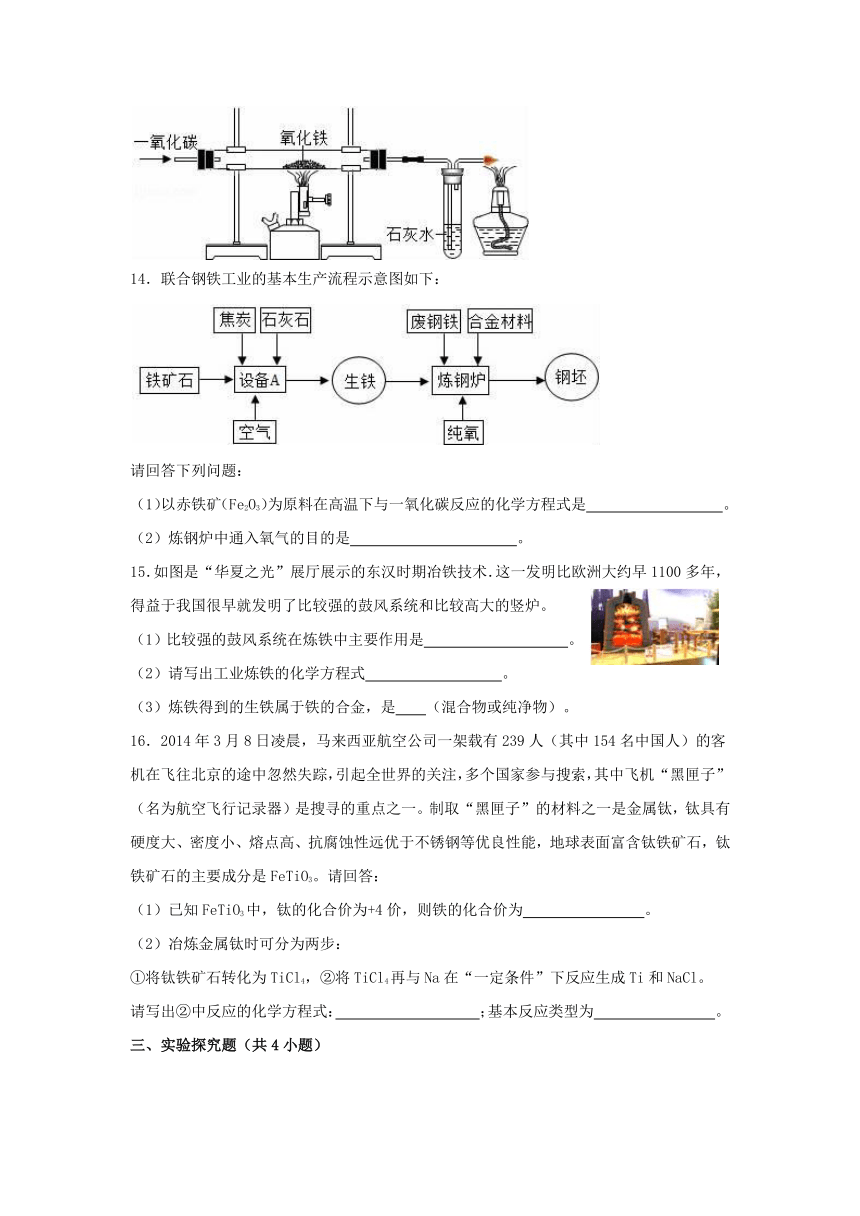
9.甲图是一氧化碳还原氧化铁的装置,乙图是炼铁高炉示意图。下列叙述中正确的是( )
/
A.炼铁的主要原理是:3CO+Fe2O3/2Fe+3CO2
B.乙图炼铁中原料焦炭的作用是只提供热量
C.甲图中实验开始时应先点燃加热氧化铁的酒精喷灯
D.两图中得到的铁是完全相同的
10.炼铁厂以赤铁矿石、焦炭、石灰石、空气等为原料炼铁,主要反应过程如图所示:/
请根据题图和所学知识判断,下列说法错误的是( )
A.生铁属于混合物
B.炼铁过程中所有元素的化合价均发生了改变
C.原料中焦炭的作用是提供能量和制取一氧化碳
D.工业炼铁的设备是高炉
二、填空题(共6小题)
11.常见的铁矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2),用 矿炼铁会产生形成酸雨的有害气体。如图微观示意图表示的反应也会产生有害气体,该反应的化学方程式是 。
/
12.科学兴趣小组用以下装置探究炼铁的原理。
/
(1)为避免将CO排放到空气中,并回收利用CO,方框中连接的是C和D装置,导管接口的连接顺序应为a→ 。(用箭头和接口字母表示)
(2)玻璃管A中发生反应的化学方程式为 。
13.如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象 ,反应方程式是 ,图中右边酒精的作用是 。
/
14.联合钢铁工业的基本生产流程示意图如下:
/
请回答下列问题:
(1)以赤铁矿(Fe2O3)为原料在高温下与一氧化碳反应的化学方程式是 。
(2)炼钢炉中通入氧气的目的是 。
15.如图是“华夏之光”展厅展示的东汉时期冶铁技术.这一发明比欧洲大约早1100多年,得益于我国很早就发明了比较强的鼓风系统和比较高大的竖炉。
(1)比较强的鼓风系统在炼铁中主要作用是 。
(2)请写出工业炼铁的化学方程式 。
(3)炼铁得到的生铁属于铁的合金,是 (混合物或纯净物)。
16.2014年3月8日凌晨,马来西亚航空公司一架载有239人(其中154名中国人)的客机在飞往北京的途中忽然失踪,引起全世界的关注,多个国家参与搜索,其中飞机“黑匣子”(名为航空飞行记录器)是搜寻的重点之一。制取“黑匣子”的材料之一是金属钛,钛具有硬度大、密度小、熔点高、抗腐蚀性远优于不锈钢等优良性能,地球表面富含钛铁矿石,钛铁矿石的主要成分是FeTiO3。请回答:
(1)已知FeTiO3中,钛的化合价为+4价,则铁的化合价为 。
(2)冶炼金属钛时可分为两步:
①将钛铁矿石转化为TiCl4,②将TiCl4再与Na在“一定条件”下反应生成Ti和NaCl。
请写出②中反应的化学方程式: ;基本反应类型为 。
三、实验探究题(共4小题)
17.已知碳酸亚铁在隔绝空气的条件下,受热易分解生成氧化亚铁和二氧化碳:在空气中加热,则生成氧化铁和二氧化碳.某化学兴趣小组用如图所示的装置模拟炼铁过程,并测定某样品中碳酸亚铁的含量(该装置气密性良好,B中氢氧化钠溶液足量)。
/
实验过程中,先打开K通入一氧化碳再加热;装置A中固体质量不再减少后,停止加热,待装置A冷却到室温后关闭K,实验测得装置A中固体质量减少了a g,装置B中液体质量增加了b g。
回答下列问题:
(1)仪器①的名称是 ;
(2)写出装置A中发生的一个反应的化学方程式 ;
(3)能判断生成的二氧化碳全部被装置B吸收的依据是:装置B的质量增加且 ;
(4)若生成的二氧化碳全部被装置B吸收,不考虑水的蒸发且该样品中所含杂质不参加反应,则a b(填“>”“=”或“<”)。
(5)D处为收集尾气的装置,应选择 装置(填“甲”“乙”或“丙”)。
18.实验室根据工业炼铁的原理设计了如图所示装置进行实验.请回答:
(1)主要成分为氧化铁的矿石名称为 ;图中还原氧化铁的化学方程式为: 。
(2)“加热”和“通气”(通入CO)的操作顺序是 。
/
19.钛和钛合金被认为是21世纪的重要金属材料,被广泛用于火箭、导弹、航天飞机、船舶等,如图为某化工企业生成钛流程示意图:
/
请回答下列问题:
(1)FeTiO3中钛元素的化合价为 ;
(2)①中化学方程式为2FeTiO3+6C+7Cl2/2X+2TiCl4+6CO,则X为 (填化学式);
(3)②中CO和H2以化学计量数1:2恰好完全反应,则该反应的基本反应类型是 ;
(4)③中氩气的作用是 ,该反应的化学方程式为 。
20.铝和铝合金是一类重要的金属材料、工业上用铝土矿(含有Al2O3和SiO2,不考虑其它杂志)制取金属铝的基本流程如下:
已知:①SiO2是一种难溶于水,也不与盐酸、硫酸反应的物质。
②铝盐与氨水反应,生成氢氧化铝沉淀和铵盐。
请回答下列问题:
(1)Al2O3与稀硫酸反应的化学方程式为 。
(2)操作Ⅱ的名称是 。
(3)滤液Ⅱ中溶质的用途之一是 。
(4)电解熔融的Al2O3,除得到金属铝之外,还可得到的气体产物是 (填化学式)。
工业上电解熔融的Al2O3时,还加入了冰晶石(Na3AlF6)作熔剂,其作用是降低Al2O3的熔点,冰晶石在物质中的分类属于 (填字母)。
A.酸 B.碱 C.盐 D.氧化物
/
参考答案
1. C
2. D
3. B
4. B
5. A
6. C
7. D
8. A
9. A
10. B
11.黄铁矿(或FeS2) 2H2S+3O2/2SO2+2H2O
12.(1)d→b→e (2)Fe2O3+3CO/2Fe+3CO2
13.固体由红棕色变化为黑色 Fe2O3+3CO/2Fe+3CO2 点燃没有参与反应的CO
14.(1)3CO+Fe2O3/2Fe+3CO2
(2)使生铁中碳充分反应,降低碳的含量
15.(1)提供充足氧气(空气)
(2)Fe2O3+3CO / 2Fe+3CO2
(3)混合物
16. +2 4Na+TiCl4/Ti+4NaCl 置换反应
17.(1)酒精灯
(2)Fe2O3+3CO/2Fe+3CO2
(3)C中澄清的石灰水不变浑浊
(4)<
(5)乙
18.(1)赤铁矿 3CO+Fe2O3/2Fe+3CO2
(2)通气、加热
19.(1)+4
(2)FeCl3
(3)化合反应
(4)作保护气,2Mg+TiCl4/Ti+2MgCl2
20.(1)Al2O3+3H2SO4=Al2(SO4)3+3H2O
(2)过滤
(3)氮肥
(4)O2
(5)C
一、选择题(共10小题)
1.下列矿石中,其主要成分不属于氧化物的是( )
A.赤铁矿 B.磁铁矿 C.菱铁矿 D.铝土矿
2.菱铁矿的主要成分是FeCO3,下列有关说法正确的是( )
A.菱铁矿是铁的合金
B.菱铁矿中铁元素的质量分数为48.3%
C.FeCO3中铁的化合价为+3
D.FeCO3是含有氧元素的化合物
3.下列说法中,正确的是( )
A.地壳中含量最多的金属元素是铁
B.赤铁矿、磁铁矿是重要的金属资源
C.铝比铁活泼,所以铁比铝耐腐蚀
D.纯铜的熔点小于铜锌合金
4.把铁矿石、焦炭和石灰石一起加入到高炉中进行冶炼,得到的产物是( )
A.钢 B.生铁 C.纯铁 D.锰钢
5.下列关于工业炼铁的叙述中错误的是( )
A.主要原理为:利用焦炭的还原性置换出铁矿石中的铁
B.主要原料为铁矿石、焦炭和石灰石等
C.主要设备为高炉
D.主要产物为生铁
6.炼铁高炉中发生了下列反应:①高温下一氧化碳将铁矿石还原为铁 ②高温煅烧石灰石 ③灼热的焦炭和二氧化碳反应 ④焦炭充分燃烧
其中属于化合反应的是( )
A.①和④ B.②和③ C.③和④ D.只有④
7.能反映相关实验过程中量的变化的图象是( )
////
A B C D
A.用一氧化碳还原氧化铁
B.等质量镁、锌分别和足量等质量分数的盐酸反应
C.镁在氧气中燃烧
D.等质量、等质量分数的双氧水完全分解
8.工业上可利用黄铁矿(主要成分是FeS2)煅烧的产物冶炼铁和生产硫酸,其反应方程如下:
①FeS2+11O2/2Fe2O3+8SO2 ②Fe2O3+3CO/2Fe+3CO2
③2SO2+O2/2SO3 ④SO3+H2O=H2SO4
元素的化合价发生变化的是( )
A.①②③ B.①②④ C.②③④ D.①③④
9.甲图是一氧化碳还原氧化铁的装置,乙图是炼铁高炉示意图。下列叙述中正确的是( )
/
A.炼铁的主要原理是:3CO+Fe2O3/2Fe+3CO2
B.乙图炼铁中原料焦炭的作用是只提供热量
C.甲图中实验开始时应先点燃加热氧化铁的酒精喷灯
D.两图中得到的铁是完全相同的
10.炼铁厂以赤铁矿石、焦炭、石灰石、空气等为原料炼铁,主要反应过程如图所示:/
请根据题图和所学知识判断,下列说法错误的是( )
A.生铁属于混合物
B.炼铁过程中所有元素的化合价均发生了改变
C.原料中焦炭的作用是提供能量和制取一氧化碳
D.工业炼铁的设备是高炉
二、填空题(共6小题)
11.常见的铁矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2),用 矿炼铁会产生形成酸雨的有害气体。如图微观示意图表示的反应也会产生有害气体,该反应的化学方程式是 。
/
12.科学兴趣小组用以下装置探究炼铁的原理。
/
(1)为避免将CO排放到空气中,并回收利用CO,方框中连接的是C和D装置,导管接口的连接顺序应为a→ 。(用箭头和接口字母表示)
(2)玻璃管A中发生反应的化学方程式为 。
13.如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象 ,反应方程式是 ,图中右边酒精的作用是 。
/
14.联合钢铁工业的基本生产流程示意图如下:
/
请回答下列问题:
(1)以赤铁矿(Fe2O3)为原料在高温下与一氧化碳反应的化学方程式是 。
(2)炼钢炉中通入氧气的目的是 。
15.如图是“华夏之光”展厅展示的东汉时期冶铁技术.这一发明比欧洲大约早1100多年,得益于我国很早就发明了比较强的鼓风系统和比较高大的竖炉。
(1)比较强的鼓风系统在炼铁中主要作用是 。
(2)请写出工业炼铁的化学方程式 。
(3)炼铁得到的生铁属于铁的合金,是 (混合物或纯净物)。
16.2014年3月8日凌晨,马来西亚航空公司一架载有239人(其中154名中国人)的客机在飞往北京的途中忽然失踪,引起全世界的关注,多个国家参与搜索,其中飞机“黑匣子”(名为航空飞行记录器)是搜寻的重点之一。制取“黑匣子”的材料之一是金属钛,钛具有硬度大、密度小、熔点高、抗腐蚀性远优于不锈钢等优良性能,地球表面富含钛铁矿石,钛铁矿石的主要成分是FeTiO3。请回答:
(1)已知FeTiO3中,钛的化合价为+4价,则铁的化合价为 。
(2)冶炼金属钛时可分为两步:
①将钛铁矿石转化为TiCl4,②将TiCl4再与Na在“一定条件”下反应生成Ti和NaCl。
请写出②中反应的化学方程式: ;基本反应类型为 。
三、实验探究题(共4小题)
17.已知碳酸亚铁在隔绝空气的条件下,受热易分解生成氧化亚铁和二氧化碳:在空气中加热,则生成氧化铁和二氧化碳.某化学兴趣小组用如图所示的装置模拟炼铁过程,并测定某样品中碳酸亚铁的含量(该装置气密性良好,B中氢氧化钠溶液足量)。
/
实验过程中,先打开K通入一氧化碳再加热;装置A中固体质量不再减少后,停止加热,待装置A冷却到室温后关闭K,实验测得装置A中固体质量减少了a g,装置B中液体质量增加了b g。
回答下列问题:
(1)仪器①的名称是 ;
(2)写出装置A中发生的一个反应的化学方程式 ;
(3)能判断生成的二氧化碳全部被装置B吸收的依据是:装置B的质量增加且 ;
(4)若生成的二氧化碳全部被装置B吸收,不考虑水的蒸发且该样品中所含杂质不参加反应,则a b(填“>”“=”或“<”)。
(5)D处为收集尾气的装置,应选择 装置(填“甲”“乙”或“丙”)。
18.实验室根据工业炼铁的原理设计了如图所示装置进行实验.请回答:
(1)主要成分为氧化铁的矿石名称为 ;图中还原氧化铁的化学方程式为: 。
(2)“加热”和“通气”(通入CO)的操作顺序是 。
/
19.钛和钛合金被认为是21世纪的重要金属材料,被广泛用于火箭、导弹、航天飞机、船舶等,如图为某化工企业生成钛流程示意图:
/
请回答下列问题:
(1)FeTiO3中钛元素的化合价为 ;
(2)①中化学方程式为2FeTiO3+6C+7Cl2/2X+2TiCl4+6CO,则X为 (填化学式);
(3)②中CO和H2以化学计量数1:2恰好完全反应,则该反应的基本反应类型是 ;
(4)③中氩气的作用是 ,该反应的化学方程式为 。
20.铝和铝合金是一类重要的金属材料、工业上用铝土矿(含有Al2O3和SiO2,不考虑其它杂志)制取金属铝的基本流程如下:
已知:①SiO2是一种难溶于水,也不与盐酸、硫酸反应的物质。
②铝盐与氨水反应,生成氢氧化铝沉淀和铵盐。
请回答下列问题:
(1)Al2O3与稀硫酸反应的化学方程式为 。
(2)操作Ⅱ的名称是 。
(3)滤液Ⅱ中溶质的用途之一是 。
(4)电解熔融的Al2O3,除得到金属铝之外,还可得到的气体产物是 (填化学式)。
工业上电解熔融的Al2O3时,还加入了冰晶石(Na3AlF6)作熔剂,其作用是降低Al2O3的熔点,冰晶石在物质中的分类属于 (填字母)。
A.酸 B.碱 C.盐 D.氧化物
/
参考答案
1. C
2. D
3. B
4. B
5. A
6. C
7. D
8. A
9. A
10. B
11.黄铁矿(或FeS2) 2H2S+3O2/2SO2+2H2O
12.(1)d→b→e (2)Fe2O3+3CO/2Fe+3CO2
13.固体由红棕色变化为黑色 Fe2O3+3CO/2Fe+3CO2 点燃没有参与反应的CO
14.(1)3CO+Fe2O3/2Fe+3CO2
(2)使生铁中碳充分反应,降低碳的含量
15.(1)提供充足氧气(空气)
(2)Fe2O3+3CO / 2Fe+3CO2
(3)混合物
16. +2 4Na+TiCl4/Ti+4NaCl 置换反应
17.(1)酒精灯
(2)Fe2O3+3CO/2Fe+3CO2
(3)C中澄清的石灰水不变浑浊
(4)<
(5)乙
18.(1)赤铁矿 3CO+Fe2O3/2Fe+3CO2
(2)通气、加热
19.(1)+4
(2)FeCl3
(3)化合反应
(4)作保护气,2Mg+TiCl4/Ti+2MgCl2
20.(1)Al2O3+3H2SO4=Al2(SO4)3+3H2O
(2)过滤
(3)氮肥
(4)O2
(5)C
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
