鲁教版九年级上册化学 5.2 化学反应的表示 课件(26张PPT)
文档属性
| 名称 | 鲁教版九年级上册化学 5.2 化学反应的表示 课件(26张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 326.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2019-10-27 00:00:00 | ||
图片预览








文档简介
课件26张PPT。课题2
化学反应的表示【复习提问】参加化学反应的各物质 等于反应后生成的各物质 ,这一规律叫质量守恒定律。1. 什么是质量守恒定律?质量总和质量总和2. 化学反应中质量守恒的原因在一切化学反应中,反应前后原子的 ,原子的 ,原子的 。所以参加反应的各物质的质量之和必然等于反应后生成的各物质质量之和。
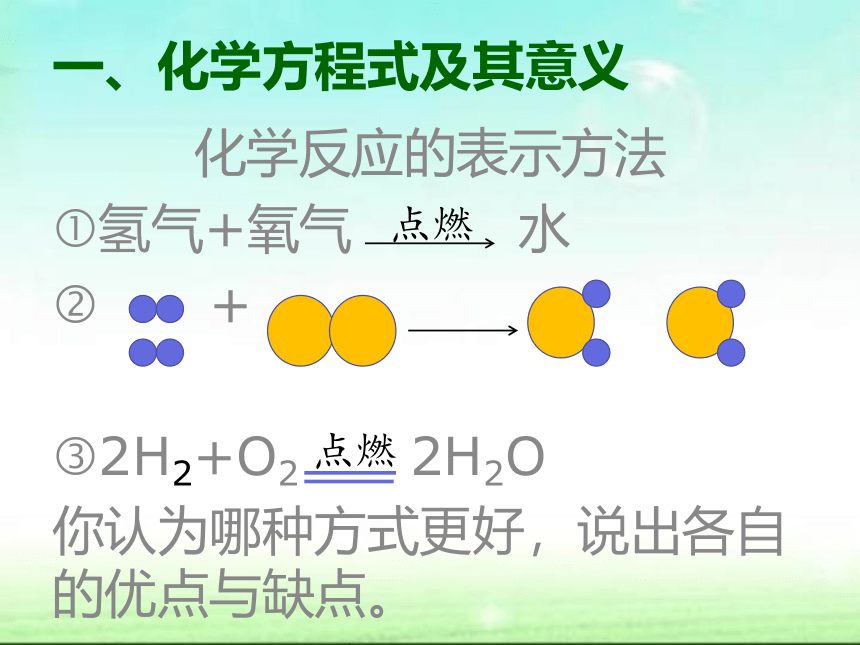
种类不变 数目不变质量不变一、化学方程式及其意义化学反应的表示方法
?氢气+氧气 水
? +
?2H2+O2 2H2O
你认为哪种方式更好,说出各自的优点与缺点。 点燃点燃1、化学方程式:
概念:用化学式来表示化学反应的式子。举例:氢气在氧气中燃烧生成水。反应物生成物反应
条件2、化学方程式的读法 2H2+O2 = 2H2O
粒子数目之比: 2 : 1 : 2
相对质量之比:(2x2): (1x32) : (2x18)
物质的质量之比: 4 : 32 : 36点燃(1)宏观:氢气和氧气在点燃的条件下反应生成水。
(2)注意符号的读法:“+”读作“和”“与”;“=”读作“反应生成”。(3)微观:在点燃的条件下,2个氢气分子,和1个氧分子完全反应,生成2个水分子。
(4)质量:在点燃的条件下,每4份的氢气,和32份质量的氧气恰好完全反应,生成36份质量的水。
1、表示反应物、生成物及反应条件。2、表示各物质粒子数之比。3、表示各物质之间的质量比。
各物质间的质量比=各物质相对分子质量和之比2H2+O2 = 2H2O点燃3、化学方程式的涵义课堂练习1: 说出下列方程式的涵义及其正确的读法。
(1)C+O2=CO2
点燃(1)反应物是C和O2、生成物是CO2、条件是点燃。
(2)粒子数之比为1:1:1
(3)质量之比为12:32:44
1、书写化学方程式遵循的两个原则(1)以客观事实为依据
(2)遵循质量守恒定律二、化学方程式的书写磷在氧气中燃烧的化学方程式如下,判断正误【问题讨论】(1)P + O2 PO2凭空臆造成生成物PO2?,与事实不符任意改动氧气化学式,也与事实不符反应前后各原子个数不相等,违背了质量守恒定律点燃注明反应条件和生成物的状态。 2、书写化学方程式的步骤:把短线改为等号。左右两边同种元素的原子总数相等。查化学式、查配平、查条件等“注'反应条件、生成物状态(1)反应条件只有一个写在等号的上方;若需2个或多个条件,则分开写在等号上下方
(2) 常见的反应条件
点燃,加热,催化剂,高温等; 点燃≠加热(△) ;点燃≠燃烧(不能写燃烧);高温≠加热(△)”标状态“:如果生成物中有气体放出或沉淀生成,一般在它们的化学式的后面用”↑”或”↓”注明。学霸笔记:
若反应物中有气体,生成物中就不需用“↑”。
若反应物中有固体,生成物中就不需用“↓”。
2 KMnO4 = K2MnO4 + MnO2+ O2△↑CuSO4+2NaOH=Cu(OH) 2 +Na2SO4↓H2O+O2由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式写出反应物和生成物的化学式并用短线或箭头相连。H2O2H2O+O2由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式配平化学方程式H2O222H2O+O2由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式注明反应发生的条件和生成物的状态 2H2O22MnO2↑H2O+O2↑由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式把短线改为等号。 2H2O22MnO2H2O+O2↑由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式查化学式、查配平、查条件等 2H2O22MnO2配平依据:质量守恒定律配平目的:是使方程式左右两边 的同种元素的原子总数相等。观察法、最小公倍数法、奇数配偶法等配平方法:在化学式前配上适当的化学计量数。学霸笔记: 2、配平化学方程式的方法①观察法2222↑↑(1) Mg +O2 = MgO
(2)CO2 + C = CO点燃练一练:配平下列化学方程式22高温2?最小公倍数法Al + O2 Al2O3点燃324 P + O2 P2O5 524点燃 练一练:配平下列化学方程式 (1) Fe + O2 = Fe2O3
(2) Fe + O2 = Fe3O4
(3) CO2 + Ca(OH)2=CaCO3 +H2O324点燃23↓小结: 1. 化学方程式的书写原则(1)以客观事实为基础,
(2)遵守质量守恒定律2.化学方程式的书写步骤五字口诀: 写---配---注---等---查3. 配平化学方程式的方法①观察法
?最小公倍数法
化学反应的表示【复习提问】参加化学反应的各物质 等于反应后生成的各物质 ,这一规律叫质量守恒定律。1. 什么是质量守恒定律?质量总和质量总和2. 化学反应中质量守恒的原因在一切化学反应中,反应前后原子的 ,原子的 ,原子的 。所以参加反应的各物质的质量之和必然等于反应后生成的各物质质量之和。
种类不变 数目不变质量不变一、化学方程式及其意义化学反应的表示方法
?氢气+氧气 水
? +
?2H2+O2 2H2O
你认为哪种方式更好,说出各自的优点与缺点。 点燃点燃1、化学方程式:
概念:用化学式来表示化学反应的式子。举例:氢气在氧气中燃烧生成水。反应物生成物反应
条件2、化学方程式的读法 2H2+O2 = 2H2O
粒子数目之比: 2 : 1 : 2
相对质量之比:(2x2): (1x32) : (2x18)
物质的质量之比: 4 : 32 : 36点燃(1)宏观:氢气和氧气在点燃的条件下反应生成水。
(2)注意符号的读法:“+”读作“和”“与”;“=”读作“反应生成”。(3)微观:在点燃的条件下,2个氢气分子,和1个氧分子完全反应,生成2个水分子。
(4)质量:在点燃的条件下,每4份的氢气,和32份质量的氧气恰好完全反应,生成36份质量的水。
1、表示反应物、生成物及反应条件。2、表示各物质粒子数之比。3、表示各物质之间的质量比。
各物质间的质量比=各物质相对分子质量和之比2H2+O2 = 2H2O点燃3、化学方程式的涵义课堂练习1: 说出下列方程式的涵义及其正确的读法。
(1)C+O2=CO2
点燃(1)反应物是C和O2、生成物是CO2、条件是点燃。
(2)粒子数之比为1:1:1
(3)质量之比为12:32:44
1、书写化学方程式遵循的两个原则(1)以客观事实为依据
(2)遵循质量守恒定律二、化学方程式的书写磷在氧气中燃烧的化学方程式如下,判断正误【问题讨论】(1)P + O2 PO2凭空臆造成生成物PO2?,与事实不符任意改动氧气化学式,也与事实不符反应前后各原子个数不相等,违背了质量守恒定律点燃注明反应条件和生成物的状态。 2、书写化学方程式的步骤:把短线改为等号。左右两边同种元素的原子总数相等。查化学式、查配平、查条件等“注'反应条件、生成物状态(1)反应条件只有一个写在等号的上方;若需2个或多个条件,则分开写在等号上下方
(2) 常见的反应条件
点燃,加热,催化剂,高温等; 点燃≠加热(△) ;点燃≠燃烧(不能写燃烧);高温≠加热(△)”标状态“:如果生成物中有气体放出或沉淀生成,一般在它们的化学式的后面用”↑”或”↓”注明。学霸笔记:
若反应物中有气体,生成物中就不需用“↑”。
若反应物中有固体,生成物中就不需用“↓”。
2 KMnO4 = K2MnO4 + MnO2+ O2△↑CuSO4+2NaOH=Cu(OH) 2 +Na2SO4↓H2O+O2由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式写出反应物和生成物的化学式并用短线或箭头相连。H2O2H2O+O2由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式配平化学方程式H2O222H2O+O2由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式注明反应发生的条件和生成物的状态 2H2O22MnO2↑H2O+O2↑由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式把短线改为等号。 2H2O22MnO2H2O+O2↑由书写步骤写一写
例1:书写过氧化氢制取氧气的化学方程式查化学式、查配平、查条件等 2H2O22MnO2配平依据:质量守恒定律配平目的:是使方程式左右两边 的同种元素的原子总数相等。观察法、最小公倍数法、奇数配偶法等配平方法:在化学式前配上适当的化学计量数。学霸笔记: 2、配平化学方程式的方法①观察法2222↑↑(1) Mg +O2 = MgO
(2)CO2 + C = CO点燃练一练:配平下列化学方程式22高温2?最小公倍数法Al + O2 Al2O3点燃324 P + O2 P2O5 524点燃 练一练:配平下列化学方程式 (1) Fe + O2 = Fe2O3
(2) Fe + O2 = Fe3O4
(3) CO2 + Ca(OH)2=CaCO3 +H2O324点燃23↓小结: 1. 化学方程式的书写原则(1)以客观事实为基础,
(2)遵守质量守恒定律2.化学方程式的书写步骤五字口诀: 写---配---注---等---查3. 配平化学方程式的方法①观察法
?最小公倍数法
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
